抽象
我们讨论病毒和免疫介导的肺损伤和流感感染后的修复的新方面http://ow.ly/JGhC6
抽象
流感病毒是一些最重要的人类病原体,造成大量的季节性和流行性发病率和死亡率。在人体内,下呼吸道感染可导致肺泡隔,因呼吸衰竭急性呼吸窘迫综合征而死亡的发展的泛滥。流感介导的自以下组合气道的损害,肺泡上皮和肺泡内皮的结果:1)固有病毒致病,归属于它的向性主机气道和肺泡上皮细胞;和2)一个健壮宿主先天免疫应答,其,同时促进病毒的清除,可以恶化肺损伤的严重程度。在这次审查中,我们的流感病毒感染过程中总结的病毒主机接口的分子事件,凸显了一些重要的细胞反应。我们讨论免疫介导的病毒清除,促进或延续肺损伤,流感诱发的损伤后肺再生,在流感预防和治疗的最新进展的机制。
介绍
在发达国家,季节性A型流感病毒(IAV)感染是肺炎相关死亡的最常见原因,而在大流行期间,由IAV感染导致的死亡率可能要高得多。例如,在2009年大流行期间,IAV感染上升为美国第九大死亡原因[1,2]。IAV主要目标气道和肺泡上皮细胞,因为它们表达唾液酸残基的功能受体的病毒,导致上皮损伤和流体和蛋白质渗出到气管和肺泡空间,威胁气体交换[3-7]。在临床上,严重IAV感染可与低氧血症呼吸衰竭双侧肺浸润和低氧血症,它定义急性呼吸窘迫综合征(ARDS),死亡目前是一个主要贡献者死亡率[8-14]。Ťhe overall incidence of ARDS attributable to seasonal IAV infection has been estimated at 2.7 cases per 100 000 person-years and can account for 4% of all hospitalisations for respiratory failure during the influenza season [15]。我们发现它在概念上非常有用考虑IAV感染的过程分为三个阶段,与许多这些过程同时发生通过损伤过程的理解。第一个是气道和肺泡上皮和其在这些细胞中,复制的病毒感染,在此期间的策略,限制病毒进入或复制可以防止或减弱感染的严重程度[3,16,17]。第二个是先天随后适应性免疫应答的病毒,这是病毒清除重要的,但也能诱导到肺泡上皮和内皮[显著损害18,19]。第三是长期免疫的伴随着浸润和受损的肺组织的再生的分辨率,在此期间,存在增加的易感性的继发性细菌感染(感染的病毒株的发展图1)[20-22]。B型流感病毒在形态上与IAV相似;然而,可能由于人类和海豹是B型流感病毒的唯一宿主,这些病毒的遗传多样性仅限于两种流行毒株,儿童更容易受到感染[23,24]。最近的文献复习建议,临床表现和儿童乙型流感感染的并发症是相似的IAV;然而,作者指出,文学不足以排除重要的区别[24]。对于本次审查的部分,我们限制了我们IAV讨论时明确指出除。⇓
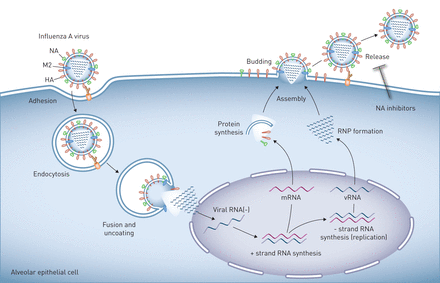
甲型流感病毒在肺上皮的复制。流感病毒粒子表面表达的血凝素(HA)与与细胞表面聚糖相连的唾液酸残基结合,诱导病毒粒子与靶细胞的质膜结合和融合。人类病毒中的HA与与表面聚糖相连的唾液酸残基相互作用通过α-2,6键,其在所述上和下气道的人类上皮和II型肺泡细胞中发现。相反,在与在α-2,3-键的唾液酸残基禽病毒相互作用的HA。然后,病毒进入细胞通过内吞作用或micropinocytosis和投放到其中酸化激活质子选择性基质蛋白-2病毒通道(M2)的溶酶体,诱导膜融合和病毒核蛋白(RNP)芯,然后将其输送至细胞核的离解,其中病毒RNA的复制发生。子代病毒RNP核心被在胞质溶胶中产生的,并与病毒表面蛋白,HA和神经氨酸酶(NA),和其它病毒蛋白,集中在在质膜和邻近脂筏。这些细胞膜区域的出芽形成完整病毒后代,其被链接到由HA /唾液酸相互作用质膜。的神经氨酸酶由释放病毒后代,这样他们就可以自由感染其它细胞,其可通过NA抑制剂可以防止唾液酸残基的裂解。肺泡上皮细胞被示为一个例子,但生命周期是在气道上皮细胞相似。
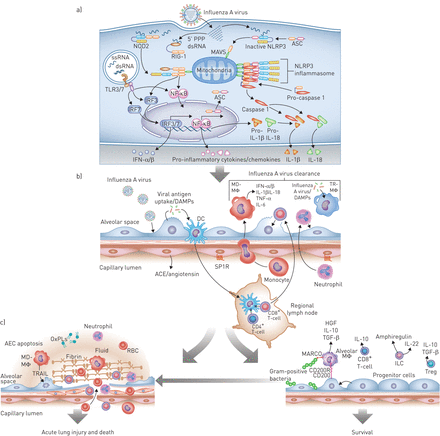
流感感染导致肺部有益和有害的宿主免疫途径的顺序启动。一)最早的响应出现在受感染的气道或肺泡上皮细胞(AEC)。从左至右,细胞内病毒RNA的存在激活Toll样受体(TLR),主要是TLR7和TLR3,以诱导途径即达到高潮中的干扰素调节因子活化(IRF)3或IRF7,这增加了类型的转录我干扰素(IFN)-α/β。这个通路的激活也可以通过激活核因子(NF)-κB诱导促炎性细胞因子和趋化因子的转录。5'三磷酸化的双链RNA(5'-PPP的dsRNA)在流感感染诱导的构象变化释放到胞质溶胶中视黄酸可诱导的基因-I(RIG-I),其与线粒体抗病毒信号蛋白(MAVS)允许它相互作用来激活核苷酸结合寡聚化结构域的蛋白质(NOD)2。这也导致I型干扰素的转录通过IRF3和促炎性细胞因子通过NF-κB。inflammasome蛋白质ASC(适配器蛋白质凋亡speck-like蛋白质包含一张卡片),pro-interleukin (IL) 1β和pro-IL-18 NF-κB引起的。在病毒RNA的存在,ASC与NLR家庭,pyrin domain-containing (NLRP) 3和小牛诱导激活NLRP3 inflammasome,劈开和激活caspase-1生成IL-1β和地震,从而放大炎症级联。b)气道或肺泡II型细胞感染后可释放损伤相关分子模式分子(DAMPs)和病原体相关分子模式分子(PAMPs),被常驻树突状细胞(DCs)感知。树突状细胞向区域淋巴结转移,激活细胞毒性(CD8)+)和辅助(CD4+)T细胞,以及能够诱导特异性抗病毒应答的稀有记忆T细胞(未示出)。与此同时,DAMP的,的PAMP,内吞病毒和或许流感感染本身诱导I型干扰素和炎性细胞因子的从组织驻留肺泡巨噬细胞(TR-MΦ)和DC释放(未示出)。这些细胞因子/趋化因子诱导的中性粒细胞的募集和外周血单核细胞的募集和分化成单核细胞衍生肺泡巨噬细胞(MD-MΦ)。两个中性粒细胞和MD-MΦ放大炎性反应。损坏底层内皮导致炎性细胞募集和炎症的负调节,包括通过鞘氨醇-1-磷酸受体(SP1R)信令和血管紧张素释放的损失通过血管紧张素转化酶(ACE),从而放大炎症反应。c)中所得到的I型干扰素和炎性细胞因子和细胞毒性T细胞的作用的释放对于病毒临界
肺上皮细胞和病毒复制的感染
流感病毒是负性RNA病毒;因此,成功的病毒复制需要通过病毒RNA聚合酶从病毒基因组中产生感觉信使RNA [17]。病毒基因组包括总共11种蛋白质的(编码8个RNA节段表1)[17]。一个成熟的病毒粒子包含八种这样的蛋白质,它们被一个蛋白质包膜所包围,包膜包括两种病毒抗原决定因子,血凝素(HA)和神经氨酸酶(NA) [6,28,32,51-55]。HA蛋白与表达在气道或肺泡上皮上的唾液酸残基结合,引发病毒粒子的内吞作用[56]。核内体酸化导致病毒HA与核内体膜融合,激活M2离子通道,使质子进入病毒核内,解离核蛋白复合物,然后将其导入病毒复制发生的细胞核内[57]。病毒的组装、出芽和切断是通过细胞膜上的脂筏进行协调的[17]。断裂后,在新形成的病毒体的HA结合到细胞表面上的唾液酸受体。这些链路由NA裂解,释放出病毒后代,然后感染其它细胞或叶的各个通过气雾呼吸道分泌物滴[17]。金刚烷胺和金刚乙胺目标病毒的M2通道,但几乎是普遍的抵抗这些药物现在排除其使用[58]。目前可用于治疗IAV感染的药物,包括奥司他韦和扎那米韦,可抑制病毒NA [58]。因此,它们是最有效的在免疫功能低下患者感染的和的早期阶段限制病毒复制,并且一旦抗病毒先天免疫应答被建立是不太有效的[59,60]。
季节性IAV病毒在冬季的几个月里引起感染(十二月至四月北半球和六月至九月在南半球),在湿度较低的水平建议,以促进病毒传播[61-63]。每年,IAV具有不同的抗原性菌株由于HA和NA基因(抗原性漂移)循环突变在北半球。新颖,重配株IAV被认为从持久的病毒储库的区域出现,其中病毒发病率少季节性和人类和其他物种窝藏不同IAV菌株(主要是家禽和猪)之间的相互作用是比较常见的。在这种情况下,分段的病毒基因组提供的遗传多样性的连续源;当单个细胞是通过两种病毒株感染,基因组片段被容易地互换,以创建不同的菌株(抗原性转变)55,62,63]。引入新的IAV亚型从先前流行株进入人群体中的结果在大流行波的连续不同。从流行病季节IAV中表现出较高的传递率和死亡率的一个更高的速率不同,尤其是谁缺乏免疫力相似历史流行株[年轻患者8-10,14,64-69]。例如,1918年的甲型H1N1流感起源于禽流感IAV和全世界造成大约4000名万人死亡[55,62,64]。导致1957年H2N2和H3N2 1968年流感大流行[出现类似重组事件70],和禽类,猪和人类病毒之间的多个重新花色品种导致2009 H1N1流感菌株66,70]。自1997年以来,人类反复感染与禽类病毒(亚型H5N1,H7N7,H9N2,H7N2和H7N9)和高死亡率提出了有关高致病性禽流感病毒跨越物种屏障,并获得流行潜力[关注69,71]。
感染了2009年H1N1病毒的患者仔细的临床和病理研究揭示重要的见解[14]。虽然病毒复制在最大症状的时间通常达到顶峰,之后下降,病毒的检测延长部分患者有轻微的疾病持续了几天。在患者出现呼吸衰竭,感染后的部分患者周上,下呼吸道检测到病毒。尸检研究表明,严重感染流感损害呼吸道和肺泡上皮细胞造成细菌并发肺炎弥漫性肺泡损伤,最常见的是肺炎链球菌和金黄色葡萄球菌,患者[一个显著的少数(26-38%)14]。
病毒-宿主界面的分子和细胞相互作用
在IAV靶向的上部,并通过HA的任2,3-或结合降低呼吸道2,6-连接的唾液酸的上皮细胞[4,52,72,73]。季节性,以及大流行,菌株显示出的特异性对于在人类气管显着表达2,6-连接的唾液酸,而禽类病毒优先结合到在II型肺泡细胞中表达的2,3-连接的唾液酸[4,五,74]。不同的病毒唾液酸特异性已经提出来解释为什么有些病毒似乎比其他人[更具杀伤力五,73,75]。
胞质中病毒RNA的存在激活了细胞内三种主要的免疫通路,启动了对病毒的先天免疫应答:维甲酸诱导的基因-1 (RIG-1)蛋白,toll样受体(TLRs);主要是TLR3和TLR7以及炎性小体(图。2A)[76]。绑定的病毒RNA解旋酶域RIG-1引发其与线粒体有关抗病毒信号蛋白(小牛),诱导产生的I型和III干扰素(IFN-α/β和-λ)和激活炎性转录因子核转录因子(NF) -κB [77]。此外,病毒RNA作用通过在上皮细胞和通过nucleotide-binding oligomerisation domain-containing蛋白质像receptor-3 inflammasome髓细胞激活,导致释放IL-1β和地震76,78,79]。干扰素通过受体广泛表达于骨髓和感染肺上皮细胞增加数百IFN-regulated基因的转录和释放,而激活inflammasome和NF-κB诱导释放促炎细胞因子和趋化因子76]。所有这些反应的促进病毒清除;然而,他们也可能会导致组织损伤[80-82]。
受感染的上皮细胞后,组织驻留肺泡巨噬细胞是第一反应对病毒感染的肺(图。2B)。它们可以通过吞噬集落调理的病毒颗粒或受感染的凋亡细胞(胞吐),并释放大量的炎性细胞因子和趋化因子来启动和驱动免疫反应,从而促进病毒清除[83-86]。在猪中,IAV感染前肺泡巨噬细胞的耗竭导致病毒载量增加,I型IFN的产生减少,发病率和死亡率增加[87,88]。I型IFN的主要来源,驻留肺泡巨噬细胞也可刺激记忆CD8+与t细胞受体无关的t细胞[89]。值得注意的是,病毒诱导灭杀[90]或居民肺泡巨噬细胞的位点特异性抑制可以促进疾病的严重程度。有证据表明,组织居民巨噬细胞的抗病毒能力,可以增强;例如,通过CD200R,具有胶原结构(MARCO)的巨噬细胞受体的缺失或泛素 - 蛋白质编辑肿瘤坏死因子(TNF)-α诱导IAV感染,前蛋白3,其导致更快的病毒清除和更好的结果[91-93]。
促炎性细胞因子的释放诱导单核细胞循环的前体到肺和它们分化成单核细胞衍生肺泡巨噬细胞和树突细胞(DC),包括TNF /诱导型一氧化氮合酶(iNOS)产生的DC的募集。单核细胞衍生肺泡巨噬细胞从组织驻留不同肺泡巨噬细胞中,前者释放更高水平的促炎性细胞因子通常与经典的活化或“M1”偏振,包括TNF-α和iNOS,这促进IAV相关肺泡损伤[相关联的94-98]。通过删除CCR2或它的配体预防这些巨噬细胞的募集到肺,例如,减少IAV感染的严重程度,而不影响病毒清除[99-102]。因此,针对这些巨噬细胞疗法可能会感兴趣。例如,吸鼠肺的以定殖金黄色葡萄球菌影响单核细胞来源的肺泡巨噬细胞的极化并减弱IAV感染,提示一种以前未被描述的机制,通过该机制,气道微生物群可以保护免受流感介导的致命炎症的影响[103]。
在感染过程中,病毒蛋白激活固有凋亡通路,炎症细胞因子激活外在凋亡通路,导致气道和肺泡上皮细胞凋亡,有时甚至坏死,这是iav诱导的ARDS的典型特征(图。2C)[104-106]。例如,响应于IAV,促凋亡细胞因子肿瘤坏死因子相关凋亡诱导配体(TRAIL)对小鼠和支气管肺泡灌洗的巨噬细胞单核细胞衍生肺泡巨噬细胞,强烈表达从患者大流行H1N1流感诱导ARDS [107]。TRAIL可以通过与死亡受体5,该高度在肺上皮在基线表示并由I型IFN在病毒感染期间上调的相互作用直接诱导的肺泡上皮细胞凋亡[107,108]。防止trail诱导的细胞凋亡的策略在不影响病毒载量的情况下减轻小鼠IAV肺炎的严重程度[107,108],而那些促进它恶化损伤[109]。
DCs是肺内对IAV感染的先天免疫应答的另一个关键组成部分[110]。不同的DCs亚群存在于肺和气道中,并对IAV感染作出反应。的CD103+DC的子集(主要组织相容性复合体II类嗨表面CD11c嗨CD103+起着特别重要的作用。这些细胞存在于肺上皮细胞中,并从肺上皮细胞向气道管腔延伸;在这里,它们遇到病毒颗粒或被病毒感染的细胞的残余。在炎症细胞因子从肺上皮细胞和炎症细胞释放的情况下,如。那些由炎性(IL-1β和IL-18)或粒细胞 - 巨噬细胞集落刺激因子产生(GM-CSF)[110-113],它们被诱导迁移至引流淋巴结。在淋巴结,CD103+DCs是激活幼稚CD8的有效的抗原提呈细胞+和CD4+T细胞和用于适应性免疫所需的病毒抗原病毒特异性罕见记忆T细胞的呈现[114,115]。
幼稚CD8的膨胀+和CD4+病毒特异性记忆t细胞是IAV感染适应性免疫应答的关键。抗原CD8+t细胞诱导感染iav的细胞裂解通过在抗原作用下释放细胞毒性颗粒,并与单核细胞来源的肺泡巨噬细胞共同诱导细胞死亡通过外在凋亡途径通过释放TNF-α或TRAIL [116,117]。被激活的t细胞也会分泌一系列促炎细胞因子(如。TNF-αCCL3和CCL5),但这些细胞因子在病毒性间隙的作用和/或诱导肺损伤是不清楚118]。有趣的是,大量证据表明效应t细胞的细胞溶解活性和细胞因子功能受到感染iav的肺部炎症环境中存在的因素的影响[119-122]。这些相互作用的复杂性在发现hHigh mobility group protein B1 (HMGB1)(从受感染的上皮细胞释放的损伤相关分子模式(DAMP)分子促进IAV抗原特异性CD8的dc依赖性激活时得到了强调+T-效应细胞通过与RAGE(晚期糖基化终产物受体)的相互作用[123]。
新出现的证据强调了内皮组织对IAV感染免疫反应的重要性。例如,在感染过程中,内皮细胞上的sphingosine-1磷酸受体的上调需要协调炎症细胞进入和排出损伤的肺[18,124]。此外,肺部内皮是血管紧张素转化酶(ACE)生产的主要位点之一。ACE2,ACE的密切同系物,用作血管紧张素系统的负调节物,并防止IAV诱导ARDS [125,126]。凝血和纤溶级联的成分也与促进iav诱导的肺损伤有关[127,128]。在该领域的新出现的概念是来自宿主的分子模式或DAMP,如HMGB1或氧化磷脂,驱动肺损伤通过IAV感染时TLR4通路的激活[80,129]。最后,低亲合力,非保护性抗体,并与肺中的内皮细胞的补体激活免疫复合物沉积在一起的高滴度的存在是与肺损伤的严重程度在感染了2009大流行的H1N1 IAV [患者有关130]。
病毒清除与免疫介导的肺损伤
在死于IAV感染的患者中,事后剖析对肺的检查几乎总是发现弥漫性肺泡疾病,但病毒RNA只存在于一小部分患者中[14]。这些结果和发表的关于动物IAV感染的研究结果表明,IAV感染的死亡率可能是由于过度的免疫反应或病毒清除功能受损造成的[76,131]。对中性粒细胞在IAV感染中的作用的研究提供了一个说明性的例子。利用一种优雅的系统生物学方法,研究人员发现,炎症信号网络的过度激活将小鼠的致死和亚致死感染区分开来,而预测致命性的转录特征在很大程度上可归因于中性粒细胞[131]。一些研究发现,中断CXCL2或CXCL10策略IAV感染过程中涉及驱动中性粒细胞减少肺损伤的前馈电路[131-134]。尽管这样,前IAV感染中性粒细胞的完全耗尽被与病毒清除的失败和恶化肺损伤IAV感染后相关联,这表明嗜中性粒细胞在肺中的病毒多细胞协调响应中发挥作用[135]。与这些研究结果相一致,中性粒细胞减少被认为是在造血干细胞移植受者的队列[流感相关死亡的独立危险因素136]。
肺损伤的解决和肺泡再生
NA和HA表面的中和抗体的诱导与感染性病毒的清除有关,对于防止同一IAV株的再次感染是必要的[137]。然而,即使没有交叉反应中和抗体,CD8+保守的流感表位特异性t细胞可能足以介导对人类严重流感的交叉保护[138]。病毒清除与急性炎症的解决有关(图。2C)。这一过程是通过多种机制介导的,越来越多的证据表明,不同的t细胞群都参与了这一过程。CD8+T细胞IAV感染来衰减和解决炎症[期间产生抗炎IL-10139]。活化的巨噬细胞表达共刺激分子CD86,促进FOXP3的扩张+调节性T细胞(Treg)抑制嗜中性粒细胞驱动的细胞因子释放[140]。突出这些细胞的重要性,调节性T细胞的过继转移到免疫缺陷小鼠控制IAV感染期间由先天免疫细胞所介导的其他致命炎症[141]。所述I型干扰素可以抑制T辅助17应答的激活和中性粒细胞的募集减少至肺。从活化的T细胞释放的IFN-γ抑制清道夫受体的MARCO肺泡巨噬细胞的表达[142]。虽然所有这些方法的限制的免疫应答,他们来以提高的敏感性为代价继发性细菌感染,特别是革兰氏阳性生物体。事实上,从1918年和2009年流感大流行尸检标本进行回顾性研究表明,相当多的患者比例由细菌感染该病毒的清除成功后死亡[14,143]。
流感病毒感染导致呼吸道上下大面积基底膜剥落,肺的微结构丧失,形成微肺和大肺不张。因此,为了恢复气体交换和防止继发性微生物感染,需要一个强健的再生反应,这必须包括炎症的终止、基质沉积、祖细胞增殖和肺泡-毛细血管屏障的重建。最近的一些研究强调了先天淋巴样细胞在粘膜表面维持和再生中的重要性。淋巴组织诱导细胞,参与淋巴组织的发育,先天淋巴细胞分泌IL-22,这是一种组织保护细胞因子,诱导IAV感染后对肺再生很重要的基因的表达[144-147]。此外,IL-22可以刺激肺上皮细胞增加抗菌基因,如脂质运载蛋白2,其可以是用于保护从继发性细菌性肺炎的重要[145,148],增加b细胞淋巴瘤(B-cell lymphoma, Bcl)2和Bcl-2l1等抗凋亡蛋白编码基因的表达[149]。先天淋巴也需要细胞IL-33的释放,其诱导双调蛋白的分泌,表皮生长因子(EGF)家族的成员,对于维持上皮完整性和正确的道重塑[是必不可少150]。值得注意的是,双调蛋白的重组小鼠施用共感染IAV和细菌显著改善肺上皮再生和存活[151]。最后,调节性T细胞被发现直接驱动以下的内毒素诱导的肺损伤,促进肺修复皮祖细胞增殖;然而,它不知道他们是否IAV感染后发挥类似的作用[152]。这些发现非常重要,因为他们可能会建议治疗,可以促进重症患者IAV引起的肺损伤组织的再生病毒清除达到后。
m2极化的巨噬细胞与急性肺炎症的组织修复有关[153]。然而,在呼吸系统病毒性疾病相似的作用的实验证据是有限的。单核细胞衍生肺泡巨噬细胞中发现分泌肝细胞生长因子(HGF),一种有效的肺上皮细胞促分裂原,从而诱发II型肺泡上皮细胞的增殖在小鼠IAV感染模型[154,155]。组织驻留肺泡巨噬细胞促进内毒素诱导的肺损伤后II型肺泡上皮细胞的再生通过需要TNF-α和GM-CSF,对于肺上皮另一个增殖和抗凋亡因子的通路156,157]。有证据表明这同一途径IAV感染的分辨率期间有效[113]。
IAV感染后广泛损伤的气道和肺泡上皮修复的机制尚不完全清楚。一个或多个气道和肺泡祖细胞的增殖可替代受损或剥落的上皮细胞;气道或上皮间隙内的部分分化细胞,可根据周围间质提供的环境线索进行自我更新和分化[20]。这些细胞包括表达p63和角蛋白5的气道基底细胞群、包括itgb4在内的远端气道球杆细胞亚群+CD24低在支气管肺泡导管连接处的支气管肺泡干细胞的数量。在肺泡内,itgb4+细胞,“双潜能” I型和II肺泡上皮细胞祖细胞和肺泡II型细胞修复过程中已被归因干细胞/祖细胞功能[158,159]。尽管所有这些人都被报道肺损伤的不同型号的扩大,P63阳性和角蛋白5阳性上皮荚肺泡腔的出现只被严重IAV引起的肺损伤后观察到160,161]。无论这是伴随着其他祖池膨胀或是否响应于病毒感染的更远端的祖细胞群体直接或免疫介导的损伤必要呼吸道干细胞库的膨胀是未知的。参与这些反应可溶性生长因子包括,除其他外,成纤维细胞生长因子,EGFs,HGFS,和转化生长因子β[158],其中一些在IAV感染被诱导[150,154,162,163]。我们自己的数据显示,一ITGB4+在iav诱导的小鼠肺损伤后,祖细胞群对支气管和肺泡的修复至关重要,这一过程包括与驻留间充质生态位细胞、细胞外基质层蛋白和FGF10的交互作用(S. Herold和G.R.S. Budinger;未发表的观察)。
治疗
For patients who present with <4 days of fever, myalgia, headache, fatigue, dry cough, sore throat and rhinorrhoea during the influenza season, and in patients who require hospitalisation for respiratory symptoms during the influenza season, the use of rapid diagnostic tests may help to guide therapy [14,164]。最常见的是流感快速诊断试验,这是一种免疫分析方法,用于确定呼吸道标本中是否存在甲型或乙型流感病毒核蛋白抗原。快速流感诊断测试的结果约为15分钟,但敏感性和特异性有限。IAV或B型流感病毒RNA的快速反转录PCR检测是在鼻咽拭子或其他呼吸道样本上进行的,可区分不同的流感毒株,具有高度特异性(>90%),但相对不敏感(40-70%)[14]。病毒培养可用于诊断不确定需要额外检测或怀疑有新流感毒株的患者。对于症状出现后尽早使用NA抑制剂治疗:症状出现后48小时内出现确诊或疑似IAV的患者;高危或住院患者,包括2岁以下儿童和65岁的成人>;慢性病患者、免疫抑制、妊娠;及疗养院居民[14,58]。治疗严重IAV与ARDS包括使用更高的剂量,静脉NA抑制剂和积极的支持性护理。有几个小组报道了使用体外膜氧合来支持因IAV引起的严重低氧性呼吸衰竭患者的良好临床结果[165]。
高危人群
季节性IAV感染导致老年人不成比例的死亡。例如,与18-49岁的人群相比,儿童因IAV感染导致的呼吸衰竭发生率较低,而65-74岁的患者则高出20倍[15]。相比之下,大流行IAV往往会导致年轻的人不相称的死亡率[8,9,14,65,69]。这被认为是从由曝光赋予在老年个体历史流行株部分免疫引起的。在流感大流行造成2009年H1N1病毒,哮喘或慢性阻塞性肺疾病的严重长期加重了患者报告了14-15%,在一项研究中,儿童的29%,与IAV住院的成年人27%有一位前哮喘的诊断[9,14]。事后对2009年H1N1流感大流行期间收集的数据的分析也表明,肥胖是导致呼吸衰竭和死亡的独立危险因素[10,166,167]。怀孕是不良后果的另一个危险因素,在孕晚期的风险最高。在1918年,1957年和2009年的流感大流行,妊娠与呼吸衰竭而死亡的风险大约五倍以上的人口作为一个整体较高,怀孕也是季节性IAV感染后预后不良的危险因素[168]。目前还不清楚这是由于免疫系统的变化,还是怀孕期间心血管和肺部的变化增加了急性肺损伤的可能性。据报告,在2009年H1N1流感大流行期间,免疫抑制患者表现出较长时间的病毒脱落,并且出现较差临床结果的风险增加[14]。患者轻微此流行病表明富集住院期间,由于甲型H1N1流感病毒感染IFITM3(干扰素诱导的跨膜蛋白3)等位基因由于单核苷酸多态性改变了IFITM3蛋白的功能,强调遗传易感性可能导致严重的iav相关疾病[169]。
新的治疗策略
M2通道抑制剂(金刚乙胺和金刚烷胺)不再推荐用于治疗流感由于电阻的广泛出现(> 99菌株的%)和其针对流感B.缺乏这种功效的叶NA抑制剂(扎那米韦,奥司他韦,拉尼米韦和帕拉米韦)作为唯一的目前推荐的疗法为IAV感染[57,170,171]。不幸的是,奥司他韦抗病毒的报告,在最近几年迅速增加[172,173]。虽然一些研究人员质疑奥司他韦对非复杂的IAV和B型流感病毒感染的临床益处[174,175],多数研究在病情严重的患者建议改善临床结果,即使治疗的感染相对较晚给予[59,60],而治疗严重室内空气质素感染或乙型流感病毒感染的病人,建议采用较高剂量的肠外治疗[176]。
病毒复制机器是流感抗病毒药物特定的开发有吸引力的目标。的大化合物文库筛选确定了几个小分子的病毒聚合酶复合物[目标成分177]。法匹拉韦(T-705;www.clinicaltrials.gov标识符NCT01068912),核苷抑制剂PB1的有效块中的RNA合成的活性,可能是最先进的化合物迄今为止,目前在III期临床试验[178,179]。另一种小分子,DAS181,是一种唾液酸酶融合蛋白,吸入时可裂解肺上皮上的唾液酸,使其不易被病毒感染。在小鼠模型和II期临床试验中,DAS181可有效降低病毒载量[180,181]。avi7100的临床试验,这是一种设计用来干扰M1和M2基因表达的磷酸二氨基吗啉低聚物(www.clinicaltrials.gov标识符NCT01747148),以及flufirvitide,抑制剂结合至HA和抑制融合的肽(www.clinicaltrials.gov标识符NCT01990846),目前正在进行(表1)。
多家代理与潜在的免疫调节作用,包括免疫球蛋白,NgydF4y2Ba乙酰半胱氨酸,大环内酯类,过氧化物酶体增殖物激活受体激动剂,塞来考昔和美沙拉嗪,已经被建议用于临床使用[182],但只有少数人达到了临床试验。他汀类药物被其免疫调节和抗炎作用显示出调节宿主免疫和首先建议作为一个潜在的治疗策略来降低IAV诱导的炎症在2005年[183]。然而,罗苏伐他汀治疗没有IAV感染的小鼠模型和他汀类药物治疗的患者ARDS继发于败血症最近多中心试验后改善结果产生的负的结果[184,185]。
流感病毒复制关键取决于细胞NF-κB活动(186)和NF-κB是一个至关重要的促炎症信号模块,暗示策略来抑制NF-κB通路可能适合干预。气管内的应用程序NF-κB抑制剂乙酰水杨酸的致命感染小鼠显著提高生存,因为它的抗病毒和额外的抗炎作用[187]。这些数据,为基础的乙酰水杨酸衍生的NF-κB抑制化合物目前正处于II期临床试验用于严重流感(使用www.clinicaltrialsregister.eu/ctr-search/trial/2012-004072-19/DE)。在相关的方法中,蜂窝的Raf / MEK / ERK级联,这是众所周知的的小分子抑制剂有效地支持病毒复制和居间促炎性事件,IAV感染的小鼠胙强的抗病毒效果,并在相我正在评估到相对于III其他适应症的临床试验[186,188]。最后,GM-CSF,抗病毒宿主防御的重要介质,促进肺泡上皮细胞修复因子[113,156],已施用通过吸入中度至重度肺炎相关ARDS患者(包括IAV感染患者),结果支持未来的临床试验[189]。
疫苗接种
接种IAV/ B型流感病毒疫苗是限制流感对公共卫生影响的关键。世界卫生组织的研究人员每年都会更新流感疫苗,他们与美国和欧洲的合作伙伴一起工作,以确定在接下来的季节中最有可能导致感染的人群中流行病毒的变种[190]。大多数疫苗是灭活流感疫苗,其中含有两种IAV和一种或两种B型流感病毒株的三(三价)或四(四价)抗原,并通过肌肉注射;一种三价减毒活疫苗被批准用于儿童并经鼻给药[191]。四价疫苗很可能在未来被广泛采用。虽然具体建议因国家而异,但大多数机构建议为大多数(≥85%)人口接种流感疫苗,特别是对正在或计划怀孕的妇女。例如,美国疾病控制和预防中心建议所有6个月大的婴儿接种疫苗。对于未获批准接种疫苗的6个月以下婴儿,可由其母亲接种疫苗给予保护[191,192]。Ťhe morbidity associated with influenza is probably further reduced by the administration of pneumococcal vaccine to all children aged <5 years, older individuals (>65 years of age) and younger individuals with immunocompromising conditions [191]。
研究挑战
目前的疫苗接种计划的成功和在地平线上的亮点都在前人研究的成功,需要进行更多的研究流感病毒感染的病理生理的新疗法的阵列,然而,显著挑战依然存在。研究调查流感毒力的遗传基础产生了有力的公开辩论中,科学界一直认为,对诊断,疫苗和治疗进展的信息广泛传播的公共健康收益大于感知的关注生物恐怖[193]。由于人类(以及一些猪和鸟的变种)是唯一的IAV自然宿主,使用老鼠模型进行研究代表了另一个重要的挑战。虽然他们不能完全概括人类疾病,小鼠模型已经允许研究人员使用遗传策略来阐明IAV反应的关键途径在活的有机体内,其中许多已在先前已被描述过[76]。改进这些模型,例如,通过使用具有完全人源免疫系统的小鼠,可协助调查的诊所翻译[194]。Finally, the time between research discoveries in the laboratory and the development of therapies remains fixed at 15–20 years [195]。为了对抗像IAV这样迅速进化的病原体,我们需要找到更快的机制,将最近发现的策略(包括本文中描述的许多策略)应用到患者的护理中。
结论
该IAV相关肺损伤的结果是由病毒和宿主因素来确定,表明活性的最佳范围为对病毒感染的免疫应答是越来越明显。IAV感染的病理生物学的增强的理解表明,新疗法靶向与常规的抗病毒疗法组合主机可能是有益的。这样的治疗策略可以与病毒复制所需的宿主信号通路干扰,抑制夸张炎症,或促进组织再生,以努力以抑制器官功能障碍和损伤[196]。战略,限制的免疫应答,例如,通过用氧化的磷脂抑制TLR4的激活[80,197],靶向S1P受体或血管紧张素/ ACE系统[124,126,197,198]或甚至减少I型干扰素的产生[107],已经显示出减少在鼠模型IAV诱导的死亡率的严重程度。同样,促进免疫分辨率或组织再生的策略,如。T细胞共刺激因子,resolvins的,脂氧素,所述CD200受体的抑制剂和免疫调节抗生素或格列酮类的抑制剂[93,99,199-201可能加速严重疾病患者的再生。还需要进一步的研究,以确定在感染过程中可以特异性靶向的细胞和通路,并开发临床有用的生物标志物,以确定哪些患者可以使用这些靶向治疗最有效。
确认
作者要感谢杰奎琳·谢弗创造了这些人物。
脚注
支持声明:S. Herold获得了德国研究基金会(SFB1021 C05, SFB-TR84 B2)和德国联邦研究与教育部(FluResearchNet grant 01 KI 1006M)的资助。G.R.S. Budinger和K.M. Ridge分别获得了美国国立卫生研究院(HL71643、ES015024、ES013995、HL092963和HL71643、HL124664)的资助。德国肺脏研究中心(DZL)和退伍军人管理局也为这项研究提供了资金。本文的资助信息已存入FundRef。
利益冲突:无申报。
- 收到2014年10月7日。
- 公认2015年1月7日。
- 版权所有©ERS 2015年
参考
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵
- ↵