摘要
乙酰胆碱与毒蕈碱受体结合,在哮喘的病理生理学中起关键作用,导致支气管收缩、粘液分泌增加、炎症和气道重塑。抗胆碱能药物是用于治疗慢性阻塞性肺疾病和哮喘的毒蕈碱受体拮抗剂。最近在活的有机体内和在体外我们的乙酰胆碱如何有助于理解数据增加哮喘的疾病表现,以及阐明抗胆碱能药物的作用机制。该审查评估对哮喘的病理生理学乙酰胆碱的最新文献,在其气道炎症和重塑作用一探究竟。新的洞察到抗胆碱能药物的作用机制,其对气道重塑,和功效的审查,并在治疗哮喘的长效抗胆碱能药物的安全性影响也将被覆盖,包括最新临床试验数据的汇总。
摘要
临床前研究表明,抗胆碱能药物可以减轻乙酰胆碱诱导的气道炎症和重塑http://ow.ly/xqAQ30loP8F
介绍
乙酰胆碱是气道中主要的副交感神经递质[1],和起着阻塞性气道疾病,如哮喘的病理生理学中起关键作用,通过支气管平滑肌收缩和粘液分泌[2]。临床前的证据支持在气道炎症和重塑[附加作用3.]。乙酰胆碱与毒蕈碱受体结合[2,3.,使这些受体成为治疗呼吸道疾病(如哮喘)的一个有吸引力的靶点。
抗胆碱能药已经用于治疗了好几年的慢性阻塞性肺疾病(COPD),现在作为附加治疗哮喘毒蕈碱受体拮抗剂。在这次审查中,我们在哮喘的病理生理上的乙酰胆碱评估最新的文学,包括它的气道炎症和重塑的作用。我们也回顾了新的见解抗胆碱能药物及其对气道重塑影响的作用机制。疗效和治疗哮喘的长效抗胆碱能药物的安全性的比较也将包括在内,与最新的临床试验数据的汇总。
乙酰胆碱在哮喘病理生理中的作用
哮喘患者乙酰胆碱信号传导增强
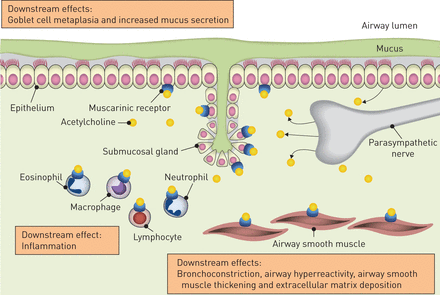
研究表明,通过乙酰胆碱信号传导,副交感神经活动在哮喘的病理生理学中增加[2,3.]。乙酰胆碱从气道神经元和非神经元细胞释放,如气道上皮细胞[4]。其它非神经元来源包括炎症细胞[2]。乙酰胆碱与呼吸道毒蕈碱受体触发平滑肌收缩和粘液分泌(图1) [2,3.]。有五种属于G-蛋白偶联受体家族识别毒蕈碱受体[5];然而,只有米1,米2和M3.受体已显示在气道生理学中发挥重要作用,并且在疾病,如哮喘和慢性阻塞性肺病[5]。米1受体由上皮细胞和神经节表达;它们分别调节电解质和水的分泌,并帮助副交感神经传递[6]。米2受体在气道平滑肌和副交感神经细胞中表达;它们对气道平滑肌的收缩作用非常有限。然而,米2受体作为副交感神经神经元的自身受体,限制乙酰胆碱的释放,从而限制迷走神经反射引起的支气管收缩和粘液分泌[2,7]。米3.受体是支气管平滑肌收缩的主要受体亚型,存在于气道平滑肌和粘膜下腺[2,5,8]。
乙酰胆碱在哮喘的病理生理作用的总结。乙酰胆碱是在呼吸道的主要副交感神经的神经递质。它是由气道的神经元和非神经元细胞,诸如气道上皮细胞,以及毒蕈碱结合解除1,米2和M3.受体。这些受体对气道上皮细胞,平滑肌细胞和粘膜下腺体发现。乙酰胆碱的结合毒蕈碱受体触发哮喘的病理生理学相关的下游效应的主机。
几种机制占哮喘气道增加神经活动[2]。建立机制包括上皮屏障功能的损失,由于炎症局部组织微环境,其暴露了神经元向气道内腔[2]。炎症介质,甚至是气道神经与嗜酸性粒细胞的直接接触,都可以激活暴露的神经元,从而触发迷走反射介导的支气管收缩[9]。这种支气管收缩因M2受体;这导致乙酰胆碱释放增加,导致气道高反应性[5]。米2在接触过敏原、臭氧和病毒感染后气道疾病的动物模型研究中发现了受体功能障碍[10个]。为了支持在哮喘方面的作用,M2毛果芸香碱激动剂从反射性支气管收缩保护正常受试者,但不是在那些患有哮喘[11个]。米2受体功能障碍被认为是由嗜酸性粒细胞和主要碱性蛋白的分泌引起的[10个,德意志北方银行]。此外,肿瘤坏死因子α出现在推动并购中发挥了关键作用2臭氧和病毒诱导的气道高反应性动物模型的自身受体功能障碍[13个,14个]。乙酰胆碱信号在M上的增加1和M3.受体和M2如以下章节所述,受体功能障碍可能导致支气管收缩、粘液分泌、炎症和气道重构的增加。
这一研究领域的一个激动人心的新进展是神经元的可塑性和重塑,这可能支持哮喘胆碱能信号的持续变化。在哮喘组织重塑机制的研究中,气道神经元很少受到关注,但在炎症损伤(包括过敏原和嗜酸性炎症)的反应中,气道神经元似乎转向了胆碱能同型并过度分支[15个,16个]。有趣的是,最近的一项研究表明,这种神经可塑性可能是生命早期接触过敏原的特点,以下其中神经营养因子NT-4介导的神经重塑和持续气道高反应超出了接触过敏原的即时期[17岁]。鉴于这一编码神经营养因子,如脑源性神经营养因子的单核苷酸多态性(SNP)的基因,可以与哮喘和过敏性鼻炎[关联的观察光18岁的临床前研究,以调查这种反应的分子控制和研究特点的病理特征的神经元重构的哮喘患者显然是需要的。
乙酰胆碱信号通路增加的下游效应:机制和治疗意义
支气管狭窄
带来由增加的乙酰胆碱信号传导有助于支气管收缩增加的迷走神经活性;我n fact, the improvement in forced expiratory volume in 1 s (FEV1)在回应tiotropium相当相似诱导β2-激动剂沙美特罗在轻度至中度哮喘患者中的应用[19个]。这是有趣的,因为长效抗胆碱能块只有一个中介,而β2激动剂是收缩的功能性拮抗剂,而不管导致该效果的介体。在动物临床前研究观察表明,这可以通过使用胆碱能系统的炎性介质,并且即使这些不直接对毒蕈碱受体起作用的支气管来解释。例如,从结果在活的有机体内致敏豚鼠过敏原引起支气管高反应性的研究表明,迷走神经源性乙酰胆碱选择性地促进了组胺诱导的过敏原动物支气管收缩[20.]。血栓素一个2,是一种有效的气道收缩介质,在健康和发炎的气道中都依赖副交感神经信号[21]。血栓素A的结合2其受体被认为是大幅度增加乙酰胆碱的释放[21]。迷走神经活动的增加也被认为有助于早期哮喘反应和晚期哮喘反应(LAR)。临床前数据在活的有机体内模型表明过敏原激活气道感觉神经,至少部分地通过瞬时受体电位锚蛋白-1通道[22]。这引发了中枢反射事件,导致乙酰胆碱引起的支气管收缩,这可能是LAR [22]。这样,胆碱能反射弧促进支气管收缩到组胺,炎症介质和过敏原。
在急性过敏性哮喘豚鼠模型,噻托溴铵甚至逆转,并防止过敏原引起的气道高反应[23]。一项临床研究比较了吲哚特罗/替奥特罗和吲哚特罗(均联合吸入皮质类固醇(ICSs))对甘露醇诱导的气道反应性的影响,发现替奥特罗在吲哚特罗的基础上对甘露醇中位有效剂量没有额外的影响(ED)50) [24],而在哮喘患者中,二氧化硫诱导的气道高反应性受胆碱能控制[11个]。因此,尽管很明显,乙酰胆碱有助于哮喘支气管收缩,胆碱能反射弧的贡献(发展)在哮喘气道高反应并不广泛报道,需要进一步研究。
粘液分泌增多
乙酰胆碱诱发粘液分泌也是哮喘的一个重要特征。粘液腺由副交感神经和释放粘液响应于电场刺激神经支配[25]. 杯状细胞确实表达毒蕈碱受体,但需要相对高浓度的毒蕈碱激动剂来促进分泌活性[26]。一个有趣的新发现是,除了对气道炎症有任何影响外,毒蕈碱受体也可能控制杯状细胞的分化。反复的乙酰胆碱挑战可促进轻度哮喘患者气道上皮黏液阳性细胞的存在[27]。在空气 - 液体界面上培养的人呼吸道上皮细胞的研究中,噻托溴铵显示出减弱由白介素诱导的杯状细胞化生(IL)-13 [28]。此外,噻托溴铵逆转建立杯状细胞增生[28];有趣的是,无外源毒蕈碱受体激动剂加入到该系统中,指示由上皮细胞本身有助于杯状细胞分化产生的非神经元乙酰胆碱。在机制上,这是依赖于由IL-13,这是防止由于噻托溴铵调节粘液细胞分化的FOXA2和FoxA3转录因子的调节。Komiyaet al。(29发现抗胆碱能替托品对IL-13诱导的杯状细胞化生或黏液分泌无影响,而中性粒细胞弹性蛋白酶刺激黏液分泌减少。il -17诱导产生乙酰胆碱促进支气管上皮细胞系16-HBE粘液分泌[30.]。
体内数据表明,当敏化M3.受体缺陷小鼠暴露于变应原刺激后,杯状细胞比野生型小鼠低30%(p<0.05)[31]。他们还发现在产粘液基因显著低增长MUC5AC与野生型小鼠相比(35%;p < 0.05) (31]. 噻托溴铵对致敏豚鼠粘液腺肥大的防治作用[32],即还报道了在小鼠中房尘螨诱导的应答[裁断33]。小鼠反复暴露于胆碱能激动剂也可促进气道上皮内杯状细胞的存在[34]。
因此,虽然杯状细胞分化的气道上皮细胞确实受胆碱能控制,但其机制尚未完全建立。胆碱能受体是G问-偶联受体因此不被认为直接与STAT(信号传感器和转录激活因子)通路激活相结合,因此对IL-13、IL-17和中性粒细胞弹性蛋白酶信号的影响不太可能是通过直接调节该活性[2]。另一个有待探索的领域是哮喘患者的杯状细胞增生是否对抗胆碱能治疗敏感。
气道炎症
除了支气管收缩和粘液分泌外,乙酰胆碱也有助于气道炎症,尽管目前仅在临床前模型中有报道,在哮喘患者中尚待证实。在体外,乙酰胆碱信号通路可导致牛支气管上皮细胞(BECs)释放嗜酸性粒细胞的趋化活性,这种趋化活性依赖于剂量和时间[35]。有趣的是,嗜酸性粒细胞已被证明的围观谁已经死亡致死性哮喘的致敏豚鼠和人的气道神经[36]。其他数据表明,乙酰胆碱信令polarises树突细胞向T辅助细胞类型2(Th2)时概况[37]。用乙酰胆碱孵育树突状细胞可刺激产生两种趋化因子,将Th2细胞引入过敏性炎症部位(巨噬细胞来源的趋化因子、胸腺和激活调节的趋化因子)[37]。从机理,效果尚不完全清楚在这个阶段,但促炎转录因子NF-κB调节的蛋白质和激酶C(PKC)由毒蕈碱受体可以起到一定的作用[38]。
体内,抗胆碱能药通过抑制趋化因子的炎症细胞的释放和招募[降低乙酰胆碱诱导的炎症反应39]。阿地尼亚,长效抗胆碱能药,已被证明在减少两个幼稚和致敏小鼠都变应原诱导和醋甲胆碱诱导气道高反应[40]。使用阿昔单抗治疗后,由过敏原引起的嗜酸性粒细胞也显著减少(56±4%),表明其具有抗炎作用[40]。同样,tiotropium显示抗炎性质:在老鼠模型中电阻的呼吸,tiotropium被证明减弱的增加支气管肺泡灌洗中性粒细胞数,IL-1β和il - 6水平,和肺损伤评分(41]。在致敏小鼠中,噻托吡肟也显示出剂量依赖性地减少炎症反应[33]。致敏小鼠的另一项研究显示,在气道炎症噻托溴铵一显著减少[42]。此外,噻托溴铵还可降低慢性感染豚鼠的嗜酸性炎症,其程度与布地奈德相似[32在相同的模型中,替托品与环索内德协同作用以减少过敏原引起的炎症反应[43]。
一个有趣而新奇的发现是胆碱能神经可能释放最近发现的神经原蛋白U,它通过直接激活嗜酸性粒细胞和潜在的2型先天淋巴细胞参与th2型炎症[44- - - - - -46]. 鉴于上述神经可塑性在哮喘中的调节,这是一个令人兴奋的新进展,将胆碱能调节与气道炎症联系起来,需要后续研究以确定其在哮喘中的重要性。抗胆碱能药物的免疫调节作用可以通过减少气道炎症和黏液的产生来预防哮喘的恶化,事实上,据报道噻托溴铵在临床上可以减轻哮喘的恶化[33]。这是否是真正由于抗胆碱能药物抗炎活性是一个重大的悬而未决的问题仍然无人应答。
气道重塑
气道重塑涉及气道的结构改变,如杯状细胞化生、气道平滑肌增厚和细胞外基质沉积[28,47]。几个途径有助于重塑,包括生长因子,介体和细胞外基质蛋白中存在的气道壁[48]。此外,有证据表明胆碱能控制气道重塑的哮喘患者。例如,tiotropium减少气道壁维度与长效β相结合2激动剂(LABA)和ICS治疗哮喘患者的评估,定量CT [49]。此外,尘螨或甲基胆碱刺激哮喘患者反复支气管收缩,增加了黏液生成细胞的上皮染色百分比和气道重塑的上皮下标记的百分比。对照组未见这种变化,而沙丁胺醇治疗可逆转这一事实表明,支气管收缩可引起过多的粘液产生,从而导致进一步的气道阻塞[27]。有趣的是,嗜酸性炎症只在接受尘螨过敏原的患者中出现。这支持了这样一种观点,即仅乙酰胆碱诱导的支气管收缩就可以诱导气道重构[27]。
在体外动物模型研究表明,这些变化主要是由M3.受体,而这又是通过乙酰胆碱激活。在体外数据显示,来自毒蕈碱受体的下游信号会触发糖原合成酶激酶(GSK)-3抑制,GSK在其活性状态下,可抑制气道平滑肌增殖。这提示了气道重塑中平滑肌积聚的可能机制[50]。毒蕈碱受体控制组合收缩蛋白的积累与转化生长因子(TGF)-β,以及通过这种依赖gsk -3的机制[51],而出现的细胞外基质蛋白的产生通过毒蕈碱性受体和TGF-β的调节协同涉及中号2受体[52]。一个在体外豚鼠肺片的模型发现,醋甲胆碱诱导的支气管收缩导致收缩蛋白的表达,如平滑肌肌球蛋白。这是由生物活性TGF-β的释放介导的[53],被认为与气道重塑的几个特征有关,如肌成纤维细胞转化,增强胶原合成和沉积在基底膜下,增加平滑肌收缩蛋白的表达[47,54]。生物活性TGF-β的响应于乙酰甲胆碱的释放[55支持这些发现。进一步的证据表明,是乙酰胆碱介导的支气管收缩的机械效应导致气道重构[3.,56,57]。当与比较的BEC从志愿者无哮喘当受到压缩力从与哮喘的志愿者得到的BEC显示增加TGF-β和粒细胞 - 巨噬细胞集落刺激因子的分泌[47]。
体内数据显示,野生型老鼠增加了1.7倍的染色α-smooth肌肉肌动蛋白过敏原后挑战;这种增加在缺乏M的小鼠中完全不存在3.受体[31]。这项研究没有发现对M的任何刺激作用3.过敏性炎症的受体,提示乙酰胆碱诱导的重构可能独立于炎症[31]。
老鼠使用tiotropium敏感导致减少杯状细胞化生,气管平滑肌厚度和TGF-β水平,这表明一个角色的tiotropium减少气道重构和高反应性42]. 对致敏豚鼠噻托溴铵的研究进一步证实了这一点,噻托溴铵对气道平滑肌质量的抑制率小于75%[32]。噻托溴铵联合环索奈治疗豚鼠慢性哮喘模型,可使致敏原引起的气道平滑肌质量显著降低81% (p<0.05) [43]。
这些数据添加洞察支气管收缩的气道重塑中的作用。然而,最近的一项研究表明小鼠在杯状细胞增生和巨噬细胞存在乙酰甲胆碱诱发的变化,重复暴露,但不会影响气道反应性[34]。很显然,需要进一步研究更详细调查的假设,支气管收缩可以驱动气道炎症独立重塑。特别是,基本的机制需要进一步澄清解释在上述不同实验模型中相对多样化的功能和病理结果。
抗胆碱能类在哮喘
抗胆碱能在阻塞性呼吸系统疾病中的应用有着丰富的经验,因为多年来抗胆碱能已被批准用于慢性阻塞性肺病[58]。目前批准用于COPD用五年抗胆碱药:异丙托溴铵[59],aclidinium [60],格隆(也称为格隆溴铵)61],芜地[62]和噻托[63]。然而,只有两种抗胆碱能药物被批准用于哮喘:异丙托品和噻托品。Ipratropium是一种短效抗胆碱能被批准用于可逆的气道阻塞的治疗在急性和慢性哮喘与β相结合2受体激动剂(5,59],而噻托溴铵是唯一获准用于哮喘的长效抗胆碱能药物,作为ICS和LABA的附加治疗[63]。
抗胆碱能类的属性
抗胆碱能药物是M的可逆竞争性抑制剂1,米2和M3.受体[6,并已被证明对所有五种毒蕈碱受体亚型均有类似的结合亲和力[64]。在毒蕈碱受体花费的时间决定每种药物的作用的持续时间。例如,长效抗胆碱能药物表现出对M动力学选择性3.受体/ M2受体(表1),因为它们与M的解离较慢3.比M受体2受体[6,65,66]。在体外数据表明,阿地解离自M稍快2和M3.受体比噻托溴铵,但慢于异丙托溴铵和格隆(居住半衰期到M3.受体显示在表1) [65]。在S阿尔蒙et al。(67],利用表达人M1−米5受体亚型表明,在pK我因为umeclidinium是9.8(米1),9.8 (M2),10.2 (M3.),10.3 (M4)和9.9(M5). 乌梅属植物与M的分离3.受体比M受体慢2受体。本研究中噻托溴铵的半衰期均比乌米啶的半衰期长2受体(39.2与分别为9.4 min、tiotropium和umeclidinium)和M3.受体(272.8与82。2 min, tiotropium and umeclidinium, respectively) [67]。Casarosaet al。(65也有报道称,氧化钛与M的解离速度更慢3.比米2受体;然而,其半衰期分别为27小时和2.6小时。在这两项研究中观察到的半衰期的差异可能是由于这两项研究使用的方法不同造成的。
作用机制的比较:抗胆碱药,短效β2-激动剂和长效β2激动剂
抗胆碱能药物具有不同的作用机制与短效β比较2受体激动剂(SABAS)和的LABAs,其结合到气道β2- 受体来触发平滑肌松弛[69,70]. 然而,数据显示,抗胆碱药与β2β受体激动剂可以提高2-agonist-induced bronchodilation通过细胞内的过程(71]。结果表明,格列溴铵能通过降低钙离子浓度而增强肌肉收缩2 +通过PKC和钙激活钾(KCa)渠道71]。这表明,PKC和KCa抗胆碱能药物与β的相互作用可能与通道有关2受体激动剂。对阿昔丁铵和富马酸福莫特罗、格列罗溴铵和富马酸印卡特罗进行的评估研究表明,对人离体支气管的气道平滑肌松弛有增强作用[72,73]。LABA和抗胆碱能药组合疗法也可以减轻交感神经和副交感神经活动的每日变化。一个clinical study in patients with COPD showed that tiotropium was associated with sustained improvements in lung function throughout 24 h, without affecting circadian variability [74]。这些数据表明抗胆碱附加疗法和β双重的支气管扩张2-agonism具有比单一的支气管扩张一个更大的好处。此外,在延长沙丁胺醇的顶部的支气管扩张作用的作用持续时间异丙托铵联合治疗[75]。These and other considerations, such as the frequent use of ipratropium (4 puffs per day), have triggered studies into the role of long-acting anticholinergics in COPD and, more recently, in asthma.
短效抗胆碱能药在哮喘中的应用
异丙托品是一种非选择性的毒蕈碱受体拮抗剂[76),批准用于急性和慢性哮喘与β相结合2受体激动剂(5,59]. 它可以作为对β-受体不敏感的哮喘患者的替代缓解剂2受体激动剂(77]。然而,数据表明,它并不像SABAS有效;188名慢性支气管炎患者(N = 113)或哮喘(N = 75)的一项研究发现,哮喘患者更可能更好地响应沙丁胺醇比异丙托[78]。
哮喘的长效抗胆碱能药物的应用
Aclidinium
阿昔丁铵仅获准用于慢性阻塞性肺病[60]。在写这篇文章的时候,还没有注册的临床试验阿昔洛铵在哮喘,所以这种抗胆碱能将不会在这篇综述进一步讨论。
格隆
Glycopyrronium也只被允许用于慢性阻塞性肺病[61]但是有研究评估了它在哮喘中的应用。在轻中度哮喘患者中,吡咯烷酮对乙酰胆碱诱导的支气管收缩的保护作用明显强于安慰剂(p<0.002)[79]。Glycopyrronium每次吸入后可使支气管扩张30小时[79]。There are currently two clinical trials assessing glycopyrronium use in patients with asthma: one study is assessing the bronchodilator effects and safety of two doses of glycopyrronium (25 µg and 50 µg) in adults with asthma receiving ICS/LABA (ClinicalTrials.gov识别码NCT03137784;竣工日期:2017年12月);另一项研究是评估在ICS/LABA治疗无效的哮喘患者中使用三联疗法(glycopyrronium, indacaterol和mometasone furoate) (ClinicalTrials.gov识别码NCT03158311;预计完工日期:2019年6月)。
芜
芜地被批准用于慢性阻塞性肺病的使用,但没有被批准用于哮喘使用[62,80]。II期临床试验发现,在波谷FEV温和改善1未接受ICS治疗的哮喘患者使用单药乌米昔单抗治疗[81]。然而,这些改善与剂量无关,也不一致,这意味着这些数据并不能最终证明单药乌米昔单抗有治疗效果。另一项II期研究评估了几剂乌米西啶联合氟替卡松呋酯治疗有症状哮喘患者的剂量反应、疗效和安全性[82]。通过FEV有明显的改善1与单用糠酸氟替卡松(p=0.018)相比,联合治疗(最高剂量的溴化乌米克利丁)[82]。目前有两个正在进行的临床试验评估固定剂量芜,丙酸氟替卡松和维兰特罗的组合哮喘患者(ClinicalTrials.gov标识符NCT03184987和NCT02924688;预计竣工日期分别为2019年6月和2019年2月)。
Tiotropium
Tiotropium被批准用于COPD作为维持治疗,以及在成人、青少年和年龄≥6岁的儿童中作为ICS/LABA的附加治疗用于哮喘[63,83]。2017年2月,美国食品和药物管理局批准噻托吡肟用于≥6岁的哮喘儿童[83]。有一项广泛的临床试验计划评估噻托溴铵在成人、青少年和儿童哮喘患者中的使用情况。Tiotropium 5µg添加至少ICS和腊八治疗成人患者的哮喘症状控制不好导致多达154毫升的改进FEV峰值1(P <0.001),21%的减少风险,严重哮喘恶化(p值= 0.03)[84]。亚组分析还报告有严重的哮喘发作的风险降低,哮喘恶化,无论基线临床特征(性别,年龄,身体质量指数,病程,发病与吸烟状况的年龄)改进哮喘控制应答率[85]。一个pooled safety analysis of seven randomised, double-blind, placebo-controlled studies (both phase II and III) found that both 2.5 and 5 µg doses of tiotropium had comparable safety and tolerability with placebo; the frequencies of patients reporting any type of adverse effect were 57.1%与55.1%和60.8%与62.5%,分别[86]。几项针对青少年和儿童的研究也显示出肺功能的显著改善,其安全性与安慰剂相当[87- - - - - -91]。总体而言,这些数据表明,噻托溴铵是有效的,并且具有在一系列成人,青少年和儿童[哮喘严重程度的一个良好的安全性19个,84- - - - - -89,92,93]。
谁可以从长效抗胆碱能药物中受益?
对于那些在接受ICS/LABA联合治疗时仍有频繁症状和加重的患者,可选择的逐步治疗方案有限[94]。此外,还有经常使用β的安全问题2激动剂在一些患者,特别是那些在β的SNP2肾上腺素能受体基因ADRB2基因型[76,95]。一些患者可能会将ICSs与系统性副作用联系起来,尤其是儿童,如骨密度和生长速度降低[96]。长效抗胆碱能药物可作为一种适当的附加治疗,用于尽管有ICS和LABA治疗仍有症状或无法接受传统治疗的患者。在对症状性哮喘控制不佳的患者进行亚组分析时,tiotropium附加治疗的益处也表明,不论基线特征如何,大范围的患者都能从抗胆碱能药物中获益[85]。
结论
乙酰胆碱在哮喘的病理生理过程中起着重要的作用通过结合呼吸道毒蕈碱受体触发支气管收缩,粘液分泌和炎症,而临床前数据突显气道重塑胆碱能介导的支气管收缩的重要性。抗胆碱能药拮抗乙酰胆碱的副交感神经影响,因此提供了治疗益处通过补充ICS和LABA作用于哮喘的机制。临床资料显示,长效抗胆碱能药物耐受性良好,副作用少而轻微。广泛的临床试验数据,特别是在哮喘研究中,证明了临床疗效和治疗效益作为附加治疗症状哮喘跨越一系列年龄组和哮喘严重程度。
然而,未来的研究需要,以阐明哮喘的病理生理的胆碱能控制的更多细节。特别是,需要进一步调查的领域是哮喘发作及其气道高反应和重塑贡献神经元可塑性;在哮喘患者抗胆碱能药的抗炎作用;和机制,巩固气道炎症和重塑的胆碱能控制,特别是Th2型炎症和支气管收缩诱导的重塑。
致谢
今次检讨的部分项目,得到香港人文及健康研究中心Johan Karlberg的鼎力支持。通过他的电子出版物,临床试验放大镜周刊(www.clinicaltrialmagnifier.org). 编辑支持(以写作辅助、表格和图表组装、作者评论整理、语法编辑和引用等形式)由英国曼彻斯特的一家核心全球公司SciMentum的Parveena Laskar提供,由Boehringer Ingelheim资助。
脚注
利益冲突:R. Gosens报告了来自Boehringer Ingelheim、Chiesi、Aquilo和Novartis的资助,以及来自Boehringer Ingelheim在进行研究期间的编辑支持(以写作协助、组合表格和数字、整理作者评论、语法编辑和引用的形式)。
利益冲突:N. Gross报告在研究进行期间来自Boehringer Ingelheim的编辑支持(以写作协助、组合表格和数字、整理作者评论、语法编辑和引用的形式)。
- 收到2017年12月22日。
- 接受2018年8月9日。
- 版权所有©ERS 2018
本ERJ开放文章是开放访问,并根据知识共享署名非商188滚球软件业许可4.0条款分发。