抽象
Until 20 years ago the treatment of pulmonary arterial hypertension (PAH) was based on case reports and small series, and was largely ineffectual. As a deeper understanding of the pathogenesis and pathophysiology of PAH evolved over the subsequent two decades, coupled with epidemiological studies defining the clinical and demographic characteristics of the condition, a renewed interest in treatment development emerged through collaborations between international experts, industry and regulatory agencies. These efforts led to the performance of robust, high-quality clinical trials of novel therapies that targeted putative pathogenic pathways, leading to the approval of more than 10 novel therapies that have beneficially impacted both the quality and duration of life. However, our understanding of PAH remains incomplete and there is no cure. Accordingly, efforts are now focused on identifying novel pathogenic pathways that may be targeted, and applying more rigorous clinical trial designs to better define the efficacy of these new potential treatments and their role in the management scheme. This article, prepared by a Task Force comprised of expert clinicians, trialists and regulators, summarises the current state of the art, and provides insight into the opportunities and challenges for identifying and assessing the efficacy and safety of new treatments for this challenging condition.
抽象
肺动脉高压临床试验设计和新治疗方法的现状和研究前景http://ow.ly/VHQ030mfRxc
临床试验设计和治疗肺动脉高压电流状态
w ^ith advances in our understanding of the pathobiology of pulmonary hypertension (PH) over the past 20 years, more than 10 drugs have been developed and approved for the treatment of pulmonary arterial hypertension (PAH) and one for chronic thromboembolic PH (CTEPH). Initial clinical trials performed in newly diagnosed PAH and CTEPH were single agent, placebo controlled, of short duration, focused on changes in measures of exercise capacity and comprised of relatively small populations of patients. However, over the past 5 years, clinical trial designs testing novel therapies for PAH have evolved into much larger, placebo controlled, on background therapy and upfront combination therapy trials. In addition, event-driven studies examining the effect of sequential combination therapy on clinical worsening have forced the community to search for more clinically relevant, novel efficacy end-points and trial design. Here, we review the evolution of clinical trial end-points, report on new therapeutic targets, evaluate clinical trial design and propose goals for clinical investigation.
在PH的临床试验终点演进
6分钟步行试验
在6分钟步行测试(6MWT),次最大运动试验,已在PH疗法的临床试验中最常用的主要终点,与第一随机对照试验(RCT)为依前列醇的药品注册在1990 [开始1]。由于该初始研究中,大多数为新颖PAH或CTEPH疗法登记研究采用在上6MWT(Δ6MWD)实现距离短期变化作为主要结果(图1)2-13]。这些研究确定了Δ6MWD,导致监管部门批准在PH使用统计学显著差异,但这些变化的临床意义仍不太明确。多篇研究Δ6MWD和短期和长期的结果,如需要住院,肺移植,抢救治疗或死亡的开始,关系未能一贯表现出显著协会[14-18]。随后的研究中定义6MWD有关患者重要的结果,如生命健康相关的质量和预测临床恶化的临床相关的变化[17,19-21]。然而,Δ6MWD的如在临床试验中一个主要结果测量的效用是有限的,特别是在涉及顺序更现代的试验中,添加治疗。这种变化是小于描述的临床相关的阈值,尽管其他的临床结果所取得的意义[7-10,22,23]。
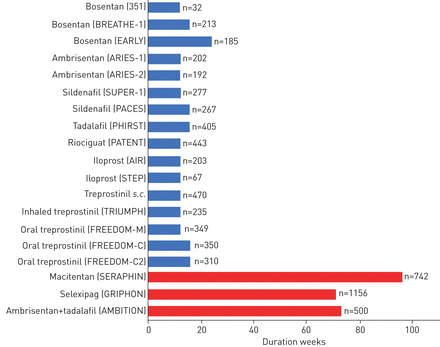
目前批准的肺动脉高压治疗的主要注册研究(随机对照试验(rct))持续时间。蓝条:以6分钟步行距离变化作为主要结果测量的随机对照试验;红色条形图:发病率和死亡率的随机对照试验。
进化到综合结果终点
为了解决一些6MWT的限制如在临床试验中一个主要结果测量和在并入复合终点反射时间临床恶化(TTCW)2000年代中期,探索新的端点,注册研究[6,7]。在临床恶化的风险降低在这些研究的动机在马西[大注册学习使用发病率和死亡率的这种复合终点作为主要结果的决定指出22]。在临床上的风险显著减少恶化治疗组间注意到没有被Δ6MWD反映。这表明对临床事件的风险显着影响与功能能力提升。类似的治疗任务之间的关联,TTCW和Δ6MWD指出selexipag[个随机对照试验的23]。与数据相结合从安立生坦和他达拉非初始组合的RCT与无论是在治疗过的队列度量的一个单独示范响应性,TTCW现在是一个经批准的终点为PAH治疗登记试验(ClinicalTrials.gov标识符NCT01908699,NCT02932410和NCT01824290)(表格1)。
限制的结果终点
未来的临床试验中需要更加高效。而TTCW作为主要终点已经被广泛接受,但不是解决办法。首先,是对整个试验TTCW没有标准的定义,限制比较研究之间的治疗效果(能力表格1)。第二,复合终点的各组分应相对于临床重要性和出现的频率来加权;TTCW在PH当前组件不是(例如死亡是罕见且临床恶化是常见的)33]。三,临床恶化和随后的生存之间的关系并不明确,而且并不总是由事件委员会,在PH(专业知识裁决表格1)34]。从塞拉芬利用数据更近的分析[22]和GRIPHON [23] TTCW试验发现,症状进展与住院治疗和3、6、12个月死亡率之间存在很强的相关性[35]。TTCW和随后发生的事件,如生存之间的关联严谨的研究,仍需要充分建立TTCW经核实的替代死亡率。
对PAH新的药物靶标
目前已获批准的药物主要用于纠正多环芳烃中血管活性因子的失衡。人们普遍认为,新药需要解决驱动血管重构的其他病理机制。具有潜在治疗价值的新型药物靶点层出不穷;目前的挑战是根据临床试验成功的可能性、副作用、生活质量和成本效益来确定候选药物的优先级。
遗传决定的目标
遗传学是确定和有信心优先新的药物靶点的强大机制。在突变BMPR2(骨形态发生蛋白受体2型),最常见的易感基因的PAH,对转化生长因子β注意力集中(TGF-β)/ BMP信号传导途径[36]。迄今为止,已用于靶向BMPR2信令在临床试验的唯一治疗是FK506(他克莫司)37],这是目前在阶段2(ClinicalTrials.gov识别码NCT01647945)。FK506结合其药理靶点FKBP12 (12-kDa FK506结合蛋白),并将其从所有三种BMPR 1型受体(ALK1、ALK2和ALK3)中去除,包括BMPR2偏爱的受体(ALK1和ALK3)。它能够激活BMPR2介导的信号,即使在没有外源性配体和BMPR2的情况下。
提出了用于校正受损BMPR2信令,超越基因治疗的抽吸策略,包括药理学方法如氯喹(其防止BMPR2的溶酶体降解),的ataluren(具有通过错义突变读取目标)和增加BMP9水平[38]。增加BMP信号的替代方案是使用一种新的活化素受体融合蛋白(sotatercept),其抑制TGF-β活性竞争性结合并中和TGF-β超家族配体[39]。当我们更好地理解多环芳烃的遗传结构,包括离子通道(KCNK3(钾通道亚家族K,成员3)),水通道蛋白和SOX17(SRY-框17)36,40]。需要进行进一步的临床前研究,以了解如何操纵这些或其信号通路以获得治疗益处。
表观遗传修饰
鲜为人知的是,PAH的表观遗传学的,但(HDAC)的临床前细胞和动物模型报道有益作用的抑制剂,组蛋白脱乙酰研究虽然心脏是一个问题[41]。要翻译多环芳烃中HDAC抑制的治疗潜力,需要对血管病理学中涉及的HDAC亚型有更清晰的认识。同样,需要更好地了解microRNAs在肺动脉高压中的作用,以便更好地从药理学角度控制其对肺血管疾病的影响[42]。
DNA损伤
聚的抑制(ADP-核糖)聚合酶(PARP)反转PAH在几种动物模型[43]。开放标签早期奥拉帕尼1周的研究中,批准用于治疗可口服PARP1抑制剂BRCA(乳腺癌基因)相关的乳腺癌,已经在PAH患者世界卫生组织功能II级,III对稳定血管活性治疗方案(ClinicalTrials.gov识别码NCT03251872)。
生长因子
酪氨酸激酶受体伊马替尼是第一个在大规模试验中直接用于多环芳烃血管重建的重要化合物。伊马替尼抑制血小板源生长因子(PDGF) receptor-α和-β[44]。PDGF是多环芳烃患者血管细胞和肺组织中的营养因子,PDGF受体表达增加。在3期PAH试验中,经安慰剂校正的6分钟步行距离平均增加32 m,肺血管阻力(PVR)下降,而TTCW未见改善。不幸的是,8例同时接受伊马替尼和维生素K拮抗剂抗凝治疗的患者出现硬膜下血肿[45]。然而,仍然特别是在酪氨酸激酶抑制剂相当大的兴趣,和伊马替尼,一些患者已经稳定下来,甚至在传闻伊马替尼治疗好转。确定患者的临床和分子特征可能响应的关键是这个计划的成功。
临床经验与其他酪氨酸激酶抑制剂敦促谨慎。事实上,接触达沙替尼与多环芳烃的发生有关[46,47]。在16周,单中心,开放标记12个例试验与PAH,所述多激酶/血管生成抑制剂索拉非尼恶化肺血流动力学和用不良事件,如在手和脚和脱发[中度皮肤反应相关48]。
代谢
胰岛素抵抗导致多环芳烃的发病率和死亡率[49]。这已导致在感兴趣的试剂的使用,如罗格列酮,二甲双胍和胰高血糖素样肽1激动剂(表2)50,51]。一个小的临床试验用二甲双胍是正在进行中,对右心室和肺动脉血流动力学的影响,详细研究。而正常的心肌用途脂肪酸氧化作为能量源,所述不适应心肌依赖于糖酵解,这是效率低得多[52]。谷氨酰胺分解也被诱导。脂肪酸氧化的抑制增加了葡萄糖氧化,导致了曲美他嗪(一种3-酮酰基辅酶A硫醇酶的抑制剂)被批准用于治疗心绞痛的可能性,可能在多环芳烃中发挥作用[53]。雷诺嗪,另一个抗心绞痛药,也是一种选择[54]。
在PAH,增殖细胞切换其代谢从氧化磷酸化到糖酵解为ATP产生。二氯乙酸(DCA),其抑制丙酮酸脱氢酶激酶,是PAH [一种潜在的治疗55]。降低SIRT (sirtuin 33)或UCP2(解偶联蛋白2)功能的基因变异影响DCA的临床反应。DCA的一项小型临床研究显示,遗传易感患者的血流动力学改善[56]。
炎症和免疫调节
肺的组织学研究、循环中的自身抗体和多环芳烃中高水平的血浆细胞因子都表明炎症是其病理的驱动因素[57]。目前的直接研究是针对多环芳烃中与结缔组织疾病相关的抗cd20单克隆抗体rituximab的临床试验(ClinicalTrials.gov识别码NCT01086540),以及多环芳烃中白介素-6受体拮抗剂托西珠单抗的试验(ClinicalTrials.gov识别码NCT02676947)(表3)。Elafin是一种内源性合成的弹性蛋白酶抑制剂,目前已进入临床试验阶段[58]。抑弹性酶蛋白是促细胞凋亡并减少在肺器官培养新生内膜病变[59]。
氧化和缺氧压力
氧化应激是已经针对性的PAH另一种机制。相较于动物研究[61,凋亡信号调节激酶1 (ASK1)抑制剂的2期研究未能显示整体改善[62]。在第二阶段的一些疗效信号(ClinicalTrials.gov识别码NCT02036970)。这种药物诱发核因子红细胞两个相关因子2 (Nrf2),调节抗氧化蛋白的转录因子,抑制促炎因子的激活NF-κB。
缺氧诱导因子(HIF)的增加的表达,具体地HIF1α和HIF2α,在PAH肺,在动物中的遗传操作[63]并且自然在人类中发生的突变(例如楚瓦什红细胞增多症[64])突出缺氧压力的PAH中的潜在重要性。几个小组已经表明,在不存在贫血缺铁常见于PAH和与存活率降低在PAH [相关联65]。开放标签研究静脉注射铁置换PAH表明,在运动能力的提高[66]和双盲研究已接近完成。
血清素和体液调节
血清素(5-HT)是一种有效的血管收缩剂和促增殖因子在肺血管细胞[67]。Terguride, 5图2A / 2B受体拮抗剂,没有表现出临床益处的2期研究中PAH [68]。这可以解释,部分,由于5-HT1B受体是多环芳烃肺动脉中最高度表达的5-HT受体。色氨酸羟化酶1 (TPH1)是5-HT生物合成的限速酶,拟与选择性抑制剂TPH1进行研究。
有一个在增强血管活性肠肽活性的作用,进一步检查的兴趣,尽管此前失望吸入给药69]。
在稳定的PAH谨慎使用β受体阻滞剂是安全的,但患者可能受益仍是一个悬而未决的问题[70]。虽然血管紧张素转换酶(ACE)抑制剂在硬皮病中具有重要的雷诺保护作用,但在多环肺动脉高压中没有显示出它们的益处。ACE的同系物ACE2将血管紧张素I和血管紧张素II转化为血管紧张素-(1-7)、血管紧张素-(1-9)和血管紧张素-(1-5),这很有趣。已经有报道在多环芳烃中发现了ACE2水平和ACE2自身抗体的降低[71]和ACE2替换使用纯化静脉注射可溶性重组人ACE2的制剂是正在进行中。两个前瞻性研究审查醛固酮拮抗剂的作用,安体舒通,也在进行中。
肺动脉去神经
肺动脉去神经支配是一种以消除交感神经对肺循环的支配为目的的介入治疗方法。在一项单中心研究中,13名患者接受了射频消融导管的治疗,平均肺动脉压显著降低,6分钟步行距离明显改善[72]。几个案件正在审理中确定PAH程序的有效性和安全性(表5)。
干细胞
有在PAH患者细胞疗法的临床很少报道。在12周的开放标签对照研究中,自体内皮祖细胞(EPCs)的输注提高6MWD和血液动力学参数的成年患者有严重的PAH [73]。类似的结果在特发性肺动脉高压儿童中观察到74]。在相位1 PHACeT试验中,内皮祖细胞转导的内皮型一氧化氮合成酶被给予患有PAH [75]。Ťhe 6MWD improved significantly at 1, 3 and 6 months post-infusion, by 65, 48 and 47 m, respectively. During the 3-day infusion protocol, no adverse haemodynamic or gas exchange parameters were observed [75]。
有几个原因相信与心脏干细胞,如cardiosphere衍生的细胞器(CDC),该疗法将PAH患者受益有或无右心室功能不全。疾病预防控制中心已被证实在临床前模型来改善大部分背后病理学的不适应右心室肌和改造肺血管[两者/病理生理学的主要像差76]。他们是有力的血管生成,抗纤维化和抗细胞凋亡;他们有显著的抗炎作用;它们既衰减氧化和亚硝化应激;他们吸引内源性干细胞对血管损伤部位。近来,对于PAH同种异体疾病预防控制中心的1期试验ALPHA被发起的,与主要目的是确定由中央输注施用到患者的特发性PAH的右心室流出道的CDC的最大可行剂量和安全性概况(表6)。
临床试验失败
多环芳烃治疗的几种新药物的问世,标志着过去20年多环芳烃治疗领域药物开发的成功,但越来越多的临床试验未能达到其主要终点,或报告了主要的安全性问题(表7)。有限的数据都在这些研究中公开可用的,但更深的理解是很重要的,以降低风险,提高成功前进。
有一个高淘汰率作为药物开发的进展,通过其阶段从首次在人体研究到关键注册研究。2006年至2015年间共9985个临床试验从7455个发展计划中,只有十分之一的从第1阶段进展到审批[77]。对于心肺疾病治疗的范围为6.6-12.8%。心肺疾病相转变成功率范围估计为58.9-65.3%为相1至2,24.1-29.1%为相2〜3和55.5-71.1%为相3至新药申请。尽管这个成功的总概率差,药物开发罕见病适应症仍然跨越发展的各个阶段[较为成功的项目之一77]。
终止一种药物开发的主要原因是缺乏疗效。52%的项目因缺乏有效性而停止,相比之下,21%的项目因安全问题而停止[78,79]。我们对PH的病理驱动因素的有限理解导致了这次试验的失败率。过分强调单一机制和模型系统的局限性也限制了药物的发展[78,80]。临床前的动物模型不能完全反映真实的人类疾病。当最好的车型进行测试,新疗法尚未在后台PAH治疗的动物进行评估。此外,临床前研究不使用严酷比如样本量的决心和随机化,他们已经不是传统上评价了人体试验使用的端点。最后,可能的是,治疗反应从脱靶效应导致(即增强血液流向骨骼肌),其通常不被在动物模型[评价78,80]。克服这些潜在的前期临床因素将需要在现代表型相关的机制,通过诸如PVDOMICS举措更完整的理解(ClinicalTrials.gov识别码NCT02980887),以及技术进步,提高适用性离体和体外化验。建立严谨的标准,指导临床前动物模型测试[80]也将有可能导致提高的治疗候选者的选择和在人类临床试验环境测试时尽量减少偏差和假阳性结果的影响。
鉴于临床试验更可能“失败”不是成功,它是建立在计划从“失败”来学习的重要[81]。早期阶段的临床试验的目的和目标应该集中在安全性,内容丰富生物标志物和响应亚群的鉴定。虽然通过结合统计规范,在前期临床试验的决定不应该基于单p值阈值做出。在“机械明线规则”立足于早期发展科学,商业或政策决定,如p值<0.05为科学要求的理由的门槛可能会导致不正确的结论[82]。后来阶段的研究需要通过对剂量 - 反应关系充分的数据和病人,显示的效果信号的特性被告知。然而,数据产生的所有沿药物开发途径,而这些数据可用于仔细评估势在必行。这将通知学习动力,终点和人口选择的批判性分析。
虽然常用,临床试验的背景下,术语“失败”并不精心设计的负面研究区分与由于有缺陷的设计或操作而不确定的研究。此外,对临床试验“失败”的认知是复杂的,取决于视角。临床试验人员和科学家可能认为不符合相关主要或次要终点的干预措施是“失败的”,而患者可能认为不能改善症状的治疗是无益的。除了定义和观点方面的问题外,这些临床试验的数据通常不会公开披露,因为存在从商业议程、学术兴趣到发表偏见等多方面的问题。不成功的试验可能与“积极的”试验一样,甚至更能提供信息。IMPRES试验的数据是一个很好的例子[45]。尽管在运动能力和血流动力学方面有明显的改善,但严重不良事件和研究药物停药的高发生率最终导致决定停止开发甲磺酸伊马替尼作为PAH的附加治疗。然而,这篇论文的发表和随后的学术对话为围绕多环芳烃治疗的方法学、剂量和再利用方法的讨论提供了动力。更重要的是,这些数据增强了对整合生物标志物作为最佳临床试验候选筛选策略的实用性的讨论。使用选定的生物标志物似乎与13-21%的临床试验开发阶段之间成功过渡的概率相对增加有关[77]。
无论结果如何,所有研究的发表都有可能降低成本,改善未来的试验设计,降低流失率,最重要的是,减少接触无效药物或参与有缺陷的临床试验设计的临床试验对象的数量[83]。事实上,诸如医学出版见解和实践(www.mpip-initiative.org)等制药合作伙伴的支持,世界卫生组织,以及美国药物研究与制造商已在临床试验方案和结果[发表呼吁透明度83]。我们在PAH科学界必须认识到我们的道德义务临床试验受试者谁使我们能够让他们接触,希望增加知识将获得研究性干预措施。我们通过这种道德义务必然要学习和传播知识生产的每一个参与和每一个临床试验的主题。报告和检查阴性临床试验中,承诺的全面数据集的评估(不仅是顶线数据)的透明过程是必不可少的。这一过程应超过个别机构或医学刊物的当前数据共享政策和资助,允许通过科学委员会独立进行分析(即数据安全性与必要的专门知识监测板)(即临床试验者,伦理学家和统计学家)。这样的报告流程的义务应是平衡的(但不是以阻碍)分析证明了概念的早期阶段研究时,对数据保密的需要。
挑战未来的试验设计
药物对PAH的成功发展提供了对患者的治疗效果显著影响,但尚未产生治愈。的新的潜在选项的激增创造了临床护理和未来药物开发计划新的挑战。当然,这是一个“好”应力需要克服,但它需要的新型试验终点和设计周到的考虑。这也意味着,药理作用,药效学及药代动力学个体将成为纳入今后的研究更重要。新型生物标记和遗传关联的发现将需要真正发展和个性化的治疗方法。还有关于我们目前的药物的作用机制相当未知数,他们的在活的有机体内药理学和他们的最佳利用。另外,较大的试验将根据需要,需要在以研究疾病状态的生物标志物的潜在有意义更多的合作。在PAH试验从通过phase 1和phase 2中的临床前阶段开始应着眼于“学习”以改善整个企业的效率。另外,患者的孤儿病谁可参加临床试验的数量是有限的。当务之急是要获得与最少的患者处于危险的最多的知识。
未来的治疗方法不能再研究从头安慰剂治疗的比较组。解决这一困境的一个办法是实施创造性的适应性设计。信息学技术可以根据接收到的临床数据进行实时“调整”,调整入学率分层和结果目标,并确定无效[84]。此外,该技术可以允许测试多种治疗选择,如果所有利益相关者都愿意共同努力,找到最佳的治疗效果。对临床试验的适应性设计2018年美国食品和药物管理局的指导定义这些试验是“研究设计,其允许预先规划的修改基于来自试验对象的积累的数据设计的一个或多个方面” [85]。重要的是要认识到,一旦进行中期监察,从那时起经常进行监察的统计成本便会减少[86]。这些贝叶斯模型允许统计推论考虑到数据驱动适配,从而允许试用灵活性[87]。
最容易实施的试验是一项相2/3试验,其允许临时“看”来评估实验臂是否有效,并因此值得继续到其相3阶段[88]。这是一种更快、更有效的方法,但仅限于在达到第三阶段所需的最终终点之前使用第二阶段终点的试验。需要提前解决的问题包括设定进入第三阶段所需的回应率、选择终点,以及确定数据在分析前是否有时间延迟[89]。与此相反,传统的做法少被认为可能是一个多臂试验用针对一个单一的控制臂测试多种实验性疗法[84]。这可以用疗效和徒劳停止规则来完成每个治疗,并有可能只下降了一些武器的同时,继续与其他人[研究90]。
生物标志物驱动的试验通常包括随机分组、标记丰富和标记导向设计[87]。块设计使用所述生物标志物作为用于随机化的众多因素之一,而所述生物标志物是中央在标记定向设计治疗分配。标记富集的设计选择用于治疗应答的预后标记物或更高的风险的一个决定因素,以提高成功[87]。主自适应平台组合这些概念是主协议的方法。该方法或“平台”可以在现有的队列或新亚组添加新的治疗武器,其中一些理疗一次被测试的正在进行的审判[84]。缺点是,在后来添加的臂可以仅使用从登记的相同的时间点的随机化对照患者进行比较。这不是一项容易的任务来组织为多个行业合作伙伴需要合作的试验设计,控制和数据,资金的隐私和监管要求[91]。
在自适应设计中使用的生物标志物可以加强审判效率[92]。伞或篮试验描述设计为整合了与治疗应答相关成熟的分子,遗传或血清学标志物的主协议。这是如今在肿瘤药物开发成为可能,并可能成为PH试验中潜在的设计。一个例子可能是使用的风险评估工具,在登记或研究分层科目中的生物标志物的。最终,风险的工具然后可以随时间修改这些新的标志物,以产生预后。生物标记定义的子组可与该方法所研究的总人群的小比例。此外,能否停止无效治疗的研究,如果治疗被证明有利于提高审判效率增加手臂。根据审判阶段,证据需要满足一个成熟的门槛可能会有所不同,需要事先达成共识,审判开始[84]。
建议在今后的PAH临床试验设计
协作和利用现有资源是成功开发多环芳烃治疗的关键。无论是成功的研究还是失败的研究,在完成时检查数据的能力应该是规则,而不是例外。由于研究对象的异质性、大量背景疗法的使用、轻微疾病患者的纳入以及可能选择了错误的终点,最近1-2期药物靶向新作用机制的研究结果尚未取得成功。而不是使用传统的多环芳烃临床和血流动力学试验终点的靶向制剂(例如6MWT和PVR),结束点应根据疾病的生物学和预期的影响机制。这种做法将使潜在的监管考虑新的生物标志物。
阶段1-2的目标
1)药代动力学和药效学研究应进行评估,特别是因为我们知道一点治疗的无数组合。
2)这些试验应该包括疾病的生物和机械标记,以更好地评估对治疗的反应。
3)为提高普适性和功能性的能力看到的变化解释,早期的药物试验应该包括更均匀的目标群。
4)试验应使用风险工具作为一种丰富策略,以更好地表型一个异质群体。
5)第2期新的疗效指标(例如磁共振成像和专家的)应被掺入,然后在第3阶段使用。
很明显,执行长期的复合事件驱动的试验将是具有挑战性的,并可能通过将研究参与者投入多年来阻止新发展的激增[93]。发病率和死亡率事件试验需要大量的试验对象预先证明即使在1年的效果[35,94]。在PAH今后的临床试验将需要有临床意义的终点,反映发病率和死亡率,以及患者的感受和功能[95]。据了解,“低风险”的患者档案后PAH的初始治疗与更好的生存相关的[96-99]:一个潜在的探索性终点可能达到或根据该揭密(注册表来评估早期和长期肺动脉高压疾病管理)保持“低风险”的状态得分的能力[96]或由欧洲心脏病学会定义的低风险的标准的数量/欧洲呼吸协会PH指南[188bet官网地址94,98,100,101]。
阶段2-3的目标
总体目标应该是改善患者的生活更多的功能和满足生活的能力。
1)检查时临床起色而不是TTCW。这将需要确定在现有的终点临床显著差异,并允许这些差异审后用新标志的推导。
2)现在利用风险变化功效的标志作为一项探索性终点,以检查其在未来的临床终点预测。
3)利用新颖的生物标志物(血清,血浆,基因组学,metabolics和专家的),为探索性终点现在以检查其作为未来临床终点可预测性。
4)限制不必要的上市后和小规模的研究者发起的研究,这些研究不太可能提高我们的科学知识基础或改善病人护理。
脚注
这是由N. Galie、V.V. McLaughlin、L.J. Rubin和G. Simonneau编辑的“第六届世界肺动脉高压研讨会论文集”系列中的第8期
利益冲突:O. Sitbon报告来自MSD、Actelion Pharmaceuticals和GSK的赠款、个人费用和非财务支持,来自GossamerBio、Arena Pharmaceuticals和Acceleron Pharmaceuticals的个人费用,以及来自Bayer HealthCare提交的工作之外的赠款和个人费用。
利益冲突:M. Gomberg提出-梅特兰是一个顾问/数据安全监督委员会成员/科学顾问委员会的Actelion公司,Acceleron,复杂了,默克,Reata和联合治疗成员。INOVA的接收研究支持她从Actelion公司,AADI和联合治疗做研究。
利益冲突:J. Granton获得了Actelion、拜耳和辉瑞的支持,以支持研究者发起的研究。他是PAH Bellerophon临床试验指导委员会的成员,也是联合治疗公司(United Therapeutics)赞助的一项临床试验的评审委员会成员。
利益冲突:M.I.刘易斯报道说,ALPHA研究报告提到,由来自加州再生医学研究所(补助CLIN2-09444)基金资助项目。
利益冲突:南卡罗马报告硬皮病基金会的个人费用咨询和数据,并从Actelion公司安全监测委员会成员,从美国治疗顾问个人的费用,和赠款,提交作品之外;是科学的领导委员会的成员,肺动脉高压协会与中心的结果研究院患者的罕见疾病咨询小组。
利益冲突:雷尼西奥没有什么要披露的。
利益冲突:N.L.斯托克布里奇有没有透露。
利益冲突:M.R.威尔金斯从Actelion公司制药,拜耳医药保健,GossamerBio和形态发生-IX,外提交的工作报告个人费用。
利益冲突:室温B.Zamanian为Actelion公司制药,默克,Vivus公司和GossamerBio的顾问,并已收到补助从Actelion公司制药;并拥有专利FK506,用于治疗肺动脉高压的,发出的。
利益冲突:L.J. Rubin在研究期间报告了Actelion、Arena、Bellerophon、SoniVie和Roivant的个人费用。
- 收到2018年10月5日。
- 公认2018年10月9日。
- 这项工作的内容是作者或他们的雇主的版权。设计和品牌是版权©ERS 2019
这篇文章是开放存取并根据知识共享188滚球软件署名非商业许可证4.0的条款分发。















