抽象
自2000年以来已经出现在我们的基因的了解重大进展和肺动脉高压(PAH)基因组学,虽然仍有许多发现。根据现有的知识,诊断为特发性肺动脉高压患者25-30%有自己的病情底层孟德尔遗传原因和应列为遗传PAH(HPAH)。在这里,我们总结PAH的已知的遗传和基因组驱动程序时,这些见解提供了到病理学,并提供了新的治疗方法的发展机遇。此外,确定HPAH中观察到的不完全外显因素进行了讨论。基因检测和咨询,并与PAH患者的临床管理基因诊断的影响,目前可用的方法,现介绍。在DNA测序技术的进步正在迅速扩大我们的规模较大的同伙进行基因组学研究的能力。在未来,这样的研究将提供PAH的遗传贡献的更完整的画面,可能还有这种疾病的分子分型。
抽象
肺动脉高压的遗传学和基因组学的研究现状和前景以及对病理生物学的认识http://ow.ly/dkkq30mgDo2
介绍
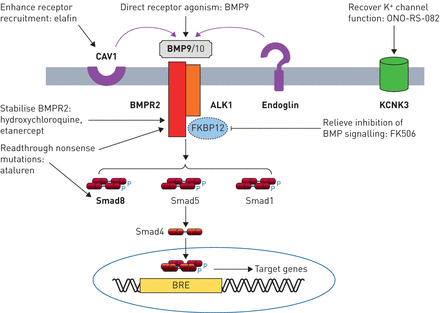
20世纪中期后的半个世纪里,当心导管术首次为临床医生提供了安全测量肺血流动力学的能力时,特发性肺动脉高压(IPAH,后来被称为原发性肺动脉高压(PPH))被认为是一种起源不明的致死性肺血管疾病。本世纪初,对PAH家族的特殊遗传倾向有了新的认识,2003年第三届世界肺动脉高压研讨会对PAH的分类进行了修正。自2000年以来,研究人员对多环芳烃的遗传学和基因组学的认识不断增加。基因测序的技术进步使得在家庭和大量患者中对基因组编码区(全外显子序列(WES))或全基因组(全基因组序列(WGS))进行廉价而快速的测序成为可能(图1)。来自人类遗传学的见解正在增进我们对多环芳烃病理生物学的了解,确定新的潜在药物靶点,并告知患者及其家属的护理。
肺动脉高压基因发现的历史。WSPH:世界研讨会肺动脉高压。
技术水平
孟德尔遗传
有PAH的患者6-10%家族史不能与其他潜在疾病有关[1]。在2000年,这样的家庭的遗传分析鉴定杂合子胚系突变在BMPR2,基因编码骨形态形成蛋白受体2型,改变成员增长factor-β(TGF-β)总科2,3]。随后,在IPAH中也发现了突变[4]。现在是公认的70-80%,与PAH和IPAH的情况下,10-20%的家庭是由突变引起BMPR2[五]。
编码BMP受体信号导致稀有序列的识别变体基因的中介的测序SMAD1,SMAD4和SMAD9[6,7]。附加标识SMAD9大量人群的突变证实了其在多环芳烃中的作用[8]. 此外,外显子组测序BMPR2阴性个体与一个以上的家庭成员被诊断为PAH透露突变CAV1,其编码小窝蛋白1和函数以物理colocalise BMP受体[9]。一种罕见的基因突变CAV1一直与脂肪营养不良和多环芳烃在一个幼儿。KCNK3(钾通道亚科K成员3)突变也通过外显子组测序鉴定,并编码一个钾通道,该通道有助于确定肺血管张力的膜电位[10]。阵列比较杂交和测序在儿童和(很少)成人发病多环芳烃确定缺失和失去功能的突变TBX4(T-box 4),该基因也与小髌骨综合征有关[11]。突变TBX4是PAH的儿童最常见的遗传原因之一,并建议PAH是至少部分发育的肺部疾病,当它呈现在生命的早期[12,13]。,严重的肺动脉高压,也可能发生在家庭中分离式遗传性出血性血管扩张症的识别(HHT)牵连ACVRL1(激活蛋白受体样激酶1 (ALK1))ENG(endoglin)在PAH中的突变[14-16]。
最近,一项大型调查在欧洲合作队列(>18岁)中进行,研究对象包括IPAH、家族性多环芳烃(FPAH)和厌食症相关多环芳烃患者[8]。超过1000例患者的这项研究证实了因果突变的存在BMPR2(15.3%),TBX4(1.3%),ACVRL1(0.9%),ENG(0.6%),SMAD9(0.4%)和KCNK3(0.4%)。无致病性编码在多个变CAV1,SMAD1或SMAD4可能是由于这些基因在成年人中很少发生突变。该研究还发现了新的多环芳烃基因的突变:ATP13A3(ATP酶13A3; 1.1%),SOX17(SRY-box 17;0.9%),AQP1(水通道蛋白1; 0.9%)和GDF2(生长分化因子2 / BMP9; 0.8%),并建议另外的基因,将需要进一步的验证。在所有这些基因的突变是常染色体显性遗传,并表现出降低的渗透率,这意味着一些个人谁携带突变没有明显的PAH。在IPAH情况下,突变可以从父不受影响继承或发生新创. 在有父母样本的地方,确定发生了突变新创可以在建立致病性有帮助。在儿科IPAH患者没有突变的已知风险基因,外显子测序揭示了一个2倍的富集新创预测有害的变异。从头在新基因变体可以解释的儿科发病IPAH箱子19%[12]。对于PAH基因中观察到的不完全外显表明额外的遗传,后生和/或环境因素导致的疾病风险/进展。
在2014年,双等位基因突变EIF2AK4,一个基因编码真核翻译起始因子2α激酶4,被确认为一种遗传原因肺毛细管haemangiomatosis (PCH) [17]及肺静脉闭塞病(PVOD) [18]。PVOD和PCH是罕见的多环芳烃的病理形态。遗传性PVOD和PCH是常染色体隐性遗传,几乎完全外显,不像其他形式的多环芳烃。诊断为偶发性PVOD或PCH的个体也可能携带双等位基因EIF2AK4突变高达病例[25%17,18]。等位基因病原的检测EIF2AK4突变建立PVOD / PCH的精确和准确的分子诊断,而不需要肺活检[19]。
HPAH患者迄今报告的基因总结如下表格1。在将一个特定基因用于临床筛选和管理之前,需要建立一个高水平的证据来证明基因突变的因果作用。
常见的遗传变异
常见的遗传变异有助于病因或PAH的临床病程的作用尚不明确。迄今为止,只有一个全基因组关联研究已经发表,以确定与PAH(N =625案件)相关变种。这项研究发现在一个显著协会CBLN2(cerebellin 2 precursor) locus mapping to 18q22.3, with the risk allele conferring an odds ratio for PAH of 1.97 (p=7.47 × 10−10)20]。另一个大的研究评估多态性之间的关联,包括在欧洲血统在STRIDE研究(西他生坦)的715名PAH患者的内皮素信号转导通路和临床结果的基因。的关联是在G蛋白γ亚单位基因的单核苷酸多态性(rs11157866)之间识别GNG2和功能类和6分钟步行距离的组合的改进[21]。在一个较小的研究中,血清内皮抑素水平,有能力的强效的抗血管发生蛋白质诱导内皮细胞凋亡和抑制内皮细胞增殖,具有差的功能状态相关,并且是死亡率的组1例在一个强有力的预测。与此相反,一个错义变异体(rs12483377)的COL18A1,编码内皮抑素,与较低的循环蛋白和降低死亡率有关[22]。在多环芳烃中,线粒体代谢异常已被广泛认识。最近的一项研究表明,线粒体基因组的变异可能会影响多环芳烃的发病风险,与最古老的人类祖先单倍群L相关的发病率较低[23]。最后,在一项对2761名健康成年人的研究中,雌二醇代谢的变异(CYP1B1(细胞色素P450 1B1))和雄激素受体基因与右心室功能相关[24]。鉴于显著性别差距PAH和以前的证据表明,CYP1B1变种可以调节疾病的外中BMPR2突变携带者(25,这些变异值得进一步研究,以确定其在多环芳烃右心室重构中的可能作用。
突变与疾病的病理生物学联系
多环芳烃突变与疾病病理生物学
BMPR2在大量细胞表面表达,但在肺血管内皮细胞上表达尤为高,与I型受体ALK1或ALK2形成复合物。特别是针对循环中的BMP配体BMP9和BMP10的ALK1/BMPR2受体复合物信号,利用ENG作为辅助受体[26,27]。ALK1和ENG也高度在肺内皮中表达,并且这要求高水平BMPR2 / ALK1在肺内皮信令可能有助于肺特异性作用BMPR2突变。BMP9(由编码GDF2)具有循环血管静息因子的功能,保护内皮细胞不发生凋亡和过度增殖,抑制血管通透性。的损失BMPR2也有利于内皮功能障碍和促进内皮 - 间质转化。鉴于突变ALK1和ENG(通常与HHT相关联的)也可引起PAH,遗传证据表明,肺的内皮细胞是在PAH病理学的重要起始细胞类型。然而,在其他细胞类型BMPR2功能丧失(例如平滑肌细胞,成纤维细胞和免疫细胞)也可能有助于疾病的病理学。例如,肺动脉平滑肌细胞与BMPR2突变是增生性的,并通过丢失抗增生性Smad1/5信号而抵抗BMPs的生长抑制作用[28]。
其他不常见的PAH突变也与BMP途径。Smad8(通过将编码的SMAD9基因)是BMP信号传导的下游介质,连同的Smad1和5的杂合突变SMAD9通过Smad4对规范BMP信令的影响相对较小,可能是由于Smad1/5功能的冗余[29]. 然而,与促进microRNA成熟的Smad4独立途径有关[三十]SMAD9突变导致功能显著丧失,提示以这种方式调控的microRNAs可能在PAH发病机制中发挥重要作用[29]。类似的结果被认为在与其中肺动脉内皮细胞进行的体细胞杂合缺失先天性心脏疾病(CHD)相关的PAH的情况下SMAD9[31]。
EIF2AK4,也称为总控制非去阻遏2(GCN2),是一种丝氨酸/苏氨酸蛋白激酶,其磷酸化真核起始因子2,其在响应于营养缺乏调节氨基酸代谢中起关键作用的α亚基。EIF2AK4通过结合至不带电荷的转移RNA检测氨基酸的缺乏。通过该该激酶的功能丧失促进PVOD / PCH发展的分子和细胞机制,目前正在积极调查。在里面EIF2AK4−−/小鼠对应激反应增强,继发于自噬减少和氧化应激增加及其对炎症活化和炎症的影响[32]。它仍然相似如果机制参与的内膜纤维化和在遗传PVOD的肺血管观察到内皮细胞增殖待证明。或者,EIF2AK4下降TRIB3功能引线的双等位基因丧失(中Tribbles样蛋白3),其下调已被证明能够抑制BMP-介导的细胞反应[33]。在这种假设下,EIF2AK4功能丧失的后果与BMPR2或SMAD9减少BMP信号的突变。
CAV1是小凹(原生质膜的瓶状凹陷)的主要组成蛋白,在内皮细胞中高表达。BMP受体定位于小凹和质膜的其他区域,研究表明,小凹是启动BMP信号的必要条件[34]. 损失CAV1decreases BMPR2 membrane localisation and signalling [35]。相反,BMPR2突变可导致小窝运输缺陷和细胞内定位[36]。最后,值得注意的是,即使在没有遗传突变的情况下BMPR2和CAV1在PAH肺组织[减小37,38]。
影响疾病的外因素
尽管致病BMPR2突变明显导致PAH,疾病表型外显率不完全。最佳估计是男性携带者的外显率约为14%,而女性的外显率约为42% [39]。因此,女性的性是影响的外显率的一个最重要的因素BMPR2在PAH突变,可能是由雌激素代谢从动[25]. 影响外显率的其他因素可能是遗传、表观遗传和/或环境因素。遗传因素可能包括野生型的表达水平BMPR2从未受影响的等位基因[40],遗传变异影响TGF-β的表达水平[41或选择性剪接BMPR2[42]。在诱导多能干细胞研究,从影响和不受影响衍生BMPR2突变载体表明,遗传背景,特别是BMP通路修饰基因表达的差异,可能有助于外显率[43]。需要对受影响和未受影响的突变携带者进行更多的大规模纵向研究,以便更系统地寻找遗传和环境外显率修饰因子。
虽然没有研究尚未解决的影响的渗透率潜在的环境因素BMPR2人类队列中的突变,研究表明炎症介质,例如脂多糖[44],肿瘤坏死因子α(TNF-α)[45和5-脂氧合酶[46],可以驱动PH的发展在遗传修饰的小鼠和患者来源的多能干细胞[47]。TNF-α直接禁止显示BMPR2mRNA和蛋白表达。此外,表观遗传机制如高甲基化BMPR2促进者可能起一定作用[48]。一些微RNA也已经显示出目标BMPR2mRNA的修改蛋白的表达水平,包括miR-21的[49]和miR-17-92 [50]。
另一个可能导致外显的因素是肺血管细胞内的体细胞突变[51]。几组与对照[比较已经确定在从PAH肺部内皮细胞和平滑肌细胞中的DNA损伤51-53]. 损失BMPR2用DNA修复的缺陷相关[54],但增加的DNA损伤也很明显在从IPAH细胞和相关的PAH的情况下,并且可以通过环境暴露例如使用甲基苯丙胺诱导[55]。需要进一步的研究来了解肺中的DNA损伤和疾病发病机制的贡献作用。
健康突变携带者的遗传咨询/检测和管理
遗传咨询
在PAH基因突变已在IPAH和FPAH,anorexigen相关PAH,PVOD / PCH已经确定,并与IPAH和PAH儿童CHD相关。有一个法医学责任告知所有患者在这组有关遗传性疾病的可能性和家庭成员可以携带增加PAH的风险,允许筛查和早期诊断的突变。即使没有进行基因检测,家庭成员应该知道的早期症状和体征,以确保及时和适当的作出诊断。如果一个突变的患者而鉴定,症状的患者应改为HPAH。
遗传教育和咨询之前应该进行基因检测的多环芳烃,解决复杂的问题不完全外显率,监测高危基因家族成员的问题,生殖问题,基因歧视的担忧,以及心理内疚和责任的问题,可以伴随遗传基础的疾病。考试前的遗传教育影响个体可以通过PAH提供者和/或遗传的专业人员来执行,并且由聚焦教育视频促进(例如www.youtube.com/watch?v=36rlvtj_Qrs)。深入遗传专业人员,包括遗传顾问或医学遗传学家遗传咨询是用于基因测试之前临界无症状家庭成员。家庭也应该,如果他们愿意考虑生育选择称为遗传咨询和/或临床遗传学家。对PAH国家参考中心的遗传咨询经验表明,在无症状的家族成员在基因检测的潜在利益[56]。
在家族遗传测试应与受影响的个人做起,只要能够确定在家庭中的相关突变。否则,一个负的遗传测试结果不受影响的家庭成员并不丰富。一世f the familial mutation is known and an unaffected family member tests negative for that mutation, the risk of PAH for that person is the same as the general population (around 1 per 1 000 000 in North America). This can provide great psychological relief to that family member and they can forgo evaluations to screen for PAH.
基因检测
基因检测可以帮助解释疾病的病因和危险分层其他家庭成员和未来的孩子。临床基因检测是在北美和欧洲上市,并且材料可以从世界其他地区被发送到美国或欧洲的遗传实验室。从约1000美元至1500美元测试范围的当前成本来分析一个家族的第一个成员。一旦家庭特有的突变是已知的,测试其他家庭成员在美国花费USD300-500。基因包含的确切数目,测试检验和保险费用由国家,保险公司变化。最常提及的原因为PAH基因检测是为大约儿童提供的信息,并在测试的兴趣特别高的小儿发病PAH [57]。
有针对性的测序
与PAH增加相关基因的数量,它已成为艰巨的测试对每个单独这些基因的。新一代测序的出现使得基因板的发展,同时询问几个基因。几种不同的技术和平台都具备了,现在很多都是临床的基础上提供(www.ncbi.nlm.nih.gov/gtr/conditions/C0152171/)。此外,一些这些基因的可分析量变化来检测缺失或一个或多个外显子的重复。这种突变是常见的BMPR2和TBX4。适当的方法,例如多重连接依赖性探针扩增,应因为这些类型的突变可以使用不容易被测序检测。检查包括在由于该组合物变化遗传学发现预先测试的时间面板中的基因是非常重要的。
全外显子组测序和全基因组测序
如果PAH基因的一个上的最新面板不能识别与家族性PAH或在儿童患者的致病变种,WES可适当识别潜在的新基因。在儿科发病PAH的情况下,测试应该理想地包括孩子和双方父母允许的容易识别新创变体。这三种方法都被用来识别CAV1和KCNK3基因[9,10]。最大的三重奏分析表明,儿童期发病IPAH的19%是由于新创突变[12]。外显子组测序比委员会更贵的基因测试,应该下令遗传专业人士可以讨论学习的选择或二次偶然发现的,目前推荐的59个基因组成的美国大学医学遗传学和基因组学,医学上可操作的和潜在的救生,包括基因遗传性癌症和心脏性猝死58]。
即将到来的是WGS的使用,它能够识别患者基因组中非编码区的变体,但还没有在临床上常规使用。随着时间的推移,随着新基因的鉴定,外显子组和基因组测序具有反复再分析的优势。
测序数据解释
WES和WGS的主要问题是在任何个体中都存在大量的变异。解释错义和非编码变体的功能后果尤其具有挑战性。因此,识别新基因中潜在的致病性变异需要基于参考等位基因频率的大型数据库过滤掉常见变异,并对可能的功能效应进行生物信息学预测。家庭内部的种族隔离研究有时可以澄清一种不确定意义的变体(VUS),特别是在这种变体存在的情况下新创或者如果它与PAH偏析于其他受影响的家庭成员[58),而赞赏外显率通常是不完整的,携带者可能不受影响。只有被归类为致病性或可能致病性的遗传变异(不是VUS)才能被用来对未受影响的家庭成员进行遗传风险分层。
社会心理因素和生育选择
基因检测结果可能会造成比某些人得不偿失,因为目前还防止没有有效的方法或PAH的差异对待遗传形式和因为突变的不完全外显的。在一个家庭中确定的突变可以与谁对突变为他们的孩子通过在父的罪恶感有关。也有关于就业和保险基因歧视的担忧。反对基因歧视的法律保障因国家而异。在美国,遗传信息无歧视法案防止在覆盖范围或医疗保险的费用歧视参保成员和就业保护不受歧视,但不反对在生活中的歧视,长期护理或残疾保险基于遗传倾向。在全民医保的国家,关于基因歧视的担心是没有那么大和基因检测的吸收率一直较高。
携带致病性突变的人的生殖选择包括采用、使用供体配子、产前检测、体外有着床前基因诊断或未考虑多环芳烃遗传状态的受精(IVF)。IVF和胚胎植入前基因诊断的可获得性和保险范围因国家而异,但由于患者的费用,保险范围往往难以获得。
遗传学和基因组学的实际应用
什么是基因诊断的肺动脉高压患者的效用?
致病的PAH突变与影响治疗和预后的疾病特征相关。例如,HPAH与BMPR2或ACVRL1突变出现在较年轻的年龄,有更严重的血流动力学异常,急性血管反应的概率非常低,并且在当前的治疗时代生存率降低[59,60]。Patients with a heritable form of PVOD are also younger at presentation than non-mutation carriers, but there is no significant difference in the event-free survival at 3 years [61]。
几项研究清楚地表明,发现致病性EIF2AK4突变是非常有用的。PVOD / PCH的诊断挑战PH临床医生,放射科医师和病理学家。等位基因的鉴定EIF2AK4突变允许遗传PVOD的确认/ PCH没有肺活检,并且识别PAH的唯一形式,它不仅不以当前PAH药物很好地响应,而且还易于发生肺水肿施用这些药物时[61]。确诊为IPAH或HPAH个体的亚组也可能携带致病等位基因EIF2AK4突变。Ťhese individuals are characterised by presenting under the age of 50 years with a diffusing capacity of the lung for carbon monoxide (dLCO) <预测的50% [62-64]。因此,我们建议临床医师测试谁具有较低的年轻PAH患者dLCO对于EIF2AK4突变,以指导治疗和风险评估家族成员[63]。
来自基因组研究的发现也开始被用来更好地理解疾病过程和治疗反应。Hemnes等。[65]鉴定患者响应于钙通道阻断剂治疗的PAH亚表型的周边血液中的RNA表达特征,提示一种非侵入性的方法来预测药物反应。使用WES,可能这背后亚表型的遗传变异也被确定[66]。如前所述,常见的遗传变异与多环芳烃的风险、生存率和/或药物基因组对治疗的反应有关。最近,研究表明,常见的功能变异SIRT3号和UCP2协议可能会在2期临床试验中PAH [由二氯乙酸预测到抑制丙酮酸脱氢酶激酶的响应67,为未来的精准医疗研究铺平了道路。
从基因疗法
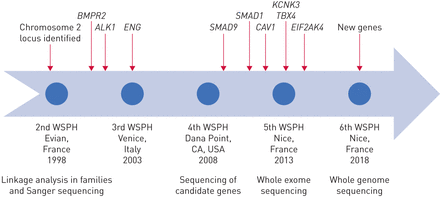
通过遗传学研究强调的分子途径,现在是几个新的治疗方法的主题(图2)。大号翁等。[68]报道杂BMP9管理的有益作用BMPR2基因敲除小鼠,这表明补偿BMPR2通过增加配体剂量的单倍性不足可能成为人类多环芳烃的靶向治疗。在受体水平,方法包括利用ataluren来恢复全长蛋白的无意义突变的翻译解读[69]或用氯喹减缓BMPR2溶酶体降解以增加细胞表面受体密度[70,71]. 两种方法都有效地恢复了BMP信号体外溶酶体阻断剂逆转了实验模型的PH值。用依那西普进行抑制TNF-α不仅目标炎症,但可以减少受体脱落和变幻虫的退化BMPR2 [45]. 埃拉芬法案通过CAV1促进受体募集,增强BMP信号,逆转实验性PH值[72]。下游BMPR2的,FK506,发现增加BMP信号,并扭转实验PH,通过结合FK结合蛋白12,BMP信号传导的抑制剂[73]. 2a期临床试验证实了低剂量FK506治疗PAH的安全性和耐受性[74]。在BMP途径之外,KCNK3突变导致降低的钾通道电导,其中,至少对于一些突变,可以通过磷脂酶A被回收2抑制剂ono - rs - 082 (10]。这些研究强调的是,已经翻译的基本遗传研究到潜在的治疗方式方面取得了长足的进步。尽管底层突变遗体直接修正目前具有挑战性的,在基因编辑技术的迅猛发展可以有针对性地提出突变修正肺血管内的未来现实的前景。
从基因到治疗:肺动脉高压(PAH)的精准医疗方法。BMP(R):骨形态发生蛋白(受体);信徒:BMP-responsive元素;CAV1: caveolin-1;FKBP12: 12-kDa fk506结合蛋白。内皮细胞中的BMP信号是由配体BMP9和BMP10介导的通过所述ALK1 / BMPR2受体复合物。内皮因子充当辅助受体。信令由受体的Smads(的Smad1,5和8),然后与Smad4的关联和易位至细胞核的磷酸化介导,调节包含在它们的启动子BREs里面的基因。CAV1促进受体共定位,而KCNK3编码钾通道有助于肺血管紧张。这是在遗传的PAH突变基因在大胆。潜在的治疗方法靶向这些途径包括:BMP9的外源性给药配体,功能性BMPR2受体(羟氯喹,依那西普)提高可用性,促进无义突变的连读恢复功能BMPR2或Smad8蛋白(的ataluren),通过减轻FKBP12抑制增强下游信号传导BMP的1型受体(FK506),促进CAV1介导的受体募集(抑弹性酶蛋白),或回收KCNK3沟道电导(ONO-RS-082)。
建议未来方向
这些不同的基因组方法强调了利用分子药物改善PAH患者护理的潜在途径。美国和欧洲目前正在进行几项大规模的遗传学/基因组学研究。值得注意的是,美国国家多环芳烃生物样本和数据库(“PAH生物样本库”;www.pahbiobank.org)正在为3000例1组PAH患者生成遗传数据(靶向DNA测序、WES和全基因组单核苷酸多态性)。英国的桥梁项目将多环芳烃作为WGS数据生成的罕见疾病之一(https://bridgestudy.medschl.cam.ac.uk/pah.shtml)。在1250 IPAH /来自欧洲的家族性肺动脉高压患者正在分析调查的基本遗传变异有助于疾病。此外,卫生PVDOMICS倡议旨在将美国国立卫生研究院通过深临床表型与多个“组学”的分析[组合定义跨越传统世界卫生组织组新的分子分类75]。只有通过这样的群组和行动,我们才能开始有足够的能力发现PAH的遗传因素范围,从而对该病提供更完整的基因组学理解。理想情况下,这将导致识别新的药物的新靶点。它还可以促进多环芳烃的预防策略和预测预后的基础上,多环芳烃的遗传分类。
脚注
在该系列由编辑N.Galiè“第六届世界研讨会肺动脉高压的论文集” 2号,V.V.麦克劳克林,L.J。鲁宾和G. Simonneau
利益冲突:N.W.莫瑞尔的报告赠款和个人费用从形态发生-IX,提交作品之外。
利益冲突:在研究过程中,M.A.Aldred报告了NIH的拨款。
利益冲突:W.K.钟有没有透露。
利益冲突:C.G.埃利奥特报告的登记和数据安全,从Actelion公司监测指导委员会工作的个人费用从拜耳和Bellerophon的,补助和个人的费用,并且是终点裁判对肺癌LLC的顾问,支付给他的雇主(的Intermountain Healthcare)的费用,外提交作品。
利益冲突:W.C.尼科尔斯有没有透露。
利益冲突:F.索布里尔无需透露。
利益冲突:R.C.Trembath无需披露。
利益冲突:J.E.劳埃德有没有透露。
- 收到了2018年10月5日。
- 公认2018年10月9日。
- 版权©2019人队
这篇文章是开放存取并根据知识共享188滚球软件署名非商业许可证4.0的条款分发。