广告
研究文章心脏病学免费获取|10.1172 / JCI32503
一个抗增殖BMP-2 / PPARγapoE轴在人类和小鼠smc及其在肺动脉高压中的作用
Georg斯曼,1、2维尼乔a·佩雷斯·德·耶稣1Tero-Pekka Alastalo,1克里斯蒂娜·m·Alvira1克利斯朵夫Guignabert,1珍妮·m·Bekker1Stefan Schellong1隆Urashima,1菱王1尼古拉斯·w·莫雷尔3和玛琳因1
1斯坦福大学医学院的儿科,斯坦福,加州,美国。2儿科、加州大学旧金山分校、旧金山,加州,美国。3大学医学系的剑桥,剑桥,英国。
通信地址:玛琳因,维拉·默尔顿墙中心肺血管疾病,斯坦福大学医学院,CCSR大厦,2245室b, 269年校园开车,斯坦福,加州94305 - 5162,美国。电话:(650)723 - 8239;传真:(650)723 - 6700;电子邮件:marlener@stanford.edu。
1斯坦福大学医学院的儿科,斯坦福,加州,美国。2儿科、加州大学旧金山分校、旧金山,加州,美国。3大学医学系的剑桥,剑桥,英国。
通信地址:玛琳因,维拉·默尔顿墙中心肺血管疾病,斯坦福大学医学院,CCSR大厦,2245室b, 269年校园开车,斯坦福,加州94305 - 5162,美国。电话:(650)723 - 8239;传真:(650)723 - 6700;电子邮件:marlener@stanford.edu。
1斯坦福大学医学院的儿科,斯坦福,加州,美国。2儿科、加州大学旧金山分校、旧金山,加州,美国。3大学医学系的剑桥,剑桥,英国。
通信地址:玛琳因,维拉·默尔顿墙中心肺血管疾病,斯坦福大学医学院,CCSR大厦,2245室b, 269年校园开车,斯坦福,加州94305 - 5162,美国。电话:(650)723 - 8239;传真:(650)723 - 6700;电子邮件:marlener@stanford.edu。
1斯坦福大学医学院的儿科,斯坦福,加州,美国。2儿科、加州大学旧金山分校、旧金山,加州,美国。3大学医学系的剑桥,剑桥,英国。
通信地址:玛琳因,维拉·默尔顿墙中心肺血管疾病,斯坦福大学医学院,CCSR大厦,2245室b, 269年校园开车,斯坦福,加州94305 - 5162,美国。电话:(650)723 - 8239;传真:(650)723 - 6700;电子邮件:marlener@stanford.edu。
1斯坦福大学医学院的儿科,斯坦福,加州,美国。2儿科、加州大学旧金山分校、旧金山,加州,美国。3大学医学系的剑桥,剑桥,英国。
通信地址:玛琳因,维拉·默尔顿墙中心肺血管疾病,斯坦福大学医学院,CCSR大厦,2245室b, 269年校园开车,斯坦福,加州94305 - 5162,美国。电话:(650)723 - 8239;传真:(650)723 - 6700;电子邮件:marlener@stanford.edu。
1斯坦福大学医学院的儿科,斯坦福,加州,美国。2儿科、加州大学旧金山分校、旧金山,加州,美国。3大学医学系的剑桥,剑桥,英国。
通信地址:玛琳因,维拉·默尔顿墙中心肺血管疾病,斯坦福大学医学院,CCSR大厦,2245室b, 269年校园开车,斯坦福,加州94305 - 5162,美国。电话:(650)723 - 8239;传真:(650)723 - 6700;电子邮件:marlener@stanford.edu。
1斯坦福大学医学院的儿科,斯坦福,加州,美国。2儿科、加州大学旧金山分校、旧金山,加州,美国。3大学医学系的剑桥,剑桥,英国。
通信地址:玛琳因,维拉·默尔顿墙中心肺血管疾病,斯坦福大学医学院,CCSR大厦,2245室b, 269年校园开车,斯坦福,加州94305 - 5162,美国。电话:(650)723 - 8239;传真:(650)723 - 6700;电子邮件:marlener@stanford.edu。
1斯坦福大学医学院的儿科,斯坦福,加州,美国。2儿科、加州大学旧金山分校、旧金山,加州,美国。3大学医学系的剑桥,剑桥,英国。
通信地址:玛琳因,维拉·默尔顿墙中心肺血管疾病,斯坦福大学医学院,CCSR大厦,2245室b, 269年校园开车,斯坦福,加州94305 - 5162,美国。电话:(650)723 - 8239;传真:(650)723 - 6700;电子邮件:marlener@stanford.edu。
1斯坦福大学医学院的儿科,斯坦福,加州,美国。2儿科、加州大学旧金山分校、旧金山,加州,美国。3大学医学系的剑桥,剑桥,英国。
通信地址:玛琳因,维拉·默尔顿墙中心肺血管疾病,斯坦福大学医学院,CCSR大厦,2245室b, 269年校园开车,斯坦福,加州94305 - 5162,美国。电话:(650)723 - 8239;传真:(650)723 - 6700;电子邮件:marlener@stanford.edu。
1斯坦福大学医学院的儿科,斯坦福,加州,美国。2儿科、加州大学旧金山分校、旧金山,加州,美国。3大学医学系的剑桥,剑桥,英国。
通信地址:玛琳因,维拉·默尔顿墙中心肺血管疾病,斯坦福大学医学院,CCSR大厦,2245室b, 269年校园开车,斯坦福,加州94305 - 5162,美国。电话:(650)723 - 8239;传真:(650)723 - 6700;电子邮件:marlener@stanford.edu。
1斯坦福大学医学院的儿科,斯坦福,加州,美国。2儿科、加州大学旧金山分校、旧金山,加州,美国。3大学医学系的剑桥,剑桥,英国。
通信地址:玛琳因,维拉·默尔顿墙中心肺血管疾病,斯坦福大学医学院,CCSR大厦,2245室b, 269年校园开车,斯坦福,加州94305 - 5162,美国。电话:(650)723 - 8239;传真:(650)723 - 6700;电子邮件:marlener@stanford.edu。
4月1日出版,2008年更多信息
收到:2007年4月25日;接受:2008年2月6日
-
文摘
丧失突变在骨形态形成蛋白受体2 (BMP-RII)与肺动脉高血压(PAH);BMP-2 BMP-RII的配体,是负的SMC增长的监管机构。在这里,我们报告PPARγ之间的相互作用及其转录目标apoE BMP-2下游信号。BMP-2 / BMP-RII信号阻止PDGF-BB-induced扩散人类和鼠肺动脉smc (PASMCs)通过减少核phospho-ERK和诱导的DNA结合PPARγSmad1/5/8无关的磷酸化。BMP-2和PPARγ受体激动剂刺激生产和分泌的apoE smc。使用各种方法,包括短发夹RNAi人力PASMCs PAH patient-derived BMP-RII突变PASMCs, PPARγ拮抗剂,和PASMCs隔绝PPARγapoE-deficient老鼠,我们证明了抗增殖效果BMP-2 BMP-RII, PPARγ,apoE的依赖。此外,我们创建了小鼠目标删除PPARγsmc和PAH发展表明,他们自发的房车收缩压升高,房车肥大,增加muscularization远端肺动脉。因此,PPARγ-mediated事件可以防止PAH, PPARγ受体激动剂可能扭转PAH患者或无BMP-RII功能障碍。
-
介绍
骨形成蛋白2 (BMP-2)是- SMC增长的监管机构,但它的机制抵消扩散引起的生长因子(即。、PDGF-BB EGF)与肺动脉高血压(PAH) (1,2)还有待特征。Loss-of-function-mutations骨形态发生蛋白受体2 (BMP-RII)基因发生在50% - -60%的患者家庭多环芳烃(FPAH) (3- - - - - -5),10% - -20%的患者特发性肺动脉高压(IPAH),和6% - -9%的患者二次形式的多环芳烃与厌食症患者药物使用(氟苯丙胺衍生物)或先天性心脏病(APAH) (6,7)。然而,独立的一个突变,患者IPAH / FPAH(以前称为“主要PH值”),甚至那些APAH(以前称为“二级”PAH),尽管在较小程度上,减少了肺的表达BMP-RII (8)。因此,有可能环境修饰符和额外的基因的表达减少和功能BMP-RII与多环芳烃的发展。这或许暗示,有可能拯救不良后遗症的表达和antimitogenic信号降低BMP-RII通过操纵其下游效应器的优势。
两个潜在的下游效应器BMP-RII信号转录因子PPARγ及其假定的目标apoE (9)。有趣的是,这两个因素的mRNA表达,除了BMP-2,减少肺组织中PAH患者(8,10,11)。配体依赖性转录因子PPARs是属于核受体超家族。配体激活,PPARs二聚化类维生素a的X受体(RXR)和PPAR响应元素绑定(ppr)监管目标基因的启动子区域(12,13)。PPARs还可以与DNA结合的信号分子调节基因的表达独立(13)。例如,PPARγ损害磷酸化(即。,ERK激活)(14,15),一个下游PDGF-BB / PDGFR-βMAPK信号与SMC增殖和迁移(12)。
有支持的证据表明链接PPARγapoE的转录。一个功能PPARγ响应元素存在于apoE催化剂(9),有条件的破坏PPARγ基因(Pparg)在小鼠结果apoE表达减少巨噬细胞(16),PPARγ激活导致apoE mRNA表达和蛋白分泌脂肪细胞细胞系(17)。载脂蛋白e抑制PDGF-BB-mediated SMC增殖和迁移(18,19)通过绑定到低密度脂蛋白受体相关蛋白(单体)和内化PDGFR-β(20.,21)。加剧动脉PDGF-BB / MAPK信号在apoE不仅明显- / -老鼠(22),但也是肺血管疾病的主要临床特征底层PAH (2,23,24)。
我们最近发现,胰岛素抵抗apoE-deficient (apoE- / -多环芳烃)小鼠高脂饮食的发展。然而,这一事实PPARγ兴奋剂逆转多环芳烃在这个模型(25)表明,PPARγ目标独立抑制肺血管重建的apoE也很重要。抗糖尿病的药物罗格列酮和吡格列酮PPARγthiazolidinedione的配体(TZD)类,抑制PDGF-BB-induced SMC增殖和迁移在文化和在动物模型的系统性心血管疾病(引用文献综述。12)。由于这些额外的抗炎和proapoptotic PPARγ激活(引用文献综述的影响。12),PPARγ受体激动剂可能有用的多环芳烃在未来治疗。
首次在这里,我们报告我们的知识PPARγ和apoE法案的下游BMP-2 / BMP-RII主要细胞(人类和鼠肺动脉SMC [PASMCs]),防止在应对PDGF-BB SMC增殖。BMP-2-mediated PPARγ激活发生早于Smad1/5/8磷酸化,因此似乎是独立的信号建立轴BMP-RII下游。BMP-2诱发核phospho-ERK减少和快速PPARγ核穿梭与DNA结合,而PDGF-BB有相反的效果。BMP-2和PPARγ受体激动剂罗格列酮刺激生产和分泌PASMCs的载脂蛋白e。在人类使用短发夹RNAi PASMCs (HPASMCs) PASMCs FPAH患者和突变BMP-RII (W9X) PPARγ拮抗剂,和PASMCs缺乏PPARγ或载脂蛋白e,我们证明的抗增殖作用BMP-2 BMP-RII, PPARγ,apoE的依赖。与这些数据一致,我们表明,老鼠与删除PPARγsmc (SM22αCre PPARγ液氧/液氧老鼠)自发发展多环芳烃。综上所述,我们的研究结果揭示了小说PPARγ/ apoE轴的下游BMP-2暗示可以解释在HPASMCs BMP-RII激活的抗增殖作用。我们的数据也表明,PPARγ受体激动剂可能会扭转SMC增殖和血管重建的PAH患者或无BMP-RII功能障碍。
-
结果
额外的补充材料中提供的结果(与本文网上;doi: 10.1172 / JCI32503DS1)。
BMP-2-mediated抑制HPASMC扩散需要BMP-RII PPARγ,载脂蛋白e。长期人类BMP-RII基因沉默,我们构建了一个pLentivirus 6提供了一个集成的短发夹寡核苷酸针对人类BMP-RII的信使rna (shRNAi)。我们通过定量rt - pcr证实,85%稳定击倒BMP-RII mRNA shBMP-RIIi与shLacZi(控制)转染HPASMCs(补充图1)。重组BMP-2 (10 ng / ml)抑制PDGF-BB-induced扩散LacZi控制而不是shBMR-RIIi HPASMCs根据细胞计数(图1)。结果MTT扩散分析补充图2所示是一致的细胞计数。我们复制growth-inhibitory BMP-2的影响,相同的低浓度(10 ng / ml) BMP-4和7,虽然比BMP-2 BMP-7似乎有较弱的影响,4。此外,与siBMP-RII(降价),有更少的增长抑制BMP-2, 4和7(补充图3)。我们还证实,siBMP-RII废除BMP-2-induced Smad1/5/8的磷酸化(补充图4)。
 图1
图1
抗增殖效果BMP-2 (一个,C,D,F),PPARγ受体激动剂罗格列酮(Rosi;B)、载脂蛋白e (E)PDGF-BB-induced扩散的人类(一个,B,C,E)和小鼠(D和F)PASMCs。PASMCs被播种在2.5×104细胞每口井500年24-well板μl生长介质和一夜之间可以遵循。PBS的细胞被洗前的饥饿媒体(0.1%的边后卫)和孵化24小时(小鼠PASMCs)或48小时(HPASMCs)然后用PDGF-BB刺激(20 ng / ml)为72小时。BMP-2 (10 ng / ml),罗格列酮(1μM)和重组人类的载脂蛋白e(1 - 10μM)添加到静止细胞PDGF-BB刺激前30分钟。PPARγ拮抗剂GW9662(千瓦;1μM)添加添加BMP-2前24小时。细胞与PBS终于洗两次,使胰蛋白酶化,并计入血细胞计数器(4项)。细胞数量控制在时间点0 (CON)和72小时没有显著不同。一个:shLacZi HPASMCs转染与短发夹LacZi pLentivirus 6(控制);shBMP-RIIi, HPASMCs转染与短发夹pLentivirus 6 BMP-RIIi(即。,BMP-RII-deficient PASMCs)。D:同窝出生的,同窝出生仔畜控制PASMCs;SMC PPARγ- / -,PASMCs隔绝SM22αCre PPARγ液氧/液氧老鼠。F:C57BL / 6小鼠PASMCs控制;apoE- / -,PASMCs隔绝apoE-deficient老鼠。酒吧代表均值±SEM (n= 3一个,D,F;n= 4B和C;n= 6E;n= 12的控制一个)。*P< 0.05;* *P< 0.01;* * *P< 0.001表示;方差分析与Bonferroni多重比较检验。
然后,我们表明,BMP-2-mediated抑制PDGF-BB-induced HPASMC扩散不仅需要BMP-RII,而且PPARγ。首先,antimitogenic BMP-2效果可以复制PPARγ受体激动剂罗格列酮(1μM)(图1B)。第二,BMP-2的抗增殖效果是迷失在不可逆转的存在PPARγ拮抗剂GW9662(图1C)。最后,BMP-2-mediated PDGF-BB-induced抑制细胞增殖与删除没有观察到小鼠PASMCs PPARγ但被发现在同窝出生仔畜PASMCs控制(图1D)。为了解决PPARγ的效果是否可以由apoE的感应,我们首先确定生理剂量的重组apoE(10μM)完全阻塞PDGF-BB-induced HPASMCs扩散(图1E)。此外,growth-inhibitory BMP-2对PDGF-BB-induced细胞增殖的影响是迷失在PASMCs载脂蛋白E- / -老鼠(图1F)。综上所述,这些数据支持的一种新型抗增殖轴的下游BMP-2需要BMP-RII信号,PPARγ激活,和生产的载脂蛋白e,脂蛋白不是先前已知的合成了SMC。文档的apoE生产和分泌HPASMCs BMP-2和罗格列酮描述如下。
反对PDGF-BB效应和BMP-2 phospho-ERK HPASMCs PPARγ激活。我们下决定是否BMP-2和PDGF-BB可能反对影响phospho-ERK的亚细胞定位和PPARγ解释他们的功能在PASMCs对抗。PPARγ可以激活磷酸酶和防止血管smc (ERK的磷酸化14,15)。此外,PPARγ激活可以直接抑制PDGF-BB-mediated phospho-ERK活动(26)通过阻断核易位(27)。相反,PDGF-BB / PDGFR-β-mediated ERK的磷酸化导致磷酸化,从而失活PPARγ的N末端(28)。
PDGF-BB刺激增加3 - 5倍phospho-ERK1/2在核提取物和增长4倍phospho-ERK1胞质提取(图2A)。BMP-2,然而,导致迅速降低phospho-ERK1/2核提取物(图2B),在胞质提取物显著降低phospho-ERK2(图2B)。PDGF-BB迅速,即使是暂时性的减少核蛋白质和DNA结合PPARγ水平。这减少PPARγDNA结合(图2C,上半部分)暂时恰逢phospho-ERK1/2的迅速出现在细胞核PDGF-BB刺激(最大5 - 10分钟;图2)没有显著改变PPARγ水平在胞质提取物(图2PDGF-BB C)。相比之下,BMP-2诱导迅速和显著增加PPARγDNA结合(图2D)与核提取物中PPARγ蛋白水平升高的。这可能代表PPARγ稳定,但由于PPARγ往往与此同时降低细胞质中提取,瞬态核穿梭PPARγ也可能(图2D)。值得注意的是,BMP-2-mediated PPARγ激活HPASMCs(图2早些时候,B和D)发生磷酸化的Smad1/5/8(补充图4),因此phospho-Smad1/5/8似乎并不协调PPARγDNA结合。
 图2
图2
PDGF-BB (一个和C)和BMP-2 (B和D)反对在HPASMCs影响蛋白质含量phospho-ERK /总ERK (一个和B在核提取物(上),PPARγDNA结合板C和D),PPARγ蛋白在核和胞质提取物(较低的面板C和D)。细胞被刺激与PDGF-BB (20 ng / ml)或BMP-2 (10 ng / ml)中描述的传奇人物1。在不同的实验中,我们确定溶剂(DMSO,无菌水;1:10,000)结果的影响。介绍了西方免疫印迹和PPARγDNA结合化验方法。PPARγDNA结合分析,酒吧代表一式三份的±SEM中值测量1代表实验2 (C)和3 (D)独立实验相似的结果。蛋白质水平细胞分数、酒吧代表均值±SEM (n= 3 - 4)。*P< 0.05;* *P< 0.01和控制;方差分析与Dunnett因果检验。
有趣的是,当我们准备包含细胞质膜的细胞溶解产物总分数,我们发现BMP-2诱发快速ERK1/2磷酸化(补充图5 a)。这个分数缺席在核和胞质提取物制剂由于高自旋的步骤。我们通过免疫组织化学方法显示,伴随的快速减少phospho-ERK1/2在细胞核(西方免疫印迹,如图所示2B), BMP-2导致强烈phospho-ERK1/2染色在细胞质膜(补充图5 B)。以前在其他细胞,phospho-ERK绑定到细胞质膜蛋白受体等先进的糖化结束产品(29日)。
BMP-2和PPARγ受体激动剂抑制PDGF-BB HPASMCs信号。我们下一个决心BMP-2和PPARγ是否激活抑制PDGF-BB-induced MAPK通路(即。phospho-ERK1/2)。BMP-2抑制PDGF-BB-induced核和细胞质ERK磷酸化(图3A)。BMP-2也阻止PDGF-BB-mediated PPARγ抑制DNA结合。事实上增加PPARγ观察DNA结合和BMP-2尽管伴随PDGF-BB刺激(图3B)。此外,24小时预孵化与PPARγ受体激动剂罗格列酮显著降低和延迟PDGF-BB-induced ERK的磷酸化总细胞溶解产物(图3C)。因此,BMP-2和PPARγ受体激动剂罗格列酮作为功能性拮抗剂PDGF-BB信号通过抑制ERK1/2磷酸化。
 图3
图3
BMP-2和罗格列酮抑制PDGF-BB-mediated ERK的磷酸化(一个和C),并伴随BMP-2和PDGF-BB刺激增加PPARγDNA结合(B在HPASMCs)。细胞与BMP-2 preincubated (10 ng / ml) 30分钟(一个和B)或罗格列酮(1μM) 24小时(C),其次是PDGF-BB (20 ng / ml)刺激10分钟(一个和B)或5-60分钟。(C)西方免疫印迹和PPARγDNA结合化验方法和图中描述2。在细胞分数(蛋白质含量一个)或细胞溶解产物(C)、酒吧代表均值±SEM (n= 3)。在C与DMSO溶液相比,所有的样品都是控制。PPARγDNA结合试验(B),一式三份酒吧代表±SEM中值的测量1代表实验3独立实验相似的结果。*P< 0.05;* *P< 0.01和控制;方差分析与Dunnett因果检验。
罗格列酮块PDGF-BB-induced BMP-RII突变HPASMCs扩散。我们下一个调查PPARγ激活能否抑制PDGF-BB-induced HPASMCs扩散与BMP-RII功能丧失的突变。因此,我们孤立PASMCs肺移植的患者FPAH已知港BMP-RII移码突变。BMP-2抑制PDGF-BB-induced扩散在WT但不是BMP-RII突变HPASMCs(图4)。相比之下,PPARγ受体激动剂罗格列酮阻塞PDGF-BB-induced扩散WT和BMP-RII突变细胞,细胞数量在如果控制(图类似4)。BMP-2和罗格列酮使用的(低)的浓度,对基底细胞增殖率无显著影响(图4)。因此,PPARγ受体激动剂有潜力拯救growth-inhibitory BMP-2效果与BMP-RII PASMCs功能障碍。
 图4
图4
抗增殖效果BMP-2和PPARγ受体激动剂罗格列酮PDGF-BB-induced人类野生型和突变PASMCs BMP-RII扩散。控制PASMCs隔绝手术切除标本来源于病人接受全肺切除术治疗或疑似肺叶切除肿瘤。附加外围肺动脉(< 1 - 2毫米外径)获得一个病人接受心肺移植FPAH和已知港BMP-RII突变(W9X)。BMP-RII突变的性质,细胞分离、培养技术,和细胞计数方法和在图中描述1。HPASMCs孵化了48小时饥饿媒体(0.1%的边后卫)然后用PDGF-BB刺激(20 ng / ml)为72小时。BMP-2 (10 ng / ml)或罗格列酮(1μM)被添加到静止细胞PDGF-BB刺激前30分钟。酒吧代表均值±SEM (n= 3)。* *P< 0.01;* * *P< 0.001表示;方差分析与Bonferroni多重比较检验。PDGF-BB-stimulated细胞的数量明显高于未经处理的控制细胞(P< 0.001)。
BMP-2 HPASMCs罗格列酮诱导apoE表达和分泌。growth-inhibitory BMP-2不在的影响以来apoE-deficient PASMCs(图1F),我们假设apoE可能的转录目标BMP-2-activated PPARγsmc。事实上,BMP-2和罗格列酮诱导的载脂蛋白e蛋白表达(细胞溶解产物)和分泌(上层清液)在HPASMCs(图5)。此外,BMP-2-mediated upregulation PASMCs apoE蛋白质减少一半的收获SM22αCre PPARγ液氧/液氧老鼠(图5B)。这表明载脂蛋白e表达的诱导BMP-2 PPARγ在很大程度上是相关的。
 图5
图5
BMP-2 PASMCs PPARγ受体激动剂罗格列酮诱导的载脂蛋白e。(一个)的载脂蛋白e蛋白表达在细胞溶解产物(左)和载脂蛋白e蛋白分泌在上层清液(右)引起BMP-2 (10 ng / ml, 24小时)和罗格列酮(1μM, 24小时)检测到免疫印迹中描述的方法(对于细胞溶解产物,光密度值修正为平等加载使用α-tubulin)。apoE分泌,3 - 4细胞培养瓶/条件的媒体集中和集中的印迹显示(代表2独立实验相似的结果)。(B)BMP-2-induced (10 ng / ml, 24小时)的apoE upregulation鼠控制PASMCs PASMCs收获从减少一半SM22αCre PPARγ液氧/液氧老鼠。PASMCs分离得到5同窝出生仔畜控制和5SM22αCre PPARγ液氧/液氧小鼠中描述的方法。PASMCs从每个基因型被汇集和亚文化与BMP-2刺激之前。2独立实验的污点代表类似的结果。在细胞溶解产物(apoE蛋白质含量一个)、酒吧代表均值±SEM (n= 3)。*P< 0.05;* *P< 0.01和控制;未配对2-tailedt测试。
建立小鼠目标删除PPARγ动脉smc (SM22αCre PPARγ液氧/液氧)。探索PPARγ的vasoprotective作用在防止PAH的发展在一个完整的动物,我们调查了转基因小鼠与目标删除PPARγ动脉smc (SM22αCre PPARγ液氧/液氧)。我们记录,通过PCR,获得一个新的基因敲除成绩单(300个基点),几乎完全丧失的700 - bp在PASMCs野生型成绩单和主动脉隔绝SM22αCre PPARγ液氧/液氧老鼠(图6A)。野生型和淘汰赛成绩单在肺中被发现SM22αCre PPARγ液氧/液氧老鼠,因为除了smc的组织包含几个细胞类型。相比之下,只有野生型记录从同窝出生仔畜控制小鼠肺组织中发现(图6)。我们还证实淘汰赛PASMCs PPARγ蛋白质的SM22αCre PPARγ液氧/液氧老鼠(图6B)。BMP-2刺激的小鼠PPARγ-deficient PASMCs显示完整phospho-Smad1/5/8早些时候发生的信号(5 - 10分钟;图6比人类控制PASMCs C),在那里观察到30分钟(补充图4)。因此,建立BMP-2 / phospho-Smad1/5/8信号通路PPARγ似乎是独立的,因为它发生在与删除PPARγPASMCs(图6C)。
 图6
图6
老鼠的目标删除PPARγsmc维持BMP-2-induced pSmad1/5/8信号。(一个和B)与目标基因的老鼠删除PPARγsmc。(一个300 - bp) PCR反应显示获得的基因敲除成绩单和几乎完全丧失的700 - bp在PASMCs野生型成绩单和主动脉SM22αCre PPARγ液氧/液氧老鼠。在肺,其中包含smc也是许多其他细胞类型,记录中发现SM22αCre PPARγ液氧/液氧只老鼠,而野生型记录检测同窝出生仔畜控制老鼠。(B)西部免疫印迹PASMC溶解产物同窝出生仔畜和孤立SM22αCre PPARγ液氧/液氧(SMC PPARγ- / -)小鼠(n= 2)显示没有检测到PPARγ蛋白表达与控制细胞相比。(C)同窝出生仔畜控制和SMC PPARγ- / -PASMCs刺激了BMP-2 5-60分钟(10 ng / ml)中描述的传奇人物1,phospho-Smad 1/5/8蛋白表达,免疫印迹检测中所描述的方法(光密度值修正为平等在装货使用α-tubulin)。1的2代表实验数据显示了类似的结果。
与目标删除PPARγ小鼠动脉smc (SM22αCre PPARγ液氧/液氧)多环芳烃。SM22αCre PPARγ液氧/液氧老鼠房车收缩压升高(RVSP)室内空气相比,控件(29.0和21.5毫米汞柱;P< 0.001;图7)。系统性血压、(RV房车功能dP / dt最大和最小)和LV功能(部分缩短,射血分数)时,心输出量没有显著不同的比较(表2组1)。与高架RVSP作为多环芳烃,SM22αCre PPARγ液氧/液氧老鼠还会表现出房车肥大(RVH),根据房车重量的比率的LV和隔膜(0.46和0.26;P< 0.0001;图7B)和房车与体重的比例(P< 0001;表1)。SM22αCre PPARγ液氧/液氧老鼠同样数量的肺动脉每100肺泡(表1每个表面积)和(数据未显示),但显示出更多muscularized肺动脉在肺泡壁层,与同窝出生仔畜相比控制(图7一部)。小肺动脉肌肉增厚在肺部分从SMC PPARγ-deficient老鼠(Movat染色;图7证实了,D和E)与特定的抗体免疫组织化学α-SMA(图7F和G)和一个增强的信号和相关细胞增殖核抗原(PCNA);图7在PASMCs H和I)。LV舒张末期内径(LVIDD), LV舒张后壁厚度(LVPWd)和舒张末期室间隔厚度(IVSd) LV扩张和LV肥大(LVH)没有2基因型之间的不同(表1)。因此,LV功能障碍不占的多环芳烃SM22αCre PPARγ液氧/液氧老鼠。SM22αCre PPARγ液氧/液氧老鼠也有类似的比容和葡萄糖值但略白细胞计数高于控制(表1)。
 图7
图7
多环芳烃与目标删除老鼠PPARγsmc。13——导管插入术15-week-old老鼠进行了房车,紧随其后的是器官收获。(一个)RVSP测量,如描述的方法。(B右心室肥大(RVH),测量的重量比房车的LV +隔(RV / LV + S)中描述的方法。(C)Muscularization肺泡壁动脉(音乐。动脉Alv。墙),描述的方法。(D)代表肺组织的显微照片(彩色Movat pentachrome) 15-week-old小鼠显示一个典型的nonmuscular外围肺泡动脉同窝出生仔畜控制鼠标。(E一个类似的部分SM22αCre PPARγ液氧/液氧(SMC PPARγ- / -)鼠标显示了肺泡壁动脉周围肌肉的边缘。(F- - - - - -我)在串行肺组织免疫组织化学部分同窝出生仔畜控制(CON)和SMC PPARγ- / -老鼠α-SMA染色(F和G)和增殖细胞核抗原(PCNA);H和我)。箭在我表明增强PASMCs PCNA染色。参见表1。酒吧代表均值±SEM (n= 5)。* * *P< 0.001和控制;未配对2-tailedt测试。
-
讨论
这份报告是据我们所知的第一个标志,BMP-2 / BMP-RII的抗增殖作用(即信号在初级细胞。,P一个SMCs) can be attributed to activation of PPARγ and its putative transcription target apoE, a protein not previously known to be synthesized and secreted by SMCs (Figure8A)。此外,我们建立内源性表达PPARγsmc可以预防PAH的自发发展。我们的实验使用PPARγ拮抗剂和PPARγ-deficient PASMCs需要进一步证明PPARγBMP-2-mediated PDGF-BB PASMC增殖抑制诱导。利用RNAi和PASMCs BMP-RII已知功能丧失的突变,我们表明,BMP-2要求BMP-RII块SMC增殖并提供证据表明BMP-RII功能障碍发生有或没有BMP-RII突变(3,4)可能会导致无对手的促有丝分裂的SMC刺激PDGF-BB和其他生长因子(图8然而,B)。BMP-RII功能障碍可能获救的PPARγ受体激动剂如吡格列酮或罗格列酮(图8C),我们演示了PDGF-BB-stimulated BMP-RII变异HPASMCs。
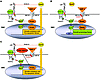 图8
图8
模型:一种新型抗增殖BMP-2 / PPARγapoE轴对多环芳烃的保护。这个模式包含描述的发现我们的文章和文学作为讨论的日期。(一个通过PPARγ和apoE) BMP-2抑制SMC增殖。apoE损害PDGF-BB / MAPK信号通过绑定到低密度脂蛋白受体相关蛋白(单体),从而启动内吞作用和退化的单体/ PDGFR-βPDGF-B复杂。PPARγ引发单体和其他growth-inhibitory / smc proapoptotic基因和抑制细胞循环和其他刺激基因如端粒酶,细胞周期蛋白D1和视网膜母细胞瘤蛋白。此外,PPARγ诱发可以直接灭活phospho-ERK磷酸酶。(B)BMP-RII障碍促进PAH SMC增殖和生存。加强PDGF-BB信号导致PAH的SMC增殖是一个关键的临床特征。缺乏apoE和提高部队的促有丝分裂的PDGF-BB / MAPK信号。丧失BMP-RII基因的突变会减少内源性PPARγ活动,导致无对手的MAPK信号、SMC增殖和生存,最终PAH的发展。TF,转录因子。(C)PPARγ受体激动剂可以拯救BMP-RII障碍和反向多环芳烃。PPARγ受体激动剂如罗格列酮和吡格列酮可能会扭转SMC增殖和血管重建的PAH患者或无BMP-RII障碍通过诱导apoE基因和其他growth-inhibitory / proapoptotic(表示),通过刺激基因的镇压(没有显示)。
在这项研究中,我们调查是否BMP-2和PDGF-BB可能反对影响growth-inhibitory转录因子PPARγ和刺激MAPK核phospho-ERK (30.)。我们观察到BMP-2激活PPARγHPASMCs独立phospho-Smad1/5/8通路,但与降低核phospho-ERK表情,大概由于磷酸酶PPARγ激活(14,15)或抑制phospho-ERK核易位(27)。相反,PDGF-BB / PDGFR-β-mediated感应与减少相关的核phospho-ERK PPARγDNA结合,可能由于磷酸化和失活PPARγ的N末端(28)和/或增强的核出口(31日)或泛素/ proteasome-mediated退化和快速PPARγ周转率(32)。因此,它可能是连续的内生BMP-2 / BMP-RII信号作为看门人是必要的,以防止失活PPARγ和核易位phospho-ERK PDGF-BB / PDGFR-β刺激的反应。
低剂量罗格列酮和生理剂量的重组apoE完全阻塞PDGF-BB-induced HPASMCs扩散,与以前的工作相一致系统性smc (12,33)。因为我们表明BMP-2和罗格列酮诱导apoE HPASMCs蛋白质合成和分泌,我们原因,除了降低phospho-ERK在细胞核,PPARγ-mediated诱导apoE抑制PDGF-BB / PDGFR-β信号(20.,21)。apoE的一些upregulation BMP-2甚至发生在PPARγ-deficient smc表明载脂蛋白e也可以由PPARγ-independent通路。进一步的研究使用的载脂蛋白e promoter-reporter化验会描绘PPARγ-mediated的本质这一目标基因的转录激活。
的自发的开发的多环芳烃SM22αCre PPARγ液氧/液氧老鼠是apoE相比我们的观察- / -老鼠在相似年龄发展PAH只有当喂高脂肪的食物导致胰岛素抵抗(25)。因为我们发现PPARγ受体激动剂罗格列酮可以完全颠覆apoE的多环芳烃- / -鼠标,多个其他PPARγ-dependent机制除了apoE感应可以防止PASMC增殖和生长因子多环芳烃的反应。在我们之前的研究中,我们认为的救助效果PPARγ激活增强脂联素的生产,一个能隔绝配体PDGF-BB adipocytokine,从而抑制SMC增殖和生存(34)。然而,我们无法在HPASMCs检测脂联素mRNA和蛋白表达。尽管如此,激活PPARγ可以诱导多种其他growth-inhibitory proapoptotic基因产物和抑制血管细胞(图刺激因素8C)。例如,PPARγ激活块PDGF基因表达(35)和引发单体的表达(36),所需的受体apoE-mediated抑制PDGF-BB信号(20.,21)(图8A和C)。PPARγ激活水平也会降低endothelin-1 (ET-1) (37)和内源性一氧化氮合酶抑制剂不对称dimethylarginine (ADMA) (38,39),与多环芳烃的病理学因素(39)。此外,激活细胞周期蛋白依赖性激酶抑制剂p27 PPARγ稳定KIP1(40)和抑制端粒酶活性(41)、视网膜母细胞瘤蛋白磷酸化(40),并最终G1相变,细胞循环发展,血管SMC增殖(40)。通过阻断激活PDGFR-β的重要生存通路下游,即。PI3K (42),PPARγ受体激动剂也导致细胞凋亡增殖血管细胞(12,43)。此外,众所周知,PPARγ配体损害生产基质金属蛋白酶(44),可以由弹性蛋白酶激活(45)。我们小组已经表明,抑制蛋白水解的级联不仅可以防止反转先进致命的多环芳烃在大鼠(46)。
先前的研究显示BMP-2有利影响(47),PPARγ激活(引用文献综述。12)、载脂蛋白e (18,19)在预防系统性血管病理,但我们的观察是第一个迹象据我们所知,所有3因素有关。最近,PPARγ之间的连接和载脂蛋白e在阿尔茨海默病的患者,与罗格列酮,认知功能的改善不明显的患者携带apoEε4等位基因(48)。因此,这部小说轴我们描述可能相关的解决机制,构成许多不同的病理过程。
总之,我们的数据揭示了小说PPARγ/ apoE轴下游HPASMCs BMP-2信号。未能激活PPARγ回应BMP-2 BMP-RII障碍时可以将病人的风险PAH的开发或发展。我们建议PPARγ受体激动剂可能拯救BMP-RII障碍和反向SMC增殖和血管重建PAH患者甚至可能有用的抗增殖药物在患者没有BMP-RII功能障碍。
-
方法
更多和更详细的方法提供的补充材料。
建立与目标删除PPARγ小鼠动脉smc使用Cre-loxP系统。我们杂交SM22αpromoter-driven Cre-transgenic小鼠PPARγ纯合子液氧老鼠。两株从杰克逊实验室获得,十字架了SM22αCre PPARγ液氧/液氧(SMC PPARγ- / -老鼠)。后代基因型测定PCR(见补充方法)。PCR条件和引物可从杰克逊实验室的信息。下面描述的实验涉及PASMC隔离和亚文化,apoE-deficient (B6.129P2-Apoetm1Unc / J)和控制C57BL / 6小鼠购自杰克逊实验室。
基因分型/ rt - pcr分析。检测的删除PPARγ第1外显子和外显子2,两个引物设计和位于外显子A1和外显子4的Pparg1rt - pcr基因识别的长篇(700个基点)和重组mRNA(300个基点),(如前所述)(49)(引物PCR协议,见补充方法)。总RNA提取PASMCs、主动脉和肺有三zol试剂(表达载体)。PASMCs得到的肺动脉SM22αCre PPARγ液氧/液氧老鼠和同窝出生仔畜控制老鼠和培养10天。然后从细胞被反向转录RNA样本使用上标三世逆转录酶工具包(表达载体)。使用Taq DNA聚合酶PCR应用于cDNA工具包(表达载体),并记录运行在1%琼脂糖凝胶。
慢病毒shRNAi人类BMP-RII的基因沉默。长期基因沉默的BMP-RII HPASMCs,我们构建了一个pLentivirus 6和一个集成的短发夹寡核苷酸针对人类BMP-RII的信使rna,使用诱导H1 RNAi条目矢量工具和一个慢病毒RNAi表达系统工具包(K4920-00 K4943-00;表达载体)所描述的制造商(详情,请参见补充方法)。慢病毒是由细胞和传播在293英尺,和HPASMCs转染中描述的补充方法。12天的杀稻瘟菌素的选择后,我们确认了85%稳定的人类BMP-RII击倒而shLacZi控制HPASMCs(补充图1)和继续进一步的实验。
细胞培养。主要鼠PASMCs是从13到15-week-old apoE孤立的- / -和C57BL / 6小鼠,以及SM22αCre PPARγ液氧/液氧和同窝出生仔畜控制老鼠,使用修改后的弹性蛋白酶、胶原酶消化协议(如前所述)(50)。主要HPASMCs购自级联生物制剂。此外,控制PASMCs隔绝手术切除标本来自一个病人接受全肺切除术治疗或疑似肺叶切除肿瘤。额外PASMCs获得从一个病人接受心肺移植FPAH和已知港BMP-RII的突变(W9X),(如前所述)(51)。BMP-RII突变的性质,介绍了细胞分离和培养技术补充方法。
细胞增殖检测。测定细胞数量,PASMCs被播种在2.5×104细胞每口井500年24-well板μl生长介质和一夜之间可以遵循。中被删除和细胞洗3次与PBS除了饿死前媒体(DMEM, 0.1%的边后卫,青霉素和链霉素)和孵化37°C, 5%的公司224小时(小鼠PASMCs)或48小时前(HPASMCs) PDGF-BB刺激(20 ng / ml) 72小时(治疗和浓度图传说)。媒体有或没有生长因子和/或抑制剂是改变每24小时。细胞与PBS洗两次,并在150年使胰蛋白酶化μl胰蛋白酶/ EDTA 7分钟,其次是增加150μl胰蛋白酶中和剂(级联生物制剂)。细胞被resuspended和计算血细胞计数器(每3 - 6井条件下,4项每)。生化MTT细胞增殖测定(写明ATCC)中描述的补充方法。在细胞增殖的研究中,BMP-2 (10 ng / ml;Sigma-Aldrich),罗格列酮(1μM;Alexis)或重组人类的载脂蛋白e(1 - 10μM;Chemicon)添加到静止细胞促有丝分裂的刺激与PDGF-BB(前30分钟20人,ng / ml;研发系统)为72小时。 The PPARγ antagonist GW9662 (1 μM; Cayman) was added 24 hours prior to the addition of BMP-2. The media with or without growth factors and/or inhibitors was changed every 24 hours.
蛋白表达和区划的本地化。小鼠和人类PASMCs(野生型、shLacZi控制或shBMP-RIIi)增长到70%融合和饥饿培养媒体(DMEM, 0.1%的边后卫,100 U /毫升青霉素,链霉素0.1毫克/毫升;Gibco;分别表达载体)24和48小时。PDGF-BB, BMP-2、载脂蛋白e或罗格列酮是添加到静止细胞5-60分钟和24小时(治疗和浓度表示的图传说)。除了总细胞溶解产物,亚细胞分数(核矩阵,核提取物、胞质提取)是准备使用修改后的低盐和高盐协议(如前所述)(52)。详情,请参见补充方法。
载脂蛋白e蛋白的分泌。静HPASMCs培养在T75细胞培养烧瓶(75厘米血压得到较好的控制2)最小覆盖媒体(1毫升),然后用BMP-2刺激(10 ng / ml)或罗格列酮(1μM) 24小时。浮在表面的媒体收集从3细胞培养瓶/条件,集中,集中使用一个Amicon-4 Centriprep设备(微孔)。蛋白质提取然后准备中描述的补充方法,和20每示例加载μg蛋白质sds - page免疫印迹(表达载体)。
西方的免疫印迹。制备亚细胞分数(核矩阵,核提取物、胞质提取)和全细胞溶解产物(蛋白质提取物)和免疫印迹技术中所描述的补充方法。主要抗体phospho-ERK1/2, ERK 1/2, phospho-Smad1/5/8 Smad1(所有细胞信号技术),PPARγ(圣克鲁斯生物技术有限公司)、载脂蛋白e (Abcam) BMP-RII (BD生物科学- Pharmingen),和α-tubulin (Sigma-Aldrich)。
PPARγDNA结合分析。一个多路复用DNA结合转录因子分析(Marligen生物科学)如前所述执行(53)。短暂,核提取物被孵化的生物素化的DNA探针不同的转录因子结合位点(例如,PPARγ,5′-TGACCTTTGACCTAGAA-3′),每个包含一个独特的单链序列作为捕获标签。转录因子结合反应后,样本孵化与专用试剂消化任何DNA探针不绑定到转录因子。反应被孵化与含有可怕地独特的珠集的混合,和完整的生物素化的调查被捕获到相应的焊道表面capture-tag和anti-tag序列相互作用。珠子被清洗和streptavidin-PE使用滤板和彩色。与转录因子结合位点相关联的荧光信号局部表面的幽灵似地不同的珠子用luminex - 100测量仪器。每个反应进行了一式三份,300年取得了不同的数据分样本进行分析。
实验设计研究的转基因小鼠。SM22αCre PPARγ液氧/液氧或同窝出生仔畜控制老鼠维持在普通食物免费获取饮用水。所有研究进行了13 - 15-week-old老鼠在斯坦福大学的协议动物保健委员会批准后美国生理协会的指导方针。
血流动力学测量。RVSP和房车dP / dt测量中执行15-week-old nonventilated小鼠异氟烷麻醉下(1.5% - -2.5%,2 l O21.4 /分钟)插入一个F导管(米勒仪器)通过右颈静脉如前所述(25)。nonanesthetized系统性血压测定,14 - 15-week-old老鼠的尾巴袖口方法使用BP 2000分析系统(Visitech系统)。心输出量和功能测定在13到15-week-old小鼠异氟烷麻醉下超声心动图(1%,1 l O2/分钟)和超声波机(生动的7;通用电气医疗系统)使用13-MHz线性阵列传感器(见补充方法)。
RVH LVH。RVH测量如前所述(54),房车的重量相对于LV +隔。LVH测量的绝对重量LV +隔相对于体重。LV扩张是由超声心动图评估M-mode LVIDD的测量。
肺组织准备。与生理盐水灌注肺,一夜之间在10%福尔马林固定,然后嵌入石蜡常规组织学(圆)、弹性蛋白van Gieson Movat pentachrome),(如前所述)(25,54)。左肺的一个子集(大约一半)注射barium-gelatin通过肺artery-inserted油管(25)标签边缘的形态学分析肺动脉(见补充方法)。
的形态学分析。Barium-injected,横向左肺一步部分是由弹性蛋白染色的范Gieson方法。从所有的老鼠,我们把相同的全剖面的明显barium-injected左肺门平行和嵌入式它以同样的方式。肺动脉muscularization评估×400放大通过计算的比例完全和部分muscularized外围(肺泡壁)肺动脉总外周肺动脉5随机领域(1场=×200放大)。肺泡壁的总数的比例和动脉导管被表示为每100人肺动脉肺泡数量和每个表面积的肺动脉数量(5×200放大随机字段)。大约1000个肺泡被数/动物。所有测量是由调查人员盲基因型和条件。
免疫组织化学。石蜡包埋的部分通过分级deparaffinized二甲苯和水化酒精。抗原进行检索使用heat-mediated抗原决定基检索方法通过加热部分的柠檬酸缓冲(10毫米柠檬酸钠,0.05% Tween-20, pH值6.0)10分钟95°C,然后允许部分冷却至室温。与主要抗体特定部分被孵化PCNAα-SMA (Abcam)一夜之间在4°C。染色当时完成使用Vectastain精英ABC工具包(向量实验室)根据制造商的指示,使用3,3-diaminobenzidine作为过氧化物酶的底物,并与苏木精复染色。
禁食遗传损伤测量。尾静脉穿刺,nonanesthetized overnight-starved老鼠,随后立即复制遗传葡萄糖测量一个自由式;Abbott),排除任何影响SMC-targeted PPARγ击倒在葡萄糖止血。额外的血液通过心脏穿刺后血流动力学测量。白细胞计数和比容被斯坦福大学动物设施评估实验室(见补充方法)。
统计数据。从多个实验值表示为±SEM。统计学意义是决定使用1路的方差分析。当只有两组比较,统计与未配对2-tailed差异进行评估t测试。一个P值小于0.05被认为是重要的。每组样本或动物的数量显示在图的传说。
-
确认
我们感谢皮特克劳森(Marligen生物科学)帮助与多路复用DNA结合试验和数据分析。这项工作是支持的博士后奖学金从美国心脏协会/肺动脉高压协会g·汉斯曼(0425943小时);美国国立卫生研究院(1-R01-HL074186-01)和德怀特·维拉Dunlevie赋予教授m .发布;国家心脏、肺和血液研究所国家研究服务奖J.M. Bekker (2-T32-HL007708-14);和博士前的奖学金美国Schellong勃林格殷格翰集团资金。西北莫雷尔接到英国心脏基金会赠款资金。
-
脚注
使用非标准缩写:BMP-2,骨形成蛋白2;BMP-RII,骨形态发生蛋白受体二世;FPAH家族多环芳烃;人类PASMC HPASMC,;多环芳烃、肺动脉高血压;PASMC肺动脉SMC;RVSP,房车收缩压。
利益冲突:作者宣称没有利益冲突的存在。
参考信息:j .中国。投资。118年:1846 - 1857 (2008)。doi: 10.1172 / JCI32503
-
引用
- Merklinger, S.L.琼斯,P.L.,Martinez, E.C., Rabinovitch, M. 2005. Epidermal growth factor receptor blockade mediates smooth muscle cell apoptosis and improves survival in rats with pulmonary hypertension.循环。112年:423 - 431。
- Schermuly,保留时间,等。2005。PDGF抑制实验性肺动脉高压的逆转。j .中国。投资。115年:2811 - 2821。
- 车道,K.B.,et al. 2000. Heterozygous germline mutations in BMPR2, encoding a TGF-beta receptor, cause familial primary pulmonary hypertension. The International PPH Consortium.Nat,麝猫。26:81 - 84。
- 邓,Z。,et al. 2000. Familial primary pulmonary hypertension (gene PPH1) is caused by mutations in the bone morphogenetic protein receptor-II gene.点。j .的嗡嗡声。麝猫。67年:737 - 744。
- 纽曼,J.H.,et al. 2004. Genetic basis of pulmonary arterial hypertension: current understanding and future directions.j。科尔。心功能杂志。43:33 s-39s。
- 亨伯特,M。,et al. 2002. BMPR2 germline mutations in pulmonary hypertension associated with fenfluramine derivatives.欧元。和。J。20.:518 - 523。
- 罗伯茨动向,et al. 2004. BMPR2 mutations in pulmonary arterial hypertension with congenital heart disease.欧元。和。J。24:371 - 374。
- 阿特金森,C。,et al. 2002. Primary pulmonary hypertension is associated with reduced pulmonary vascular expression of type II bone morphogenetic protein receptor.循环。105年:1672 - 1678。
- Galetto, R。,et al. 2001. Identification of a peroxisome-proliferator-activated-receptor response element in the apolipoprotein E gene control region.物化学。J。357年:521 - 527。
- Ameshima, S。,et al. 2003. Peroxisome proliferator-activated receptor gamma (PPARgamma) expression is decreased in pulmonary hypertension and affects endothelial cell growth.中国保监会,Res。92年:1162 - 1169。
- Geraci,分子量,et al. 2001. Gene expression patterns in the lungs of patients with primary pulmonary hypertension: a gene microarray analysis.中国保监会,Res。88年:555 - 562。
- 马克思,N.N.,Duez, H.H., Fruchart, J.C., Staels, B.B. 2004. Peroxisome proliferator-activated receptors and atherogenesis: regulators of gene expression in vascular cells.中国保监会,Res。94年:1168 - 1178。
- Gilde,抗干扰,Fruchart, J.C., Staels, B. 2006. Peroxisome proliferator-activated receptors at the crossroads of obesity, diabetes, and cardiovascular disease.j。科尔。心功能杂志。48:A24-A32。
- Benkirane, K。Amiri F。,Diep, Q.N., El Mabrouk, M., Schiffrin, E.L. 2006. PPAR-gamma inhibits ANG II-induced cell growth via SHIP2 and 4E-BP1.点。j .杂志。心中国保监会。杂志。290年:H390-H397。
- Wakino, S。,et al. 2001. Peroxisome proliferator-activated receptor gamma ligands inhibit mitogenic induction of p21(Cip1) by modulating the protein kinase Cdelta pathway in vascular smooth muscle cells.生物。化学。276年:47650 - 47657。
- 秋山,式样,et al. 2002. Conditional disruption of the peroxisome proliferator-activated receptor gamma gene in mice results in lowered expression of ABCA1, ABCG1, and apoE in macrophages and reduced cholesterol efflux.摩尔。细胞。医学杂志。22:2607 - 2619。
- 悦,L。,Rasouli, N., Ranganathan, G., Kern, P.A., Mazzone, T. 2004. Divergent effects of peroxisome proliferator-activated receptor gamma agonists and tumor necrosis factor alpha on adipocyte ApoE expression.生物。化学。279年:47626 - 47632。
- 泽里尼,M。,Swertfeger, D.K., Weisgraber, K.H., Hui, D.Y. 2002. Distinct apolipoprotein E isoform preference for inhibition of smooth muscle cell migration and proliferation.生物化学。41:11820 - 11823。
- Ishigami, M。,Swertfeger, D.K., Granholm, N.A., Hui, D.Y. 1998. Apolipoprotein E inhibits platelet-derived growth factor-induced vascular smooth muscle cell migration and proliferation by suppressing signal transduction and preventing cell entry to G1 phase.生物。化学。273年:20156 - 20161。
- 鲍彻,P。,Gotthardt, M., Li, W.P., Anderson, R.G., Herz, J. 2003. LRP: role in vascular wall integrity and protection from atherosclerosis.科学。300年:329 - 332。
- 牛顿、C.S.,et al. 2005. Platelet-derived growth factor receptor-beta (PDGFR-beta) activation promotes its association with the low density lipoprotein receptor-related protein (LRP). Evidence for co-receptor function.生物。化学。280年:27872 - 27878。
- 斯莱虽然,M。,et al. 2004. Imatinib attenuates diabetes-associated atherosclerosis.Arterioscler。Thromb。Vasc。医学杂志。24:935 - 942。
- 亨伯特,M。,et al. 1998. Platelet-derived growth factor expression in primary pulmonary hypertension: comparison of HIV seropositive and HIV seronegative patients.欧元。和。J。11:554 - 559。
- Ghofrani, H.A.西格,W。,Grimminger, F. 2005. Imatinib for the treatment of pulmonary arterial hypertension.心血管病。j .地中海。353年:1412 - 1413。
- 斯曼,G。,et al. 2007. Pulmonary arterial hypertension is linked to insulin resistance and reversed by peroxisome proliferator-activated receptor-gamma activation.循环。115年:1275 - 1284。
- Ghosh、轮,et al. 2003. PPARgamma ligand attenuates PDGF-induced mesangial cell proliferation: role of MAP kinase.肾脏Int。64年:52 - 62。
- 戈艾滋,S。,et al. 2001. Peroxisome proliferator-activated receptor-gamma ligands inhibit nuclear but not cytosolic extracellular signal-regulated kinase/mitogen-activated protein kinase-regulated steps in vascular smooth muscle cell migration.j . Cardiovasc。杂志。38:909 - 921。
- 胡,E。,Kim, J.B., Sarraf, P., Spiegelman, B.M. 1996. Inhibition of adipogenesis through MAP kinase-mediated phosphorylation of PPARgamma.科学。274年:2100 - 2103。
- 石原,K。,Tsutsumi, K., Kawane, S., Nakajima, M., Kasaoka, T. 2003. The receptor for advanced glycation end-products (RAGE) directly binds to ERK by a D-domain-like docking site.2月。550年:107 - 113。
- Sarjeant, J.M.,et al. 2003. Apolipoprotein D inhibits platelet-derived growth factor-BB-induced vascular smooth muscle cell proliferated by preventing translocation of phosphorylated extracellular signal regulated kinase 1/2 to the nucleus.Arterioscler。Thromb。Vasc。医学杂志。23:2172 - 2177。
- Burgermeister E。,等。2007。与MEK的差别会导致核出口和对这些交互过氧物酶体proliferator-activated受体γ。摩尔。细胞。医学杂志。27:803 - 817。
- 弗洛伊德,Z.E.,Stephens, J.M. 2002. Interferon-gamma-mediated activation and ubiquitin-proteasome-dependent degradation of PPARgamma in adipocytes.生物。化学。277年:4062 - 4068。
- Ishigami, M。,et al. 2000. Apolipoprotein E inhibition of vascular smooth muscle cell proliferation but not the inhibition of migration is mediated through activation of inducible nitric oxide synthase.Arterioscler。Thromb。Vasc。医学杂志。20.:1020 - 1026。
- Arita Y。,et al. 2002. Adipocyte-derived plasma protein adiponectin acts as a platelet-derived growth factor-BB-binding protein and regulates growth factor-induced common postreceptor signal in vascular smooth muscle cell.循环。105年:2893 - 2898。
- 张,J。傅,M。,Zhao, L., Chen, Y.E. 2002. 15-Deoxy-prostaglandin J(2) inhibits PDGF-A and -B chain expression in human vascular endothelial cells independent of PPAR gamma.物化学。Biophys。Commun >,298年:128 - 132。
- 附近,一个。,Vassiliou, G., Benoist, F., McPherson, R. 2003. Adipocyte low density lipoprotein receptor-related protein gene expression and function is regulated by peroxisome proliferator-activated receptor gamma.生物。化学。278年:11945 - 11953。
- Martin-Nizard F。,等。2002。过氧物酶体proliferator-activated受体激活物抑制氧化低密度lipoprotein-induced endothelin-1在内皮细胞分泌。j . Cardiovasc。杂志。40:822 - 831。
- Wakino, S。,et al. 2005. Pioglitazone lowers systemic asymmetric dimethylarginine by inducing dimethylarginine dimethylaminohydrolase in rats.Hypertens。Res。28:255 - 262。
- Kielstein, j.t,等。2005。不对称dimethylarginine特发性肺动脉高血压。Arterioscler。Thromb。Vasc。医学杂志。25:1414 - 1418。
- Wakino, S。,et al. 2000. Peroxisome proliferator-activated receptor gamma ligands inhibit retinoblastoma phosphorylation and G1--> S transition in vascular smooth muscle cells.生物。化学。275年:22435 - 22441。
- 小川,D。,et al. 2006. Activation of peroxisome proliferator-activated receptor gamma suppresses telomerase activity in vascular smooth muscle cells.中国保监会,Res。98年:e50-e59。
- Vantler, M。,Caglayan, E., Zimmermann, W.H., Baumer, A.T., Rosenkranz, S. 2005. Systematic evaluation of anti-apoptotic growth factor signaling in vascular smooth muscle cells. Only phosphatidylinositol 3′-kinase is important.生物。化学。280年:14168 - 14176。
- Bruemmer D。,et al. 2003. Regulation of the growth arrest and DNA damage-inducible gene 45 (GADD45) by peroxisome proliferator-activated receptor gamma in vascular smooth muscle cells.中国保监会,Res。93年:e38-e47。
- 沃利,jr,et al. 2003. Metalloproteinase expression in PMA-stimulated THP-1 cells. Effects of peroxisome proliferator-activated receptor-gamma (PPAR gamma) agonists and 9-cis-retinoic acid.生物。化学。278年:51340 - 51346。
- 敌人,H。,Enghild, J.J., Suzuki, K., Salvesen, G. 1990. Stepwise activation mechanisms of the precursor of matrix metalloproteinase 3 (stromelysin) by proteinases and (4-aminophenyl)mercuric acetate.生物化学。29日:5783 - 5789。
- 考恩,K.N.,et al. 2000. Complete reversal of fatal pulmonary hypertension in rats by a serine elastase inhibitor.Nat,地中海。6:698 - 702。
- Nakaoka, T。,et al. 1997. Inhibition of rat vascular smooth muscle proliferation in vitro and in vivo by bone morphogenetic protein-2.j .中国。投资。One hundred.:2824 - 2832。
- Risner、,et al. 2006. Efficacy of rosiglitazone in a genetically defined population with mild-to-moderate Alzheimer’s disease.药物基因组学J。6:246 - 254。
- Hevener, A.L.,et al. 2003. Muscle-specific Pparg deletion causes insulin resistance.Nat,地中海。9:1491 - 1497。
- Fouty, B.W.,et al. 2001. p27(Kip1) is important in modulating pulmonary artery smooth muscle cell proliferation.点。j .和。细胞摩尔。生物。25:652 - 658。
- 杨,X。,Lee, P.J., Long, L., Trembath, R.C., Morrell, N.W. 2007. BMP4 induces HO-1 via a Smad-independent, p38MAPK-dependent pathway in pulmonary artery myocytes.点。j .和。细胞摩尔。生物。37:598 - 605。
- 米塔尼,Y。,扎伊迪,萨达姆政权,Dufourcq, P., Thompson, K., Rabinovitch, M. 2000. Nitric oxide reduces vascular smooth muscle cell elastase activity through cGMP-mediated suppression of ERK phosphorylation and AML1B nuclear partitioning.美国实验生物学学会联合会J。14:805 - 814。
- Shurin,逝者,et al. 2005. Loss of new chemokine CXCL14 in tumor tissue is associated with low infiltration by dendritic cells (DC), while restoration of human CXCL14 expression in tumor cells causes attraction of DC both in vitro and in vivo.j . Immunol。174年:5490 - 5498。
- 扎伊迪,萨达姆政权,你,X.M.、Ciura年代。,Husain, M., Rabinovitch, M. 2002. Overexpression of the serine elastase inhibitor elafin protects transgenic mice from hypoxic pulmonary hypertension.循环。105年:516 - 521。
-
版本历史
- 第1版(2008年4月1日):没有描述
- 第2版(2008年5月1日):没有描述




