文摘
世界卫生组织(WHO)建议各国实施药物警戒和收集信息在活跃的药物安全监测(aDSM)和不良事件的管理。
这项前瞻性研究的目的是评估不良事件的频率和强度,抗结核(TB)在连续的结核病患者药物治疗的新(即。bedaquiline delamanid)和改造(即。基于药物氯法齐明,linezolid) aDSM项目。前瞻性地收集了不良事件归因到一个特定的药物与人口后,细菌、放射学和临床信息在诊断和治疗。这个临时分析包括患者完成或还在处理数据收集的时间。
45来自26个国家/地区的中心报道,全球658名患者(68.7%的男性,4.4%的艾滋病毒感染)治疗如下:与bedaquiline 87.7%, 18.4% delamanid (6.1%), 81.5% linezolid和32.4%氯法齐明。总体而言,504副反应事件被报道:447(88.7%)归类为小(1 - 2年级)和57例(11.3%)(3 - 5年级)那么严重。大多数57严重不良事件报告55例(51 57,89.5%)最终解决。患者报告严重不良事件,一些药物停用:负责bedaquiline 0.35%(两个577),delamanid 0.8%(121年的),linezolid 1.9%(10 536)和氯法齐明在1.4%(213)的患者。严重不良事件报告了6.9%(131)的阿米卡星,患者的0.4%(221年的)乙硫异烟胺/ prothionamide, 2.8% (15 536) linezolid和1.8%(498)的环丝氨酸/ terizidone。
aDSM研究提供有价值的信息,但实现需要扩大支持病人护理。
文摘
以前的不良事件是可以从单一研究证据。这个全球项目(来自26个国家的658名患者)演示了aDSM是可行的和推荐的药物严重不良事件相当低(整体57 504,11.3%)。http://bit.ly/2kzvbqe
介绍
> 558 000例由世界卫生组织(世卫组织)估计2017年(1),利福平,耐多药结核病(mdr - tb)是一种临床和公共卫生的优先级1,2]。从公共健康的角度来看,必须防止耐药菌株的选择结核分枝杆菌药物敏感结核病患者的有效治疗和减少耐药菌株的传播迅速和有效地诊断和治疗他们3]。耐多药和广泛耐药的临床管理(XDR)一样,是昂贵的和医学上具有挑战性:临床医生只剩下更少的有效药物,从而导致更频繁的严重不良事件比用于药物敏感结核病的治疗(1,2,4,5]。自全球方法的实现与二线药物治疗耐多药结核病(称为“点+”策略)(4)、监视、记录和报告的不良事件变得更为重要。
近年来,新(即。delamanid和bedaquiline)和改造,介绍了抗结核药物治疗耐多药结核病[2]。Bedaquiline最近被包含在耐多药结核病的新分类(6,7优先)药物(a组)后,越来越多的证据表明,疗效和耐受性8- - - - - -14]。Delamanid是在C组(附加代理)(6),一个有前途的安全性(15- - - - - -18]。
这些抗结核药物(6,19]linezolid [20.,21和氟喹诺酮类原料药19已经包含在A组,氯法齐明在B组(22)和imipenem / meropenem在C组(23- - - - - -25),主要基于有效性研究、毒性和编程方面的考虑。
尽管更多的证据变得可以从抗结核药物毒性试验和观察性研究,全球活动性结核病药物安全监测和管理不良事件(aDSM)下面是失踪的信息:1)新药;2)linezolid和氯法齐明;3)药物组合包括药物如bedaquiline delamanid氯法齐明和氟喹诺酮类原料药,增加心电图QT间隔(可能危及生命的心律失常)26,27];d)阿米卡星(C组和其他second-line-injectable药物)、环丝氨酸/ terizidone (B组)、乙硫异烟胺/ prothionamide para-aminosalycilic酸(PAS)、乙胺丁醇、吡嗪酰胺(C组)和高dose-isoniazid [6,19]。
世卫组织建议药物警戒和aDSM,邀请国家结核病规划实施“积极的、系统的临床和实验室的评估患者治疗新的结核病药物,或新的耐多药结核病疗法以检测和报告潜在或证实药物毒性”(28- - - - - -30.]。
今天,没有全球研究报告基于潜在的抗结核药物不良事件aDSM方法患者包括新药bedaquiline delamanid和特制药物如linezolid和氯法齐明。
这种方法有可能通过全球结核病网络(31日),最近报道的研究设计首先aDSM项目最初涉及27个国家(30.]。
目前基于寄存器的研究的目的是前瞻性评估不良事件的频率和强度将在一群抗结核药物连续结核病患者接受新的和改造药物在26个国家的原则和方法aDSM项目(28- - - - - -30.,32]。我们总结一个临时的结果分析的患者完成或还在治疗时的数据收集。
方法
研究设计
试点研究是2015年实施评估项目的可行性和实用程序以及数据流进行预测和分析。研究协调中心的伦理委员会批准7月11日,2017年。研究提出了临床中心或国家结核病规划参与网络。每个中心或国家签署了一项与协调中心和机密性和数据共享协议获得当地伦理委员会批准或放弃表示没有伦理批准由于地方性法规要求。
从2017年7月,参与中心签署了项目之后,所有连续患者(包括儿童和青少年)接受治疗bedaquiline和/或delamanid为基于他们的药物暴露30.]。没有特定的病人采用排除标准选择。墨西哥、巴拉圭、西班牙、斯洛伐克和苏丹开始报道第一例在全国发起bedaquiline和/或delamanid抗结核治疗。
任何药物不良事件的参与治疗方案的前瞻性收集,确保一个概率因果关系分配机制(如。不良事件的归因到一个特定的药物根据其循证资料)。每个临床单位参与这项研究有一个consilium-like不良事件的管理机制(5]。所有不良事件和提出归因到一个或多个特定的药物是由国际协调小组讨论和修订报告医生。可用的科学证据在研究期间开车特定药物不良事件的归因基于概率的方法。任何差异都是通过共识来解决。重新编码后我们联系人员,以确保准确性和验证数据集的前最后的分析。临床报告的数据中心和国家结核病规划每年更新两次。目前的手稿报告临时结果分析进行数据报道8月28日,2019年。
变量和定义
获得的数据通过电子格式的集合形式根据世卫组织的模板,尽管额外的临床细节要求(30.]。年度数据收集发生两次,是基于所提供的资料的临床文件招募临床中心。
收集的信息包括匿名病人的人口统计数据、细菌学的放射性和临床状态诊断,治疗期间和治疗数据安全。
根据世界卫生组织aDSM项目,严重不良事件包括死亡或危及生命的事件,住院治疗或延长住院治疗,持续或严重残疾,或先天性异常。严重不良事件包括3 - 5级不良事件(三年级:严重;4级:危及生命;五年级:死亡)13,28,32]。轻微不良事件包括1级(轻度)和2级(中等)13,28,32]。
每当发生不良事件时,临床医生使用一种形式报道总结不良事件的细节,包括年级、药物(s)负责(具体剂量和相应的药物),考试了,行动,持续时间和事件的结果(恢复/解决,恢复/解决,后遗症,没有恢复/解决,死了,未知)。
数据分析
一个描述性的分析组患者进行评估。分析分层的地理区域(如。欧洲与non-Europe,欧洲指的是世卫组织欧洲区域和non-Europe谁比欧洲其它地区),性别、风险因素(如。艾滋病毒sero-status、糖尿病)和不良事件严重性。
定性和定量变量概括使用绝对频率、比例中位数(四分位范围(差),意味着±sd。卡方或Fisher精确测试被用来比较定性变量,和t检验或Mann-Whitney测试被用来统计比较定量变量。
每个药物不良事件分析了“”(比例与给定的药物治疗的患者中,经历了不良事件归因于这种药物)和组织(器官/系统)的不良事件根据格式允许国际比较13]。
的地图图1创建使用ggplot2和3.5.1 rworldmap包R版本(10,33]。
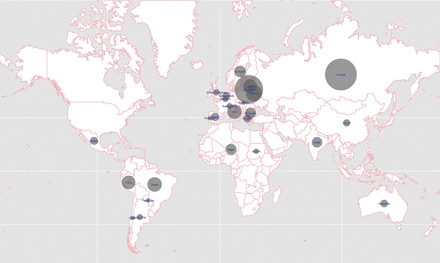
全球分布的临床中心参与研究。灰色圆点的大小反映了报道的患者数量。
结果
总的来说,来自26个国家/地区所有大洲的45中心报道658例8月28日,2019 (图1,附件1 - 3)。
阿根廷、澳大利亚维多利亚(状态)、巴西、保加利亚、智利、中国(浙江)、希腊、立陶宛、墨西哥、荷兰、尼日尔、巴拉圭、葡萄牙、俄罗斯(莫斯科和阿尔汉格尔斯克的州),斯洛伐克,西班牙,苏丹,瑞典和瑞士沃州(县)报道,100%的病人治疗新药在国家/地区,而白俄罗斯、比利时、印度、意大利、拉脱维亚、秘鲁和英国国家患者的比例从15%到80% (附件1)。
患者的人口统计学、流行病学和临床特点总结表1(分层地理区域,欧洲与其他比欧洲)。每个药物不良事件的情况下完成或还归纳了接受治疗表2和3(每个药物:许多患者不良事件/患者数量的药物)和附件3。总结了严重心脏不良事件表4(严重的QT延长和严重心律失常)和次要的附件4。每个器官/系统严重不良事件的总结概括图2和药物附件5。药品监督管理局和不良事件发生之间的间隔,根据治疗效果的研究数据收集、总结附件6。
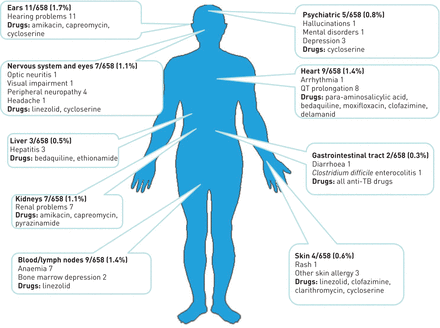
总结57严重不良事件的分布的器官/系统。
的658个患者中,577(87.7%)接受bedaquiline(与delamanid流行性流感减毒活疫苗,结合或顺序,在40例)和121年(18.4%)和delamanid: 161(24.5%)结核病耐多药结核病或rifampicin-resistant菌株引起的结核分枝杆菌224 (34%)pre-XDR菌株(125耐多药结核病与额外的耐氟喹诺酮类和99到一种可注射的药物),245(38.6%)广泛耐药结核菌株,19例(2.9%)呈现不同的其他抗性解释新药物的处方(包括三个pan-susceptible结核病患者:两个一线药物严重不良反应事件和每个临床决策一个)(附件2)。
大多数患者是男性(n = 452, 68.7%)和(差)的年龄中值为42(33-53)年。有85(13.0%)移民。艾滋病毒合并感染被报道在29(4.4%)的653个病人(三个未知状态)与中值(差)的CD4细胞计数94(30 - 212)细胞·毫米3。绝大多数(93.1%)n = 27日接受抗逆转录病毒治疗。共有47(7.2%)人失访。
648年被诊断为肺结核658例(98.5%),37有参与肺和肺外的网站和10与孤立肺外疾病(n = 4淋巴结,n = 3胃肠道,n = 2胸膜,n = 1睾丸和n = 1腰大肌脓肿)。
痰涂片和培养阳性患者的百分比在诊断分别为68.7%(451 657)和89.8%(590 657),分别;其余患者积极分子测试或治疗基于索引的电阻剖面(n = 5),不良事件(n = 2)和临床决策(n = 1) (附件2)。
均值±sd数量的药物结核分枝杆菌耐药是6.2±2.5。总的来说,439人(66.7%)的658名患者在先前接受过结核病。
整体耐药性的流行,相关国家耐药性患病率和样本大小,是如下:链霉素n = 415(86.3%)、吡嗪酰胺n = 368(77.0%)、乙胺丁醇(n = 476(75.1%)、氟喹诺酮类原料药n = 385(61.9%)、乙硫异烟胺/ prothionamide n = 285(60.8%)、卡那霉素n = 315(52.9%)、卷曲霉素n = 180(31.0%)、阿米卡星n = 171(30.3%),不是n = 86(23.1%)、环丝氨酸/ terizidone n = 25(7.9%)和linezolid n = 12 (4.7%)。
治疗方案包括,除了bedaquiline和/或delamanid, linezolid(81.5%)、莫西沙星(37.1%)、左氧氟沙星(36.6%)、氯法齐明(32.4%)、卷曲霉素(28.4%)、阿米卡星(19.9%)和碳青霉烯(11.2%)。
中位数(差)行政采购bedaquiline延迟的范围是0(划分)天。
患者接触到bedaquiline值(差)的170(99 - 239)天,并delamanid 168(145.5 -182)天。辅助外科手术治疗和随后的肺康复进行77年(11.9%)的病人。
在队列中值(差)治疗持续时间是385(231 - 545)天,包括233名患者(35.9%)完成了治疗,369名(56.7%)仍在治疗(150例(44.2%)的339有6个月的bedaquiline和49(67.1%)的73个delamanid) 8月28日,2019年。
不良事件
总的来说,504个不良事件集被临床报道中心的447(88.7%)被归类为小(1 - 2年级)和57个(11.3%)被列为严重(3 - 5年级)(附件5)。
严重不良事件
总的来说,57例(11.3%)严重不良事件报告55例不同器官/系统(表2和3,附件5),所有解决/解决除了6(10.5%)如下:n = 2肠胃,n = 7神经系统,皮肤n = 4, n = 11听证会,n = 5精神,n = 9血,n = 9心脏,肝和n n = 3 = 7肾(附件3)。
总体比例的患者报告严重不良事件相关linezolid,氯法齐明,bedaquiline患者和delamanid这些药物是2.8%(15 536),1.4%(213年的),1.0%(577年的)和0.8%(121年的),分别为(表2)。在完成治疗的患者严重不良事件的比例高(无意义的)(表3)。
临床医生报道不良事件通知到他们国家的卫生当局如下:3(52.6%)57严重,19(4.3%)的447个小不良事件。
心脏不良事件
总的来说,17例(2.6%)的658个病人经历了Fridericia-corrected QT延长(QTcF)≥500毫秒。其中,16收到bedaquiline(6严重和10次要不良事件;其中两个与流行性流感减毒活疫苗delamanid)。仅在一个单一的情况下,对待delamanid,严重不良事件报告和归因于莫西沙星(表4)。
QTcF间隔延长造成严重心脏不良事件报告了8例患者(表4);药物在4名患者bedaquiline负责,氯法齐明在两个病人,莫西沙星,不是在一个病人,而在另一个病人由于non-TB药物(阿米替林、数据未显示)。没有死亡的记录。那些收到bedaquiline,两个病人的药物才撤回报告严重不良事件(577年)两个(0.35%),而在两个病人的QT正常化后打断氯法齐明伴随的管理。所有QT-related严重不良事件/解决解决。
一个病人有一个轻微的不良事件相关QTcF延长要求撤军的药物(莫西沙星取而代之的是左氧氟沙星)(附件4)。
总的来说,32名患者出现轻微的不良反应相关的QT延长,大多数由于bedaquiline (n = 28日87.5%)和氟喹诺酮类原料药(n = 3, 9.3%) (附件4)。
一个病人停止delamanid在经历严重不良事件(室性二联治疗心律失常出现4天)(表4)。
讨论
本研究的目的是前瞻性评估不良事件的频率和严重程度由于抗结核药物后连续的病人谁aDSM工程的原则和方法。
项目做一个“注册”国家项目根据世界卫生组织的建议,旨在促进定期监测不良事件,以及收集和报告信息在细菌学上的状态诊断、期间和治疗结束时最终结果(7,29日,30.]。世卫组织建议国家使用他们现有的监测方法(电子注册或现有的电子医疗记录系统)提取数据和用于临床和公共卫生目的(29日]。
国家结核病规划面临困难在实施aDSM和导致全球数据库。虽然数量和类型的信息收集是已知的和有足够负担的病人来满足需要建立一个常规不良事件记录和报告系统,现有的监测系统目前不具备收集和分析相关的变量。
目前的项目代表第一个文档aDSM的可行性方法和收集科学证据质量不良事件在新的和改造药物患者”字段条件”从各大洲的国家。可用的科学证据在安全性和耐受性方面更好的抗结核药物可以从单一检索观察和实验研究。这个项目提供了一个国际评估基于寄存器的方法。
第一个研究的重要发现是,当治疗方案包括bedaquiline和delamanid,不良事件的总体比例相当低(8.7%的患者严重不良事件(3和4年级,没有5级不良事件))。
值得注意的是,注射剂(和乙硫异烟胺)是药物造成更多不良事件(表2和3)。世卫组织新口服方法(6,7)和新药的可用性,卷曲霉素将不再被使用,和阿米卡星以及乙硫异烟胺/ prothionamide (PAS)将越来越少。相比之下,linezolid将越来越多地使用,药物频繁和严重不良事件20.)需要平衡功效和毒性34]。治疗药物监测可以帮助实现治疗目标曲线下的面积/最小抑制浓度> 11935]而保持低槽浓度足以阻止毒性(36]。
本研究的第二个重要成果是仔细分析造成的不良事件bedaquiline delamanid和特制的药物。而总体11.1%的患者不良事件delamanid bedaquiline和13.2% (表2),由于这些药物严重不良事件很少,只有两个病人中断bedaquiline(0.35%)和一个中断delamanid(0.8%),因为心脏不良事件(14,37]。
病人报告严重不良事件相关的比例linezolid clofazimine-treated患者3%和1.4%,分别为(附件3)。
总体而言,5.8%的患者经历了不良事件与莫西沙星与左氧氟沙星和3.8%,而只有两个病人有严重不良事件与莫西沙星在正常剂量。所有的12名患者接受高剂量异烟肼和高剂量莫西沙星报告不良事件。
令人担忧的是,一个重要的比例保健提供者没有确认的不良事件报告给卫生当局在国家层面。我们推测,不良事件的解释漏报包括缺乏认识,行政负担(需要向国家报告和aDSM系统和不同形式的药物制造商和多个步骤),保密问题,不同行业的参与(公共和私人监狱,等)和责任的恐惧。
此外,有一些差异在不良事件的分级延长“高职院校学前教育专业”。在4名患者不良事件最初归类为小,即使他们已经导致违规药品的撤军。医生同意这些不良事件被重新归类为严重。延长无症状疾病如高职院校学前教育专业需要清晰和盛传的准确的评分标准。QTc间隔监测通常是表现在耐多药结核病患者暴露于bedaquiline和delamanid世卫组织欧洲区域;虽然罕见的致命的事件记录,心电图是一个具有成本效益的预防干预对于那些患心脏不良事件的风险(38]。
可用的有效的药物,避免过早停药国家或国际专家小组可以咨询指导(5,31日]。医疗条件可以显著增加心脏不良事件的概率在耐多药结核病患者(即。低钾血症和艾滋病)应该严密监控39]。
相比,最近的荟萃分析个人数据进行五组(亚美尼亚、格鲁吉亚、南非、法国和詹森治疗组)患者537 bedaquiline(使用13),不良事件的比例似乎相当符合这些在我们的研究中发现。例如,4.9%的患者遭受心脏不良事件在five-cohort研究类似于我们的研究5.5%(分母:bedaquiline患者)。同样,中断bedaquiline治疗的比例在我们的研究中由于QTcF增加(0.35%)是一致的,在最近的一次系统的回顾文献描述(0.68%)(26]。
这项研究有几个优点,包括参与的国家数量(26)和一个大样本量(据我们所知最大的跨国公司之一群耐多药结核病患者bedaquiline——和/或delamanid-containing方案基于aDSM协议),未来的设计和信息采集的准确性的国家不同的流行病学和经济背景。最后,但并非最不重要的是,大多数的国家/州/地区(26)21日bedaquiline患者提供连续的所有数据,在研究期间delamanid。
所代表的一个限制是使用一个一致同意的过程属性到一个特定的药物不良事件,包括当地的专家小组和aDSM国际集团面板。科学证据在安全性和耐受性方面更好的一个单一的药物或药物组合的司机采用识别药物不良事件的责任;证明因果关系的概率在特定患者,科学证据在哪里差,非常低。进一步的研究主要集中在抗结核药物的安全性,基于回头挑战方法(即。药品监督管理局后中断发生后不良事件)可能有助于阐明抗结核药物的不良事件概要。此外,只有少数中心进行治疗药物监测评估不良事件之间的关系和药物暴露(剂量和频率管理)。此外,没有变量相关伴随药物,这可能会影响药物接触,都被记录下来,与艾滋病毒治疗患者的艾滋病毒感染的唯一例外。不可能使用方法如Naranjo分数或耶鲁算法(40,41]。第二个限制是,一些儿科病人(四个人年龄< 18岁)和艾滋病毒携带者(n = 29, 4.4%)包括在队列允许特定subanalyses。
心理所扮演的角色提供信息在停药后的治疗失败的风险,以及潜在的偏见与移民和临床沟通(如。门诊),可能会影响病人的耐受性和不良事件的报告。不幸的是,我们没有收集任何变量,可以评估这些重要特性。
此外,我们评估不良事件的发生在两个人完成方案和仍在治疗,对他们来说,累积药物毒性(如。从linezolid)可能被低估。完成治疗的患者中,累积的毒性可以充分评估,不良事件的比例高(不重要的)。
我们没有收集任何基因/药物基因组学数据,这可能会增加一些不良事件的风险。未来的研究需要更好的澄清主机所扮演的角色和环境特征的不良事件的发生。
最后,正如大多数国家开始的aDSM项目这一研究中,预选或under-notification不良事件(特别是小的和那些没有相关新药)不能被排除在外。漏报在现实世界的环境可以是一个关键问题在评估药物的安全性/药物疗法。医务工作者和患者都应该意识到的重要性报道不良事件的发生,更好地理解药理安全性和处方的效益/风险比。分类偏见的一些不良事件应考虑:尽管所有临床中心参加项目后协议对不良事件的报告,当地审计旨在评估标准操作程序的实现(如。常规的听力测定)没有进行,因为金融约束。
不幸的是,一些国家(在美国、亚洲和撒哈拉以南的非洲地区)拒绝当被要求参与,针对研究的自愿视为“困难”或“耗时”没有提供额外的资源。出于这个原因,因为不同的入境时间的研究(这是一个“注册”),这项研究不允许我们评估耐药性的流行程度在不同的设置。目前迫切需要克服报告不良事件所涉及的行政负担,易于使用的电子表单,可以自动编译来自医疗记录。
早期研究将继续评估治疗结果和最终为定期更新发生,因此“队列”是一个“生活”。这个队列允许小说评价治疗和组合在一个相对较短的时间框架;特别重要的实质性的变化在国际实践和指南推荐的以人为本的治疗耐多药结核病[42,43]。
这种方法将允许参与国家评估治疗的“质量”服务和减少后处理后遗症的风险责任的功能损害和损害生活质量(44- - - - - -46]。
总之,研究结果证实aDSM患者接受抗结核治疗新药物是可行的。此外,研究重申了相对安全的新药物推荐的新的指导方针,为严重不良事件的发生在这个群体的病人来自26个国家中观察到< 10%的病人。更多采用推荐aDSM地方,国家和国际水平可能通过改善质量的过程(即。标准化、活跃和定期记录和报告基于共享标准操作程序)。
补充材料
补充材料
请注意:补充材料并不是由编辑部,编辑和上传已由作者提供。
补充附件1erj - 01522 - 2019. - supplement_1
补充附件2erj - 01522 - 2019. - supplement_2
补充附件3erj - 01522 - 2019. - supplement_3
补充附件4erj - 01522 - 2019. - supplement_4
可共享的PDF
确认
作者要感谢Algirdas Gauronskis,维塔Globytė(肺结核和肺学诊所,共和党Šiauliai县医院,Šiauliai,立陶宛),安塔纳斯·Strazdas(部门的肺结核,Alytus县结核病医院,Alytus,立陶宛)和Paola Castellotti(地区结核病参考中心,别墅公司研究所Niguarda医院,米兰,意大利)为他们的贡献。
脚注
可以从本文的补充材料www.qdcxjkg.com
作者贡献:手稿设计,计划,编写、编辑和批准使用一个协作方法,遵循内部GTN国际(全球结核病网络)和作者承认规则,基于上述步骤主要知识贡献。这项研究是一项全球性努力,涉及26个国家在所有大洲。g . Sotgiu s Tiberi r .好像l D 'Ambrosio和G.B. Migliori写的协议。g . Sotgiu l . Saderi和r . Duarte修订了方法论的内容。g . Sotgiu l . Saderi r .好像和l D 'Ambrosio进行分析。s Tiberi r .好像'Ambrosio l . D, e . Pontali J-W。Alffenaar, J.A. Caminero, g . Sotgiu G.B. Migliori写了初稿的手稿。鲍里索夫,j . Bruchfeld a . Piubello O.W. Akkermann, j . Denholm J-M。Garcia-Garcia, r . Laniado-Laborin j . Mazza-Stalder a . Matteelli m . Munoz-Torrico m . van den繁荣,d . Visca J.A. Caminero和g Sotgiu写的部分手稿(第二稿)。a . Spanevello J-M。 García-García, Z.F. Udwadia, E. Danila, A. Maryandyshev and M. Dalcolmo provided comments to the second draft (third draft). A. Maryandyshev, S. Miliauskas, L. Kuksa, S. Manga, A. Skrahina, S. Diktanas, L.R. Codecasa, A. Aleksa, A. Koleva, E. Belilovski, E. Bernal, M.J. Boeree, J. Cadiñanos Loidi, Q. Cai, J.J. Cebrian Gallardo, M. Dara, E. Davidavičienė, L. Davies Forsman, J. De Los Rios, S.E. Elamin, N. Escobar Salinas, M. Ferrarese, A. Filippov, B. Gadzheva, A. Garcia, R. Gayoso, R. Gomez Rosso, V. Gruslys, G. Gualano, W. Hoefsloot, J. Jonsson, E. Khimova, H. Kunst, Y. Li, C. Magis-Escurra, V. Manfrin, V. Marchese, E. Martínez Robles, C. Moschos, H. Mustafa Hamdan, B. Nakčerienė, L. Nicod, M. Nieto Marcos, D.J. Palmero, F. Palmieri, A. Papavasileiou, M-C. Payen, A. Pontarelli, S. Quirós, A. Rendon, L. Saderi, A. Šmite, I. Solovic, M.B. Souleymane, M. Tadolini, M. Vescovo, P. Viggiani, A. Yedilbayev, R. Zablockis, D. Zhurkin and M. Zignol provided additions to the fourth draft. S. Tiberi and J. Denholm proofread the manuscript. All co-authors approved the final manuscript.
利益冲突:美国鲍里索夫没有披露。
利益冲突:大肠Danila没有披露。
利益冲突:a . Maryandyshev没有披露。
利益冲突:m . Dalcolmo没有披露。
利益冲突:美国Miliauskas没有披露。
利益冲突:l . Kuksa报告个人费用审判参与大冢和Tibotec的个人费用讲座从强生服务公司在提交工作。
利益冲突:美国漫画没有披露。
利益冲突:a . Skrahina没有披露。
利益冲突:美国Diktanas报告个人费用审判参与大冢,拨款会议出席的詹森(Sirturo),在提交工作。
利益冲突:L.R. Codecasa没有披露。
利益冲突:a . Aleksa没有披露。
利益冲突:j . Bruchfeld没有披露。
利益冲突:a . Koleva没有披露。
利益冲突:a . Piubello没有披露。
利益冲突:Z.F. Udwadia没有披露。
利益冲突:O.W. Akkerman没有披露。
利益冲突:大肠Belilovski没有披露。
利益冲突:e·伯纳尔没有披露。
利益冲突:M.J. Boeree没有披露。
利益冲突:j . Cadinanos Loidi没有披露。
利益冲突:问:Cai没有披露。
利益冲突:J.J. Cebrian Gallardo没有披露。
利益冲突:m·达拉没有披露。
利益冲突:大肠Davidavičienė没有披露。
利益冲突:l·戴维斯Forsman声称通过没有披露。
利益冲突:j·德洛里奥斯没有披露。
利益冲突:j . Denholm没有披露。
利益冲突:j . Drakšienė没有披露。
利益冲突:r·杜阿尔特没有披露。
利益冲突:S.E. Elamin没有披露。
利益冲突:n Escobar萨利纳斯没有透露。
利益冲突:m . Ferrarese没有披露。
利益冲突:a . Filippov没有披露。
利益冲突:加西亚没有披露。
利益冲突:J.M. Garcia-Garcia没有披露。
利益冲突:即Gaudiesiute没有披露。
利益冲突:b Gavazova没有披露。
利益冲突:r . Gayoso没有披露。
利益冲突:r·戈麦斯罗索没有披露。
利益冲突:诉Gruslys没有披露。
利益冲突:g . Gualano没有披露。
利益冲突:w . Hoefsloot没有披露。
利益冲突:j·琼森没有披露。
利益冲突:大肠Khimova没有披露。
利益冲突:h . Kunst没有披露。
利益冲突:r . Laniado-Laborin没有披露。
利益冲突:y李没有披露。
利益冲突:c . Magis-Escurra没有披露。
利益冲突:诉Manfrin没有披露。
利益冲突:诉Marchese没有披露。
利益冲突:e·马丁内斯罗伯斯没有披露。
利益冲突:a . Matteelli没有披露。
利益冲突:j . Mazza-Stalder没有披露。
利益冲突:c . Moschos没有披露。
利益冲突:m . Munoz-Torrico没有披露。
利益冲突:h·穆斯塔法哈姆丹没有披露。
利益冲突:b Nakčerienė没有披露。
利益冲突:l . Nicod没有披露。
利益冲突:m .分担马科斯没有披露。
利益冲突:D.J. Palmero没有披露。
利益冲突:f . Palmieri没有披露。
利益冲突:a . Papavasileiou没有披露。
利益冲突:mc。Payen没有披露。
利益冲突:a . Pontarelli没有披露。
利益冲突:美国奎洛斯没有披露。
利益冲突:a .瑞没有披露。
利益冲突:l . Saderi没有披露。
利益冲突:a .Šmite没有披露。
利益冲突:即Solovic没有披露。
利益冲突:M.B. Souleymane没有披露。
利益冲突:m . Tadolini没有披露。
利益冲突:m . van den繁荣没有披露。
利益冲突:m . Vescovo没有披露。
利益冲突:p . Viggiani没有披露。
利益冲突:a . Yedilbayev没有披露。
利益冲突:r . Zablockis没有披露。
利益冲突:d Zhurkin没有披露。
利益冲突:m . Zignol没有披露。
利益冲突:d Visca没有披露。
利益冲突:a . Spanevello没有披露。
利益冲突:正当Caminero没有披露。
利益冲突:J-W。Alffenaar没有披露。
利益冲突:美国Tiberi没有披露。
利益冲突:r .好像没有披露。
利益冲突:l D 'Ambrosio没有披露。
利益冲突:大肠Pontali没有披露。
利益冲突:g . Sotgiu没有披露。
利益冲突:G.B. Migliori没有披露。
支持声明:所支持的项目是全球结核病网络(GTN;委员会在结核病治疗,临床试验和全球结核Consilium),是欧洲呼吸学会拉美项目合作ALAT (Asociacion拉丁裔美国德Torax -拉丁裔美国胸腔协会)和SBPT(巴188bet官网地址西社会的肺学和结核病)。本文属于世卫组织合作中心的科学活动肺结核和肺部疾病,Tradate, ita - 80, 2017 - 2020 GBM / RC / LDA。
- 收到了2019年8月1日。
- 接受2019年9月17日。
- 版权©2019人队















