摘要
在之前的一项安慰剂对照二期试验(TMC207-C208;NCT00449644).目前的2期多中心、开放标签、单臂试验(TMC207-C209;NCT00910871)的研究是为了证实贝达喹啉的安全性和有效性。
根据国家结核病规划治疗指南,新诊断或以前治疗过的耐多药结核病(包括前广泛耐药结核病或广泛耐药结核病)患者接受贝达喹啉治疗24周,同时继续接受抗结核药物背景治疗方案。患者在服用贝达喹啉期间和120周后进行评估。
在233名入选患者中,63.5%患有耐多药结核,18.9%患有前广泛耐药结核,16.3%患有广泛耐药结核,87.1%在入选前服用了二线药物。死亡16例(6.9%)。20例患者(8.6%)在第24周前停药,最常见的原因是不良事件或耐多药结核病相关事件。不良事件通常与耐多药结核病治疗相关。在有效人群(n=205)中,120周时培养转化(缺失结果归为失败)为72.2%,在耐多药结核、前广泛耐药结核和广泛耐药结核患者中分别为73.1%、70.5%和62.2%。
在这个临床相关的耐多药结核病患者队列中,在背景方案中添加贝达喹啉具有良好的耐受性,并导致了良好的结果。
摘要
贝达喹啉在广泛耐药结核(包括广泛耐药结核)患者治疗中的安全性数据(C209研究)http://ow.ly/TcZBh
简介
耐多药结核病(MDR-TB),定义为由细菌菌株引起的疾病结核分枝杆菌至少对异烟肼和利福平具有耐药性,有可能削弱全球结核病控制的进展[1].耐药性可随着对至少一种注射用药物(阿米卡星、卡那霉素、曲霉素)或氟喹诺酮类药物出现耐药性而进一步恶化[2](一些作者认为是前广泛耐药(前xdr)结核病[3.)或两者兼而有之(广泛耐药结核病)。2013年估计发生了48万例耐多药结核,其中9%为广泛耐药结核[1].据其他报道,约50%的耐多药结核病患者对治疗反应良好[1,4],承认这一比例可能会更高,因为合并数据集中所包括国家的病例持有量和监测得到改善。XDR分离株患者的反应率非常低[1,5- - - - - -8].据世界卫生组织(世卫组织)报告,来自40个国家的1269名广泛耐药结核病患者的治疗结果很差,其中35%的患者死亡,10%的患者失败,33%的患者失去随访,只有22%的患者成功完成治疗[1].迫切需要新的药物来改善现有的治疗方案[1].
具有新型抗结核作用机制的二芳喹啉化合物贝达喹林[9],已在美国(2012年)和欧洲(2014年)获得加速或有条件批准用于耐多药结核病,世卫组织为其提供了临时使用指南[10].在一项随机安慰剂对照试验(TMC207-C208)中,24周的贝达喹啉治疗显著提高了耐多药结核病患者的培养转换率[11].不良事件(AEs)的总体发生率相似,但贝达喹啉组的死亡人数高于安慰剂组(10(12.7%))。与分别为2 (2.5%))[11].根据C208二期临床试验的中期结果分析,贝达喹啉于2011年在目前40个国家获得监管机构批准之前可用于医疗用途。几个小组最近报告了他们在同情使用项目中的经验,该项目为全球700名患者提供了机会[12- - - - - -15].此外,与美国国际开发署合作,在4年内向100个有资格获得全球基金资助的国家免费提供贝达喹啉。
本研究(TMC207-C209)的目的是评估贝达喹啉联合背景方案(BR)治疗更广泛的耐药结核病患者(包括前xdr和广泛dr - tb)的安全性、耐受性和有效性。在这里,我们报告了这项2期开放标签试验的最终安全性和有效性数据,并讨论了它与其他贝达喹啉治疗耐多药结核病的研究的关系[11,16- - - - - -17].
方法
参与者
参与者在亚洲11个国家(中国、韩国、菲律宾、泰国)和东欧(爱沙尼亚、拉脱维亚、俄罗斯、土耳其、乌克兰)以及秘鲁和南非的31个地点被招募。
我们招募了年龄≥18岁的肺耐多药结核病患者,他们的痰涂片或培养呈耐多药结核病阳性米.肺结核,并于过去6个月内经培养药敏试验(DST)或快速核酸筛选试验证实对异烟肼和利福平耐药。如果XDR-TB患者的分离株可能对其BR中的三种或三种以上抗结核药物敏感,那么他们就符合条件[18].带有CD4的hiv感染者+细胞计数<250细胞·mm3或患有除结核病以外的艾滋病定义疾病的人被排除在外。接受抗逆转录病毒疗法(ART)的艾滋病毒患者如果符合特定的标准,就有资格接受治疗,但没有人被纳入研究。排除标准包括结核复杂或严重的肺外表现;预计在未来6个月内接受结核病手术;严重的心律失常需要药物治疗;fridericia校正QT (QTcF)间期>450 ms;有尖扭转病史或危险因素;延长QT/QTc间期的伴随药物,包括莫西沙星和加替沙星;药物超敏反应;酗酒或吸毒; pregnancy or breastfeeding; and prior receipt of bedaquiline.
研究设计
这是一项二期、多中心、开放标签、单臂试验(www.clinicaltrials.gov:NCT00910871)(网上补充图S1)。参与者接受400mg贝达喹啉,每天1次,持续2周,然后每周3次,200mg,持续22周,与研究者根据国家结核病规划(NTP)指南选择的BR药物联合使用。贝达喹啉片早餐后用水服用。在贝达喹啉治疗后,参与者被进一步随访96周,在此期间BR完成(在线补充图S1)。贝达喹啉和BR的摄入量根据NTP指南进行直接观察治疗。过早停药的患者被认为是治疗失败,但随访收集生存数据(除非撤回同意)直到试验结束。
研究评估
筛选后,在基线、1天(贝达喹啉治疗开始)后以及2、4、8、12、16、20和24周安排了门诊访问。所有患者随后随访96周,每12周进行一次门诊检查。
每次就诊时,患者都要进行体检,评估ae、生命体征和心电图。hiv阳性患者有CD4+细胞和病毒载量监测。在筛查、基线、4周、12周和24周及所有后续随访时进行实验室参数测定。微生物学和传染病司的成人毒性表用于分级不良事件的严重程度[19].通过标准化MedDRA查询数据库,确定了感兴趣的特定ae(基于贝达喹啉的非临床和临床数据)[20.急性胰腺炎、横纹肌溶解/肌病、严重皮肤ae和尖扭转/QT延长,以及药物相关肝脏疾病的未标准化MedDRA查询(见附录)表4).
每次就诊均使用三份点痰样本(首剂日除外),采用分枝杆菌生长指示管(MGIT;Becton Dickinson, Sparks, MD,美国)。
对贝达喹啉和其他抗结核药物进行DST(在比利时安特卫普热带医学研究所进行),在基线和贝达喹啉治疗24周后,对恢复培养阳性的患者进行DST。在7H11琼脂上测定贝达喹啉的最低抑菌浓度(MIC)定义为最低浓度(µg·mL)−1的生长结核分枝杆菌了99%。
研究终点和统计方法
约225例患者的样本量被认为足以得出有关贝达喹啉安全性的有意义的结论,因为任何预计在单个患者中发生的概率为1%的AE都将以90%的概率观察到。
对意向治疗(ITT)人群进行了安全性分析,其中包括所有至少服用过一次贝达喹啉的随机患者。对改良ITT (mITT)人群进行疗效分析,其中排除了药物敏感结核病患者或筛查和/或基线培养阴性的患者。
主要疗效终点是在贝达喹啉治疗24周内确认痰培养转化的时间(连续两次从至少相隔25天收集的斑点痰中进行阴性MGIT培养,随后没有确认阳性培养)。未进行培养转换、死亡或在考虑的时间点之前停用的患者被归类为无应答者(缺失=失败),无论他们在退出或死亡时的培养状态如何,并且在最后一次评估时审查了培养转换的时间。还根据世卫组织对耐多药结核病的结果评估了治愈率[21,并修改了完成治疗和治愈的定义是基于完成研究而不是完成治疗。
道德
当地伦理委员会批准了所有研究地点的方案。该研究按照赫尔辛基宣言和良好临床实践的原则进行,所有患者(或其代表)均提供书面知情同意。
结果
研究人群
在2009年8月20日至2010年9月27日筛查的294例患者中,233例入选并纳入ITT(安全)人群(在线补充图S2)。其中,179例患者(76.8%)完成了研究,54例患者(23.2%)停止了研究,17例患者(7.3%)因包括耐多药结核病相关事件在内的ae而停止研究。179例完成试验的ITT患者中有32例(17.9%)在研究结束时仍在接受BR治疗。mITT(疗效)人群包括205例患者,排除了3例药物敏感结核病患者和25例筛查和/或基线培养阴性的患者。安全性和有效性人群的特征相似(表1).关于安全人群(n=233), 39.9%(93/233)有耐多药结核(不包括前广泛耐药结核和广泛耐药结核),23.6%(55/233)有耐异烟肼和利福平耐多药结核,但未确定前广泛耐药或XDR状态,18.9%(44/233)有前广泛耐药结核,16.3%(38/233)有广泛耐药结核。大多数患者hiv阴性(96.0%),有空腔疾病(63.5%),在入组前接受二线抗结核药物(87.1%)的中位数为36天(范围6-2647天)(表1).在疗效人群中的8名艾滋病毒阳性患者中,3人感染了耐多药结核,3人感染了前广泛耐药结核,1人感染了广泛耐药结核;1名患者患有耐多药结核病,但未确定其XDR前或XDR状态。表2显示有效人群中最常见的BR药物(n=205)。关于其他值得注意的BR药物,13例患者在基线时接受氯法齐明治疗,120周研究期间36例患者接受氯法齐明治疗,利奈唑胺分别为12例和34例。在试验期间没有患者接受delamanid治疗。
不良事件
最常见的AEs (表3)与耐多药结核病治疗队列中经常描述的情况相似[22,23],其中大部分为一级或二级[19].高尿酸血症(9.4%)和天冬氨酸转氨酶(AST)升高(3.4%)是最常见的≥3级AEs。ae的发生率在试验的前12周内最高。47例(20.2%)患者报告了严重的ae;其中,呼吸道感染/疾病最为常见(网上补充表S1)。
死亡16例(233例患者中的6.9%)(表4),其中四次发生在退出研究后。死亡个案并无固定模式(图1).试验中只有一名同时感染艾滋病毒的患者死亡。该患者在基线时分离出XDR菌株。在贝达喹啉治疗期间发生了3例死亡(因肾损害和2例死于结核病)。调查人员报告的16个死亡原因中有9个是由结核病或结核病相关疾病引起的,其中8个没有转化或恢复为培养阳性。另有四人死于呼吸系统疾病。16例死亡被认为与贝达喹啉无关(表4).
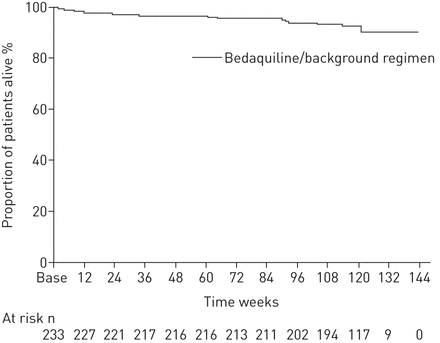
死亡时间(安全(治疗意愿)人群)的Kaplan-Meier图。基础:基线。
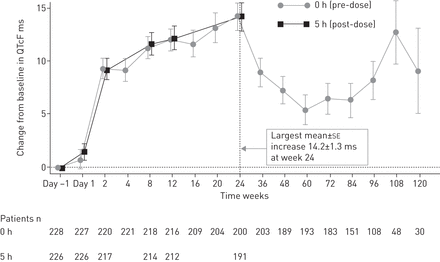
QTcF间隔延长的ae报告不常见(表3).QTcF间隔>500 ms增高的2例患者均服用氯法齐明,1例患者并发低钾血症。未报告有临床意义的诵读困难发作。QTcF间隔较基线的平均最大变化为14.2 ms。停用贝达喹啉后,这下降到<10 ms (图2).在第24周服用氯法齐明的患者(n=17)中,QTcF间隔从基线到第24周的平均最大变化为31.9 ms,而未服用氯法齐明的患者(n=177)的平均最大变化为12.3 ms。
fridericia校正的QT (QTcF)变化来自参考(安全(意图治疗)人群)。数据以均数±表示se.第96周后出现宽误差条的原因是在这些时间仍在接受治疗的患者数量较少,只有接受治疗的患者进行了心电图评估(第108周n=48,第120周n=30)。由于广泛的标准误差和评估的患者数量有限,60周至108周之间的增量增加被认为与临床无关。
转氨酶升高被报道。1例患者服用多种具有潜在肝毒性的背景药物,在第32周时符合Hy定律的实验室标准(治疗时出现的血清丙氨酸转氨酶(ALT)或AST >3倍正常上限,同时血清总胆红素>2倍正常上限)[24然后康复了。大多数治疗后出现的AST或ALT≥3级升高(≥3倍正常上限)(表3)在贝达喹啉治疗24周后发病。在一项超过120周的更详细分析中,42例患者(18.0%)发现了肝脏相关ae,主要是AST/ALT升高(表3),研究者认为至少有4例患者(1.7%)可能与贝达喹啉有关。这四例中有一例没有解决,但患者同时患有丙型肝炎感染。15例(6.4%)患者出现3级或4级肝相关AEs,但仅1例患者被认为至少可能与贝达喹啉有关。
微生物的结果
培养转换的时间(缺失=失败)显示在图3.基于24周数据的中位数时间为57天。24周时痰培养转化率为79.5%(163/205例),120周时痰培养转化率为72.2%(148/205例)(图4).24周时的培养转换是持久的,并与120周时的高应答可能性相关:24周应答者中有85.3%(139/163例患者)在120周时仍有应答。在120周时被分类为无应答的患者中,大多数在文化转换后停止了治疗(19/24),其中5人在早期转换后恢复为文化阳性。24周时42例无反应患者中有9例在120周时有反应。
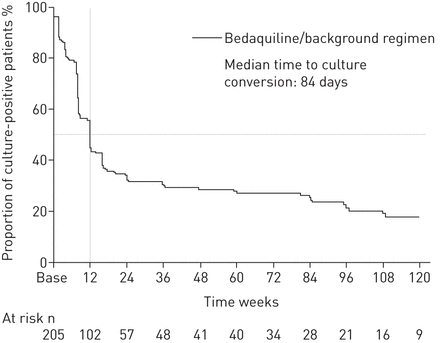
确认培养转化(疗效(改良治疗意向)人群)的时间Kaplan-Meier图。竖线表示文化转换的中位数时间。基础:基线。
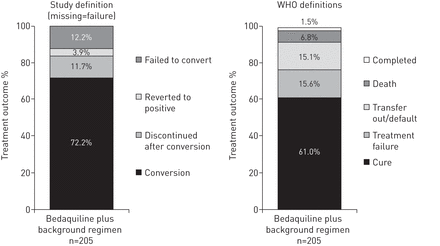
基于方案定义的分析方法(缺失=失败)和世界卫生组织(WHO)对耐多药结核病的修改的结局定义的有效(修改的治疗意向)人群的第120周结局[21].治疗:患者完成研究,并在研究的最后12个月内持续培养阴性(从至少间隔30天收集的样本中至少连续5次培养阴性)。如果在此期间只报告了一次阳性培养,则仍然认为患者已治愈,前提是在此阳性培养后至少连续进行三次阴性培养,间隔至少30天。治疗失败:完成研究但未按上述定义治愈的患者。转出/违约:因任何原因中止研究的患者。死亡:在研究期间死亡的患者。在120周窗口期之前或以内的生存随访中死亡的患者也包括在这一类别中。在120周后的生存随访中死亡的患者不包括在这一类别中,因为事件发生在计划的试验持续时间(120周)之后。完成:完成研究但不符合治愈定义或因缺乏细菌学结果导致治疗失败的患者。
在120周时57例(27.8%)无应答患者中,24例(11.7%)在培养转化后停用,25例(12.2%)转化失败,8例(3.9%)恢复培养阳性(图4),平均恢复时间为基线后382天。在研究结束时,根据修改后的WHO MDR-TB结局定义,125/205例mITT患者(61.0%)被“治愈”,3/205例(1.5%)完成治疗,32/205例(15.6%)治疗失败,31/205例(15.1%)转出/拖欠,14/205例(6.8%)死亡[21] (图4).
耐多药结核患者的转换率为73.1%(95%精确CI为62.9-81.8%)(仅限于异烟肼和利福平耐药),前广泛耐药结核患者的转换率为70.5%(95%精确CI为54.8-83.3%),广泛耐药结核患者的转换率为62.2%(95%精确CI为44.8-77.6%)。所有23名培养转化并完成研究的XDR-TB患者在120周时都有反应。虽然其中一些患者在第120周随访时仍接受BR治疗,但大多数患者(16/23)未接受BR治疗,中位无治疗随访时间为5.4个月。因此,在至少一些XDR-TB患者中,6个月的贝达喹啉与优化BR一起给予,然后继续单独BR有助于痰培养转换和预防停止治疗6个月后的早期复发。基线贝达喹啉MIC与终点培养转换率之间也没有明确的关系。
在试验期间,93例基线耐多药结核患者中没有人发生前广泛耐药结核,但在44例基线前广泛耐药结核患者中,3例无反应(均对氧氟沙星产生耐药性)发生了广泛耐药结核。基线DST显示贝达喹啉MIC结核分枝杆菌分离株范围为0.0075 ~ 0.24 μ g·mL−197.0%的菌株。有效率人群中有24例患者在第24周或之后重复进行了贝达喹啉DST。其中12株在基线后贝达喹啉MIC升高≥4倍,采用24位点分枝杆菌间作重复单位变数串联重复(MITU-VNTR)基因分型证实成对菌株为同一株;12例中9例MIC≥0.24µg·mL−18例MIC为>0.48µg·mL−1.基线后贝达喹啉MIC升高几乎只出现在前广泛耐药结核(4/12)和广泛耐药结核(7/12)患者中。这些基线后分离株均无ATP操纵子多态性,但所有12株均有Rv0678基线后突变[25].在24周或之后,贝达喹啉MIC增加≥4倍的12例患者中有5例在终点时治疗成功,而在24周时培养仍呈阳性且贝达喹啉MIC增加<4倍的5例患者中有3例在终点时治疗成功。
讨论
本研究的主要目的是获得贝达喹啉在更大、更异质人群中的进一步安全性数据。本研究的一项重要发现是,C208第2期的总死亡率为6.9%,而此前报道的死亡率为12% [11].6.9%的死亡率与其他队列相比是有利的(如。在大型元分析中为15% [4]),并对退出研究的患者进行了严格的生存验证。不出所料,死亡主要是由呼吸系统病理造成的。除一名死于结核病或结核病相关疾病的患者外,所有患者要么没有转化为阳性,要么恢复为阳性。没有证据表明贝达喹啉与死亡率之间存在因果关系。
最常见的不良事件与耐多药结核病治疗队列中经常描述的不良事件相似[22,23].在目前的研究中,与C208相比,个别ae报告的频率普遍较低,且严重程度较低[11].这可能是由于在当前研究中纳入了先前接受过耐多药结核病治疗且同意退诊的患者。在这项更大规模的试验中,没有发现与贝达喹啉相关的新的安全信号。此前曾报道贝达喹啉可增加肝转氨酶[11],但6.4%的肝相关不良事件发生率低于其他耐多药结核病队列中报道的发生率[26].仅有2例患者临床显著QTcF延长(>500 ms),且均服用氯法齐明,1例患者低钾血症。因此,当贝达喹啉与氯法齐明合用时,建议进行更密集的心电图和电解质监测。
在第24周,C209中确诊培养转化的患者比例与C208相似(79.5%)与C208为78.8%,120为72.2%与62.1%) (11].C209组的中位痰培养转换时间较短,可能是因为大多数患者在基线时接受二线治疗。基于修订的世卫组织耐多药结核病结局定义的治愈率[21]为61.0%与C208为57.6%,贝达喹啉治疗至120周的持久疗效也与C208一致[11],加强了24周培养转化率可预测耐多药结核病长期治疗结果的观察。研究结果之间的任何比较都需要考虑患者群体的差异。C209研究纳入的感染艾滋病毒的患者比例较低(4.0%)与10.1%)和有空化现象(63.5%)与75.9%)高于C208,但关键还包括广泛耐药结核患者(16.3%),这是一种疗效特别差的耐多药结核,特别是当有艾滋病毒合并感染时[5- - - - - -7,27].
在这项研究中,MDR-TB患者亚组(仅对异烟肼和利福平耐药)和前xdr - tb患者亚组的培养转换相似(73.1%)与70.5%),但在广泛耐药结核亚组中数值较低(62.2%)。在比较各研究时要谨慎,这些观察到的反应率比其他研究报道的要高[5- - - - - -8,27,28],但与贝达喹啉同情使用方案报告的反应率一致[13,15].在试验期间转换为广泛耐药结核的患者没有复发。总的来说,这些结果表明,贝达喹啉添加到患者的BR中,在广泛的患者中产生了良好的培养转化率,包括大多数广泛耐药结核患者。
尽管有广泛的既往治疗,并纳入了前广泛耐药结核患者(21.5%),但进展为广泛耐药结核(通过获得额外耐药性)的患者并不多见,在基线时仅在3名前广泛耐药结核患者中发现。这与C208研究一致[11在该研究中,与接受安慰剂的患者相比,接受贝达喹啉的患者获得额外耐药性的人数较少,并支持将贝达喹啉纳入耐多药结核病方案可防止对重要的伴药产生耐药性。贝达喹啉mic的增加很少发生,几乎只在前xdr和XDR-TB患者中出现。重要的是,所有12例贝达喹啉MIC基线后≥4倍增加的患者都存在Rv0678突变,Rv0678是MmpS5-MmpL5外排泵的转录抑制因子[25].最近,这种新型的耐药性外排机制已被确定,可导致对贝达喹啉和氯法齐明的低水平耐药性[25,29,30.].目前的数据并不表明由于Rv0678突变导致的贝达喹啉MICs增加对治疗反应有负面影响。
单臂设计和缺乏接受ART治疗的hiv阳性患者是本研究的局限性。另一个限制是,在55/233对异烟肼和利福平耐药的患者中,未确定对氟喹诺酮类或二线注射药物的耐药(XDR前或XDR状态)。需要进一步的研究来证实贝达喹啉在接受抗逆转录病毒治疗的患者中的安全性。选择开放标签研究设计和纳入标准是为了纳入更能代表临床实践的大量研究人群。尽管如此,低死亡率与其他耐多药结核病队列[4],无意外药物不良反应,临床缓解率高,支持贝达喹啉可安全用于加强MDR-TB和XDR-TB治疗方案。快速的培养转化率和高的整体治疗反应也表明贝达喹啉与优化的BR联合使用可以缩短耐多药结核病人传人的时间。3期研究(STREAM 2期;www.clinicaltrials.gov:NCT02409290)将招募更多的患者,并在对照设计中评估使用“改良孟加拉方案”给予贝达喹啉9个月的疗效[31,32].贝达喹啉与其他药物联合使用(已获批准或目前处于临床开发阶段)也有可能为耐多药耐药亚型(如XDR- tb或XDR亚型)患者提供更有效的治疗方案[8].预计这些新的药物和方案将成为世卫组织新的以消除结核病为重点的全球战略的重要组成部分[33- - - - - -35].然而,额外的安全性研究(如。在ACTG A5343中,将调查贝达喹啉和德拉曼尼联合使用时QT延长的评估)可能需要与适当的强力疗效研究一起进行(如。流阶段2)。
确认
医学写作支持由英国Macclesfield阿什菲尔德公司Zoetic Science的Ian Woolveridge提供;这项支持是由杨森制药公司资助的。
我们要感谢患者及其家属、调查人员、研究中心工作人员和杨森研究人员,特别是Chrispin Kambili和Els De Paepe,感谢他们对这份手稿的投入。我们也感谢曾在杨森制药公司工作的大卫·麦克尼利的贡献。
TMC207-C209研究组包括以下主要研究人员:Francesca Conradie,陈晓红,Chu Naihui, Charoen Chuchottaworn, Manfred Danilovits, Jorge De Los Rios, Andreas Diacon, Dina Diaz, Vladislav Erokhin (Irina Vasilyeva), Victor Flores, Sung Chul Hwang, Carlos Iberico, Boris kazenyi, Young Sam Kim, Anu Kurve, Mykhaylo Kuzhko, O Jung Kwon, Vaira Leimane, Svetlana Lyepshina, Andrey Maryandyshev, Vasiliy Melnyk, Ronelle Narasimooloo (Alexander Pym),邱丽华,Gönenç Ortaköylü, Seref Ozkara, Rafael Reano, Tae Sun Shim, Tang - jie,Eduardo Ticona Chavez, Tawatchai Wiwatworapan,张霞。
脚注
编辑评论见呼吸呼吸J2016;47: 394-402 [doi:10.1183/13993003.01891 -2015].
这篇文章有补充资料可从www.qdcxjkg.com
支持声明:本研究得到了Janssen Pharmaceuticals的支持。研究发起人参与了试验的设计和实施,以及数据的收集和分析。通讯作者对该临床试验报告有完全的查阅权,并对投稿发表负有最终责任。本文的资助信息已存入FundRef.
临床试验:本研究注册于www.clinicaltrials.gov标识符编号NCT00910871.
利益冲突:可以在本文的在线版本中找到信息披露www.qdcxjkg.com
- 收到了2015年5月8日。
- 接受2015年10月2日。
- 版权所有©ERS 2016