摘要
迄今为止,还没有大型研究评估亚胺培南/克拉维酸的有效性、安全性和耐受性与美罗培南/克拉维酸用于治疗耐多药和广泛耐药结核病(耐多药结核病和广泛耐药结核病)。这项观察性研究的目的是比较亚胺培南/克拉维酸的治疗作用与美罗培南/克拉维酸添加到治疗耐多药和广泛耐药结核病例的背景方案中。
84例使用含亚胺培南/克拉维酸方案的患者显示出相似的抗生素耐药中位数(8与8)但氟喹诺酮类耐药较多(79.0%)与48.9%, p<0.0001)和更高的广泛耐药结核患病率(67.9%)与49.0%, p=0.01),与96例接受美罗培南/克拉维酸方案的患者相比。患者接受亚胺培南/克拉维酸和美罗培南/克拉维酸含方案治疗的中位数(四分位数范围)为187 (60-428)与分别为85(49-156)天。
痰涂片转换率与培养转换率差异有统计学意义(79.7%)与94.8%, p=0.02和71.9%与94.8%, p<0.0001)和成功率(59.7%)与77.5%, p = 0.03)。亚胺培南/克拉维酸和美罗培南/克拉维酸的不良事件仅在5.4%和6.5%的病例中报告。
我们的研究表明,美罗培南/克拉维酸在治疗耐多药/广泛耐药结核病患者方面比亚胺培南/克拉维酸更有效。
摘要
美罗培南/克拉维酸在治疗耐多药和广泛耐药结核病患者方面比亚胺培南/克拉维酸安全有效http://ow.ly/Z4S2o
简介
据世界卫生组织(世卫组织)估计,2014年发生的耐多药结核病新发病例超过48万例,死亡病例19万例,目前只有四分之一的耐多药结核病病例得到诊断和治疗[1].2014年向世卫组织通报的12.3万例耐多药结核病病例中有一半发生在印度、俄罗斯联邦和南非。在全球范围内,3.3%的结核新病例和20%的以前治疗的结核病例携带耐多药结核毒株结核分枝杆菌.总体而言,9.7%的耐多药结核毒株符合广泛耐药结核的标准(如。对至少一种氟喹诺酮类药物和一种二线注射药物的耐药性),这一比例在一些前苏联国家(白俄罗斯29%,拉脱维亚15%和格鲁吉亚15%)要高得多[1,2].
最近的证据表明,使用目前可用的药物治疗耐多药和广泛耐药结核病患者时间长、费用高、复杂,并伴有频繁的不良事件[3.- - - - - -8].
目前,世卫组织建议逐步使用二线抗结核药物(分为五组)[7,9].
临床医生治疗耐多药和广泛耐药结核病例面临的主要困难是确定至少四种活性药物,这是根据世卫组织指南设计有效的多药方案所必需的[3.,4,7,10,11].新药,如德拉曼尼,[12- - - - - -14和苯达奎林[15- - - - - -20.],以及一些改变用途的药物(目前列入世卫组织第5类药物,即。疗效和/或耐受性证据未知/有限的药物)目前正引起科学界的兴趣[7,21],其中利奈唑胺[10,22- - - - - -28和碳青霉烯类[29- - - - - -34].碳青霉烯类药物,包括美罗培南、亚胺培南和厄他培南,目前被用于治疗耐多药结核病和广泛耐药结核病病例,尽管关于其有效性、安全性和耐受性的现有证据极其有限[29- - - - - -34].
不幸的是β-内酰胺类抗生素的有效性是有限的结核分枝杆菌是通过β-内酰胺酶保护的,由blaC基因(35,36].最近的研究表明,克拉维酸(β-内酰胺酶抑制剂)可以抑制β-内酰胺酶的活性blaC编码的产品在体外[36].美罗培南为水解提供了有限的底物,显示出很高的杀菌性在体外与棒骨酸盐缔合的活性结核分枝杆菌(易感、耐多药和广泛耐药结核株)以及在活的有机体内能在两周内对培养物进行消毒[37,38].此外,一项研究表明,与阿莫西林和美罗培南协同作用[39].这已在小鼠模型中得到证实[40].最初在10例或以下的两份病例报告中提出其有效性[30.,41,然后被两个病例对照研究证实。第一项研究样本量有限(一个中心37名患者),结果表明该药是有效的(提供高达20-30%的杀菌力),且耐受性良好[29].第二项较近的研究是由国际碳青霉烯类研究小组(ICSG,前身为欧洲碳青霉烯类研究小组)在欧洲和拉丁美洲的17个中心和6个国家进行的,有超过90例病例。它证实美罗培南/克拉维酸酯是安全的,并且该药物组合的活性是有希望的,因为病例和对照组之间的痰涂片转换、培养转换和治疗成功率已被确定,尽管对照组的耐药模式比美罗培南/克拉维酸酯治疗的病例要轻得多[42].
关于亚胺培南/克拉维酸的证据更加有限,包括一系列10例患者和1例病例报告[33,34].
最近,国际结核病研究小组辖下的结核病参考资料中心[31,42]开展了一项大型观察性研究,评估在治疗耐多药结核病和广泛耐药结核病病例时(根据世卫组织指南)将亚胺培南/克拉维酸酯添加到背景方案中的治疗作用。
本研究的目的是比较美罗培南/克拉维酸和亚胺培南/克拉维酸在耐多药结核病患者的一个大型观察队列中的有效性、安全性和耐受性。
材料与方法
方法特征已在前面描述过[42].位于欧洲和南美国家的耐多药结核病参考中心招募了培养确认的耐多药结核病患者,年龄≥15岁。耐多药结核病例定义为由结核分枝杆菌菌株表型耐异烟肼和利福平。根据患者在强化期和/或持续期对美罗培南/克拉维酸酯和亚胺培南/克拉维酸酯的暴露情况,对患者进行连续选择。
根据外部质量保证实验室进行的药敏试验(DST)结果,实施了个体化结核病方案[11].主治医师在处方抗结核药物时没有任何强制性的实验方案标准,因此没有遵循盲法或随机方法。美罗培南/克拉维酸以每日剂量美罗培南1 g,每日三次静脉注射加阿莫西林/克拉维酸1.2 g,每日三次。唯一的例外是比利时中心,美罗培南的每日剂量为2g,每日三次(17/180,9.4%)。亚胺培南/克拉维酸按500 mg亚胺培南剂量每日四次加阿莫西林/克拉维酸如上所述。
标准化特别的制作电子表格,收集流行病学资料(即。住院时间、年龄、出生地点、性别、居住地、来自结核病高负担国家的移民)、临床(即。艾滋病毒感染状况、艾滋病毒药物的使用、以前的结核病诊断和治疗、以前的治疗结果、放射学检查结果、结核病治疗和相关不良事件、美罗培南/克拉维酸和亚胺培南/克拉维酸暴露时间、手术、治疗基线时痰涂片和培养阳性、30天、60天和90天痰涂片和培养转换时间、世卫组织治疗结果)和微生物(即。DST结果来自官方医疗档案的信息。
定性和定量变量以百分比和平均值±进行总结sd或中位数(四分位范围(IQR)),取决于它们的常态。定性变量和定量变量分别采用卡方或费雪精确量检验和曼-惠特尼检验进行比较。亚胺培南/克拉维酸组和美罗培南/克拉维酸组在痰涂片和培养转换方面的差异采用生存分析和log-rank检验进行评估。p值<0.05(双侧)被认为有统计学意义。使用Stata 13.0 (StataCorp, College Station, TX, USA)进行统计计算。
根据ICSG不同国家和协调中心实施的法律,参与机构的机构审查委员会获得了对收集和分析匿名和回顾性数据以及对药物的同情使用的伦理批准。
结果
选取180例耐多药结核病患者进行分析:96例(53.3%)暴露于美罗培南/克拉维酸,84例(46.7%)暴露于亚胺培南/克拉维酸(表1).
队列的主要性别为男性(105,58.3%),中位(IQR)年龄为35(26-45)岁(表1).
来自结核病高流行国家的移徙者占100名(55.6%)患者,而感染艾滋病毒的比例很低(5.8%)。流动人口比例较高(76.0%)与32.1%, p<0.0001)和出生在欧洲的患者(75.0%)与美罗培南/克拉维酸酯治疗组为45.2%,p<0.0001) (表1).
179例(98.3%)病例中有176例诊断出肺结核。痰涂片阳性和痰培养阳性的比例分别为89.4%和97.8% (表2).
半数以上的人受到广泛耐药结核的影响(57.8%;亚胺培南/克拉维酸组和美罗培南/克拉维酸组分别为67.9%和49.0%,p=0.01),但耐药中位数相似(8与美罗培南/克拉维酸组和亚胺培南/克拉维酸组分别为8例,p=0.34) (表2).
超过四分之三的病例以前曾接受过对药物敏感或耐药结核病的治疗;然而,暴露于含亚胺培南/克拉维酸的方案的患者在之前的结核病诊断中更频繁地接受治疗(91.7%)与69.5%, p < 0.0001)。然而,美罗培南/克拉维酸和亚胺培南/克拉维酸治疗组之前抗结核治疗的中位数(IQR)数相似(2 (1-4))与2 (1-3)) (表1).
在亚胺培南/克拉维酸酯治疗的病例中,对任何氟喹诺酮类药物的耐药发生率显著高于对照组(79.0%)与48.9%, p < 0.0001);此外,对卷曲霉素的耐药发生率较高(63.9%)与46.9%, p=0.04)和卡那霉素(75.8%)与49.3%, p<0.002)与美罗培南/克拉维酸酯治疗组比较。两组患者对阿米卡星耐药的发生率相似(50.0%)与分别为48.8%)(表1).
患者接受美罗培南/克拉维酸和亚胺培南/克拉维酸含方案治疗,中位(IQR)分别为85(49-156)和187(60-428)天(表3).18.2%的病例接受了辅助手术治疗。
美罗培南/克拉维酸组的痰涂片和培养转换率(分别为94.8%和94.8%)显著高于亚胺培南/克拉维酸组(分别为79.7%和71.9%,p=0.02和p<0.0001)。根据耐多药/广泛耐药结核状态和耐药中位数(即。耐药≥8例)(表2).
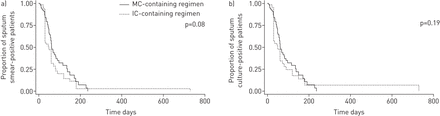
美罗培南/克拉维酸组的培养转化时间比亚胺培南/克拉维酸组短(44 (28-75))与60(30-90)天,p=0.05) (表2而且图1).
a)使用美罗培南/克拉维酸(MC)-治疗的多药和广泛耐药结核病患者的痰涂片和b)培养转换与含亚胺培南/克拉维酸(IC)的方案。
总体而言,美罗培南/克拉维酸治疗的病例比亚胺培南/克拉维酸治疗的病例获得了更高的具有统计学意义的成功率(77.5%)与59.7%, p=0.03) (表2).
不良事件仅在6例(6.5%)美罗培南/克拉维酸治疗患者和3例(5.4%)亚胺培南/克拉维酸治疗患者中报告(p=1.0) (表3).
讨论
本研究的目的是回顾性比较美罗培南/克拉维酸和亚胺培南/克拉维酸在一大批XDR- tb和MDR-TB患者中的有效性、安全性和耐受性。
我们的研究结果表明,总体而言,含美罗培南/克拉维酸酯方案比含亚胺培南/克拉维酸酯方案取得了更好的效果。特别是,1)培养转换率在统计学上更高(在整个队列和XDR/MDR-TB亚组中),2)培养转换率的时间更短,3)美罗培南/克拉维酸盐组的治疗成功率显著高于含亚胺培南/克拉维酸盐组(在整个队列和耐药≥8的患者中)。
此外,该研究表明这两种药物耐受性良好,不良事件很少(美罗培南/克拉维酸组只有6.5%,而含亚胺培南/克拉维酸组只有5.4%)。
据我们所知,这是科学文献中描述含亚胺培南/克拉维酸方案的有效性、安全性和耐受性的第一项研究,并比较了两种核心碳青霉烯类药物的临床表现(即。亚胺培南/克拉维酸和美罗培南/克拉维酸)在XDR和MDR-TB患者的一大队列中进行了研究。
在之前同一小组的一项研究中[42含美罗培南/克拉维酸钠方案的性能与对照组进行比较。研究结果表明美罗培南/克拉维酸酯是活性的,因为含美罗培南/克拉维酸酯的方案与对照组相比取得了相同的结果,尽管有更严重的耐药情况。
尽管很难将观察到的结果归因于美罗培南/克拉维酸和亚胺培南/克拉维酸,但我们可以强调,含亚胺培南/克拉维酸的方案在细菌学和治疗成功率上与其他耐多药结核病病例队列相当[3.,4],而含美罗培南/克拉维酸的方案有良好的结果(94.8%的痰涂片和培养转化,77.5%的治疗成功)。为了消除观察设计造成的“背景噪声”,研究结果需要通过随机对照临床试验来确认。
从分子作用机制来看,亚胺培南比美罗培南更有活性[43].然而,这并不一定转化为更好的临床结果。药代动力学/药效学指标,以及游离药物浓度超过最小抑制浓度,可能有利于使用美罗培南/克拉维酸酯方案的组。此外,本研究中所处方的碳青霉烯类药物与其他抗结核药物的协同作用可能有所不同。
美罗培南/克拉维酸酯似乎对结核分枝杆菌与亚胺培南/克拉维酸相比,前者在治疗耐多药结核病中应优先使用。美罗培南/克拉维酸是否不可用,更高剂量的亚胺培南/克拉维酸是否可用假单胞菌感染可能会被注射(即。1克,每日四次),因为该药耐受性良好。
在这项研究的优势中,我们提到了亚胺培南/克拉维酸和美罗培南/克拉维酸组群的规模,以及从欧洲和拉丁美洲的参与中心收集的详细信息。在美罗培南/克拉维酸组和亚胺培南/克拉维酸组中,耐药模式、以前的抗治疗周期数以及大多数人口统计学、流行病学和临床变量没有显著差异。
然而,该研究的观察性和回顾性设计决定了一些解释的局限性。特别是,我们提到了对样本量的预研究定义缺失,以及随机化和确保盲性的可能性,这可能会增加选择偏差的概率。此外,在亚胺培南/克拉维酸队列中,对任何氟喹诺酮类药物的耐药发生率较高,以及对三分之二的二线抗结核注射剂(卡那霉素和卷曲霉素)的耐药发生率较高,显然突出了后一种方法问题。此外,在亚胺培南/克拉维酸组中,既往抗结核治疗的暴露和既往治疗失败的比例较高。
由于美罗培南/克拉维酸酯似乎表现更好,但亚胺培南/克拉维酸酯更便宜,更容易获得,经济分析对最终评估这些化合物的未来作用将是重要的。然而,这项观察性研究提供的新信息使管理难治性结核病病例的临床医生知道,在缺乏设计有效方案所需的最低活性药物数量时,如何使用碳青霉烯类和其他重新使用的药物[3.,4,9,44- - - - - -47].
在这种情况下,其他二线药物,如氟喹诺酮类或氯法齐明,可能导致心脏病或其他不良事件[48].与上述所有药物不同的是,重新使用的碳青霉烯类药物通常具有良好的耐受性,且很少发生药物-药物相互作用,如果有需要,可基于其优越的安全性和耐受性替代其他结核病药物。这组作者认为,使用β-内酰胺治疗结核病的好处超过了进一步产生抗微生物药物耐药性的风险。
尽管新的化合物有望很快出现,以支持消除结核病的行动[49,碳青霉烯类被证实具有特殊作用。作者建议在强化治疗阶段使用美罗培南/克拉维酸,特别是在达到细菌转化之前处理最严重的病例。如果在继续期缺乏有效药物设计有效方案,可以在继续期考虑厄他培南/克拉维酸或法罗培南/克拉维酸。鉴于阿莫西林/克拉维酸在社区中广泛使用,建议在用药方案中使用该药物之前对美罗培南/克拉维酸进行DST。
脚注
利益冲突:没有声明。
版权所有©ERS 2016
- 收到了2016年1月28日。
- 接受2016年2月26日。
- 版权所有©ERS 2016