摘要
系统回顾贝达喹啉在新的有效耐多药/广泛耐药结核治疗方案中作用的现有科学证据http://ow.ly/V68ZF
世界卫生组织(世卫组织)新的“终止结核病战略”强调了充分管理耐多药结核病和广泛耐药结核病病例对控制和消除结核病的重要性[1,2]作为第一支柱(以病人为中心的综合护理和预防;要点2:治疗所有结核病患者,包括耐药结核病,以及对患者的支持)以及最近发表的《低发病率国家消除结核病框架》的优先行动5(优化耐药结核病的预防和护理)和相关背景文件[3.- - - - - -5].此外,在终结结核病战略(支柱3:加强研究和创新)和在低发病率国家消除结核病框架(优先行动7:投资于研究和新工具)中,都强烈强调需要新的抗结核药物[1,3.,6].如果你仔细观察耐多药结核病流行的各个方面以及迄今取得的治疗成功,就会发现需要新的抗结核药物的原因是相当明显的。
在世卫组织估计的2014年发生的48万例耐多药结核病病例中,只有12.3万例(四分之一)得到诊断和通报[1].总的来说,3.3%的新病例和20%的再治疗病例含有耐多药结核的耐药菌株结核分枝杆菌,其中9.7%已证实为广泛耐药结核[1].耐多药结核病例流行率最高的国家是白俄罗斯(新发病例占34%,再治疗病例占69%),据报告该国29%的病例为广泛耐药结核[1,7].
迄今为止,耐多药结核病和广泛耐药结核病的治疗已被证明是漫长、昂贵和难以管理的,不幸的是,其结果在大多数队列中都不是最理想的[8,9].尽管广泛耐药结核病例实际上只占所有耐多药结核病例的相对较小比例(9%),但它们的治疗和管理对临床医生和国家规划都具有更大的挑战性[1].在全球范围内,2012年队列中耐多药结核病病例的治疗成功率为50%(16%死亡,16%失去随访,10%失败,8%没有结果信息)。不幸的是,在耐药模式超过广泛耐药结核病的病例中,治疗成功的比例低至20%,失败和死亡的比例为49% [8,10].
设计治疗耐多药结核病和广泛耐药结核病的有效方案是基于逐步使用二线结核病药物,这些药物的选择需要通过药敏试验(DST)来指导[11- - - - - -13].不幸的是,在规划层面上,既没有所需的药物,也没有用于测试它们的特定DST总是可用的[11- - - - - -13].此外,联合二线药物设计最佳方案的可能性往往受到一些重大不良事件的影响,这些不良事件对治疗的依从性产生负面影响[14,15].
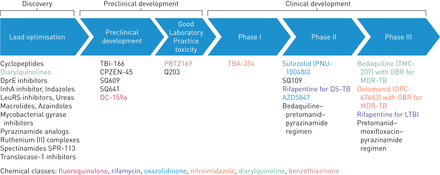
在过去几年中,治疗耐多药/广泛耐药结核病的新药在试验后开发出来,鉴于其初步(尽管不完整)疗效数据,它们已获得临时批准,而其他注册试验仍在进行中[16,17].最新的新药研发计划在图1[1].
2015年8月,结核病新药研发管道。所列项目详情可浏览http://www.newtbdrugs.org/pipeline.php没有确定先导化合物系列的正在进行的项目可以在http://www.newtbdrugs.org/pipeline-discovery.php.OBR:优化背景方案;DprE: decaprenylphosphoryl -β-D-ribose2的差向异构酶;InhA:抑制素α;LeuRS:亮氨酸- trna合成酶;耐多药结核病:耐多药结核病;DS-TB:药物敏感结核病;LTBI:潜伏性结核感染。转载自[1,并得到出版商的许可。
虽然现在对利奈唑胺的疗效和耐受性了解更多[18- - - - - -25]最近,人们对使用其他重新提出的化合物(碳青霉烯类化合物[26- - - - - -28]、磺胺类[29,30.]和甲氟喹[31],以及其他药物)、新的抗结核药物delamanid [32]和贝达喹啉尤其有希望[33- - - - - -35].
的欧洲呼吸杂志最近发表了几篇关于同情地使用贝达喹啉的文章[36,37]以及以欧洲呼吸学会/世卫组织结核病咨询为基础的delamanid同情规划[188bet官网地址38- - - - - -45].为了更好地理解贝达喹啉在未来新疗法中的作用,我们系统地回顾了该药物现有的科学证据。
使用搜索引擎PubMed,使用关键词贝达喹啉和疗效/有效性检索描述含贝达喹啉方案结果的上市后研究。采用了严格的选择标准,不包括病例报告和病例系列、信件、社论和评论。搜索中没有时间范围(直到2015年11月1日)或语言限制。共检索到216条记录。迄今为止,除了不到10个病例系列/报告(包括一项结核病/艾滋病毒合并感染者的中期队列分析)之外,还没有发表过上市后的实验研究,以评估上市前试验后对普通人群的有效性。搜索结果,其中包括Pym等.[46]的摘要表1.
在本期的收获Pym等.[46来自TMC207-C209研究的报告结果。本研究为2期多中心、开放标签、单臂试验(TMC207-C209;ClinicalTrials.gov标识符:NCT00910871),以证实贝达喹啉的安全性和有效性。该试验招募了233名患者(63.5%为耐多药结核,18.9%为前广泛耐药结核,16.3%为广泛耐药结核)。大部分(87.1%)患者在既往治疗期间曾使用过二线药物。在功效方面,Pym等.[46]观察到24周时的培养转换是持久的,并与120周时反应的高可能性相关。120周时的最终培养转化率为72.2%,当耐药模式恶化时,转化率下降,即。在耐多药结核、广泛耐药结核前和广泛耐药结核病例中分别为73.1%、70.5%和62.2%。
在考虑安全性时,最常见的不良事件是在耐多药结核病治疗期间通常观察到的不良事件。此外,只有6名(2.6%)受试者因不良事件或与耐多药结核病相关的事件在第24周之前停用贝达喹啉;背景治疗方案的终止更为频繁。必须强调的是,只有2例患者有临床显著的QTcF延长(>500 ms):其中1例在贝达喹啉组,而两人都开了氯法齐明(已知心脏毒性);1例患者报告低钾血症。观察到显著的死亡率(16例(6.9%)死亡),尽管在贝达喹啉治疗期间仅发生3例死亡(1例死于肾损害,2例死于晚期结核病)。如其他地方所述,调查人员必须更深入地评估具体的死亡原因和与死亡有关的风险因素[47].最常见的死亡原因是结核病或相关疾病,16例死亡患者中有10例从未实现痰涂片和培养转换。在修订所有患者的死亡原因后,所有死亡患者均未出现QTcF延长>500 ms或出现3级或4级肝脏不良事件(即。肝功能衰竭或肝功能测试水平高于正常水平3倍以上)。
贝达喹啉:作用机制
Bedaquiline是一种新的化合物(以前称为TMC207和R207910),属于二芳喹啉族(图2).它由Janssen Pharmaceuticals (Titusville, NJ, USA)开发[48].这种新型抗结核药物是同类药物中的第一种,它具有一个喹诺啉类中心杂环核,其中醇和胺侧链负责其抗真菌活性。它是唯一一种靶向分枝杆菌能量代谢的抗结核药物,抑制分枝杆菌ATP合成酶[48,49].贝达喹啉并非只对耐药有效M。肺结核分离株,但也针对药物敏感菌株。有效半衰期为>24 h。[48].
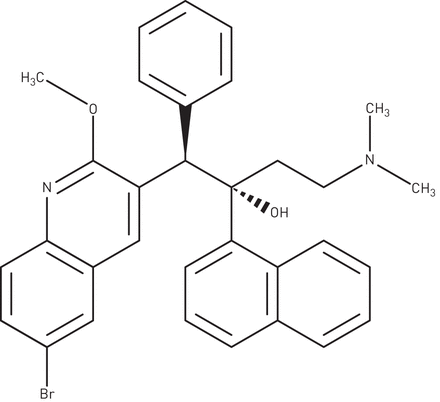
贝达喹啉的分子结构。
贝达喹啉已在美国(2012年)和欧洲(2014年)获得加速或有条件批准用于耐多药结核病,世卫组织提供了其使用的临时指南[46,50].
试验
起初进行了剂量测定研究,以调查贝达喹啉的早期杀菌活性、安全性、耐受性和药代动力学[51].随后,专注于MDR-TB的II期C208试验招募了47名患者,这些患者被随机分配给安慰剂或贝达喹啉[52].在接触贝达喹啉的小鼠中观察到较高的培养转化率。同一研究的第二阶段(C208第二阶段)是IIb期随机多中心双盲安慰剂对照研究,涉及160名受试者[53].使用贝达喹啉治疗组的痰涂片时间和痰培养转换时间显著缩短。
程序介绍的步骤
在一个新国家引进贝达喹啉治疗耐药结核病通常先于“标准监管注册”。它可以通过一些替代或互补的机制来实现[54- - - - - -57].
通过国际规划管理的同情性使用,要么由制造商发起,要么由捐助者主导。这一机制一直持续到制造商提交注册文件和地方当局允许临时注册为止,或者直到扩大准入计划开始为止。
扩大获取规划是受管制的规划,向更大的人群提供药物,但仍有限制。要求药物的处方中心通常必须满足几个条件,患者的选择应遵循特定的规则。这一直持续到项目完成(如果已经安排了最大数量的治疗)或直到药物最终注册。
临时注册允许在指定的专业临床中心处方,但该药物在该国可获得,并由当地卫生当局或健康保险报销。在这一阶段进行进一步的研究,以评估药物的疗效和安全性。此外,在当地进行药物警戒,以早期识别潜在的尚未识别的不良事件。
开放的问题
安全性和耐受性
最常见的药物不良反应(即。在对照试验中,> - 10%的患者在贝达喹啉治疗期间观察到恶心、关节痛和头痛。然而,与安全性和耐受性相关的两个关键问题仍未解决,只有其他数据,如本期《生物医学杂志》报道的数据收获,将澄清这些问题[53].
第一个问题是,在一项基于120周随访窗口的研究中,贝达喹啉治疗组报告的死亡风险增加(79人中有9人(11.4%)),而安慰剂治疗组(81人中有2人(2.5%))[53].这种报告的死亡不平衡仍然无法解释,在随后的试验中也没有得到证实[46,58,59].
第二个问题是QTc的延长。在最初的研究中,即使停药后,贝达喹啉组的QT仍持续增加。此外,贝达喹啉与其他药物合用可导致QTc延长(如。氟喹诺酮类和氯法齐明)在大多数研究中显示出额外的效果[58- - - - - -60].基于这一论点,世卫组织迄今未建议贝达喹啉和德拉马尼合用[6,45,61].实际上,它们的引入和(最终)共同管理应遵循世卫组织的建议并符合特定标准[45].事实上,世卫组织建议,新药贝达喹啉和delamanid在按照世卫组织指南设计的优化背景方案的健全结核病控制规划中开处方,使用正确的剂量,建立药物警戒系统,获得患者的知情同意并实施适当的监测(即。QT间期监测,特别是贝达喹啉)[50,61,62].在为零星病例共同用药提出的标准中,最相关的标准可能是:不可能设计出有效的治疗方案;治疗中心至少具有国家资质;可以获得知情同意;药物警戒已到位;同时开出这两种新药的选择得到了专家意见的支持。45].
耐药和药敏试验
可能对贝达喹啉产生耐药性。一个突变体atpE基因似乎是造成这种抗性的原因。63].在Pym等.[46所有12例基线后贝达喹啉最小抑制浓度增加≥4倍的患者均存在Rv0678突变,Rv0678是MmpS5-MmpL5外排泵的转录抑制因子[46,48].最近,这种新型的耐药性外排机制已被确定为对贝达喹啉和氯法齐明的低水平耐药性的原因[48,64,65].不幸的是,迄今为止,还没有制定和商定足够的测试贝达喹啉敏感性的方案[34,35].
儿科使用
一些关于贝达喹啉的研究已经完成,导致其仅被批准用于成人[46,52,53].因此,目前,如果绝对需要一种额外的活性药物来治疗受MDR/XDR-TB影响的儿童,只有在无法建立有效方案的情况下,贝达喹啉才能在个案基础上使用[66].
已计划开展一项儿科II期、开放标签、多中心研究,该研究应纳入确诊或可能患有肺部耐多药结核病的年轻受试者(0-18岁),以评估贝达喹啉与背景方案联合使用的药代动力学(ClinicalTrials.gov标识符:NCT02354014).
结论
贝达喹啉是一种治疗耐多药结核病和广泛耐药结核病的新药物。新的证据表明,耐受性比预期的好,报告的QT间期的影响可以在专门的中心得到适当的管理。
从长远来看,贝达喹啉可能被用于治疗MDR/XDR-TB的新有效方案,其中将不包括利福平和异烟肼(定义MDR- tb的两种药物)。这将(希望)允许用相同的方案治疗药物敏感和耐药病例。此外,在抗逆转录病毒药物和利福霉素之间没有任何负面相互作用的情况下,这些新方案将使艾滋病毒合并感染者更容易管理。贝达喹啉也是耐多药结核病缩短治疗方案的候选成分[67].事实上,为了找到耐多药结核病治疗带来的挑战的应对措施,国际抗结核和肺病联盟已与伦敦大学学院医学研究理事会临床试验部门合作,评估耐多药结核病的缩短治疗方案,在研究的第二阶段,贝达喹啉已被纳入测试缩短治疗方案[67,68].此外,为了促进发展中国家获得贝达喹啉和其他新的抗结核药物,2014年,由卫生伙伴(美国)提供资金的国际药品采购机制国际药品采购机制启动了一个项目,目的是在接下来的4年里用包含新的抗结核药物的方案治疗3200名耐多药结核病患者[69].
世卫组织目前不建议的德拉马尼和贝达喹啉可能联合使用的问题[45,50,61),需要进一步的证据来保护患者免受与两种新药联合相关的潜在不良事件,以及来自背景方案中使用的药物的不良事件。为指导进一步研究,可考虑的标准已于最近描述[45].
此外,贝达喹啉在治疗潜伏性结核感染方面的潜力值得未来关注[70].
脚注
利益冲突:可以在本文的在线版本中找到信息披露www.qdcxjkg.com
- 收到了2015年11月13日。
- 接受2015年11月16日。
- 版权所有©ERS 2016