文摘
Linezolid标示外使用治疗耐多药结核病(mdr - tb)在没有系统的证据。我们进行了系统回顾和荟萃分析疗效,安全性和耐受性linezolid-containing政权基于个人数据分析。
12个研究(从三大洲11个国家)报告完整的信息安全,耐受性,功效linezolid-containing政权在治疗耐多药结核病病例根据首选项报告系统评价和荟萃分析指南。荟萃分析使用个人数据执行121年的一个明确的患者治疗结果(完成治疗,死亡或失败)。
达到最耐多药结核病例痰涂片(86年(92.5%),93年)和文化(100(93.5%)107)转换后个性化治疗方案包含linezolid(中位数(内部四分位范围)次涂片和文化转换为43.5(21 - 90)和61年(29 - 119)天,分别)和99年(81.8%),121名患者被成功治愈。未发现显著差异的子群疗效分析(每日linezolid剂量≤600毫克与> 600毫克)。不良事件观察63年107例(58.9%),其中54(68.4%)的79个主要不良事件,包括贫血(38.1%),周围神经病变(47.1%)、胃肠道疾病(16.7%)、视神经炎(13.2%)和血小板减少症(11.8%)。不良事件的比例明显高于当linezolid每日剂量超过600毫克。
研究结果表明,一个优秀的功效还谨慎的必要性linezolid的处方。
结核病是全世界发病率和死亡的主要原因。在过去的几十年中耐药结核病病例,尤其是耐多药结核病(mdr - TB);定义为在体外至少耐异烟肼和利福平,两个最强大的一线抗结核药物治疗)和广泛耐药结核病(xdr - TB);定义为在体外耐异烟肼和利福平加任何氟喹诺酮类和至少一个二线注射药物:阿米卡星,或硫酸卷曲霉素),描述了在几乎所有接受调查的国家(1- - - - - -3]。
管理耐多药结核病和广泛耐药结核病仍然是一个主要问题从临床和公共健康的角度来看(1- - - - - -5]。证据表明,抗结核治疗结果为“复杂”的耐多药结核病(如。那些额外的阻力超出异烟肼和利福平)和广泛耐药结核病例仍然是次优的,强调迫切需要信息安全,耐受性和疗效的新抗生素(6- - - - - -15]。
在体外和药理数据表明linezolid oxazolidinone抗生素,可以有效治疗分枝杆菌感染,包括耐多药结核病[16- - - - - -21]。
然而,临床经验对linezolid主要局限于案例报告和小案例系列包括non-tuberculous和结核分枝杆菌疾病(22- - - - - -29日]。
由于缺乏这种困难的情况下,可用抗生素治疗linezolid药物已经用于治疗耐多药结核病在几个国家,尽管缺乏随机对照临床试验来评估疗效,安全性和耐受性以及大型回顾性和前瞻性观察性研究8,13,15]。
数据使用linezolid治疗耐多药结核病是有限的。目前,只有七军团发表利奈唑包括10得多情况下,它们的大小介于12和85例(只有45功效的信息)(8,30.- - - - - -35]。
在最近的辩论围绕新的抗结核药物的使用36- - - - - -37)的作用和贡献治疗成功linezolid由于几个原因产生了更多的兴趣。首先,有限的证据表明,药物是非常活跃的反对结核分枝杆菌,虽然,它有一个高的价格。其次,一些不良事件归因于linezolid:多达41.2%的患者主要不良事件(主要贫血、血小板减少和多神经病)发表的最大队列(8]。第三,正确的剂量,优化疗效和耐受性尚未定义(38- - - - - -40]。linezolid的可能作用在未来短方案关键取决于下列问题的答案。正确的剂量和必要的曝光时间是什么?真的有效吗?其安全性和耐受性允许政府在一个足够的时间保证功效呢?
进一步支持发展循证指南的使用linezolid难治性耐多药结核病和广泛耐药结核病的情况下,我们提出系统回顾和荟萃分析的结果有效性、安全性和耐受性的linezolid基于个人数据分析。
材料和方法
搜索策略
我们确定了临床研究评估linezolid治疗耐多药结核病和广泛耐药结核病例。
我们计算机化的书目数据库,搜索PubMed和EMBASE,从2001年1月到2011年10月。此外,我们检查所有同期发表的摘要国际期刊的肺结核和肺部疾病。
以下搜索条件的组合使用:“肺结核”,“耐多药结核病”,“广泛耐药结核病”,“耐多药”,“XDR”、“安全”、“耐受性”、“有效性”和“linezolid”。我们限制我们的搜索英文出版物。不包括未发表的数据来源,评估他们的质量没有同行评议过程无法保证。我们还手动搜索的书目检索文章和现有的系统评价和荟萃分析对MDR -耐多药/广泛耐药结核病额外的引用。
研究选择
我们包括研究报告完整的信息安全,耐受性和疗效的治疗culture-confirmed linezolid耐多药结核病和广泛耐药结核病例在人类涉及≥5个成年个体(儿科患者的比例是需要<人群总数的25%)。
以下的研究被排除在外:1)病例报告< linezolid 5例、社论和评论;2)实验室研究;3)动物研究;4)研究耐多药结核病和广泛耐药结核没有确认结核分枝杆菌培养和药物敏感性试验(DST)在质量有保证的实验室。
研究报告所需的核心信息分析被排除在第二轮选择(如。从作者未能获得信息后,按照数据提取部分)。功效分析细菌学的转换和明确的结果中描述被定义为Lasersonet al。(41]。
安全性和耐受性分析,感兴趣的变量包括:linezolid接触linezolid-containing方案的剂量和持续时间;现有的不良事件;不良事件的描述(主要定义为那些需要中断的药物或调整剂量,和小)(8];和不良事件的发生时间。
引用被三个独立筛选调查人员(e . Zampogna (EZ), r .好像(RC)和g·费拉拉(GF))通过检查标题和摘要来识别潜在的相关研究,和差异是通过共识来解决(G.B. Migliori (GBM)和g Sotgiu (GS))。这些原始的文章被检索和全文最终的包容和数据提取筛查。
数据提取
一个标准化的电子特别的数据提取的设计形式。三个评论者(EZ、RC和GF)分析和交叉核对所有选定文章独立和提取数据。在偏差的情况下,最终的文档的数据是基于共识(GBM和GS)。两分的协议获得的数据包括研究∼100%。
高级和/或通信作者所选的文件是通过电子邮件联系,以验证的准确性抽象和获取文本信息缺失;包括潜在的有用的信息评价的有效性,安全性和耐受性linezolid-based方案的概要文件。
匿名个人数据提取并证实了高级和/或信件的作者包括手稿。功效分析收集以下变量:痰涂片转换和文化转换,和最终处理结果。
安全性和耐受性分析记录的协变量是:每日linezolid接触linezolid-containing方案的剂量和持续时间;不良事件;不良事件的描述;和不良事件的发生时间。
此外,收集以下变量:日历的研究;国家的研究;性;年龄;多方案组合或规定除了linezolid(药物、剂量和持续时间);耐药性资料;以前治疗的历史;超过30天以前的治疗方案。
没有道德的间隙要求匿名的流行病学分析,因为所有选定的研究曾接到当地的机构审查委员会批准。
统计分析
定性和定量描述,变量概括了比例,中位数和四分位范围(差);他们使用卡方测试相比,Wilcoxon Mann-Whitney测试,分别。
整合计算进行患者使用个人数据取自一个明确的治疗结果(完成治疗、治疗、死亡或治疗失败)(41]。随机模型被用来解释预测之间的色散。森林土地用于图形评估变化(即。点估计的95% CI)功效/安全协变量和每个队列的权重大小的计算池估计。之间的不一致性包括研究异质性是由卡方测试评估;不一致(我2)统计评估的角色真正的可变性而非抽样误差的整体变化。
子群分析集中在安全、疗效和耐受性linezolid和患者之间进行日常养生≤600毫克linezolid与那些接受每日养生> 600毫克linezolid。假定值< 0.05被认为是具有统计学意义。统计分析与占据9.0(美国StataCorp LP,大学城,TX)和Meta-Disc 1.4版(43)软件。
结果
特征选择的研究
6(50%)的12研究[8,22,33,35,44,47)在欧洲进行,四个(33.3%)在亚洲的12 (31日,32,45,46),和两个(16.7%)的美国12 (30.,34)(表2)。八12(66.7%)的回顾性观察研究(8,22,30.,34- - - - - -35,44- - - - - -46),4(33.3%)12人潜在的31日- - - - - -33,47]。绝大多数(66.7%,8个12)的研究进行单一、大学或大专,/门诊设置(22,31日- - - - - -32,35,44- - - - - -47]。
Linezolid治疗管理的选取和nonrandomised方式;所有的研究设计是计划没有对照组(表3除了米的多中心研究igliori等。(8];一个12 (8.3%)。除了两个结核病患者进入前瞻性或回顾性研究年龄≥15岁(8,22,30.- - - - - -32,35,44- - - - - -47)和所有个性化抗结核治疗基于DST的结果(8,22,30.- - - - - -35,44- - - - - -47]。Linezolid剂量范围从300毫克b.i.d。(22,46,47)400毫克q.d。或b.i.d。(34),和450毫克q.d。(30.)600毫克q.d。(8,30.- - - - - -33,34,35,45,46),b.i.d。(8,22,31日,33- - - - - -35,44,47)或三次一个星期30.]。
国际群体的特征
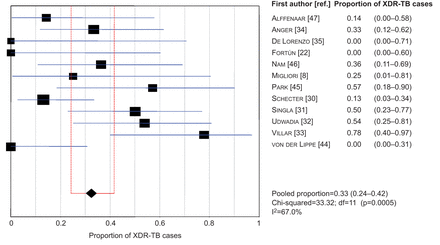
linezolid患者个体数据从121年开始在临床设置位于世界各地的(即。欧洲、北美、和亚洲)[8,22,30.- - - - - -35,44- - - - - -47收集(表1),4])。超过一半是男性(53.7%)和出生在亚洲国家(69.3%),与一个值(差)治疗发病年龄32岁(25-41)。已知的危险因素有利于结核病和耐多药/广泛耐药结核病的发展是在一些病人中发现:有35.4%是来自高结核病负担国家的移民;8.7%是HIV阳性;和76.9%以前接受抗结核治疗> 30天(中位数(差)暴露于抗结核药物的次数是1 (0 - 4))。几乎所有的个体与肺结核痰涂片阳性(102(92.7%)的110个)和显示腔的病变在基线胸片检查(79 (74.5%)。106)。广泛耐药结核诊断的人(我的32.5%2= 67.0%;图2)。四分之一的情况下进行手术,因为缺乏足够的活跃的药物或辅助干预。51岁的患者住院时间的数据,放电后发生的值(差)住院期间39(15 - 82)天。
森林图显示广泛耐药结核病(xdr - tb)患者的比例加入研究。数据提出了n (95% CI);我2:不一致性统计;df:自由度。
没有统计上显著的人口统计学、流行病学和临床特点被发现之间的每日剂量处理linezolid≤600毫克(72(59.5%)的121个),和那些接受每日剂量> 600毫克(49(40.5%)的121个)协变量除了“迁移”,“艾滋病毒积极性”和“手术”,更频繁的暴露组患者每日剂量> 600毫克。
包含linezolid政权的功效
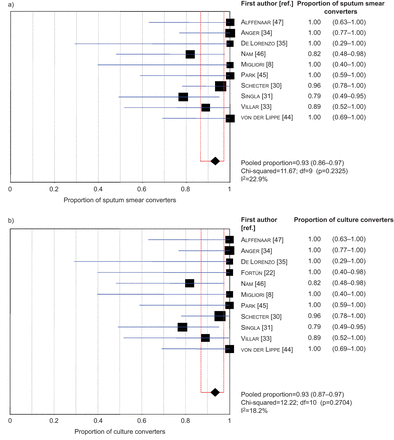
大多数的个体转化为痰涂片(86 93 (92.5%);我2= 22.9%)和文化(100 107 (93.5%);我2= 18.2%)接触后消极个性化linezolid-containing方案(表5和图3);中位数(差)痰涂片和培养时间转换为43.5(21 - 90)和61年(29 - 119)天,分别。
森林情节展示的比例)痰涂片转换器和b)文化转换器的研究。数据提出了n (95% CI);我2:不一致性统计;df:自由度。
超过80%的人成功治疗(99 121 (81.8%);我2= 44.8%),观察治疗失败和死亡的14.1%和4.1%为主题,分别是(图4)[41]。
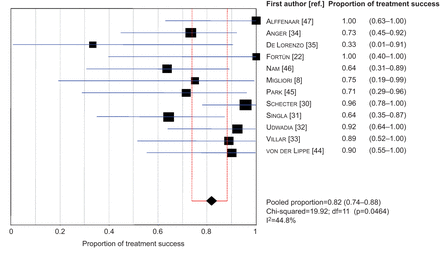
森林图显示患者的比例在注册成功的治疗研究。数据提出了n (95% CI);我2:不一致性统计;df:自由度。
未发现显著差异的子群疗效分析(每日linezolid剂量≤600毫克与> 600毫克);治愈∼80%的比例在两组和治疗失败和死亡的速度发生在不到四分之一在两组,分别。
linezolid的安全性和耐受性
大约每两个病人(63例(58.9%),107;我2= 82.2%)不良事件归因于linezolid包括54(68.4%)79(我的病人2= 73.1%)和主要不良事件,即。他们需要linezolid治疗中断或减少剂量(表6和图5)。主要的不良事件是贫血(38.1%;我2= 69.7%)和周围神经病变(47.1%;我2= 44.0%)(图6);其他血液病学的和明确的不良事件发生在较低比例的情况下,即。肠道疾病(16.7%)、视神经炎(13.2%)和血小板减少症(11.8%)。
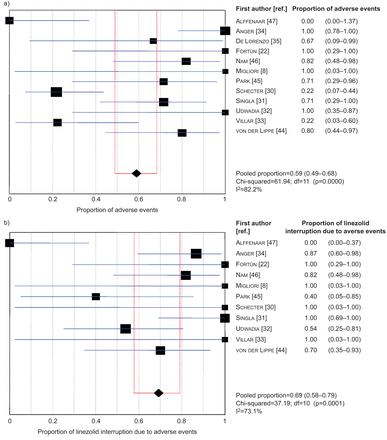
森林图显示)的比例患者不良事件的影响和b)患者中断治疗的比例由于不良事件登记研究,分别。数据提出了n (95% CI);我2:不一致性统计;df:自由度。
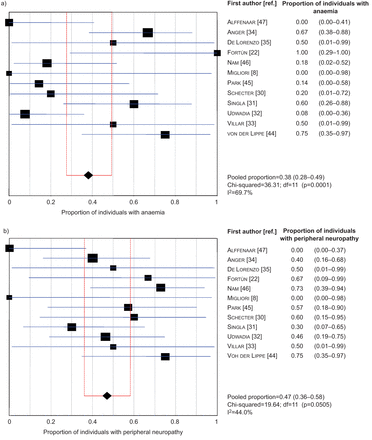
森林图显示)的比例个人影响贫血和b)的比例个人受到了研究周围神经病变的影响。数据提出了n (95% CI);我2:不一致性统计;df:自由度。
不良事件的风险显著提高归因于linezolid治疗中检测出队列处理linezolid每日剂量> 600毫克(74.5%与46.7%)。特别是,显著提高贫血(60%的概率与2.5%;p = 0.0005), leukopoenia (17.1%与2.0%;p = 0.012),胃肠道症状(29.4%与8.0%;p = 0.01)被发现尽管linezolid显著暴露时间较低(中值(差)曝光时间:252(120 - 540)天与589.5(154.5 -750)天)。
讨论
我们研究的主要结果阐明几个领域相关的临床使用linezolid,不是以前的观察性研究中描述:剂量和持续时间从一边和有效性,安全性和耐受性在另一边。大样本大小允许更多的分析和更健壮的推论,不是表现在过去。
系统回顾和荟萃分析的有效性、安全性和耐受性linezolid-containing政权的目的是支持未来的发展以证据为基础的指导使用linezolid难治性耐多药和广泛耐药结核病例。
剂量和持续时间
10的12个临床研究评价在目前分析使用linezolid在一天600毫克·−1。这个荟萃分析收集的数据在不同的设置没有发现统计学差异的治疗成功,比例的痰涂片或文化之间的转换器处理≤600毫克q.d。与这些处理> 600毫克b.i.d。
建立在每日600毫克剂量的证据可能会减少不良事件的发生,虽然不影响疗效,研究lffenaaret al。(47),提供了一个理由分装的每日总剂量600毫克,为了防止血液的峰值可能负责血液学的和明确相关的不良事件。
一个lffenaaret al。(47]表明,获得的血清浓度的linezolid后每300毫克b.i.d。都远高于最低抑制浓度(MIC),即。0.125 - -0.5 mg·L−1对结核分枝杆菌24 h)和血清浓度时间曲线/麦克风比率足够高(> 100)预测在七8位患者的疗效研究。本研究提供的证据表明,300毫克b.i.d。剂量可用于延长linezolid治疗,不良事件的持续有效性和局限性。
而正确地设计大样本随机药代动力学研究(包括比较的结果)会给一个最终答案linezolid的一剂良药,它似乎合理的执行在所有情况下暴露于药物动力学(35]。
虽然很贵,但linezolid标示外使用,非常长时间的曝光时间,超越其授权处方的长度28天(47]。在这个国际群linezolid治疗持续时间的中位数是300天(589.5天与252天的治疗linezolid≤600毫克q.d。和> 600毫克b.i.d。分别)。在两个研究规定出利奈唑酮为整个治疗期间,如。从18.6个月到20.6个月(30.,32]。最优时间linezolid使用仍然是未知的。linezolid管理更短的持续时间可能会减少不良事件的发生,但可能会影响疗效和/或获得性耐药的可能性增加。需要更多的信息关于这个主题,不能从进行观察研究。
有效性、安全性和耐受性
Linezolid证明是成功添加到DST-tailored时,个性化治疗方案由几个药物。抗结核治疗成功率和文化转换的汇集估计分别为82%和93%,分别。痰涂片和文化转换的平均时间是43.5天,61天,分别。
尽管有一定的变化,但所有的研究包括高百分比的严重耐多药结核病例和广泛耐药结核病患者;广泛耐药结核病例的混合比例是32.5%,67.0%的不一致,反映出不同的处方习惯的设置进行了研究。成功接受每天的病人之间相当linezolid≤600毫克剂量和高剂量,尽管发现定义广泛耐药结核患者,以及谁将为成功的可能性低于其他耐多药结核病患者,也分布在两个治疗组。
另一方面,研究结果证实linezolid管理受到一些毒性,尽管一个大变化主要不良事件已被观察到。正如前面所讨论的那样,毒性摄入量有关,低剂量时≤600毫克q.d。使用(47]。在八12的研究分析≥25%的病例主要不良事件,使中断的药物(或它的再度调整剂量)必要的。荟萃分析表明,任何不良事件的混合比例为59%,其中69%是主要的不良事件。
的优点和缺点
系统评价是基于一个样本量207例来自三大洲和11个国家(白俄罗斯、德国、印度、意大利、韩国、荷兰、挪威、葡萄牙、西班牙瑞士和美国)。
个人数据的荟萃分析包括大样本大小(n = 121例),代表所有的情况下有一个明确的结果(唯一例外的情况下,德国最大的气候资料(8])。虽然没有特定的人群从非洲和拉丁美洲,比例情况下出生在这些大洲都包含在我们的研究(分别为8%和6.7%)。
个人先于允许所有变量的分析计划,以便最终结论足够强劲,尽管不一定代表,他们可以谨慎地普遍。此外,亚组分析在两组相比,除了少数一些人口统计学上显著差异,流行病学和临床变量。荟萃分析的基础是由于nonrandomised,选取观测数据;因此,选择偏见不能排除在最初的研究中,以及发表偏倚。
此外,由于大多数入学的回顾性本质研究,不出利奈唑酮的疗效加权抗结核药物组合和其他临床和流行病学混杂变量。有利的结果可能是未被充分代表的比例如果linezolid被用作抢救药物,比被规定在受损的病人能够更好地容忍不良事件。
除了回顾研究发生的大时间跨度不大可能有偏见的结果。因此这个全球研究增加了新的信息,不是在迄今为止最大的单一研究[8)或其他选择较小的研究(30.- - - - - -35,44- - - - - -47]。
结论
我们研究的结果暗示一个优秀的功效还谨慎的必要性的处方linezolid用于治疗耐多药结核病。虽然在治疗耐多药结核病和广泛耐药结核病例有效,政府应该限制在严重的情况下额外的积极抗结核药物是必要的。它的作用在未来一代的短方案需要进一步的评估,尽管不支持一个简单outpatient-based使用药物特点结合新药,它预计将在不久的将来在市场上推出。≤600毫克/天的剂量(作为一个单一剂量或分为两个剂量)看上去是最好的建议,因为它最大限度地减少不良事件的发生而不影响疗效。高比例的病例出现不良事件,并要求药物中断或减少剂量表明使用linezolid应限于专业耐多药结核病参考中心,住院病人和门诊病人可以仔细监控任何严重不良事件的发生,设施装备精良管理任何严重的问题(包括可能需要输血)。
确认
作者的联系细节如下:g . Sotgiu和p . Castiglia:流行病学和医学统计单位,部门的生物医学科学,萨萨里大学,萨萨里,意大利;r .好像'Ambrosio l . D, e . Zampogna G.B. Migliori:世界卫生组织合作中心肺结核和肺部疾病,基金会Maugeri,保健和研究所Tradate,意大利;J-W.C。Alffenaar:格罗宁根大学、格罗宁根大学医疗中心,医院和临床药学部门,格罗宁根,荷兰;H.A.愤怒:纽约市卫生部门和心理卫生,结核病控制,纽约,纽约,美国;肺病学j Caminero:耐多药结核病的单位,部门,大学总医院大加那利岛”博士。•奈”,拉斯帕尔马斯,西班牙和国际防痨和肺部疾病联合会(工会),巴黎,法国;美国德洛伦佐:AOVV大肠Morelli医院,参考耐多药和艾滋病结核病医院,Sondalo,意大利;g·费拉拉:肺Allergi Kliniken,卡罗琳斯卡大学医院,斯德哥尔摩,瑞典,和部分的呼吸道疾病,内科医学部门,佩鲁贾大学特尔尼,意大利;W-J。 Koh: Division of Pulmonary and Critical Care Medicine, Dept of Medicine, Samsung Medical Center, Sungkyunkwan University School of Medicine, Seoul, Republic of Korea; G.F. Schecter: Tuberculosis Control Branch, Division of Communicable Disease Control, Center for Infectious Disease, California Dept of Public Health, Richmond, CA, USA; T.S. Shim: Division of Pulmonary and Critical Care Medicine, University of Ulsan College of Medicine, Asan Medical Center, Seoul, Republic of Korea; R. Singla: Dept of Tuberculosis and Chest Diseases, Lala Ram Sarup Institute of Tuberculosis and Respiratory Diseases, New Delhi, India; A. Skrahina: Clinical Dept, National Research and Practical Centre for Pulmonology and Tuberculosis, Minsk, Belarus; A. Spanevello: Università degli Studi dell'Insubria, Varese, and Fondazione S. Maugeri, Care and Research Institute, Tradate, Italy; Z.F. Udwadia: Dept of Pulmonary medicine, P.D. Hinduja National Hospital and Medical Research Centre, Veer Savarkar Marg, Mahim, Mumbai, India; M. Villar: Lung Diseases Centre of Venda Nova, Amadora, Portugal; J-P. Zellweger: TB Clinic, Dept of Ambulatory Care and Community Medicine, University of Lausanne, Lausanne, Switzerland; A. Zumla: Dept of Infection, Division of Infection and Immunity, Centre for Clinical Microbiology, University College London, London, UK.
脚注
支持声明
当前研究的资金参与机构和欧洲共同体第七框架计划(fp7/2007 - 2013)根据授权协议fp7 - 223681之下。
感兴趣的语句
没有宣布。
- 收到了2012年2月7日。
- 接受2012年3月19日。
- ©2012人队