摘要
自1973年第一届世界肺动脉高压研讨会(WSPH)以来,肺动脉高压(PH)被任意定义为静息时平均肺动脉压(mPAP)≥25 mmHg,通过右心导管测量。正常人的最新数据显示,正常的mPAP为14.0±3.3 mmHg。高于该平均值两个标准差表明mPAP高于正常上限(高于97.5%)。这个定义不再是武断的,而是基于科学的方法。然而,mPAP异常升高并不足以确定肺血管疾病,因为它可能是由于心排血量或肺动脉楔压增加所致。因此,第六届WSPH工作组建议将肺血管阻力≥3个木单位纳入与mPAP >20 mmHg相关的所有形式的毛细血管前PH的定义中。需要前瞻性试验来确定这些PH人群是否可以从特定管理中受益。
在临床分类方面,主要的工作组变化是将“肺动脉高压(PAH)对钙通道阻滞剂的长期反应者”亚组纳入第1组,这是由于这些患者的特定预后和管理,以及“具有明显静脉/毛细血管(肺静脉闭塞疾病/肺毛细血管瘤病)累及特征的PAH亚组,这是由于有证据表明动脉、多环芳烃的毛细血管和静脉受累。
摘要
肺动脉高压的血流动力学定义和临床分类的研究现状与展望http://ow.ly/TJeR30mgWKj
介绍
我们工作组的主要目的是重新评估肺动脉高压(PH)的血流动力学定义和临床分类。
关于定义,我们解决了两个问题:
1)我们是否应该重新定义PH和毛细管前PH?
2)应该重新引入运动PH作为PH定义的一部分吗?
另一个课题是更新临床分类,采用一些基本原则:1)维持目前成人和儿童PH分类的总体架构,2)只提供相关的修改,3)简化分类的核心
血液动力学的定义
PH的定义
1961年,世界卫生组织(WHO)慢性肺心病专家委员会的一份报告明确指出,受试者躺卧休息时,平均肺动脉压(mPAP)通常不超过15 mmHg,且该值受年龄影响较小,从未超过20 mmHg [1]。
自1973年世界卫生组织在日内瓦举办的第一届世界肺动脉高压研讨会(WSPH)以来,PH被定义为在休息时平卧位通过右心导管(RHC)测量的mPAP≥25 mmHg [2]。世卫组织日内瓦会议专门讨论了原发性酸碱度,这是一种严重的酸碱度,发生在与摄入厌食性药物氨基厌食症(aminorex)有关的疾病爆发几年之后。3.]。会议的报告承认,25毫米汞柱的正常平均血压上限多少是根据经验和任意界定的[2]。然而,这个保守的临界值使医生能够区分由原发性PH引起的严重PH和以低mPAP为特征的其他形式的PH(主要由肺部疾病引起)。该定义在1998年至2013年的会议期间保持不变[4- - - - - -6],至少部分是为了防止潜在的过度诊断和过度治疗PH。
正常mPAP的上限是多少?
2009年,Kovacs等。[7]分析了健康个体RHC研究获得的所有可用数据,以确定休息和运动时mPAP的正常值。分析了来自47项研究的1187名正常受试者的数据。静息时mPAP为14.0±3.3 mmHg;该值与性别和种族无关,仅受年龄和姿势的轻微影响。考虑到mPAP为14 mmHg,两个标准偏差表明mPAP bb0 20 mmHg高于正常上限(即。高于97.5%)。因此,这个定义不再是武断的,而是基于科学的方法。
单独使用的mPAP值不足以准确表征临床状况
无论确定PH值的mPAP临界值是多少(≥25或≤20 mmHg),必须强调的是,单独使用的该值不能表征临床状况,也不能定义病理过程本身。PAP升高确实可能有几种不同的原因,有不同的处理和结果,包括心排血量(CO)增加、左向右心脏分流、左心疾病(LHD)肺动脉楔压(PAWP)升高和高粘度。这种异常升高也可能是由于肺血管疾病(PVD)与小肺动脉结构改变有关。在目前的临床PH分型中,1、3、4组有毛细血管前PH, 5组有部分患者有毛细血管前PH和毛细血管后PH合并,2组很少有。
为了识别提示PVD存在的毛细血管前PH值,应将肺血管阻力高于正常水平的升高包括在定义中
将肺血管阻力(PVR=(mPAP - PAWP)/CO)纳入毛细血管前PH值的定义是必不可少的,这样可以区分PVD引起的PAP升高与paap升高或高CO引起的PAP升高。自2003年举行的第三届WSPH以来,第1组(肺动脉高压)的毛细血管前PH值被定义为mPAP≥25 mmHg, paap正常≤15 mmHg, PVR升高≥3 Wood Units (WU) [4- - - - - -6]。PVR≥3wu的临界值也是相当任意的,因为最近的一些数据表明PVR bbbb2wu也可以被认为是异常的[6]。从这个意义上说,使用PVR≥3wu的临界值是保守的,表明存在明显的毛细血管前ph。PVR≥3wu的值在不同的临床情况下被认为具有临床相关性,表明存在明显的PVD。如。它已被用作矫正先天性系统-肺分流的阈值[8]。此外,有研究表明,PVR≥3wu升高与心脏移植后生存不良相关[9]。在2018年第6届WSPH期间,对于第2组患者,LHD所致PH工作组推荐PVR临界值≥3wu来定义有毛细血管前成分的患者[10],即所谓的毛细血管前后联合PH值,与较差的预后相关。
我们建议将PVR≥3wu不仅包括在第1类预毛细PH的定义中,而且包括在所有形式的预毛细PH的定义中。
在慢性阻塞性肺疾病引起的PH患者中,严重PH (bbb40 mmHg)的PVR显著增加(约10 WU);这些患者通常有轻度PH (mPAP 20-30 mmHg),与较低的PVR相关,但通常保持bb3 WU [11],特发性肺纤维化患者也是如此[12]。在这些不同的慢性肺部疾病中,即使mPAP适度升高(20-29 mmHg)也与预后不良相关[13]。
在慢性血栓栓塞(第4组)中,一项大型国际登记报告了严重的毛细血管前PH值,mPAP为47 mmHg,平均PVR为8.9 WU [14]。在这种情况下,即使在轻度mPAP升高(20-24 mmHg)的患者中,PVR通常为bb0.3 WU。
PVD患者与mPAP 21-24 mmHg的预后
越来越多的数据表明,许多与mPAP升高相关的PVD患者,但低于先前定义PH的阈值(≥25 mmHg),有疾病进展的风险。
在系统性硬化症中,最近发表了诊断时mPAP在21 - 24 mmHg之间的患者的结果数据。2013年,一项单中心队列研究报道了228例系统性硬化症患者因怀疑PH而行RHC [15]。86例患者在基线时记录了mPAP 21-24 mmHg;其中,38例在随访期间(中位随访48±35个月)发生第二次RHC,其中16例(42%)出现明显的PH (mPAP≥25 mmHg)。16例患者基线时的平均mPAP和PVR分别为22±2 mmHg和2.9±0.6 WU;随访时,平均mPAP和PVR分别升高至31±6 mmHg和6.9±1.7 WU。诊断时所谓的边缘性mPAP的患者比mPAP≤20 mmHg的患者更容易发展为显性PAH (p<0.001;风险比(HR) 3.7)。在该队列中,PAH的事件发展不是良性的,尽管随后引入了双重口服联合治疗和/或治疗,但随访期间有5例死亡注射。环前列腺素。
最近,一项双中心队列研究确定了21例系统性硬化症患者,mPAP基线为21 - 24 mmHg [16];这些患者接受了第二次RHC,中位随访时间为3年。基线时,平均mPAP和PVR分别为22±1 mmHg和2.3±0.8 WU。随访时,mPAP和PVR分别升高至25±4 mmHg和3.2±1.6 WU。其中,7例(33%)患者出现明显的PH(3例PAH, 3例与间质性肺疾病相关的毛细血管前PH, 1例由LHD引起的PH) (J.G. Coghlan,英国伦敦皇家自由医院心脏科;个人沟通)。
2017年,一个奥地利组织[17]发表了一系列547例接受RHC的不明原因呼吸困难和/或有PH风险的患者。290例患者有明显的PH值(mPAP≥25 mmHg), 64例患者有边缘性PH值(mPAP 21-24 mmHg), 193例患者mPAP≤20 mmHg为“正常”;其中mPAP≤15mmhg的低正常137例。该队列中位随访时间为45.9个月;随访期间共有161名患者(29%)死亡。在多变量模型中,考虑到年龄和合共病,与“较低正常”组相比,临界PH和明显PH与较差的生存率显著相关,HR为2.37 (95% CI 1.14-4.97;p=0.022),危险度5.05 (95% CI 2.79-9.12;分别为p < 0.001)。在基线时,mPAP 21-24 mmHg组的PVR中位数为2.7 WU, 36%的患者PVR为bb30 WU。
另一个可以在早期诊断毛细血管前PH值的例子是慢性血栓栓塞,在这种情况下,由于死区通气增加导致通气效率降低,在静止时没有明显PH值时,运动限制可能会发生。最近,两组分别有42例和23例患者报道了广泛的持续性血栓栓塞,但没有PH [18,19]。诊断时mPAP为15-24 mmHg, PVR为2-3 WU。这些患者接受了肺动脉内膜切除术(PEA),并在WHO功能分级、运动能力和生活质量方面有了显著改善,6个月时无住院死亡率。在这两个中心,这种形式的慢性血栓栓塞对应于接受PEA治疗的总体人群的4%和7%。
总结与观点
mPAP为20 mmHg为正常值上限。这个新的定义最近由其他人提出[20.- - - - - -22]。然而,单独的mPAP异常升高不足以定义PVD,因为它可能是由于CO或paap升高引起的。
毛细管前PH最好通过同时存在mPAP bb0 20 mmHg, paap≤15 mmHg和PVR≥3wu (表1),强调RHC必须强制测量一氧化碳和精确测量pap。
多年来,PH的诊断是基于mPAP≥25 mmHg的任意值,可能是因为对过度诊断和过度治疗的担忧是可以理解的。事实上,过度诊断和治疗毛细前PH的主要原因是RHC诊断的不确定。
相反,这种困境的另一面可能是对一些PAP异常升高但不符合经典ph定义的患者治疗不足。今天,越来越多的证据表明,在一些pvd(主要是与系统性硬化症、慢性血栓栓塞和慢性肺部疾病相关的PAH)中,即使mPAP轻度升高(21-24 mmHg)的患者也有运动限制的症状,可能预后较差。然而,由于pvd导致的PH血液动力学定义的改变并不意味着要治疗这些额外的患者,但强调了在这一人群中密切监测的重要性。需要前瞻性试验来确定这些PH人群是否可以从特定管理中受益。
运动PH的定义
2004年,PH被定义为静息mPAP >25 mmHg或运动mPAP >30 mmHg [8]。然而,在2008年第四届世界湿地保护海港会议上,该定义的“运动”部分已被删除[23]。这在很大程度上是由于对正常衰老、CO变化与运动和肺血管生理之间相互关系的不确定性。在2018年的第六届WSPH上,这个问题再次被重新审视。
为什么锻炼PH值是相关的?
静息PH值升高是pvd自然史上的晚期事件,因为微血管“储备”。只有当微循环损失≥50%时,PAP才会升高[24]。很多努力都是为了在更早(可能更容易治疗)的阶段检测PVD。直观地说,通过增加CO来“揭露”PVD以显示增加的电阻是一个合乎逻辑的想法。此外,PH患者首先在运动时出现症状。
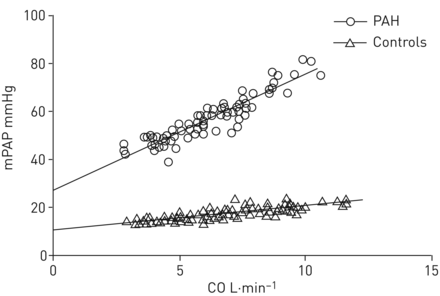
许多研究试图通过“压迫”肺循环,通过直立姿势的肺血流重新分配来揭开PVD的面纱[25]或增加CO [26]。这就产生了“多点mPAP”的概念- - - - - -“CO”曲线,其中mPAP随CO增加的上升速率提供了信息(图1)。一般情况下,正常受试者每升CO中mPAP升高≥1 mmHg;PVD患者每升CO升高≥3 mmHg,反映阻力增加[27]。然而,产生这样的数据是具有挑战性的,因为运动RHC测量耗时,困难,并且由于快速呼吸周期和运动CO和paap测量不准确而产生的误差可能会使其复杂化。从而产生mPAP- - - - - -个别患者的CO图作为临床常规是不切实际的。
平均肺动脉压(mPAP)斜率- - - - - -正常对照组心输出量(CO)关系不同与肺动脉高压(PAH)受试者。复制及修改自[26得到允许。
为什么界定运动PH和PAH是困难的?
许多变量影响运动时mPAP的“正常”变化,这反过来又使任何试图将“运动PH”作为病理状态建立阈值的尝试复杂化。随着正常的衰老而发生的生理变化[7]和mPAP也随CO的增加而升高;因此,在科目(如。精英运动员),他们可以将CO提高到30-40 L·min−1在运动高峰时,mPAP可超过以往正常[28]。然而,最大的困难是用运动来推断PVD的存在,因为运动也会导致PAWP的升高。因此,如果PVR=(mpap - paap)/CO,则必须测量运动paap来推断运动相关PAP异常高的发病机制。由于LHD是静息PH的最常见原因,LHD患者的左房压随运动异常升高,因此测量运动时paap(左房压)的变化成为评估运动PH喘不过气的患者PVR的关键决定因素。
这种诊断鉴别能力的缺乏(运动PH是由于LHD还是PVD)已经被H观察et al。[29]。尽管总肺阻力为每升一氧化碳3毫米汞柱,可将健康对照者与LHD或PVD患者区分开来,但无法准确地将LHD与PVD患者区分开来。图2)。需要注意的是,准确测量运动时的paap在技术上具有挑战性,这与paap患者的呼吸波动过大有关,部分原因是在剧烈运动时难以将球囊导管充分“楔入”。
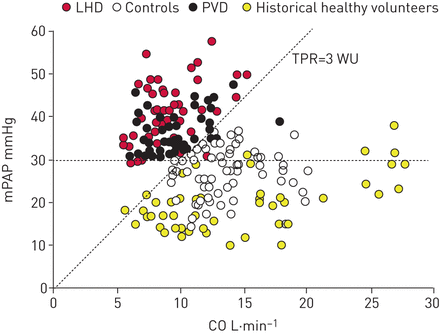
平均肺动脉压(mPAP) -心输出量(CO)关系的知识不能区分左心疾病(LHD)和肺血管疾病(PVD)患者;还需要了解运动肺动脉楔压。TPR:全肺阻力;吴:木质单位。转载自[29得到允许。
总结与观点
尽管测量运动血流动力学在早期阶段检测PVD比在休息时测量更有直观的吸引力,但仍然存在太多的不确定性,无法重新引入临床有用的运动ph定义。关于衰老、高CO的正常变化,特别是关于区分运动相关的paap变化(由于LHD)和PVD变化,需要更多的信息。我们相信这些将是未来研究的富有成果的领域。
更新了PH的临床分类
PH临床分类的一般目的是根据相似的病理生理机制、临床表现、血流动力学特征和治疗管理对与PH相关的临床条件进行分类。在儿童和成人PH的临床分类的全面和简化版本提出了表2。对于合并先天性心脏病的PAH患者,四个亚组(Eisenmenger综合征、从左到右分流、巧合或小缺陷和术后/闭合缺陷)保持不变[30.]作为缺陷关闭的指示(请参阅专题小组的文章)欧洲呼吸杂志[31])。第2、第3和第4组的最新情况载于本刊的专责小组文章欧洲呼吸杂志[10,32,33]。
第1组更新:多环芳烃
1.3组:药物和毒素诱导的多环芳烃
我们建议将与药物和毒素相关的多环芳烃特征简化为两个亚组,以帮助医生确定需要特定监测的药物。"明确关联"包括基于疫情、流行病学病例对照研究或大型多中心系列研究数据的药物。“可能的关联”是由多个病例系列或具有类似作用机制的药物的病例提出的。根据最近的数据,多环芳烃与两种药物和毒素(安非他明/甲基苯丙胺和达沙替尼)的关联现在被认为是明确的(表3)。
Zamanian等。[34]报道了90例多环芳烃与甲基苯丙胺相关的多环芳烃相关病例;这些受试者不太可能是女性,在诊断时有更多的血流动力学损害,结果比IPAH差。该分析证实了甲基苯丙胺/安非他命使用与多环芳烃相关住院之间的关联(相对风险2.64,95% CI 2.18-3.2;p < 0.001)。有趣的是,病理评估显示与IPAH相似的特征性血管改变,包括血管瘤样丛状病变,但也有增生性毛细血管,如肺毛细血管血管瘤病(PCH)或肺静脉闭塞病(PVOD)所描述的。达沙替尼是第二代酪氨酸激酶抑制剂,据报道与多环芳烃相关;在法国,暴露于达沙替尼的患者发生PAH的最低估计值为0.45% [35]。达沙替尼引起的PAH经常在停药后改善,但超过三分之一的患者持续存在[35,36]。
在过去的5年中,新药已被确定或怀疑为多环芳烃的潜在危险因素。已报道了几例博舒替尼开始治疗后达沙替尼相关PAH恶化或复发的病例[37- - - - - -39];这些病例的特征还包括停药博舒替尼后PAH的改善。使用新型直接作用抗病毒药物,包括治疗丙型肝炎病毒感染的索非布韦,已经出现了严重门脉性肺动脉高压的病例[40,41]。来氟米特,一种改善疾病的抗风湿药物,与多环芳烃的几个病例有关[42- - - - - -44]。最近,日本肺动脉高压登记处(Japan Pulmonary Hypertension Registry)报道了与未经批准的中草药天然靛蓝(青黛)相关的潜在可逆多环芳烃病例[45,46]。青黛的有效成分为靛玉红,可诱导肺内皮细胞凋亡在体外[46]。
1.5组:多环芳烃对钙通道阻滞剂有长期反应
尽管肺动脉重构是PAH的主要病理表现,但肺血管收缩在PAH病理生理中也起着重要作用,尤其是在血管反应性患者中。
在1992年发表的64名患者的一系列研究中,R我等。[47的研究报道,对钙通道阻滞剂(CCBs)有急性血管扩张反应的患者在接受长期CCBs治疗后,生存率显著提高。2005年,Sitbon等。[48]在557例PH患者的大系列研究中表明,12.5%的特发性PAH (IPAH)患者可观察到急性血管扩张剂反应,总体而言,6.8%的患者CCBs有长期临床和血流动力学改善。这项研究确定了确定急性血管扩张剂反应的最佳标准,即。降低mPAP≥10 mmHg,达到mPAP≤40 mmHg的绝对值,而CO增加或不变。对于血管反应性测试,吸入10 - 20 ppm的一氧化氮是首选剂,但注射。epoprostenol,注射。腺苷或吸入伊洛前列素可作为替代方案(表4)。对CCBs的长期应答定义为临床改善(纽约心脏协会功能I级或II级)和仅服用CCBs至少1年后持续的血流动力学改善(与急性试验相同或更好,通常在CO升高或正常的情况下获得mPAP < 30mmhg) (表4)。仅推荐IPAH、遗传性PAH或药物性PAH患者进行肺血管反应性检测,以确定适合CCB治疗的患者。在所有其他形式的多环芳烃和PH中,结果可能具有误导性,长期应答者很少[49]。
多环芳烃与血管反应性的病理生理学在很大程度上是未知的。最近,Hemnes及其同事发现,与IPAH相比,具有血管反应性的PAH具有特定的血液特征(培养淋巴细胞微阵列)和不同的基因变异(全外显子组测序)[50,51]。这些结果表明,这是一种特殊的实体,具有独特的临床病程,其特点是预后明显较好,治疗方法独特,病理生理不同(表2)。
1.6组:以静脉/毛细血管(PVOD/PCH)受累为明显特征的PAH
据报道,在许多已知的PAH病因中,如系统性硬化症,明显的肺静脉和/或毛细血管受累。在以前的分类中,PVOD/PCH被描述为一个独特的亚群。
PVOD/PCH和PAH有相似的病因和相关条件,即使其中一些更经常与更明显的静脉/毛细血管受累有关(表5)。由于真核翻译起始因子2α激酶4的双等位基因突变,PVOD/PCH的可遗传形式在近亲家族中被发现具有隐性遗传。EIF2AK4基因[52- - - - - -54]。职业性接触有机溶剂,特别是接触三氯乙烯,与毛细血管前PH值的形成以及静脉和毛细血管明显受损伤有关[55]。
肺功能检查(肺对一氧化碳的扩散能力降低)可强烈怀疑肺静脉/毛细血管受累(PVOD/PCH)的诊断。DLCO)经常<理论值的50%),动脉血气(严重低氧血症)和胸部高分辨率计算机断层扫描(室间隔线,小叶中心毛玻璃影/结节和纵隔淋巴结肿大)(表5) [53,54,56]。更明显的肺静脉/毛细血管受累与预后不良、对多环芳烃治疗的反应有限以及这些治疗的肺水肿风险相关[53,57]。
PAH和PVOD/PCH通常具有大致相似的血流动力学特征和临床表现。值得注意的是,双等位基因中有明显的肺动脉重构EIF2AK4突变携带者[58肺隔静脉的肌肉重构BMPR2(骨形态发生蛋白受体2型)突变载体[59]。在实践中,重要的是肺静脉/毛细血管介入毛细血管前ph的临床后果。因此,我们认为PAH和PVOD/PCH属于pvd的一个谱系,而不是代表两个明确的不同实体。我们建议将“有明显静脉/毛细血管(PVOD/PCH)累及特征的PAH”纳入修订后的PAH(第1组)。表2)。
第5组更新:PH具有不明确和/或多因子机制
自1998年我们的分类体系基础建立以来,第5组经历了重大变化。最初描述“直接影响肺血管系统的疾病”,然后在2003年第三届世界卫生大会上命名为“杂项”[60],最终达到目前的表现,这一组包括不清楚和/或多因素机制的PH形式[30.,61]。从一开始,与其他组相比,这一组代表了较少研究的PH形式;然而,目前第5组中的许多PH形式代表了尚未认识到的全球PH负担的重要组成部分[62]。
第5组临床情况的一个主要特征是,没有确定的主导机制驱动PH的发展,可能有多种病理生理现象参与这一过程(表7)。在这次更新的分类中,只考虑对现有文献支持明确重新定位的亚型进行更改。
5.1组:血液病
慢性溶血性贫血明显与PH风险增加有关[63]。自2013年第五届WSPH以来,目前对镰状细胞病(SCD)中PH的众多表现的理解很少增加。然而,很明显,在这种情况下,PH通常是多因素的,包括CO升高、LHD、血栓栓塞性疾病、血液粘度改变和主要由一氧化氮消耗引起的内皮功能障碍[64- - - - - -67]。最近,限制性心肌病在临床和实验研究中得到了更好的认识和描述[68]。这些数据强调了这种特殊形式的PH的极端重要性以及在该领域进行持续调查的必要性[64,65]。此外,近年来,关于另一种重要的慢性溶血性贫血,即。β地中海贫血。对包括PH在内的主要疾病并发症的危险因素有了更好的了解[69]。此外,维erchi等。[70]通过侵入性血流动力学评估评估PH的患病率,类似于在SCD中所做的工作[71- - - - - -73]。在1309名接受筛查评估的患者中,有2.1%的病例确认了毛细前PH值,而0.3%的病例发现了毛细后PH值[70]。高龄和脾切除术是与PH相关的明显危险因素。尽管本研究提供了关于PH在这种临床情况下的重要性的重要信息,但仍需要更多关于血管受损伤的组织病理学以及这些患者PH发展的病理生理机制的数据,以更好地制定潜在的管理策略。
脾切除术值得特别讨论。脾切除术与PH的首次关联[74],目前尚不清楚这是一种风险因素还是一种特殊情况。从那时起,脾切除术与许多血液病的PH发展有关,如前面提到的β-地中海贫血[69,70]。最重要的是,它与慢性血栓栓塞性PH的发展密切相关[75]。然而,没有其他特定的表型或临床行为的改变与脾切除术的存在相关,这表明它应该被更好地视为PH的危险因素,而不是一个值得特定分类的特定条件。
5.2组:全身性和代谢性疾病
需要强调的是,支持将具有全身性表现和明显的PH风险的临床状况分类为第5组的概念,同样是由于缺乏可靠的数据,无法明确识别主要的病理生理机制,或描述组织病理结果,或描述管理策略。因此,有几种情况被归为这一组,包括结节病、淋巴管平滑肌瘤病(LAM)、肺朗格汉斯细胞组织细胞增多症、甲状腺疾病、戈谢病、糖原蓄积病和神经纤维瘤病
关于LAM,最近的一项筛选研究[76],在超过100名LAM患者的重要队列中,强化了LAM的PH通常是轻微的,如前所述[77]。在6例(5.7%)出现毛细血管前PH的患者中,没有一例患者的mPAP浓度低于30 mmHg。此外,PH的存在与肺功能不良有关,这表明肺压升高与实质受累有关,最近的超声心动图研究进一步证实了这一点[78]。基于这些发现,在第3组中,LAM的PH似乎可以更好地与其他肺实质疾病分类。
结节病是一个更具挑战性的情况,因为PH的发展可能是由不同的因素引起的,从肺实质疾病到肺血管的外源性压迫、直接心肌受累甚至肉芽肿性动脉病变[79]。在结节病相关的PH患者中,明显的肺实质疾病非常普遍[80,81],尽管左心室功能障碍的存在不容忽视[80]。然而,仅仅考虑肺实质受累是很难对结节病进行重新分类的,因为还有许多其他因素尚未明确,包括结节病中常见的肺血管的不同组织病理学模式,在某些情况下会形成肉芽肿[79],而不是第三组的其他疾病。虽然这些特征得到了更好的研究,但结节病仍被归为第5组。
从自身免疫到高或低一氧化碳,左心室功能障碍,甚至血管增生,甲状腺疾病和PH的共存有很强的理论基础。多环芳烃患者甲状腺疾病的患病率增加[82,83];此外,在这种情况下,甲状腺功能障碍的程度也与预后有关[84]。然而,与脾切除术类似,甲状腺功能障碍的存在不一定是特定临床状况的特征;它更像是一个风险因素或合并症,应该在PH管理过程中加以具体控制。除非有新的数据证明,否则将甲状腺疾病从分类中删除作为一个特定实体并更好地讨论其作为危险因素和/或相关合并症的作用是一个共识。
许多与PH相关的不同疾病仍需要更好地设计研究,以增加对疾病发展的理解。我们建议只有在生成可靠的数据来支持这种重新分类之后才进行更改。
结论
该工作组首先重新审视了PH的定义,提出了一个新的压力水平来定义mPAP异常升高bb0 - 20mmhg,并且需要PVR≥3wu来定义毛细前PH的存在。此外,工作组建议简化PH临床分类的核心(表2),并已编制在其他表格中。第1组(PAH)的两个主要变化包括:1)指定了一个亚组“PAH对CCBs的长期应答者”;2)纳入了一个亚组“具有明显静脉/毛细血管(PVOD/PCH)累及特征的PAH”。第5组(PH不明确和/或多因素机制)简化为:1)切除脾切除术和甲状腺疾病;2)第3组lam相关的PH与其他肺实质疾病的分类。第2、3和4组的重要新见解已由各自的工作队在本期的欧洲呼吸杂志[10,32,33]。
脚注
N. Galiè, V.V. McLaughlin, L.J. Rubin和G. Simonneau编辑的“第六届世界肺动脉高压研讨会论文集”系列中的第4篇
利益冲突:G. Simonneau报告了在提交的工作之外,来自Actelion制药公司、拜耳医疗保健公司、默克公司和葛兰素史克公司的赠款、个人费用和非经济支持。
利益冲突:D. Montani报告了在提交的工作之外,来自Actelion Pharmaceuticals、Bayer Healthcare、Merck和GSK的赠款、个人费用和非经济支持。
利益冲突:D.S. Celermajer是Actelion赞助的两项临床试验的研究者。
利益冲突:Denton报告了在研究过程中来自Actelion和Roche的拨款和个人费用,来自GSK的拨款以及来自Bayer和Boehringer Ingelheim的个人费用;在提交的作品之外,Inventiva和CSL Behring的补助金和个人费用,以及Leadiant的个人费用。
利益冲突:M.A. Gatzoulis报告了在研究进行期间,Actelion制药公司指导委员会成员的个人费用,以及Actelion Global、辉瑞和葛兰素史克的资助。
利益冲突:M. Krowka在提交的工作之外,是由Actelion赞助的PORTICO(门状肺动脉高压研究的Macitentan)的指导委员会成员。
利益冲突:除了提交的工作外,P.G. Williams还从Aspen SA和GSK那里收取了顾问委员会会议的个人费用。
利益冲突:R. Souza报告了Actelion、拜耳、葛兰素史克和辉瑞在提交的工作之外的演讲和咨询费。
- 收到了2018年10月6日。
- 接受2018年10月9日。
- 版权所有©ERS 2019
本文在知识共享署名非商业许可4.188滚球软件0的条款下开放获取和分发。