摘要gydF4y2Ba
呼吸道合胞病毒(RSV)细支气管炎是婴儿入院的最常见原因,但对其发病机制的了解有限,也没有特定的抗病毒治疗。使用一个小说gydF4y2Ba体外gydF4y2Ba初发性培养中性粒细胞迁移模型和创新的成像方法,我们表明鼻腔气道上皮的RSV感染增加了中性粒细胞培育性迁移和粘附对感染的上皮细胞,这与上皮细胞损伤和减少的睫状搏动频率有关,但也减少了传染病病毒载荷。gydF4y2Ba
在迁移后,与跨越模型感染的鼻上皮细胞迁移的中性粒细胞相比,RSV感染导致中性粒细胞激活,中性粒细胞激活,下嗜中性粒细胞弹性蛋白酶释放到气道表面培养基中。阻断中性粒细胞上的配体之间的相互作用(βgydF4y2Ba2gydF4y2Ba-Integrin LFA-1)用于上皮细胞上的细胞内粘附分子(ICAM)-1降低中性粒细胞粘附到RSV感染的细胞和上皮细胞损伤对预感染水平,但未减少迁移或预防减少的中性粒细胞的数量在传染病病毒载荷。gydF4y2Ba
这些发现为中性粒细胞对气道损伤和病毒清除的贡献提供了重要的见解,这与RSV毛细支气管炎的病理生理学相关。该模型是一种方便的、定量的临床前模型,将进一步阐明驱动疾病严重程度的机制,并在抗病毒药物发现中具有实用价值。gydF4y2Ba
摘要gydF4y2Ba
中性粒细胞减少呼吸道病毒载量,但能粘附气道上皮细胞gydF4y2Ba通过gydF4y2BaβgydF4y2Ba2gydF4y2Ba-整合素LFA1造成侧气道损伤gydF4y2Bahttp://bit.ly/38zoin7.gydF4y2Ba
介绍gydF4y2Ba
呼吸道合胞病毒(RSV)是支气管炎的主要原因,以及儿童住院的最普遍的病毒原因<1年的[gydF4y2Ba1gydF4y2Ba].目前没有疫苗可防止RSV感染,没有具体的抗病毒治疗。结构生物学的最新进展恢复了RSV疫苗和抗病毒发育,有几种疫苗[gydF4y2Ba2gydF4y2Ba抗病患者[gydF4y2Ba3.gydF4y2Ba- - - - - -gydF4y2Ba5gydF4y2Ba通过治疗管道。扩大我们对RSV细支气管炎病理生理学机制的理解,对于支持RSV特异性治疗的发展非常重要。研究使用gydF4y2Ba体外gydF4y2Ba人呼吸道合胞病毒感染纤毛气道上皮细胞模型对宿主对呼吸道病毒的反应有重要的了解[gydF4y2Ba6gydF4y2Ba- - - - - -gydF4y2Ba9gydF4y2Ba].然而,与呼吸道合胞病毒婴儿的肺组织不同[gydF4y2Ba10.gydF4y2Ba,gydF4y2Ba11.gydF4y2Ba),这些gydF4y2Ba体外gydF4y2Ba模型显示RSV感染期间的细胞病理学征象很少,这对它们在研究婴儿RSV毛细支气管炎的病理生理学方面的用途提出了疑问。gydF4y2Ba
中性粒细胞是招募到呼吸道合胞病毒毛细支气管炎婴儿肺部的主要免疫细胞[gydF4y2Ba12.gydF4y2Ba,gydF4y2Ba13.gydF4y2Ba].它们在宿主防御中的作用尚不完全清楚。我们假设中性粒细胞在rsv感染的鼻气道上皮细胞(nAECs)中的迁移有助于细胞损伤,并揭示了重要的宿主应答机制。我们之前开发了一个中性粒细胞迁移模型[gydF4y2Ba14.gydF4y2Ba,gydF4y2Ba15.gydF4y2Ba使用的是常用于研究RSV感染的人肺泡II型细胞系(A549)gydF4y2Ba体外gydF4y2Ba[gydF4y2Ba15.gydF4y2Ba- - - - - -gydF4y2Ba17.gydF4y2Ba].然而,透明的气道上皮细胞是RSV感染的主要靶标,但不朽的细胞系往往缺乏适当的细胞偏振,并且在气道中发现许多其他重要特性,例如粘液。因此,为了进一步询问中性粒细胞术后性迁移,我们开发了更具生理学相关的gydF4y2Ba体外gydF4y2Ba使用在气液界面(ALI)生长的原代人鼻上皮细胞的模型(gydF4y2Ba图1gydF4y2Ba).原代气道上皮细胞种植在多孔膜插入物的底部,而不是传统ALI培养的顶部。这是因为,尽管有人认为中性粒细胞在重力作用下可以迁移,但我们的初步研究表明,恢复的中性粒细胞数量非常低(约2500个细胞)。我们的重力喂养系统已被证明是研究中性粒细胞经上皮细胞迁移后功能的理想系统。我们观察了中性粒细胞在初级分化nAECs中的趋化性,并首次测量了中性粒细胞的粘附和相关的上皮损伤,包括纤毛搏频,这是对细胞毒性的敏感评估。gydF4y2Ba
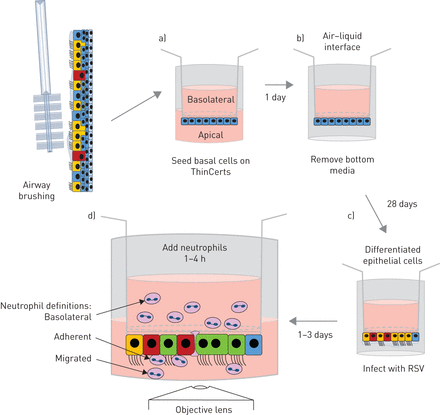
原代人鼻气道上皮细胞中性粒细胞迁移模型示意图。a)将初级鼻气道上皮基底细胞种植在3µm孔径的聚对苯二甲酸乙二醇酯ThinCert膜插入物的下面,并附着4小时。随后将膜插入物倒置并在培养基中维持1天,使单层上皮形成融合。b)将膜插入物暴露在气液界面中,使其完全分化28天。c)将膜插入物倒置,用绿色荧光蛋白呼吸道合胞病毒(RSV)或模拟感染2 h,使感染进展24或72 h。d)将静脉血中分离的超纯中性粒细胞加入到膜嵌件基底外侧,并允许其迁移1或4 h。确定结果衡量标准。gydF4y2Ba
材料和方法gydF4y2Ba
参与者gydF4y2Ba
外周血和气道上皮细胞取自伦敦大学学院(UCL)大奥蒙德街儿童健康研究所(伦敦,英国)的健康成人捐赠者。在参加研究之前,所有的捐赠者都获得了书面的知情同意。研究获得了伦敦大学学院研究伦理委员会的批准(4735/002)。所有方法均按照相关指南和规定进行。gydF4y2Ba
病毒纯化和定量gydF4y2Ba
具有绿色荧光蛋白(GFP)的重组RSV A2菌株 - 用于在含有复制病毒的上皮细胞中表达GFP的GFP,是由F的gydF4y2BaIX.gydF4y2Ba等等。gydF4y2Ba[gydF4y2Ba18.gydF4y2Ba].如前所述,使用HEp-2细胞(ATCC CCL-23)从连续稀释的nAEC上清中制备病毒库和定量病毒滴度[gydF4y2Ba14.gydF4y2Ba,gydF4y2Ba15.gydF4y2Ba].使用Taqman Universal Mast Mix II进行定量逆转录酶PCR,用UNG(Applied Biosystems,California,USA)进行。将总体积为20μl,每次反应中的1μLcDNA使用。使用引物,探针和反应条件如前所述[gydF4y2Ba14.gydF4y2Ba,gydF4y2Ba19.gydF4y2Ba].含有N蛋白序列的质粒[gydF4y2Ba20.gydF4y2Ba用于量化Naec上清液中的N蛋白拷贝数和细胞内。RSV载荷从已知的N蛋白拷贝的标准曲线外推。gydF4y2Ba
中性粒细胞培育迁移测定gydF4y2Ba
如前所述,原代气道上皮细胞来自鼻刷[gydF4y2Ba21.gydF4y2Ba或购买上皮elix Sàrl(日内瓦,瑞士)。我们方法的图表见gydF4y2Ba图1gydF4y2Ba和nAEC培养的详细协议可在gydF4y2Ba补充方法gydF4y2Ba.我们发现,从刷牙或商业供应商(gydF4y2Ba补充图S1gydF4y2Ba).简单地说,祖基底细胞与3T3-JF小鼠成纤维细胞饲养层共培养,如前所述[gydF4y2Ba22.gydF4y2Ba].初级nAECs以5×10的密度被播种到饲养层gydF4y2Ba5gydF4y2Ba每瓶f -培养基(以3:1比例添加1×penicillin链霉素的DMEM和Hams F12培养基,7.5%胎牛血清(Gibco, Waltham, MA, USA), 5 mM Y-27632 (Abcam, Cambridge, UK), 25 ng·mLgydF4y2Ba−1gydF4y2Ba氢化可的松0.125 ng / mLgydF4y2Ba−1gydF4y2Ba表皮生长因子(Sigma,St路易斯,Mo,USA),5毫克·mLgydF4y2Ba−1gydF4y2Ba胰岛素(Sigma),0.1nm霍乱毒素(Sigma)和两性霉素B(2.50μg·mlgydF4y2Ba−1gydF4y2Ba))和培养直到汇合。然后通过差分胰蛋白酶解离,如前所述[incormate)分离初级NAECs和3T3-J2成纤维细胞[gydF4y2Ba22.gydF4y2Ba].在新鲜f培养基中收集基底细胞,200×离心gydF4y2BaggydF4y2Ba3分钟。gydF4y2Ba
胶原蛋白涂层3 μm孔膜插入件(ThinCert;格雷纳,克伦斯蒙斯特,奥地利,文化表面33.6毫米gydF4y2Ba2gydF4y2Ba)被倒置,300 000个细胞·厘米gydF4y2Ba−2gydF4y2Ba将70 μL f -培养基中的nAECs接种于插入物底部,37℃5%二氧化碳(CO ., CO .)孵育gydF4y2Ba2gydF4y2Ba) 4-6小时。孵育后,将膜片倒置至24孔板中,在膜片下分别加入500 μL新鲜f -培养基和100 μL添加30 μg·mL f -培养基gydF4y2Ba−1gydF4y2Ba胶原蛋白I和5%(v / v)matrigel(康宁,康宁,纽约,美国)添加到膜嵌件的顶部。将细胞在37℃5%CO中温育24-48小时gydF4y2Ba2。gydF4y2Ba在此之后,将细胞置于ALI中。从膜插入物两侧抽吸培养基,细胞基底外侧灌注100 μL ALI培养基(1:1 DMEM:气道上皮细胞生长培养基(PromoCell,海德堡,德国),并添加所有补充物,再添加2.5 μg·mLgydF4y2Ba−1gydF4y2Ba两性霉素B, 1×penicillin/链霉素和1 μm维甲酸(Sigma)。每1-2天更换一次培养基,细胞在37°C 5% CO下孵育gydF4y2Ba2gydF4y2Ba在高湿培养箱中培养4周/28天,使细胞分化。一旦分化,细胞像以前一样被RSV感染[gydF4y2Ba19.gydF4y2Ba].gydF4y2Ba
根据制造商说明,使用阴性免疫选择中性粒细胞分离试剂盒(Stemcell Technologies, Vancouver, Canada)从10ml外周静脉血中纯化中性粒细胞。中性粒细胞的平均数量为1.5×10gydF4y2Ba7gydF4y2Ba经流式细胞仪检测纯度为99.8-99.9%的细胞(gydF4y2Ba补充图S1dgydF4y2Ba).如前所述,用细胞特征Calcein红橙色细胞染色(Thermofisher,Waltham,Ma,USA)染色中性粒细胞染色[gydF4y2Ba14.gydF4y2Ba].gydF4y2Ba
实验组(模拟感染、RSV感染、模拟感染暴露于由RSV感染细胞或n -甲硫氨酸-leucyl-phenylalanine (fMLP)采集的根尖表面培养基),分别在膜插入器下放置400 μL根尖表面培养基进行中性粒细胞转移。探讨整合素白细胞的交互关联antigen-1F (LFA1)细胞内细胞粘附分子ICAM-1,我们补充顶端表面媒体从RSV-infected收集细胞1μM (2 e) 1 - (4-acetyl-1-piperazinyl) 3 -[4 -((2 -(1 -甲基乙基)苯基)硫代的)3-nitrophenyl] 2-propen-1-one (A286982,TOCRIS BioTechne, Minneapolis, MN, USA), LFA-1 CD11a I域的有效拮抗剂(抑制剂)[gydF4y2Ba23gydF4y2Ba].基于其他研究中使用的中使用35-44nm的中值抑制浓度[gydF4y2Ba24gydF4y2Ba,gydF4y2Ba25gydF4y2Ba].中性粒细胞(5×10gydF4y2Ba5gydF4y2Ba)加入到膜嵌件基底外侧,静置1或4 h。迁移后,从上皮细胞的顶端采集中性粒细胞进行定量(见后面)。收集顶端表面培养基(包含上皮分泌因子,包括细胞因子),固定膜片并对ICAM-1、乙酰化微管蛋白(纤毛)或粘附中性粒细胞进行染色(见后面)。gydF4y2Ba
定义gydF4y2Ba
基底外侧:中性粒细胞停留在上皮的基底外侧(上腔),不能穿过上皮。迁移:中性粒细胞穿过上皮细胞并脱离顶端表面培养基(下腔)。粘附性中性粒细胞:中性粒细胞穿过上皮细胞并继续粘附于气道上皮细胞(gydF4y2Ba图1gydF4y2Ba).gydF4y2Ba
ICAM1表达分析gydF4y2Ba
在RSV感染24和72小时后量化纤毛NAEC的ICAM1表达水平。提供了关于染色程序的详细方法gydF4y2Ba补充材料gydF4y2Ba.在共聚焦显微镜(Zeiss LSM710,Oberkochen,Germany)上获得Z堆叠使用×40物镜,每个图像之间具有5μm距离和高达50μm的范围。gydF4y2Ba
迁移和粘附中性粒细胞的定量gydF4y2Ba
如前所述,对迁移的中性粒细胞数量进行了量化[gydF4y2Ba14.gydF4y2Ba].如前所述进行CD11b表达对迁移和基石中性粒细胞的流式细胞术分析[gydF4y2Ba14.gydF4y2Ba].在×40物镜下共聚焦显微镜(蔡司LSM710)上获得粘附中性粒细胞的图像。使用ImageJ计数工具计数中性粒细胞。gydF4y2Ba
上皮损伤的定量gydF4y2Ba
如前所述,细胞损伤通过经上皮细胞电阻(TEER)、红色葡聚糖渗透性、乳酸脱氢酶(LDH)释放和计算残留在膜插入物上的上皮细胞数量来量化[gydF4y2Ba14.gydF4y2Ba),在gydF4y2Ba补充图S2gydF4y2Ba.为了确定睫状搏动频率(CBF),将培养皿置于孵育室(37°C, 5% CO)中gydF4y2Ba2gydF4y2Ba)附在倒置显微镜系统上,如前所述[gydF4y2Ba9gydF4y2Ba].使用×20物镜和互补金属氧化物半导体数码摄像机(日本静冈县滨松)以每秒198帧的速度录制视频(如图所示为纤毛区域的一个示例视频)gydF4y2Ba视频1gydF4y2Ba).在每个条件下,对每个膜插入的12个区域进行录像。ciliaFA软件通过快速傅里叶变换计算CBF (Hz) [gydF4y2Ba26gydF4y2Ba].gydF4y2Ba
统计分析gydF4y2Ba
通过配对的T检验分析暴露于不同测试条件的相同供体细胞之间的差异。在执行多种比较时使用具有Bonferroni校正的配对双向ANOVA(GraphPad Prism V4.0; San Diego,CA,USA)。使用attase 15执行所使用的测试和数据建模的验证(Statacorp,College Station,TX,USA)(gydF4y2Ba辅助数据文件gydF4y2Ba).gydF4y2Ba
结果gydF4y2Ba
我们的模型(gydF4y2Ba图1gydF4y2Ba)在rsv感染后24小时和72小时都有类似的发现,我们在图中显示了两个时间点,但为了可读性和清晰度,在文本中,我们仅参考了感染后72小时收集的数据。未发现中性粒细胞迁移的原代纤毛nAECs RSV感染资料gydF4y2Ba补充图S2gydF4y2Ba.gydF4y2Ba
RSV感染增加泛虫的Naecs迁移的中性粒细胞的数量,并将其解离顶端表面介质gydF4y2Ba
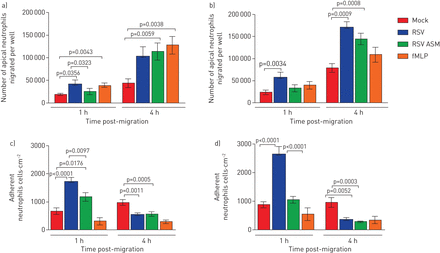
使用我们的分化原代气道鼻上皮细胞模型(gydF4y2Ba图1gydF4y2Ba),我们通过测量顶端表面培养基中荧光标记的中性粒细胞的数量来检测游走于上皮细胞和游离于上皮细胞的中性粒细胞的数量。我们发现在感染RSV 1小时后,超过2倍的中性粒细胞在感染RSV的纤毛上皮上迁移72小时,平均±1小时gydF4y2Ba扫描电镜gydF4y2Ba中性粒细胞5.7×10gydF4y2Ba4gydF4y2Ba±1.2×10gydF4y2Ba4gydF4y2Ba与模拟感染的上皮细胞相比,每孔迁移(2.3×10gydF4y2Ba4gydF4y2Ba±5.2×10gydF4y2Ba3.gydF4y2Ba) (p = 0.034) (gydF4y2Ba图2 bgydF4y2Ba)(24小时数据显示在gydF4y2Ba图2一个gydF4y2Ba).这相当于为RSV感染的上皮细胞添加的总嗜中性粒细胞的11.4%,并且对于嘲讽感染的上皮细胞为4.6%。在嗜中性粒细胞迁移4小时后,我们发现34%的中性粒细胞迁移跨过RSV的上皮细胞迁移72小时(1.7×10gydF4y2Ba5gydF4y2Ba±1.3×10gydF4y2Ba4gydF4y2Ba),同样是在模拟感染的上皮细胞中迁移的中性粒细胞数量的两倍多(15.8%)(7.9×10gydF4y2Ba4gydF4y2Ba±9×10gydF4y2Ba3.gydF4y2Ba) (p = 0.0009) (gydF4y2Ba图2 bgydF4y2Ba).gydF4y2Ba
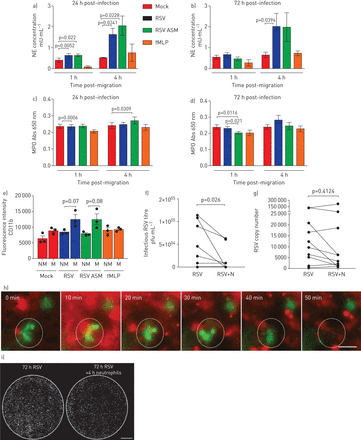
呼吸合胞病毒(RSV)增加了迁移受感染的鼻上皮细胞培养物的中性粒细胞的数量。a)跨过RSV感染的气道上皮细胞培养物迁移的顶端中性粒细胞的数量,并在24小时感染后释放到顶端表面介质中。b)在72小时感染后迁移过RSV感染的气道上皮细胞培养物的顶端嗜中性粒细胞的数量并释放到顶端表面介质中。数据显示为平均值±gydF4y2Ba扫描电镜gydF4y2Ban=6个上皮性献血者中,n=6个异体献血者。c)感染24小时后,假体或rsv感染的人鼻纤毛上皮细胞上附着的中性粒细胞数量。d)模拟感染或rsv感染的人鼻纤毛上皮细胞感染72 h后,嗜中性粒细胞的数量。用平板读卡器在顶端表面培养基中定量中性粒细胞浓度,并对照标准曲线进行读数。使用ImageJ计数工具计数粘附中性粒细胞,显示所有图像中中性粒细胞的平均数量(每个孔5张,分别来自n=3个上皮捐赠者、n=2个异体献血者和n=1个同源献血者)。条形图表示平均值±gydF4y2Ba扫描电镜gydF4y2Ba对于模拟感染、rsv感染、模拟感染和暴露于根尖表面培养基(ASM)的培养,或模拟感染和暴露于化学引诱剂n -甲硫氨酸-leucyl-苯丙氨酸(fMLP)的培养。各组间采用配对t检验进行统计学比较。显示了统计学意义。gydF4y2Ba
为了研究来自RSV感染的上皮细胞的分泌因子是否有助于中性粒细胞的迁移增加,我们测量跨越从来自RSV感染的上皮细胞收集的顶端表面培养基孵育的模型感染上皮迁移的中性粒细胞的数量。与从感染的细胞暴露于感染的细胞的嘲笑感染的上皮细胞相比,在模型感染的上皮细胞相比,迁移的中性粒细胞迁移后迁移中性粒细胞1小时的数量没有差异。与感染的细胞暴露于感染后的RSV 72h(gydF4y2Ba图2 bgydF4y2Ba).然而,在从感染的细胞中迁移到仔细观察的上皮细胞跨嘲弄的上皮细胞,从感染的细胞暴露于72小时,1.4×10gydF4y2Ba5gydF4y2Ba±1.3×10gydF4y2Ba4gydF4y2Ba细胞已经迁移,这是仅暴露于培养基的模拟感染细胞的1.7倍(7.9×10gydF4y2Ba4gydF4y2Ba±9×10gydF4y2Ba3.gydF4y2Ba)(p = 0.0008)。gydF4y2Ba
RSV增加了对被感染的纤毛上皮粘附的中性粒细胞的数量gydF4y2Ba
我们发现,中性粒细胞迁移1 h后,数量(平均值±gydF4y2Ba扫描电镜gydF4y2Ba),中性粒细胞粘附于72 h rsv感染的上皮细胞(2.6×10gydF4y2Ba3.gydF4y2Ba±2.7×10gydF4y2Ba2gydF4y2Ba中性粒细胞·厘米gydF4y2Ba−2gydF4y2Ba)比模拟感染的上皮细胞大于三倍(8.6×10gydF4y2Ba2gydF4y2Ba±1×10gydF4y2Ba2gydF4y2Ba中性粒细胞·厘米gydF4y2Ba−2gydF4y2Ba) (p < 0.0001) (gydF4y2Ba图2 dgydF4y2Ba),与感染RSV 24 h相比,RSV感染72 h后粘附的中性粒细胞更多(gydF4y2Ba图2 cgydF4y2Ba) (p < 0.05)。有趣的是,我们发现粘附中性粒细胞的数量在中性粒细胞迁移4小时后减少(3.6×10gydF4y2Ba2gydF4y2Ba±7.4×10gydF4y2Ba1gydF4y2Ba中性粒细胞·厘米gydF4y2Ba−2gydF4y2Ba)(gydF4y2Ba图2 dgydF4y2Ba)比1小时(2.6×10gydF4y2Ba3.gydF4y2Ba±2.7×10gydF4y2Ba2gydF4y2Ba中性粒细胞·厘米gydF4y2Ba−2gydF4y2Ba) (p<0.0001),感染RSV 24 h后差异相似。这对rsv感染的上皮细胞是特异性的,作为模拟感染的上皮细胞,在中性粒细胞迁移4小时后粘附的中性粒细胞数量(8.8×10gydF4y2Ba2gydF4y2Ba±1×10gydF4y2Ba2gydF4y2Ba中性粒细胞·厘米gydF4y2Ba−2gydF4y2Ba)的水平与1小时时的水平相似(9.2×10gydF4y2Ba2gydF4y2Ba±1×10gydF4y2Ba2gydF4y2Ba中性粒细胞·厘米gydF4y2Ba−2gydF4y2Ba).为了研究rsv感染的上皮细胞分泌的因子是否有助于增加中性粒细胞的粘附,我们测量了中性粒细胞的数量,中性粒细胞粘附在模拟感染的上皮细胞与从rsv感染的上皮细胞收集的根尖表面培养基孵育。我们发现,从rsv感染的细胞中收集的顶端表面培养基添加到模拟感染的上皮细胞中,并没有增加中性粒细胞的粘附,在1小时后,我们检测到粘附的中性粒细胞比rsv感染的上皮细胞少2 - 3倍(p<0.0001) (gydF4y2Ba图2 cgydF4y2Ba和d)。gydF4y2Ba
RSV感染期间中性粒细胞经上皮细胞迁移导致上皮细胞损伤并降低纤毛搏动频率gydF4y2Ba
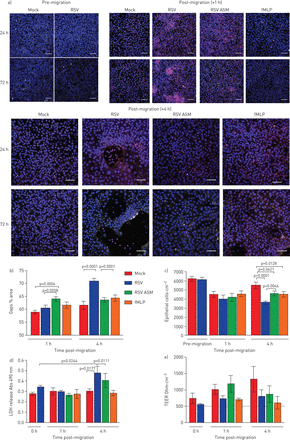
在RSV后24小时后,我们没有检测到中性粒细胞培训后的上皮损伤的任何迹象(gydF4y2Ba补充图S3gydF4y2Ba).中性粒细胞在感染RSV的上皮细胞上迁移1小时,72小时后,我们也没有检测到上皮损伤标志物的增加(gydF4y2Ba图3 bgydF4y2Ba).然而,在中性粒细胞穿过感染RSV的上皮细胞迁移72 h后4 h,与模拟感染的上皮细胞(61.6±6.0%)相比,我们发现RSV感染的上皮细胞层有较大的间隙(70.8±4.6%的面积)(p<0.0001)(代表图像见图gydF4y2Ba图3一gydF4y2Ba,定量数据见gydF4y2Ba图3 bgydF4y2Ba).通过延时显微镜观察,这些间隙与上皮圆形相关(gydF4y2Ba补充视频2.gydF4y2Ba),上皮细胞的缺失(gydF4y2Ba图3 cgydF4y2Ba)和乳酸脱氢酶释放增加(gydF4y2Ba图3 dgydF4y2Ba(p<0.0001)。有趣的是,这种上皮细胞的损失并不与红葡聚糖通量的增加相对应(gydF4y2Ba补充图S4gydF4y2Ba)或TEER下降(gydF4y2Ba图3 egydF4y2Ba).我们没有发现TEER与暴露于rsv感染根尖表面培养基或fMLP的模拟感染细胞相比有任何差异(gydF4y2Ba图3 egydF4y2Ba).为了确定是否可以改变红色葡聚糖和电流输出的物理障碍在上皮细胞中的损失中进行补偿,我们在显微镜下观察到随时间的显微镜(膜嵌件顶部),发现在4小时后,基底外粒细胞有累积为沉积物(gydF4y2Ba补充图S5gydF4y2Ba).gydF4y2Ba
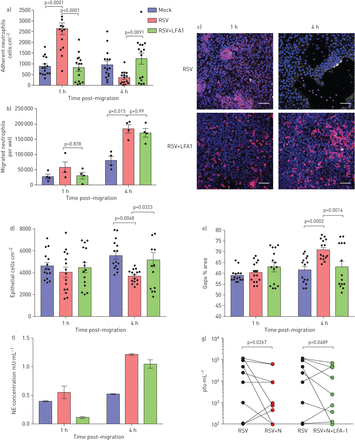
中性粒细胞促进迁移增加对呼吸道合胞病毒(RSV)的损伤 - 摄入纤毛的上皮。a)在嗜中性粒细胞(红色)Transepearlial迁移的空气液界面以1或4h的空气液体界面生长的RSV感染的人鼻纤维的上皮细胞的代表性共焦图像。用抗乙酰化小管蛋白的抗体染色细胞以检测睫状微管(白色),并且使用Hoechst(蓝色)染色核。上皮层中的间隙由大(>500μm)表示gydF4y2Ba2gydF4y2Ba黑色区域。规模酒吧= 50μm。b)差距分析。c)重组RSV感染72 h和中性粒细胞迁移1、4 h后粘附于膜插入物上的上皮细胞数量。通过计数dapi染色的细胞核>50µm来定量上皮细胞gydF4y2Ba2gydF4y2Ba在区域中使用ImageJ。条形图表示平均值±gydF4y2Ba扫描电镜gydF4y2Ba每孔5张图像中,n=3个上皮献血者,n=2个异体献血者,n=1个自体献血者。d)感染后72 h,检测中性粒细胞迁移后1和4 h鼻腔气道上皮细胞(nAECs)顶端表面培养基中乳酸脱氢酶(LDH)的释放情况。条形图表示平均值±gydF4y2Ba扫描电镜gydF4y2Ba4例上皮性献血者,3例异体献血者,1例同源献血者。e)用伏安计测量每孔的经上皮电阻(TEER)。数据以平均值±表示gydF4y2Ba扫描电镜gydF4y2Ban = 4个上皮供体,n = 3异源血液供体,n = 1个同源血液供体,用于嘲笑,RSV感染,嘲弄,感染和暴露于由RSV感染细胞或模拟的顶端表面介质(ASM)。感染并对化学侵入剂N-甲酰甲基硫氨氨酸 - 苯基丙氨酸(FMLP)感染和暴露。显示统计学意义。gydF4y2Ba
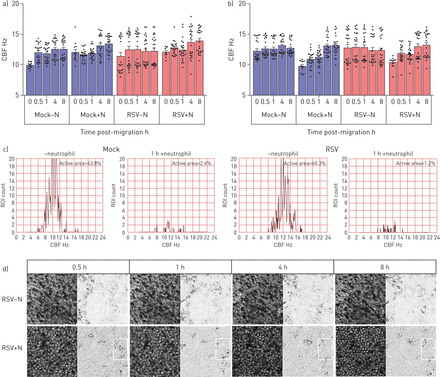
利用高速视频显微镜,我们研究了中性粒细胞迁移是否改变纤毛活动,这是细胞毒性的敏感指标。我们发现加入中性粒细胞30分钟后,平均值±gydF4y2BasdgydF4y2BaCBF为36 2856-μmgydF4y2Ba2gydF4y2Ba从RSV感染72小时的培养物中缉获的感兴趣区域为12.84±0.79 Hz,而RSV感染培养物中的15.06±0.95 Hz没有中性粒细胞(gydF4y2Ba图4 bgydF4y2Ba) (p < 0.05)。虽然这并不统计学不同,但2 Hz的CBF的绝对差异在减少粘液间隙时已经显示出临床显着性[gydF4y2Ba27gydF4y2Ba].加入中性粒细胞8小时后,模拟和rsv感染培养物的平均CBF似乎恢复到中性粒细胞前水平(gydF4y2Ba图4 bgydF4y2Ba).然而,当仔细检查,比较随时间推移的单个感兴趣区域时,可以清楚地看到,中性粒细胞迁移导致的显示活跃搏动纤毛(定义为> 3hz)的区域要少得多(在没有中性粒细胞的rsv感染培养中,这一比例是1.4%,而40.3%)(gydF4y2Ba图4 cgydF4y2Ba).gydF4y2Ba
呼吸道合胞病毒(RSV)的作用和中性粒细胞迁移transepithelial纤毛拍频(CBF)人类的纤毛上皮细胞感染模拟或RSV A2) 24 h或b) 72 h确定使用快速傅里叶变换的高速视频显微镜由ciliaFA视频。条形图表示平均值±gydF4y2Ba扫描电镜gydF4y2Ban=每孔12个区域用于培养模拟感染、中性粒细胞经上皮细胞迁移后模拟感染、rsv感染或中性粒细胞经上皮细胞迁移后rsv感染。各组间采用配对t检验进行统计学比较。N =3个上皮性献血者,N =3个异体献血者。显示了统计学意义。c)一个代表性视场的1600个感兴趣区域的CBF频率分布的代表性直方图。d) rsv感染(感染后72小时)的感兴趣纤毛区域的代表性图像,中性粒细胞迁移后0.5、1、4和8h,阳性或阴性中性粒细胞。相位图(左)和CiliaFA读数图(右),显示在CiliaFA分析中发现的移动纤毛细胞(黑色)。gydF4y2Ba
上皮损伤与中性粒细胞脱颗粒和高浓度的中性粒细胞弹性蛋白酶有关gydF4y2Ba
中性粒细胞释放几种有毒产物,包括髓过氧化物酶(MPO)和中性粒细胞弹性酶。为了确定这些产物的存在是否与上皮损伤相关,我们测量了这些产物在根尖表面培养基中的浓度。我们发现,在nAEC培养的根尖表面培养基中,中性粒细胞弹性蛋白酶的浓度在感染后72小时(而不是1小时)穿过rsv感染的上皮4小时(而不是1小时)后增加了3倍以上(gydF4y2Ba图5一个gydF4y2Ba和b)平均值±gydF4y2Ba扫描电镜gydF4y2Ba2.0±0.6亩·毫升gydF4y2Ba−1gydF4y2Ba,相比于0.6±0.1μm·mLgydF4y2Ba−1gydF4y2Ba在模拟感染培养中(p=0.039) (gydF4y2Ba图5 bgydF4y2Ba).在中性粒细胞迁移1或4小时后,我们没有发现rsv感染培养物的根尖表面培养基中的MPO与模拟感染培养物相比有显著差异(p=0.0006) (gydF4y2Ba图5 cgydF4y2Bad)。此外,与rsv感染的上皮细胞相比,我们没有发现迁移到mock的中性粒细胞的MPO细胞表达有差异(数据未显示)。gydF4y2Ba
通过呼吸道合胞病毒(RSV)感染的纤毛上皮细胞经上皮细胞迁移后中性粒细胞来源产品的释放和中性粒细胞的激活在中性粒细胞迁移1和4小时后,通过模拟或rsv感染(24小时/72小时感染)纤毛单层上皮细胞迁移后,测量顶端表面培养基中中性粒细胞弹性酶(NE)和c,d)髓过氧化物酶(MPO)的水平。对于所有人来说,条形图显示的是平均值±gydF4y2Ba扫描电镜gydF4y2Ba4名上皮性献血者中,3名异体献血者,1名同源献血者。各组间采用配对t检验进行统计学比较。显示了统计学意义。e)与未迁移的中性粒细胞相比,转染rsv感染的上皮细胞72 h后,中性粒细胞表面CD11B表达增加。流式细胞术检测细胞表面CD11B (PE)表达,计算表达CD11B的迁移(M)和非迁移(NM)中性粒细胞的百分比。中性粒细胞最初使用一个pe阳性的门控。利用该群体,计算了PE荧光的几何平均荧光强度。酒吧展示意味着±gydF4y2Ba扫描电镜gydF4y2Ban=3个上皮性献血者中,n=3个异体献血者。有统计学意义,p<0.05。f)空斑实验(pfu·mL)测定感染后72 h病毒滴度gydF4y2Ba−1gydF4y2Ba)或g)全孔裂解物的定量逆转录酶- pcr显示感染性RSV在中性粒细胞迁移4小时后下降。N =10次技术重复,来自N =6上皮性献血者,N =5异体献血者和N =1同源献血者。h)延时荧光显微镜显示,在上皮细胞基底外侧加入中性粒细胞(红色)后50分钟内,绿色荧光蛋白阳性(绿色)上皮细胞消失。这也在gydF4y2Ba视频3gydF4y2Ba.比例尺= 50μm。i)中性粒细胞迁移前(左)和后4小时(右)感染RSV的典型膜插入物的全荧光显微镜扫描。每一个白点表示一个被rsv感染的上皮细胞。i)使用荧光显微镜进行整体扫描,显示中性粒细胞迁移对RSV感染的上皮细胞总数的影响(RSV+ve细胞=白色)。gydF4y2Ba
我们发现,细胞中性粒细胞活化标志物CD11b的表达较大1.4倍,含有液体粒细胞,其在感染72小时的上皮内迁移(平均值±gydF4y2Ba扫描电镜gydF4y2Ba1.2×10的荧光强度gydF4y2Ba4gydF4y2Ba±1.5×10gydF4y2Ba3.gydF4y2Ba)相比<8.5×10gydF4y2Ba3.gydF4y2Ba±4×10gydF4y2Ba2gydF4y2Ba非迁移中性粒细胞(p<0.05) (gydF4y2Ba图5 egydF4y2Ba),并与未接触上皮细胞的中性粒细胞(5.6×10gydF4y2Ba3.gydF4y2Ba±1.7×10gydF4y2Ba3.gydF4y2Ba) (p < 0.05)。此外,我们发现1小时后,在rsv感染的上皮细胞上迁移的中性粒细胞比在模拟感染的上皮细胞上迁移的中性粒细胞表达更大(p<0.05) (gydF4y2Ba图5 egydF4y2Ba).gydF4y2Ba
嗜中性粒细胞促进迁移减少了传染性病毒载量gydF4y2Ba
迁移4小时后采集的顶端表面培养基和顶端细胞层显示1.6×0的病毒滴度显著降低gydF4y2Ba4gydF4y2Ba空斑形成单位·毫升gydF4y2Ba−1gydF4y2Ba在rsv感染的nAEC纤毛培养物中进行了中性粒细胞迁移,并与4.4×10进行了比较gydF4y2Ba5gydF4y2Ba空斑形成单位·毫升gydF4y2Ba−1gydF4y2Ba无中性粒细胞迁移的rsv感染nAECs (p=0.03) (gydF4y2Ba图5 fgydF4y2Ba).这是一个平均值±gydF4y2Ba扫描电镜gydF4y2Ba病毒滴度差异为- 2.7×10gydF4y2Ba4gydF4y2Ba±1.2×10gydF4y2Ba4gydF4y2Ba空斑形成单位·毫升gydF4y2Ba−1gydF4y2Ba(gydF4y2Ba补充图S6AgydF4y2Ba).这些发现被中性粒细胞迁移后较少的gfp阳性细胞所证实(gydF4y2Ba图5我gydF4y2Ba)和时间流逝荧光显微镜,其显示在中性粒细胞迁移后的GFP表达较少(gydF4y2Ba视频3gydF4y2Ba和gydF4y2Ba图5 hgydF4y2Ba).中性粒细胞迁移4 h后rsv感染培养物的病毒RNA无显著差异(gydF4y2Ba图5克gydF4y2Ba和gydF4y2Ba补充图S6B.gydF4y2Ba).有趣的是,中性粒细胞暴露在不含nAECs的RSV中,4 h后感染性病毒载量也降低,病毒滴度差异为- 1.1×10gydF4y2Ba5gydF4y2Ba±1.3×10gydF4y2Ba4gydF4y2Ba空斑形成单位·毫升gydF4y2Ba−1gydF4y2Ba(gydF4y2Ba补充图S7AgydF4y2Ba);病毒RNA也没有差异(gydF4y2Ba补充图S7B.gydF4y2Ba).gydF4y2Ba
阻断中性粒细胞β.gydF4y2Ba2gydF4y2Ba-整合素LFA-1减少中性粒细胞粘附和上皮损伤gydF4y2Ba
与模拟感染的上皮细胞相比,在72小时rsV感染后,在上皮细胞上,ICAM-1表达明显大幅度gydF4y2Ba补充图S2gydF4y2Ba),所以我们的研究集中在这个时间点。我们发现,当接触阻断中性粒细胞LFA-1和ICAM-1在上皮细胞上相互作用的抑制剂时,与单独感染rsv的上皮细胞相比,粘附在rsv感染上皮细胞上的中性粒细胞较少(p<0.0001) (gydF4y2Ba图6AgydF4y2Ba).此外,我们观察到使用LFA-1抑制剂时,与rsv感染的上皮细胞相比,中性粒细胞聚集更小、更少(观察数据)。与RSV组相比,RSV+LFA-1组的中性粒细胞迁移数量没有差异(gydF4y2Ba图6B.gydF4y2Ba),建议添加LFA-1抑制剂的添加不会影响整个上皮的中性粒细胞趋化性。gydF4y2Ba
阻断中性粒细胞β.gydF4y2Ba2gydF4y2Ba-Integrin白细胞功能相关的抗原-1f(LFA1)降低中性粒细胞粘附和上皮损伤。a)与膜插入物72h后呼吸后的合胞病毒(RSV)感染和迁移后1和4小时的嗜中性粒细胞的数量用或不添加LFA1抑制剂。使用imagej计算中性粒细胞;显示了来自所有图像的平均中性粒细胞数(每个供体的五个图像,n = 3个上皮供体,n = 2异源血液供体和n = 1个同源血液供体)。b)在24和72h RSV感染后在RSV感染的纤维化细胞单层迁移的中性粒细胞数量用或不添加LFA1抑制剂。LFA1组是一种RSV感染的膜插入物,其LFA1嵌段器添加到从下面的RSV感染的细胞收集的顶端表面培养基中(顶端)。c)用RSV感染的纤维上皮单层的代表性显微镜图像24和72h,用核染色(Hoechst)染色中性粒细胞(红色)迁移为1和4小时,或不加入LFA1抑制剂。规模酒吧= 50μm。d)在中性粒细胞迁移1和4小时的中性粒细胞迁移到具有或不添加LFA1抑制剂的基团之后,定量附着于膜插入物的上皮细胞数。使用Imagej计算上皮细胞,显示来自所有图像的平均上皮细胞数(每个供体的五个图像,n = 3个上皮供体,n = 2异源血液供体和n = 1个同源血液供体)。 e) Lactate dehydrogenase (LDH) release was measured in apical surface media of airway epithelial cells post-neutrophil migration for 1 and 4 h in RSV-infected groups with or without addition of an LFA1 inhibitor. f) Neutrophil elastase (NE) was measured in apical surface media after migration across 72 h RSV-infected ciliated epithelial monolayers with and without LFA-1 inhibitor following neutrophil migration for 4 h. n=2 epithelial donors, n=1 heterologous blood donor and n=1 homologous blood donor. g) Viral titre as determined by plaque assay (pfu·mL−1gydF4y2Ba)全孔裂解物,显示出在中性粒细胞迁移后传染性RSV 4 H的降低(N = 9来自N = 6个上皮供体的技术重复,N = 5个异源血液供体和N = 1个同源血液供体)。显示统计学意义。gydF4y2Ba
在4小时后,在4小时后发现较少的上皮细胞脱落和较少的间隙在接触到LFA-1抑制剂的上皮后,在上皮层中形成的间隙较少(gydF4y2Ba图6C.gydF4y2Ba-e),而rsv感染的上皮细胞(p=0.003)。与之前一样,我们在rsv感染的上皮细胞暴露于LFA-1抑制剂(gydF4y2Ba图S6gydF4y2Ba).有趣的是,我们发现,在中性粒细胞迁移4小时后,rsv感染的上皮细胞和暴露于LFA-1抑制剂的rsv感染的上皮细胞,与模拟感染的细胞相比,均表现出更高的中性粒细胞弹性蛋白酶释放(p=0.03) (gydF4y2Ba图6F.gydF4y2Ba).此外,在中性粒细胞迁移后暴露于LFA-1抑制剂减少了RSV感染的上皮细胞的病毒滴度(P = 0.049)(gydF4y2Ba图6G.gydF4y2Ba).gydF4y2Ba
讨论gydF4y2Ba
我们表明,嗜中性粒细胞迁移和依从于RSV感染的气道上皮细胞与更大的上皮细胞损伤,更大的中性粒细胞下降和传染性病毒载量的降低有关。我们表明这些效应至少部分地由β介导gydF4y2Ba2gydF4y2Ba中性粒细胞上的-整合素配体LFA-1与nAECs上的ICAM-1受体结合,因为抑制这种相互作用可以防止中性粒细胞相关的上皮损伤。gydF4y2Ba
患有呼吸道合胞病毒毛细支气管炎的婴儿的呼吸道中含有大量中性粒细胞的浸润,中性粒细胞从血流中迁移并穿过呼吸道上皮。目前对中性粒细胞的流入如何促进RSV感染的病理生理学了解有限。相比之下,以前的研究使用gydF4y2Ba体外gydF4y2BaRSV感染的人纤毛气道上皮细胞模型,虽然报道了纤毛nAECs内的病毒复制在最初的24-72 h达到高峰,但没有证据表明在RSV感染期间上皮细胞受到损害[gydF4y2Ba6gydF4y2Ba,gydF4y2Ba9gydF4y2Ba].使用这种新的人类气道模型来研究中性粒细胞介导的应答在rsv感染的纤毛上皮气道细胞和模拟感染的细胞中,我们首次证明了以下结果。gydF4y2Ba
患有RSV的感染增加了早期和晚期感染后迁移在上皮细胞的中性粒细胞的数量。在没有感染细胞的情况下,在没有感染细胞的情况下存在的存在也在72小时后实现了这种效果。这支持临床发现,患有RSV支气管炎的婴儿肺中的中性粒细胞浸润[gydF4y2Ba10.gydF4y2Ba]与疾病严重程度有关[gydF4y2Ba15.gydF4y2Ba,gydF4y2Ba28gydF4y2Ba,gydF4y2Ba29gydF4y2Ba].此外,呼吸道合胞病毒感染上皮细胞后,更多的中性粒细胞粘附在上皮细胞上,而不脱离顶端表面的培养基。与暴露于感染细胞顶端表面培养基的模拟感染细胞的比较表明,中性粒细胞粘附的增加依赖于存在于上皮细胞或周围的RSV感染颗粒。粘附的中性粒细胞形成大簇,提示中性粒细胞协调或定位其迁移。这和Y的结果类似gydF4y2BaonkergydF4y2Ba等等。gydF4y2Ba[gydF4y2Ba30.gydF4y2Ba发现中性粒细胞经上皮细胞迁移穿过感染的上皮细胞gydF4y2Ba铜绿假单胞菌gydF4y2Ba导致中性粒细胞聚集。在其他感染和炎症疾病中也观察到中性粒细胞群集[gydF4y2Ba31gydF4y2Ba- - - - - -gydF4y2Ba33gydF4y2Ba].gydF4y2Ba
中性粒细胞在感染RSV的分化的人气道原代上皮细胞间迁移与上皮损伤有关,包括细胞脱落和CBF减少。我们检测到中性粒细胞通过感染RSV的纤毛上皮迁移24小时后,CBF立即(0-30分钟)下降。这种敏感的读数可能是细胞损伤的早期迹象,中性粒细胞经上皮迁移导致纤毛迅速减慢。在中性粒细胞经上皮细胞迁移4小时后,rsv感染的上皮细胞的CBF增加,恢复到中性粒细胞前水平。这可能表明中性粒细胞迁移导致慢跳动或受损纤毛的丧失,从而解释了在感染持续时间后采样区域的平均跳动频率更高的原因。gydF4y2Ba
上皮损伤与较大的中性粒细胞激活和脱粒有关,具有将嗜中性粒细胞弹性蛋白酶释放到顶端表面介质中。中性粒细胞脱粒是RSV感染的宿主响应和病理生理学的重要特征[gydF4y2Ba34gydF4y2Ba,gydF4y2Ba35gydF4y2Ba].前一个gydF4y2Ba体外gydF4y2Ba研究表明RSV可刺激中性粒细胞释放MPO [gydF4y2Ba36gydF4y2Ba,这与我们的发现是一致的。痰液和支气管肺泡灌洗液中中性粒细胞弹性蛋白酶、MPO和基质金属蛋白酶9的水平也被证明与气道疾病的疾病严重程度指数相关[gydF4y2Ba37gydF4y2Ba,gydF4y2Ba38gydF4y2Ba].gydF4y2Ba
上皮细胞的丧失并增加LDH释放对RSV感染的上皮有特异性。我们没有检测到Teer的变化。这可能是由于在膜的基底外侧形成沉积物的非侵略性嗜中性粒细胞,这可以增加电阻并补偿我们检测到的顶端上皮细胞中的间隙。尽管朝向从RSV感染的细胞或中性粒细胞趋化术中收集的顶端表面培养基类似数量的中性粒细胞迁移,但与在RSV感染的上皮的迁移相比,这不会导致上皮细胞脱落或LDH释放。这表明损害取决于RSV感染的上皮细胞的存在。这些感染的上皮细胞的脱落可能导致年轻婴儿的小气道中的阻塞[gydF4y2Ba39gydF4y2Ba].在动物模型中,RSV NS2蛋白已被证明有助于上皮脱落和急性气道阻塞[gydF4y2Ba11.gydF4y2Ba].gydF4y2Ba
此外,我们还发现中性粒细胞介导的rsv诱导的上皮损伤导致了病毒载量的降低。这种抗病毒活性可以直接由中性粒细胞介导,通过脱颗粒或吞噬rsv感染的细胞,从而阻止病毒进一步传播。在没有感染nAECs的情况下,对中性粒细胞和RSV进行的其他实验支持了这一发现,中性粒细胞具有抗病毒作用,因为它们减少了感染性颗粒的数量,但没有减少RNA的数量(gydF4y2Ba补充图S7gydF4y2Ba).先前的一些研究支持这一发现,中性粒细胞已被证明对病毒性呼吸道感染有益[gydF4y2Ba40gydF4y2Ba- - - - - -gydF4y2Ba42gydF4y2Ba]被认为有助于抗病毒防御[gydF4y2Ba43gydF4y2Ba,gydF4y2Ba44gydF4y2Ba].然而,使用中性粒细胞耗尽小鼠的研究得出结论,中性粒细胞不太可能在RSV感染期间的病毒清除中发挥主要作用,因为病毒载量[gydF4y2Ba45gydF4y2Ba]及肺损伤[gydF4y2Ba40gydF4y2Ba]相当于野生型小鼠中报道的那些。我们发现中性粒细胞培养型迁移减少了传染性RSV的量,但没有改变从RSV感染的纤毛上皮中恢复的病毒RNA的量。这种差异可能是由于嗜中性粒细胞和/或上皮细胞中存在的灭活病毒颗粒的测定的敏感性,其具有完整或部分碎片化病毒RNA。gydF4y2Ba
由于我们在较少的中性粒细胞粘附的条件下观察到较少的上皮损伤,因此我们假设中性粒细胞粘附对RSV感染的上皮的粘附是对上皮损伤的原因。为了研究这一点,我们使用抑制剂,其阻断LFA-1对中性粒细胞和ICAM-1之间的相互作用在NAEC上。该抑制剂降低了中性粒细胞粘附到RSV感染的上皮,并且显着降低的上皮损伤,尽管迁移的中性粒细胞和中性粒细胞弹性蛋白酶释放的数量不受影响。这表明上皮损伤是由中性粒细胞与RSV感染上皮的接近或直接相互作用介导的。粘附中性粒细胞的组织和聚类可能是驱动RSV疾病严重程度的重要机制。以前的报道表明,局部白三烯B4信号传导负责中性粒细胞蜂拥而合,中性粒细胞的协调聚集可以加速中性炎症[gydF4y2Ba33gydF4y2Ba].我们模型中感兴趣的细胞的可访问性提供了方法的优势gydF4y2Ba在活的有机体内gydF4y2Ba以及活体方法,这可以让我们在单个细胞水平上研究人类细胞和转录组的变化。我们小组未来的工作旨在比较RSV感染期间中性粒细胞的转录组和功能行为。gydF4y2Ba
总之,本研究揭示了中性粒细胞经上皮细胞迁移和粘附上皮细胞迅速导致纤毛功能较差,组织损伤和增加病毒杀伤的rsv感染纤毛细胞培养。进一步研究迁移机制,包括中性粒细胞动力学、信号传递、集群和激活,可以提高我们对呼吸道合胞病毒毛细支气管炎婴儿免疫反应的理解,并帮助开发新的治疗方法。gydF4y2Ba
补充材料gydF4y2Ba
补充材料gydF4y2Ba
请注意:gydF4y2Ba编辑部没有编辑补充材料,并随着作者提供的,上传。gydF4y2Ba
补充的方法gydF4y2Baerj - 02216 - 2019.的方法gydF4y2Ba
补充数据gydF4y2Baerj - 02216 - 2019. -数据gydF4y2Ba
补充统计信息gydF4y2BaERJ-02216-2019.STATS.gydF4y2Ba
补充视频1gydF4y2Baerj - 02216 - 2019。Video_1gydF4y2Ba
补充视频2gydF4y2Baerj - 02216 - 2019。Video_2gydF4y2Ba
补充视频3gydF4y2Baerj - 02216 - 2019。Video_3gydF4y2Ba
可分享的PDF.gydF4y2Ba
脚注gydF4y2Ba
作者贡献:J.A. Herbert开发并优化了倒置中性粒细胞迁移模型,使用来自鼻刷的初级AECs,参与研究设计、数据采集和分析,以及手稿的组装。邓元对研究的设计、数据的获取和分析,以及手稿的组装做出了贡献。P. Hardelid对数据的统计分析做出了贡献。罗宾逊对数据的获取和分析以及手稿的审查做出了贡献。Ren l对数据的获取和分析,以及手稿的编写做出了贡献。D.模塑有助于获取和分析数据,并审查手稿。R.L.史密斯对研究的概念、数据分析、手稿的组装和最终批准作出了贡献。C.M.史密斯构想了这项研究,对研究设计、数据分析、组装和手稿的最终批准做出了贡献。gydF4y2Ba
这篇文章有补充资料可从gydF4y2Bawww.qdcxjkg.comgydF4y2Ba
利益冲突:J.A.赫伯特没有什么可以披露的。gydF4y2Ba
利益冲突:邓永明没有什么可披露的。gydF4y2Ba
利益冲突:p·哈德利德没什么可透露的。gydF4y2Ba
利益冲突:e·罗宾逊没有什么可披露的。gydF4y2Ba
利益冲突:任磊没有什么可披露的。gydF4y2Ba
利益冲突:D.模塑没有什么可以披露的。gydF4y2Ba
利益冲突:R.L.史密斯没有什么可透露的。gydF4y2Ba
利益冲突:C.M.史密斯没有什么可披露的。gydF4y2Ba
支持声明:Y. Deng和L. Ren获得了美国医学科学院的牛顿奖学金(参考文献0403和NIF004/1012)。C.M. Smith是威康信托基金(212516/Z/18/Z)的获得者。R.L.史密斯是由大奥蒙德街儿童慈善机构(赠款代码W1802)资助的。这项研究得到了国家卫生研究所大奥蒙德街医院生物医学研究中心的支持。显微镜检查在伦敦大学学院GOS儿童健康研究所的光学显微镜核心设施进行,该设施得到了NIHR GOSH BRC奖17DD08的支持。所表达的观点是作者的观点,不一定是国家医疗服务体系、国家卫生保健机构或卫生部的观点。本文的资金信息已存入gydF4y2BaCrossref资助者注册表gydF4y2Ba.gydF4y2Ba
- 已收到gydF4y2Ba2019年5月31日。gydF4y2Ba
- 接受gydF4y2Ba2020年3月8日。gydF4y2Ba
- 版权©2020人队gydF4y2Ba
这个版本是在知识共享署名许可证4.0的条款下发布的。gydF4y2Ba
参考gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba