摘要
介绍随机对照试验证实了抗白细胞介素-5单克隆抗体mepolizumab的有效性;有关其在日常临床实践中对现实世界的影响的数据开始出现。我们评估了现实世界中为患者开出的美泊珠单抗的有效性和安全性。
方法REALITI-A是一项全球性、前瞻性、观察性队列研究,从哮喘患者的常规医疗访问中收集数据。新开美波利珠单抗治疗严重哮喘患者12例 纳入了美波利珠单抗治疗前的相关病史(回顾性收集)。对完成1 进行了为期一年的随访(截至2019年2月28日)。主要目的是比较临床显著恶化(需要口服皮质类固醇(OCS)和/或住院和/或急诊)的发生率美波利珠单抗治疗前后;需要住院和/或急诊科就诊的病情恶化和维持OCS使用的改变是次要目标。报告了与治疗相关的不良事件。
结果总体而言,包括368名接受美波利珠单抗治疗的患者。与需要住院和/或急诊就诊的患者一样,临床显著恶化的发生率降低了69%,从治疗前每人每年4.63例降至随访期间每人每年1.43例(p<0.001)(每人每年从1.14减至0.27;减少77%)。在治疗前有维持OCS剂量数据的159名患者中,中位日剂量从10.0(治疗前)减至5.0 毫克·天−1随访21-24周,持续至53-56周。没有新的安全信号被报道。
结论这些数据表明,mepolizumab的有效性与现实环境下的临床试验结果一致,显著减少了加重和每日维持OCS剂量。
摘要
Mepolizumab已经在临床试验的受控环境中证明了对严重嗜酸性哮喘患者的疗效。这些来自前瞻性REALITI-A研究的初始数据表明,在真实世界的环境中也获得了类似的结果。https://bit.ly/3hINnFO
介绍
在全球估计的3亿哮喘患者中,预计5-10%将经历严重疾病,给患者和卫生保健系统带来重大负担[1- - - - - -6].许多严重哮喘患者在接受最大限度的吸入控制药物治疗后,病情继续恶化[1]严重嗜酸性哮喘是严重哮喘的几种表型之一,与持续嗜酸性炎症、肺功能降低、哮喘控制不良和反复发作有关,使用/不使用全身性皮质类固醇(SCS)[1,7- - - - - -11].
Mepolizumab是一种抗白细胞介素-5单克隆抗体,选择性抑制嗜酸性炎症[12].在临床试验中,根据标准护理,添加美波利珠单抗治疗,可减少病情恶化,降低口服皮质类固醇(OCS)依赖性,改善肺功能、哮喘控制和与健康相关的生活质量与有急性加重史的严重嗜酸性哮喘患者的配对安慰剂[13- - - - - -16].它被批准作为严重嗜酸性哮喘患者的附加治疗[17,18].
临床试验合格标准通常导致患者人群在人口特征和疾病特征方面比在常规临床实践中治疗的患者更加同质[8,19].虽然临床试验有很高的内部效度,但它们不能复制真实世界的条件[20.]事实上,呼吸有效性小组的一份宣言指出,有必要从现实世界中接受外部有效性治疗的患者身上获取结果数据,以补充临床试验并指导治疗相关决策[21].为期24个月的REALITI-A研究评估了mepolizumab在临床实践中的应用。在这里,我们报告了一项对截至2019年2月28日mepolizumab启动后完成12个月随访的患者数据的初步分析。它们代表了现实世界临床实践中第一批使用美泊珠单抗的患者。
方法
主题
符合条件的患者年龄≥18岁,目前临床诊断为哮喘,医生决定启动美泊珠单抗治疗,并在入组前有≥12个月的相关医疗记录,并为参与研究提供知情同意。允许先前使用其他生物药物;那些在入学前一年接受美泊珠单抗治疗的患者被排除在外。在入组前一年内参加过介入临床试验的患者也被排除在外。患者来自7个国家的51个中心(表1).
研究设计
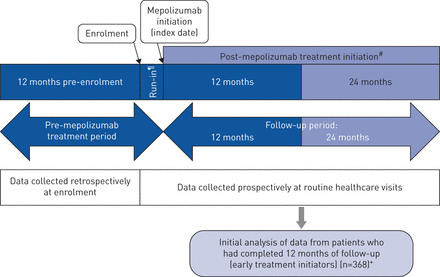
realit -a (GSK研究标识号204710)是一项全球、前瞻性、单组、观察性队列研究,纳入确诊为哮喘并接受新开mepolizumab治疗的患者(由医生决定)(图1和补充材料)。索引日期是首次服用美波利珠单抗。登记可在索引日期之前或之后进行;如果在索引日期之前进行,则有一个可变长度的磨合期(由当地处方和配药实践驱动)在登记日期和索引日期之间,继续进行相同的治疗。登记日期和索引日期相同或登记日期晚于索引日期(最多7天)时,没有磨合期 从索引到注册允许的天数)。
研究设计。#:将对全部研究人群(主要和次要目标)进行为期12个月的中期分析,并对全部研究人群(次要目标)进行为期24个月的分析。¶:如果在指标日期之前登记,则有一个可变长度的磨合期,患者继续接受相同的治疗;当报名日期与指数日期在同一天或指数日期在报名前发生时,没有冲突期。+:数据截止日期2019年2月28日。
mepolizumab前治疗期在指标日结束,并开始:1)如果指标日在登记日之前,则在365天登记前;2)如索引日期与报名日期相同,则365天(+1天);如报名日期为索引前日期,则365天(+磨合期+1天)。在入组时回顾性收集前一年的医疗记录和患者召回数据(如果相关,在磨合期间前瞻性收集)。
mepolizumab启动后的12个月随访期从指标日(+1天)到第一个:死亡、撤回同意或随访结束。目前的分析是在该研究的第一组参与者中进行的,这些参与者在2019年2月28日开始使用mepolizumab后完成了12个月的随访。在指标后的12个月期间,前瞻性地收集哮喘保健门诊(常规或计划外)的数据;本观察性研究没有特别安排来访。本次分析纳入的研究人群子集为2016年12月至2018年2月;2019年10月31日完成全部研究人口注册。
结果
主要目的是比较mepolizumab治疗前的临床显著哮喘加重率与随访12个月。临床显著恶化定义为需要sc的哮喘恶化(任何剂量;口服类固醇(如。强的松)≥3天或单次全身给药(静脉/肌肉注射)和/或住院和/或急诊。对于已经接受维持性SCS治疗的患者,至少需要两倍于现有维持剂量,持续≥3天。使用糖皮质激素疗程间隔小于7天的急性加重被归类为同一急性加重(根据医生输入的数据)。
次要目标比较了同一时期的下列结果:需要住院和/或急诊科就诊,或仅住院的哮喘加重率,无临床显著加重的患者比例,以及在临床显著加重率中>0 - <50%和≥50-100%降低的患者比例。此外,对于登记时报告的患者,他们正在接受维持型OCS (补充材料)中位每日维持OCS剂量从治疗前的变化和减少百分比为12 在开始美波利珠单抗治疗数月后进行评估。还报告了接受美波利珠单抗治疗前的维持性OCS患者中停止使用美波利珠单抗维持性OCS的比例。还评估了血液嗜酸性粒细胞计数与基线相比的变化。安全目标包括报告的美波利珠单抗相关不良事件和严重不良反应不良事件。不良事件与美波利珠单抗的关系由研究者确定,无需进一步裁决。
分析
假设25%的患者会在整个研究期间退出(补充材料),对200例患者进行12个月的mepolizumab治疗期,预计有90%的能力检测到在双侧5%水平上临床显著恶化的35%下降。用于所有有效性和安全性评估的治疗人群包括所有接受了一剂或更多mepolizumab剂量的入组患者。亚组分析采用血液嗜酸性粒细胞计数(<150,≥150 - <300和≥300 cells·µL)−1)或索引前可用的最近计数。额外的事后在治疗前期间,通过维持OCS使用和剂量对临床显著加重进行亚组分析(是的与没有<10与≥10 mg·−1)、入学年龄(<65岁)与≥65岁)和终生使用过奥玛珠单抗(是的与no),以及治疗前维持OCS使用和剂量的血液嗜酸性粒细胞计数。
本研究使用了一种治疗停药的治疗政策评估方法,该方法利用12个月随访期间收集的所有数据对美泊珠单抗的预期效果进行了评估,无论患者是否停用了美泊珠单抗。该分析与临床试验中的意向治疗分析相一致。
治疗前和12个月随访期间的加重率使用负二项回归分析,时间周期(治疗前和12个月随访)作为协变量。使用广义估计方程(GEEs)对平均估计方差进行患者内相关性校正。使用logistic回归和治疗前分析无临床显著加重的患者比例与比较治疗后起始期数据通过时间周期是协变量。临床显著加重率降低≥50%的患者比例也有报道。在治疗前和12个月的随访期间,计算每个患者28天内的平均OCS剂量。在计算平均值时,如果某一天没有记录数据,则假设剂量为0毫克(补充材料);如果无法解释记录的剂量,则平均值基于具有可解释数据的天数。汇总统计(包括中位数)OCS维持剂量的百分比基于前面所述计算的平均值。在每个治疗后时间点计算维持OCS每日剂量相对于基线的患者特定百分比变化。应用无分布方法[22,从基线开始治疗12个月后(95%置信区间)估计中位百分比下降(95%置信区间)。即周53-56)。使用混合模型重复测量法评估血液嗜酸性粒细胞计数与基线的比率。本研究仅收集美泊珠单抗相关不良事件或GSK其他产品的数据。
这项研究是根据《赫尔辛基宣言》进行的。每个研究地点都获得了当地的伦理批准。
结果
患者
总的来说,在接受治疗的人群中,有368例患者接受了一次或更多剂量的美泊珠单抗治疗。在这项分析中,英国纳入的患者最多(n=136) (表1).入校时平均体重指数为28.7 kg·m−2, 39%(364例中有143例)的患者目前是吸烟者或已戒烟者,48%(365例中有174例)的患者正在接受mepolizumab前OCS维持治疗(表1).在基线血嗜酸性粒细胞计数数据可用的患者中,357人中有51人(14%)基线血嗜酸性粒细胞计数<150个细胞·µL−1在357人中,有45人(13%)进行了计数≥150– <300 细胞微升−1357个细胞中有261个(73%)细胞计数≥300个−1.根据基线血嗜酸性粒细胞计数进行分层时,<150的患者中,51名患者中有32名(63%)、45名患者中有32名(71%)和258名患者中有108名(42%),≥150– <300及≥300 细胞微升−1各亚组分别报告了在治疗前使用维持OCS。此外,38%(140 / 368)的患者有鼻息肉的临床病史。
在数据截止时,患者接受平均值±sdmepolizumab治疗11.4±3.11,平均±sd疗程340.4±87.24天。总的来说,368例患者中有70例(19%)在12个月的随访期间停用了美泊珠单抗;最常见的原因是参与者决策(368例中有27例(7%)),而368例中有13例(4%)患者报告缺乏疗效(补充表S1).
恶化
临床显著恶化率从mepolizumab治疗前每人每年4.63下降到12个月随访期间每人每年1.43,相当于显著降低69%(比率0.31 (95% CI 0.27-0.35);p < 0.001) (图2).在基线血嗜酸性粒细胞计数亚组中,急性加重率降低相似(图2).
mepolizumab治疗前(入组前365天加上入组期间开始的任何急性发作)和12个月随访期间的哮喘加重率。BEC:血液嗜酸性粒细胞计数。n值表示患者人数。
需要住院和/或急诊科就诊的恶化率也显著降低了77%,从治疗前每人每年1.14降低到随访期间每人每年0.27(比率为0.23 (95% CI 0.18-0.30);p < 0.001);所有基线血嗜酸性粒细胞计数亚组均出现下降(图2)此外,治疗后需要住院治疗的总体人群的恶化率显著降低(p<0.001),在所有基线血嗜酸性粒细胞计数亚组中观察到类似的趋势。
总的来说,67%(366名患者中247名)的患者在治疗前到mepolizumab启动12个月后的临床显著加重缓解≥50%;如果排除治疗前无加重史的患者,这一比例升至73%(340人中247人)(表2).此外,随访期间没有出现临床显著恶化的患者比例明显更高(48%)。与预处理(7%;或12.13 (95% ci 8.03-18.33);p < 0.001) (图3).在基线血嗜酸性粒细胞计数亚组中,随访期间无临床显著恶化的患者比例上升到38-49%与预处理期间的7-9% (图3).通过前治疗期维持OCS使用和剂量、入组时的年龄和之前使用奥玛珠单抗评估的临床显著恶化在补充图S1.
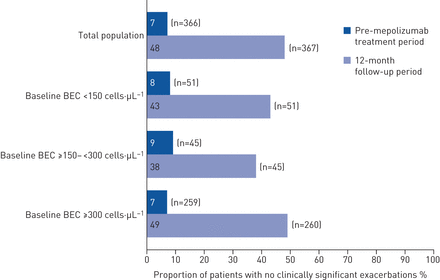
美波利珠单抗治疗前未出现临床显著恶化的患者比例(365 入学前天,加上磨合期间开始的任何恶化)和12个月的随访期。BEC:血液嗜酸性粒细胞计数。n值表示患者数量。
维修法团
159例患者治疗前OCS维持剂量数据(补充材料)每日维持OCS剂量的中位数(四分位间距(IQR))从10.0(5.0–15.0)下降 毫克·天−1预处理至5.0 (0.9-10.0)mg·d−1在第21-24周时(5.0 (0.0-7.5)mg·day),并保持相同水平直到第53-56周−1).相应的中位百分比下降为52%(95%可信区间50.0% - 75.0%)(即周53-56)(图4a).在有数据可用的在53-56周接受维持OCS治疗的125例患者中,82例在53-56周仍在接受OCS治疗,34%(125例中43例)的患者在接受美泊珠单抗治疗时停止了OCS(数据来自治疗时中断治疗的预判)(图5).
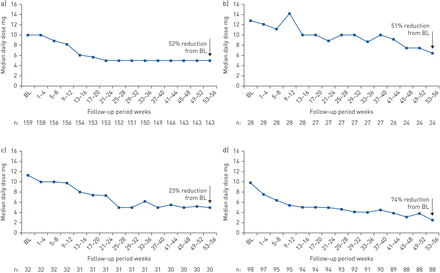
mepolizumab治疗开始后,维持口服皮质类固醇(OCS)用于a)总体人群和根据以下基线(BL)血嗜酸性粒细胞计数亚组:b) <150, c)≥150 - <300和d)≥300细胞·µL−1.使用无分布方法计算中值百分比变化[22以以BL为变量的患者特异性百分比变化。n值表示患者人数。
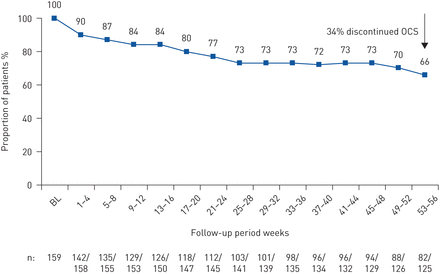
在接受美泊珠单抗治疗后继续口服皮质类固醇维持治疗(OCS)的患者比例。伯恩·隆伯格:基线。数据来自治疗中停止治疗的估计(即数据考虑到治疗中止)。n值表示接受OCS数据的患者人数(连同有OCS数据的患者人数)。
<150、≥150 - <300和≥300细胞·µL−1在基线血嗜酸性粒细胞计数亚组中,治疗前每日维持OCS的中位剂量从12.8、11.3和9.8 mg·d降低到6.5、5.0和2.5 mg·d−1分别在第53-56周出现;分别在第9-12周、第13-16周和第5-8周出现下降(图4b–d).在第53–56周,在<150周内,与基线相比,OCS每日维持剂量中位数减少的中位数百分比,≥150– <300及≥300 细胞微升−1基线血嗜酸性粒细胞计数亚组分别为51% (95% CI 22-74%)、23% (95% CI 0-69%)和74% (95% CI 50-100%)。
血嗜酸性粒细胞计数
mepolizumab治疗开始后,血液嗜酸性粒细胞计数从最小二乘几何平均值370 (95% CI 320-410)细胞·µL下降−1基线至60 (95% CI 50-80)细胞·µL−1在第9-12个月(IQR中位数),血液嗜酸性粒细胞计数值为442(270-800)个细胞·µL−190(40-100)个细胞·µL−1在第9-12个月),这相当于减少83%至60% 细胞微升−1(第9-12个月与基线的最小二乘平均比:0.17 (95% CI 0.13-0.21))。在0-3个月时观察到血嗜酸性粒细胞计数的下降,并在12个月的随访中保持不变。补充表S2通过维持OCS的使用和治疗前的剂量显示血嗜酸性粒细胞计数。
讨论
REALITI-A研究是一项前瞻性、全球、观察性、自我对照队列研究,旨在收集新近接受mepolizumab治疗的哮喘患者的真实数据。这些初步结果显示,真实世界的mepolizumab启动导致了年度哮喘加重率的显著降低,以及临床意义上的日常维护OCS剂量的减少与pre-mepolizumab治疗。此外,与之前的随机对照试验(rct)结果相比,mepolizumab没有新的安全性问题。这些初始数据证实了mepolizumab在真实环境中的有效性。
我们发现,mepolizumab治疗开始后,临床显著恶化和需要住院和/或急诊的恶化率显著降低与在开始之前。观察到临床显著恶化的减少,与年龄、入学时OCS维持或先前使用奥玛珠单抗无关。治疗政策评估包括了停用mepolizumab患者的数据,提供了保守的有效性评估。我们的研究结果支持了MENSA (ClinicalTrials.gov标识符NCT01691521)及MUSCA (ClinicalTrials.gov标识符NCT02281318),接受mepolizumab(皮下剂量)的患者在临床上显著恶化的发生率分别降低了53%和58%与安慰剂,尽管在两项研究中都观察到了安慰剂效应[14,15].此外,我们的数据也与现实生活中严重哮喘美泊珠单抗治疗的几个较小的观察性研究结果一致[23- - - - - -27].
我们还评估了日常维持OCS的使用情况。我们观察到,在美波利珠单抗治疗前维持OCS的患者随访期间,日常维持OCS的中位剂量有临床意义的减少。当通过基线血嗜酸性粒细胞计数进行评估时,减少也有意义,尽管较小的样本量导致较大的死亡率r变异性。大约三分之一的患者在第53-56周停止维持OCS。与我们的结果类似,接受美波利珠单抗的患者OCS中位剂量减少50%与安慰剂在SIRIUS试验中得到了证实(ClinicalTrials.gov标识符NCT01691508),而且在较小的真实世界观察研究中也有报道[13,23- - - - - -27].考虑到与慢性SCS使用相关的不良事件的风险(无论剂量水平如何),以及与严重哮喘患者皮质激素诱发的不良事件相关的额外医疗成本,这些降低在严重哮喘患者中尤其重要[28,29].因此,这项大型的国际前瞻性REALITI-A研究,以及这些较小的观察性研究的结果,提供了证据,证明在临床试验中观察到的美泊利珠单抗的临床益处可以转化为现实环境,并表明美泊利珠单抗可能有助于减轻严重的哮喘医疗负担。
与选定的同质人群的随机对照试验不同,这项现实世界的研究包括异质人群,共病和伴随药物的范围更广与RCT中通常允许的。此外,与随机对照试验不同,这一现实世界的人口受付款人偿付标准的约束,各国的偿付标准各不相同。来自REALITI-A的数据补充了来自RCT的数据;然而,更重要的是,他们强调了美波利珠单抗在现实临床实践中的有效性。REALITI-A患者群体患有特别严重的哮喘,因为大约一半的患者接受了美泊利珠单抗治疗前的OCS维持治疗,在12个月内,患者平均有1.2次恶化需要住院和/或急诊 6个月的学前入学。在这项分析中,这些早期治疗的始作俑者患有如此严重的疾病也许并不奇怪,因为新的治疗方法往往被引导到那些疾病谱最严重的患者身上[30.]此外,在这项初步分析中,近50%的患者来自英国,英国的治疗资格标准比临床试验中采用的入选标准和许多其他REALITI-A国家的资格标准更为严格。然而,尽管本分析中的REALITI-A人群比随机对照试验中的重度嗜酸性哮喘患者更严重[13- - - - - -16没有吸烟史或肺功能状态限制的患者,其临床结果至少与临床试验设置的患者一样好。因此,REALITI-A研究为更正式的试验提供了构象效度,从而确定美泊珠单抗的治疗益处在现实环境中得到了转化。
在先前的研究中已经确定了重症哮喘患者中较高的血嗜酸性粒细胞计数与美泊利珠单抗反应之间的关系[13- - - - - -16,越来越多的证据支持mepolizumab用于基线血嗜酸性粒细胞计数≥150细胞·µL的患者−1[31- - - - - -33].这一人群被定义为严重发病率,随着嗜酸性粒细胞计数的增加而增加(嗜酸性粒细胞计数是mepolizumab缓解恶化的预测指标)[15,34- - - - - -38].在我们的研究中,在治疗前和随访期间,所有基线血嗜酸性粒细胞亚组(包括<150细胞·µL)的临床显著恶化率和中位每日维持OCS使用量均有类似的降低−1子群。尽管美泊珠单抗已被批准用于治疗严重的嗜酸性粒细胞哮喘,并且通常需要嗜酸性粒细胞升高的证据[18,在真实环境中,接受治疗的严重哮喘人群包括51例(14%)基线血嗜酸性粒细胞计数<150个细胞·µL的患者−1在条目。然而,大多数患者的血液嗜酸性粒细胞计数≥300个细胞·µL,证实有严重的嗜酸性粒细胞哮喘−1(67%(51人中有34人))和/或在入学时需要维持居留权(63%(51人中有32人))。
现实世界研究的局限性包括从标准临床护理记录中获取数据;因此,可能存在信息缺失。为了缓解这一问题,一项研究进入标准是患者需要12 在登记前有几个月的相关医疗记录;这样做是为了尽可能准确地获得关于病情恶化史的信息。然而,由于记录或自我治疗不足,可能忽略了一些历史病情恶化,这将导致低估mepoli的影响zumab。此外,由于REALITI-A是一项现实世界的研究,患者或医生可能会中止或改变治疗。在现实世界的研究中,患者的行为可能更难控制,现实世界研究中的中止率已被证明高于随机对照试验中观察到的中止率,患者的决定和缺乏疗效对于大多数治疗撤销,ng[39].在这项为期1年的研究中,19%的患者停止了治疗,这与现实世界的其他研究中观察到的比例相似[39].其中一些患者可能对美泊珠单抗没有积极反应,因此停止了研究。一些患者在患有其他疾病的同时患有严重的嗜酸性粒细胞性哮喘是可行的,这些患者的任何持续症状可能是由于非哮喘疾病,并被错误地解释为对美泊珠单抗缺乏反应。然而,只有4%的人因为缺乏疗效而停止使用美泊珠单抗,所以这不太可能是一个重要的混杂因素。患者也可能因未能满足支付方报销标准而退出,电子病例报告表格中没有列出这一选项。此外,使用治疗中断的治疗政策评估方法,包括所有接受一次或更多剂量美泊珠单抗的患者,试图限制由于研究中途退出而产生的任何偏倚。由于这是一项正在进行的研究和对患者亚队列的临时分析,数据集可能会发生变化;然而,所有的努力都是为了使数据符合最佳标准。最后,reality - a不是一项安慰剂对照研究;因此,结果可能是治疗效果和其他行为改变的结合。 While this is inherent in all real-world open-label studies, this analysis of early initiators in the real world shows that the effects of mepolizumab are consistent with those demonstrated in the severe asthma clinical trials and identifies the clinical benefits of mepolizumab are translated in the severe asthma population in the real world.
总而言之,对常规临床治疗的哮喘患者进行mepolizumab治疗启动的初步分析数据显示,mepolizumab与哮喘加重的显著减少和OCS维持性使用的临床显著减少相关。此外,mepolizumab的耐受性良好,安全性与之前在严重嗜酸性哮喘患者中进行的临床研究相似[14- - - - - -16]这些数据还表明,在临床试验中发现的美波利珠单抗疗效转化为现实世界,并为在这种情况下治疗的患者提供了有价值的治疗结果见解。
补充材料
可共享的PDF
致谢
作者要感谢所有参与中心在最近的研究中,(葛兰素史克,斯蒂夫尼奇,英国)和莎莉沃斯利为主要研究和设计概念,和伊莱恩·欧文(葛兰素史克,斯蒂夫尼奇,英国),他Gunsoy(葛兰素史克,布伦特福德,英国),拉斐尔•阿方索(美国葛兰素史克、Collegeville PA), Namhee Kwon(葛兰素史克,布伦特福德,英国)和弗兰克·阿尔伯斯(葛兰素史克公司,(美国北卡罗来纳州三角研究园),感谢他们对研究概念和设计的支持。由Elizabeth Hutchison和Roisin McCorkell (Fishawack Indicia Ltd, Knutsford, UK)提供编辑支持(以写作协助的形式,包括研究报告初稿的开发、表格和数字的汇编、作者评论的整理、语法编辑和引用),并由GSK资助。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
数据共享:在完成初步分析后,可以要求匿名的个人参与者数据和研究文件,以进行进一步的研究www.clinicalstudydatarequest.com.
作者贡献:K. Gemzoe和M.K. Van Dyke对研究的概念和设计作出了贡献,T. Harrison、G.W. Canonica、G. Chupp、J. Lee、F. Schleich、T. Welte和A. Valero对数据的获取作出了贡献。所有作者都对数据的解释做出了贡献,对手稿的重要知识内容进行了严格的修改,最终批准了将要出版的版本,并同意对工作的所有方面负责。所有作者都可以访问研究数据。
利益冲突:T. Harrison报告称,该研究和写作支持由葛兰素史克提供资金,并在提交的工作之外,接受了葛兰素史克和阿斯利康的讲座和咨询委员会工作的个人费用,以及Vectura的咨询委员会工作的个人费用。
利益冲突:G.W. Canonica报告称,该研究和写作支持由葛兰素史克提供资金,并在提交工作之外获得了葛兰素史克、阿斯利康、赛诺菲-健赞、Regeneron和诺华的讲座和顾问工作的拨款和个人费用。
利益冲突:G. Chupp报告称,该研究和写作支持由葛兰素史克提供资金,并在提交工作之外获得了葛兰素史克、阿斯利康、Genentech、赛诺菲-健赞、Regeneron、Teva和诺华的讲座和顾问工作的拨款和个人费用。
利益冲突:j .李报道,这项研究和写作是由葛兰素史克公司的支持,收到Regeneron赠款,基因泰克,罗氏公司和武田,赠款和个人费用从葛兰素史克讲座,Sanofi-Genzyme,诺华,Medexus和阿斯利康,个人费用从Mylan讲座,Aralez和默克公司在提交工作。
利益冲突:F.Schleich报告说,研究和写作支持由葛兰素史克资助,阿斯利康为讲座和咨询委员会工作提供赠款和个人费用,捷西和诺华为讲座和咨询委员会工作提供赠款和个人费用,Menari为讲座和咨询委员会工作提供非财务支持ni和Mundifharma,葛兰素史克的演讲、咨询和顾问委员会工作的补助金和个人费用,提交的工作之外。
利益冲突:t Welte报道,这项研究和写作是由葛兰素史克公司的支持,并得到了助学金和个人费用从阿斯利康讲座和咨询委员会的工作,个人费用从诺华和赛诺菲安万特讲座和咨询委员会的工作,个人费用从葛兰素史克公司顾问委员会的工作,在提交工作。
利益冲突:A. Valero报告称,该研究和写作支持由葛兰素史克提供资金,并从阿斯利康、诺华和Mundipharma获得咨询和讲座的个人费用,从赛诺菲和勃林格获得咨询的个人费用,从Chiesi和葛兰素史克获得演讲的个人费用。
利益冲突:K. Gemzoe报告称,该研究和书面支持是由GSK资助的,是GSK的员工,并持有GSK的股份/期权。
利益冲突:A. Maxwell报告称,该研究和写作支持是由GSK资助的,并且是GSK的员工,并持有GSK的股份/期权。
利益冲突:S. Joksaite报告称,该研究和书面支持是由葛兰素史克资助的,是葛兰素史克的员工,并持有该公司的股票/期权。
利益冲突:S. Yang报道称,该研究和书面支持是由葛兰素史克资助的,并且是葛兰素史克的员工并持有该公司的股票/期权。
利益冲突:P. Howarth报告称,该研究和书面支持是由GSK资助的,并且是GSK的员工,并持有GSK的股份/期权。
利益冲突:M.K.Van Dyke报告说,研究和写作支持由GSK资助,是GSK的雇员,持有GSK的股份/期权。
支持声明:本研究由GSK (GSK研究标识符204710)资助。本文的资金信息已存入Crossref资助者注册表.
- 收到了2020年1月23日。
- 接受2020年7月23日。
- 版权©2020人队
本文是在知识共享署名非商业许可4188滚球软件.0的条款下开放获取和发布的。