文摘
当前的方法来取代受损的上呼吸道与外源性细胞上皮是有限的。现有的策略使用移植缺乏黏膜纤毛的功能,导致感染和保留分泌物和角蛋白碎片。策略,气道上皮再生黏膜纤毛的功能显然是可取的,使复杂的气道疾病的新疗法。
在这里,我们调查的影响细胞外基质(ECM)对气道上皮细胞粘附、增殖和黏膜纤毛的功能在生物工程的背景下,粘膜移植。在体外,主要人类支气管上皮细胞(HBECs)最容易坚持胶原IV。生物、仿生和合成支架比较的ECM蛋白质含量和气道上皮细胞粘附。
胶原IV和层粘连蛋白表面保留decellularised真皮和上皮细胞对decellularised真皮大于仿生或合成替代测试。阻止上皮细胞整合素α2导致减少坚持胶原IV和decellularised真皮支架。在气液界面(ALI),支气管上皮细胞培养decellularised真皮支架上形成了一个呼吸道上皮细胞分化与黏膜纤毛的功能。使用在活的有机体内小鸡绒毛膜尿囊的膜(CAM),兔气管和免疫力低下小鼠模型,我们表明短期保存移植后的细胞层。
我们的结果显示生成的可行性HBEC移植在临床上适用decellularised真皮支架和识别矩阵蛋白和整合蛋白重要的这一过程。的长期生存能力pre-differentiated上皮细胞和这种方法的相对优势移植基底细胞应该进一步评估临床前气管移植模型。
文摘
胶原IV, laminin-rich decellularised真皮支架支持黏膜纤毛的气道上皮移植在活的有机体内移植在临床前模型是具有挑战性的http://bit.ly/2IdQp5d
介绍
呼吸道粘膜行气管和支气管的内表面和由pseudostratified multiciliated含有分泌粘液上皮杯状细胞(1]。呼吸道粘膜执行一系列至关重要的功能,包括作为屏障防止感染和清除分泌物较低的航空公司通过黏膜纤毛的自动扶梯(2,3]。现有的方法来恢复呼吸道黏膜后气道重建和癌症切除依赖转移vascularised椎弓根的肌肉和皮肤移植。这些可以re-epithelialise小气道的部分,他们是不适合重建较大地区的上皮细胞保留复层鳞状组织学,因此缺乏所需的纤毛和mucosecretory细胞正常功能(4]。表皮上皮周转速度也高于呼吸道上皮细胞,这可能会导致这些患者的气道脱落和阻塞(5]。口腔上皮已成功用于粘膜移植和应用恢复一小部分气管粘膜(6];然而,由于限制捐赠组织,可以收获的程度,这种方法也不适合广泛的近端气道修复。
再生一个可移植的呼吸道粘膜层和黏膜纤毛的功能将是一个重要的一步气道再生医学领域的。它将使新疗法治疗长段粘膜上呼吸道的疾病,包括复杂的疤痕和肉芽肿性条件。这种技术也将是高度相关的基因编辑方法治疗遗传疾病,如囊性纤维化,细胞移植带来了重大挑战(7]。生物工程的例子气管更换已经被植入后缓慢mucosalisation[有限8- - - - - -10)和生物工程呼吸道粘膜移植可能提高此类程序的安全性和有效性。
目前的报道在体外生物工程上呼吸道粘膜有主要集中在再生粘膜层气管支架(11,12]。然而,在活的有机体内应用这些技术是有限的时间移植后血管发生。要克服这一点,我们设想使用一个两步的过程(13),粘膜层由呼吸道细胞(而不是其他上皮细胞的细胞,如。颊(14,15生成)在体外并可用于re-epithelialise pre-vascularised气道支架植入或直接嫁接到气道来取代受损的黏膜。这种方法更紧密地跟随自由组织转移的原则,在well-vascularised移植床是必不可少的成功结果(16]。
在制定一个方法再生呼吸道粘膜,仔细考虑需要给细胞外基质(ECM)的环境。ECM是一个复杂的大分子蛋白质网络受特定cation-dependent细胞表面受体,整合蛋白,基底外侧表面上皮细胞(17]。Integrin-ECM绑定导致细胞内的信号级联影响多种细胞过程包括附件、扩散、极性和细胞程序性死亡(18]。证据调查ECM的复层上皮细胞,以及蛋白质组学数据检查上呼吸道基底膜的组成,表明,胶原蛋白,胶原IV,层粘连蛋白,vitronectin和纤连蛋白中扮演重要的角色修改上皮细胞行为(19- - - - - -21]。在这里,这些基质蛋白对呼吸道上皮细胞的影响依恋,扩张和分化在体外研究以优化ECM环境生物工程气道粘膜。
材料和方法
主细胞培养
主要人类支气管上皮细胞(HBECs)隔绝支气管活检从成人上呼吸道或从患者的支气管肺(补充表S1)。伦理批准了从研究伦理委员会(REC引用:06 / Q0505和11 / LO / 1522)。HBECs保持在支气管上皮生长培养基(BEGM) (Lonza、绝望、英国)附件和扩散实验。分化实验,HBECs被孤立和维护在丝裂霉素C-treated 3 t3-j2支线层5µM岩石抑制剂Y - 27632 (3 t3 + Y)(恩佐生命科学,埃克塞特,英国)使用(如前所述)(22- - - - - -24]。细胞分离和扩大在BEGM段落1到3之间,而在3 t3 + Y细胞分离和扩展段落1到6之间使用。主要人类肺成纤维细胞维持在杜尔贝科修改鹰介质(DMEM)(英国)赫默尔亨普斯特德镇Gibco,含10%胎牛血清的边后卫和使用不迟于10。
塑料涂层的组织培养和细胞外基质蛋白
ECM蛋白质被用来外套组织培养塑料使用制造商推荐的浓度和一个值(高)之前,(低)浓度(媒介)。使用ECM蛋白质胶原蛋白我从人类新生成纤维细胞(美国圣地亚哥先进Biomatrix) 38.7µg·毫升−1µg·387毫升−1和968年µg·毫升−1;胶原IV从人类胎盘(C8374, Sigma-Aldrich,多塞特郡,英国)µg·10毫升−1µg·250毫升−1和500年µg·毫升−1;从人血浆vitronectin (V8379 Sigma-Aldrich) 0.5µg·毫升−11.25µg·毫升−1和2.5µg·毫升−1;层粘连蛋白从人类胎盘(L6274 Sigma-Aldrich) 1µg·毫升−12µg·毫升−1和4µg·毫升−1;从人血浆纤连蛋白和0.1% (F0895 Sigma-Aldrich) 1µg·毫升−125µg·毫升−1和250年µg·毫升−1。Non-adherent 96 -孔板(赫默尔亨普斯特德镇10 554 961,费舍尔科学、英国)被涂上一层后ECM蛋白质相关制造商的协议。
整合素阻断实验
抗体之前报道对整合素亚单位(有阻塞函数25- - - - - -32)被添加的浓度1:200 BEGM和antibody-cell悬挂被保存在冰前20分钟ECM-coated或decellularised包含井实验研究细胞真皮支架附件。未经处理的细胞被用作控制。在细胞膨胀实验,细胞被允许遵循2 h后他们用磷酸盐(PBS)和介质包含阻塞BEGM抗体所取代。实验研究分化,阻止抗体被刷新后空气介质变化如图传说所示。抗体用来阻止整合素亚单位是:α1 (5 e8d9;美国罗福斯生物nbp2 - 29757),α2 (P1E6-C5;美国圣地亚哥359 304,Biolegend),α3 (ASC-1;MAB2056Z,默克密理博,沃特福德,英国),αv (NKI-M9;32 7904 Biolegend)α5 (NKI-SAM-1;328 004,Biolegend),α6 (GoH3; 313 614, Biolegend), α9β1 (Y9-A2; OBT1715Z, Bio-Rad, California, USA) and β1 (P5D2; MAB1959Z, Merck Millipore).
附件,增殖和代谢化验
涉及ECM-coated板块的化验,non-adherent 96 -孔板与ECM如上所述涂层和细胞被播种在30分钟前BEGM孵化在37°C, 5%的二氧化碳。井与PBS洗了三次去除游离细胞和盘子被冻结在−80°C。量化细胞的数量,盘子被解冻室温和细胞裂解缓冲DNA含有绿色荧光染料(赫默尔亨普斯特德镇CyQUANT GR,生活技术,英国)是根据制造商的协议。荧光测量使用标(励磁480海里,发射520 nm)和背景荧光是减去从这些读数。确定在ECM基质细胞扩张,上述步骤进行2 h和48 h的细胞播种。手机号使用参考标准曲线计算已知的细胞数量。
评估候选人HBEC附件支架材料,细胞被播种在non-adherent包含支架的96孔板。1小时后,井与PBS洗四次去除游离细胞和胰蛋白酶是粘HBECs应用于分离。由光学显微镜支架进行评估,以确保遵循细胞分离,收集和镀到一个单独的96孔板。DNA染色(CyQUANT GR、生活技术)是用来比较细胞附件如上所述。上皮细胞的可行性评估播种decellularised真皮或气管支架,细胞生存能力分析(alamarBlue,生活技术)使用。细胞被播种到decellularised支架底部的96孔板和孵化1 h。支架与PBS被洗,转移到新井和alamarBlue细胞生存能力试剂添加在介质(1:10比例)。2 h后,荧光(励磁560海里,发射590海里)被记录和最终价值减去计算值产生负控制井包含支架但没有上皮细胞。
气液界面文化和trans-epithelial电阻
标准气液界面(ALI)文化在正电子发射断层扫描(PET)膜,HBECs (1×106)在0.4μM被播种,12毫米PET膜transwells(康宁,弗林特郡,英国)和孵化在37°C和5%二氧化碳供应33]。阿里条件培养基被从顶端2天后被应用。细胞被喂食了阿里中包含BEGM和DMEM 1:1的比例补充μg·100毫升−1链霉素·毫升和100台−1青霉素,以及刚做好的视黄酸相当于100 nM最终浓度。Trans-epithelial电阻(te)是衡量使用EVOM2电阻计和Endohm室(美国世界精密仪器)。基底的顶端和双方的文化充满了BEBM (Lonza)和三个复制数据被为每个好,每次都让值稳定5 - 10 s。
候选人的生产支架
生产decellularised真皮,glycerol-preserved尸体的皮肤是来自欧元组织银行(Beverwijk,荷兰)。Decellularisation由洗涤三次在四十八小时以上PBS和孵化的皮肤24小时在1 m氯化钠37°C所描述的Deshpandeet al。(34]。那时表皮剥落和decellularised真皮使用直接或存储长达1个月在DMEM 4°C。POSS-PCU提供的纳米技术(英国伦敦大学学院),在它被生成使用以前公布的方法(35]。仿生胶原蛋白我支架是准备使用定制的吸收器后,制造商的协议(筏™,Lonza)。总之,鼠尾胶原蛋白我(第一个链接,伍尔弗汉普顿,英国),DMEM和最小基本培养基(MEM) 10 x(英国)赫默尔亨普斯特德镇ThermoFisher科学,结合在一个8:1:1比率,与5 m氢氧化钠中和,孵化15分钟允许凝胶的解决方案。吸收器被放置在每个表面的15分钟脱水凝胶和产生半透明的胶原蛋白支架(36]。
导管从终止了decellularisation新西兰白(NZW)兔子(Envigo,亨廷顿,英国)。气管被剥夺了全部的筋膜,洗了三次在PBS含有青霉素和链霉素(1 x, Gibco)超过24小时。气管被decellularised使用双循环酶洗涤剂decellularisation协议之前发表的Conconi等。(37]。短暂,导管放置在一个4%钠脱氧胆酸盐溶液(S1827 Sigma-Aldrich) 4 h与腔的风潮在室温下,洗在PBS和导管在室温下搅拌30分钟,放入1 L, 1 m氯化钠溶液含有22.5毫克脱氧核糖核酸酶(9 003 989,σ)3 h,然后洗Milli-Q水一夜之间在40°C第二周期重复上述步骤。完成第二个周期后,导管在Milli-Q洗水3天每天40°C和水被改变了。最后,他们消毒使用电离辐射。
大会的组织工程化呼吸道粘膜
Decellularised真皮准备使用上面描述的方法剪成CellCrowns™(Sigma-Aldrich)拟合24-well板块在体外实验或12-well板块在活的有机体内实验。HBECs和肺成纤维细胞的密度co-seeded到真皮1×106每厘米2和1×104每厘米2分别在1毫升的上皮细胞培养基。支架被淹没在维护上皮细胞培养基含有5µM y - 27632 (23每天)和媒介改变了。7天之后,CellCrowns™被移除的盘子和那些包含支架放入0.4µm PET膜transwell插入(康宁)阿里文化38]。介质改为阿里介质,换了三次/周。在阿里超过2周,支架粘液的清除了每隔一天温柔的愿望。在阿里3 - 4周后,采用倒置显微镜系统高速视频(尼康,尼康Ti-U 1000年,日本)40×客观和1.5×放大镜来评估纤毛拍频和模式。数码相机(运动专业4 x;IDT,帕萨迪纳市的美国)定在512×512地区的兴趣和记录在250帧·s1纤毛拍频和500帧·s1纤毛的节奏模式。纤毛拍频分析使用CiliaFA [39)也计算确定所需的帧数五个全部清扫的纤毛小费。纤毛运动障碍评估通过定义的不协调在一条纤毛上皮纤毛节奏模式。运动障碍评分计算比例的运动障碍的纤毛细胞纤毛细胞的总数。
组织学
样品为组织学洗两次在PBS和固定在10%中性缓冲福尔马林(NBF) 1 h。Epithelialised支架被固定为30分钟和嵌入HistoGel (ThermoFisher科学)来保护上皮的表层处理期间超然。固定后,样本存储在70%乙醇脱水前在4°C使用一个自动化的系统(1050年徕卡TP,徕卡、伦敦、英国)。Formalin-fixed,石蜡包埋标本切片在5µm厚度。苏木精和伊红染色法是使用一个自动执行樱花drs - 601染色机(位于莱茵河畔,樱花、荷兰)。样本安装使用樱花Coveraid(樱花)自动cover-slipping机Tissue-Tek盖片电影(拜耳诊断、阅读、英国)。
免疫荧光
幻灯片是免疫荧光脱蜡使用一个自动化的过程(drs - 601,樱花),然后洗在蒸馏水和阻塞PBS含有10%的边后卫(块解决方案)2 h。主要抗体应用块一夜之间解决方案,并在4°C的环境。三个PBS洗,特有的二次抗体(AlexaFluor ThermoFisher科学)应用于块溶液的浓度1:200 1 h在室温下。幻灯片再洗两次在PBS和彩色4′,6-diamidino-2-phenylindole (DAPI)(5毫克·毫升−1股票,在PBS 1:10 000;生命技术)10分钟。后最后PBS洗涤步骤,幻灯片使用ImmuMount cover-slipped(美国欧文GeneTex),密封的指甲油和成像蔡司700共焦显微镜(蔡司、从、德国)。
免疫细胞化学
对于自上而下的图像,支架在PBS洗两次,固定在10% NBF 30分钟,洗两次在PBS 5分钟每个和孵化块解决方案在室温下2 h。一夜之间,主要的抗体被应用于解决方案和孵化在4°C。在PBS三5分钟后洗,特有的二次抗体应用于1:200在阻止溶液在室温下1 h。支架是洗两次在PBS和DAPI(5毫克·毫升−1股票,在PBS 1:10 000;生命技术)应用。样本洗在PBS成像原位或后切除使用ImmuMount从井和cover-slipping(美国欧文GeneTex),使用蔡司700共焦显微镜(蔡司)。
细胞支架表面的可行性,评估现场/死细胞生存能力分析(ThermoFisher科学)。钙黄绿素(3.4µL·毫升−1)和ethidium homodimer-1(4µL·毫升−1)混合介质和细胞粘附后添加到支架。支架是孵化为45分钟,安装在玻璃幻灯片自上而下,包埋在蔡司700共焦显微镜成像(蔡司)。
扫描电子显微镜
支架固定在2.5%戊二醛,用0.1磷酸盐缓冲剂(pH值7.4)和蒸馏水,在一系列分级包裹100%乙醇脱水和干燥使用二氧化碳。使用粘碳标签,支架被安装在铝存根和涂上一层2纳米金/钯使用离子束涂布机(美国加州Gatan)。支架表面使用Jeol 7401年拍摄场发射扫描电子显微镜(Jeol,韦林花园城,英国)。纤毛长度测量是在20 000×屏幕通过电子显微镜放大。
小鸡绒毛膜尿囊的膜试验
受精Bovan棕色鸡蛋由亨利·斯图尔特& Co(英国诺福克)。简而言之,在胚胎第三天,鸡蛋和70%乙醇和清洗3 - 4毫升的白蛋白被移除通过针吸顶的壳。窗户被切除一个2×2厘米从外壳的上部方面揭示胚胎和绒毛膜尿囊的膜(CAM)血管。窗户密封胶带和鸡蛋孵化了5天。在胚胎第8天凸轮气鳔,琐事别针被用来破坏几个更小的血管。部分的测试支架(2毫米2温柔地)被放置在凸轮与上皮的一面向上和多余的血液耗尽。窗口之后,卵孵化到胚胎第十天。2000年与徕卡变焦成像立体显微镜(莱卡)相机适配器(Magnifi™,大角星实验室,堪萨斯州,美国),嫁接凸轮收获和固定在4%多聚甲醛(PFA)。无菌塑料套管的一部分被用作负控制和非细胞decellularised真皮被用来检查包括人类细胞的影响。比较epithelialised支架进行至少在两个独立的实验中每个实验小组六个鸡蛋。非细胞真皮比较了在一个实验中,至少有六个鸡蛋在每个实验小组。
在decellularised气管移植的组织工程化呼吸道粘膜的兔子
岁的男性NZW兔子9至10周3重达2.5公斤的到来。全身麻醉诱导使用0.5毫升·公斤−1氯胺酮肌内和0.2毫升·公斤−1七氟醚(甲苯噻嗪,并维护所有药物由国家兽医服务,特伦特河畔斯托克,英国)。部分decellularised气管(5厘米)被pre-implanted侧胸皮瓣从胸部和颈部皮肤下隧道到颈部,以创建一个vascularised脚手架的移植工程粘膜。弗利导管(大小16 f)是通过腔插入,大小和缝合在两端有4.0缝线缝合(Ethicon,伯克希尔哈撒韦公司,英国)作为支架,防止脚手架倒塌。气管被包裹在肌肉皮瓣和担保在颈部使用3.0丝缝合(Ethicon)和伤口关闭。同时,HBECs和成纤维细胞被播种到decellularised真皮制作的呼吸道粘膜移植如上所述。pre-vascularisation 4周后,颈部切口重开,脚手架的肌肉包裹。被切开的trachealis确认,直接通过肌肉。气管环是vascularisation的视觉评估证据,结构完整性和感染的迹象,在新制造组织工程粘膜被嫁接到支架表面。弗利导管支架或Kaltostat alginate-based敷料(旗下弗林特郡、英国)放置在移植物保护上皮细胞层和支架放置,以防止位移的肌肉皮瓣移植。气管和颈切口被关闭和动物是24小时或1周post-transplantation终止。
免疫抑制的兔子被要求减少急性移植排斥的人类细胞的概率(40]。他克莫司(剑桥大学生物科学,剑桥,英国)进行皮下注射0.3 mg·公斤−1连续三天,开始一天的手术前7天,然后隔天到实验的最后。地塞米松是流行性流感减毒活疫苗在后面实验的剂量2 mg·公斤−1每日三次,开始前24小时接(补充表S2)。血液样本被那天移植物植入并送往皇家兽医学院(英国哈特菲尔德)量化的白细胞,淋巴细胞和中性粒细胞。
移植免疫抑制小鼠的组织工程呼吸道粘膜
点头SCID小鼠(Envigo)犀牛和维护与七氟醚(国家兽医服务)。5厘米横向切口的鼠标和皮下的口袋里。Decellularised dermis-based呼吸道粘膜表被铺设在肌肉和表面的一层Mepitel硅胶敷料(Molnlycke医疗,哥德堡,瑞典)是在顶部,防止剪切。7天之后,老鼠终止,伤口重新移植和移植和底层老鼠肌肉组织学处理。
统计数据
统计分析使用GraphPad棱镜(美国圣地亚哥CA GraphPad软件)表示在图的传说。假定值报告四舍五入到小数点后三位被分配和统计意义p < 0.05。所有在体外至少在技术实验进行了一式三份,除非另有指示和重复中描述图的传说。数据意味着±扫描电镜值。
结果
细胞外基质依赖人工气道上皮细胞,增殖和分化
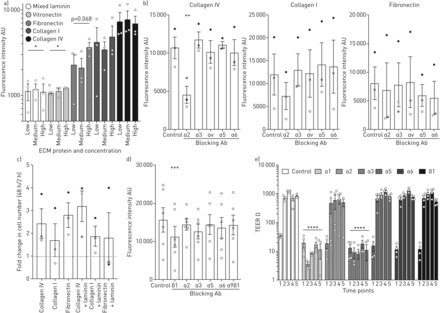
我们第一次评估附件的培养主要人类支气管上皮细胞(HBECs) [41- - - - - -43]ECM蛋白质中发现本机人工气道(补充图S1),发现胶原蛋白IV-coated井表现最好与细胞上明显多于laminin-coated或vitronectin-coated井(图1一个)。确定整合素介质ECM附件,我们执行附件化验ECM蛋白质的存在阻碍抗体各种整合素α亚基。阻断整合素α2导致上皮细胞的含量明显低于对胶原IV但阻断整合素亚单位α3,αv,α5α6没有效果(图1 b)。除了对胶原蛋白减少的趋势我存在一个整合素α2-blocking抗体,附件我或纤连蛋白胶原蛋白是变量之间的实验复制但不受这些阻碍抗体的存在(图1 b)。确定的影响ECM蛋白质后上皮增殖早期依恋,HBECs被播种到井涂以支持上皮细胞连接和细胞基质蛋白质数量2 h和48 h后确定。HBEC数无显著变化时看到这些蛋白和层粘连蛋白结合更紧密地模仿本机ECM (图1 c),但阻止抗体整合素β1显著减少早期HBEC扩张对胶原蛋白IV-coated井和laminin-coated井(图1 d)。没有抑制扩散在阻塞α2整合蛋白抗体的存在,α3,α5α6或α9β1 (图1 d)。
细胞外基质(ECM)的蛋白质的作用在人类支气管上皮细胞(HBEC)行为。HBECs (5×104)被播种non-adherent组织培养与ECM蛋白质涂塑和依恋决心在30分钟使用CYQUANT GR(英国)赫默尔亨普斯特德镇ThermoFisher科学、背景荧光减去。附件IV型胶原蛋白是大于层粘连(双向方差分析与Holm-Sidak测试多个比较)和vitronectin-coated井。实验重复了三次技术一式三份,包括使用两个独立的供体细胞培养。数据是在对数尺度。b) HBECs孵化在阻塞α2整合蛋白抗体,α3,αv,α5α6 20分钟前细胞(2×104)被播种到non-adherent组织培养塑料井涂以胶原IV,胶原蛋白我或纤连蛋白。荧光背景减去测量使用CYQUANT GR。阻断整合素α2导致胶原HBEC大大减少附件IV-coated井(单向方差分析与Holm-Sidak测试多个比较),但不是胶原蛋白I - (p = 0.141)或fibronectin-coated井(p = 0.881),而控制井。实验重复了三次技术一式三份(在黑色、灰色和白色),包括使用两个独立的供体细胞培养。c) HBEC细胞数量决定使用CYQUANT GR和标准曲线已知的细胞数量在2 h和48 h后播种HBECs (1×104)到non-adherent组织培养与ECM蛋白质涂塑。组之间无统计学差异被发现(单向方差分析与Holm-Sidak测试多个比较;所有比较p > 0.25)。实验重复了三次技术一式三份,包括使用两个独立的供体细胞培养。d)阻止抗体被添加到井2 h后播种HBECs (5×103)到胶原IV -和laminin-coated井。荧光背景减去被记录在48小时使用CYQUANT GR和无抑制性抗体相比,控制好。大大减少观察上皮细胞增殖与控制的整合素β1-blocking抗体(单向方差分析与Holm-Sidak测试多个比较)。实验重复了六次技术一式三份,包括使用两个独立的供体细胞培养。e)整合素抗体阻断被添加到气液界面阿里(ALI)文化的创造和在每一个提要。Trans-epithelial阻力(te)作为衡量上皮完整性被记录在五个时间点后空气升(1 = 0天,2 = 7天,3 = 14天,4 = 21天,5 = 28天)。封锁α1和α3整合蛋白抑制trans-epithelial阻力(双向方差分析与Holm-Sidak测试多个比较)。实验是由做三个重复测量重复井从两个独立的供体细胞培养(即。四个独立的井在每个计算)。数据是在对数尺度。*:p = 0.018;* *:p = 0.002;* * *:p = 0.006;* * * *:p < 0.001。
确定整合素的影响封锁HBEC分化,阻止α1整合蛋白抗体,α2,α3,α5,α6或β1添加到阿里文化在空气接触点(并在其后的介质变化)。上皮完整性增加在建立两极分化,分化上皮细胞层通过紧密连接的形成。检查这个过程,三通是衡量天0,7、14、21和空气接触后28。上皮完整性破坏了整合素抑制α1和整合素α3,两者都是在本地人工气道上皮细胞(补充图S2),表明适当的细胞分化的失败。三通价值观影响的阻塞α2整合蛋白抗体,α5α6或β1 (图1 e对multiciliated)和上皮分化,mucosecretory细胞没有明显改变了这些阻碍抗体,就是明证高速21天视频显微镜和免疫荧光染色的独立文化孵化与阻塞抗体(补充图S3)。在井处理整合素α1α3-blocking抗体,发现没有证据表明睫毛和细胞坚持宠物膜基本上没有与三通读数一致(图1 e)。
细胞外基质蛋白,在组织工程支架附件
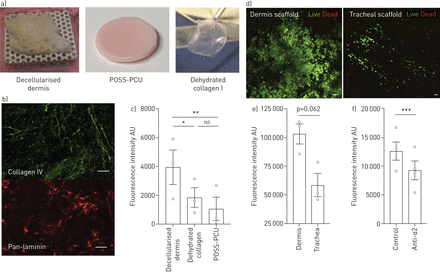
继续我们的实验对气道粘膜再生,我们调查了附件的上皮细胞三个相关支架不同ECM的复杂性(图2一个):一个复杂的生物支架保留多个ECM decellularisation后蛋白质包括第四胶原蛋白和层粘连蛋白(decellularised真皮)(图2 b);一个更简单的胶原蛋白我矩阵;和合成POSS-PCU脚手架并没有包含ECM蛋白质。上皮细胞依附于复杂decellularised脚手架是大于我和POSS-PCU支架的胶原蛋白(图2 c),这表明ECM的功能保留,尽管可能改变其结构由decellularisation引起的。我们进一步研究了decellularised真皮decellularised气管相比表现如何。生活/死后染色,丰富生活细胞表面被decellularised真皮支架,而只有稀疏覆盖被decellularised气管支架(图2 d)。相应地,在细胞alamarBlue可行性分析,荧光强度高的趋势在2 h后细胞播种到decellularised真皮支架相比decellularised气管支架(图2 e)。这表明更好的依从性和/或细胞生存decellularised真皮,是与两种decellularisation协议保持一致矩阵不同的区段(补充图S4)。类似于胶原IV(实验图1 b),上皮细胞对decellularised真皮后较低的封锁整合素α2 (图2 f)。
附件的人类支气管上皮细胞(HBECs)组织工程支架。一)数码照片的三个支架测试:decellularised真皮(生物),POSS-PCU(合成)和脱水胶原蛋白我(仿生)。b)包埋,自上而下的免疫荧光染色的基底膜蛋白胶原IV和pan-laminin decellularised真皮表明这些矩阵蛋白decellularisation后保存。c) HBECs (5×104)被播种到每个scaffold-containing。1小时后,井被清洗和胰蛋白酶应用于分离HBECs坚持支架。在一个单独的96孔板,CYQUANT GR(赫默尔亨普斯特德镇ThermoFisher科学、英国)是用来测量从种子控制支架连接细胞的荧光值减去。荧光也显著大于decellularised真皮组与胶原蛋白相比我(单向方差分析与Holm-Sidak测试多个比较)和POSS-PCU支架。实验重复了三次技术一式三份,包括使用两个独立的供体细胞培养。d)包埋,自上而下的共焦图像,图像显示了生活/死染色decellularised真皮和气管支架2 h post-epithelial细胞播种。e)上皮细胞生存能力(1.5×105)播种decellularised真皮或气管相比使用alamarBlue (ThermoFisher科学)细胞的可行性分析。荧光强度为2 h后依从性和价值观从消极控制支架被减去。荧光强度更大的真皮组织相比气管组,但发现没有达到统计学意义(双尾,配对t检验)。实验重复了三次技术一式三份,包括使用两个独立的供体细胞培养。f) HBECs (1.5×105)被播种到decellularised真皮支架有无预处理与整合素α2-blocking抗体。细胞被洗1 h和alamarBlue细胞与背景荧光减去进行可行性分析。阻断整合素α2导致大大减少附件的细胞decellularised真皮(配对t检验)。实验进行了四次技术一式三份,包括使用两个独立的供体细胞培养。所有酒吧= 50µm规模。*:p = 0.029;* *:p = 0.015;* * *:p = 0.006。
组织工程呼吸道粘膜的文化
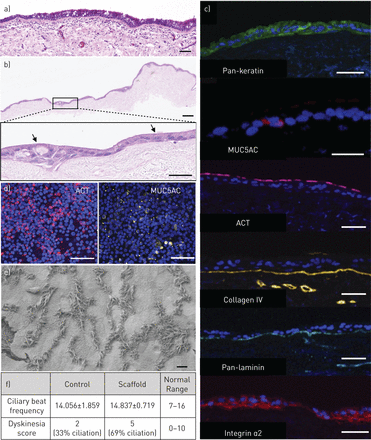
基于这些发现,我们调查的使用decellularised真皮基质作为呼吸道粘膜再生。HBECs和初级人类肺成纤维细胞(44,45)培养在decellularised真皮的阿里3周以基底细胞的诱导分化成熟上皮含有mucosecretory和纤毛细胞(38),就像在本地人工气道(图3一)。符合以前的观测使用这种支架材料(46),粘液观察表面的支架2周和3周后纤毛击败可以观察到自上而下,高速数字视频(补充材料)。Haemotoxylin和伊红染色的部分3周post-ALI演示一个完整的上皮细胞层在脚手架的程度,纤毛细胞和mucus-containing分泌细胞(图3 b)。然而,成纤维细胞的命运仍不确定,虽然成纤维细胞没有令人信服地添固有层(图3 b),非常罕见的细胞与成纤维细胞的形态学观察,免疫荧光(补充图S5)。pseudostratified层的高度是可变长度的支架,但免疫荧光染色表明角蛋白的表达,粘蛋白5 ac (MUC5AC)的mucosecretory细胞,乙酰化微管蛋白(ACT)在纤毛和基底膜ECM IV型胶原蛋白和层粘连蛋白(图3 c)。整合素的表达α2,认为早些时候的一个重要中介上皮附件(图1 b)也在分化上皮细胞(图3 c)。自上而下的免疫荧光证实存在的积极行动纤毛细胞和MUC5AC-positive mucosecretory细胞在支架的表面(图3 d)。电子显微镜的粘膜表进一步证实了上的纤毛细胞的顶端表面dermis-based支架(图3 e)。纤毛长度测量是7到10纤毛/细胞从六个不同的上皮细胞纤毛细胞从五个单独的条。从三个正常细胞的纤毛长度(长度±标准差(sd):µmµm 5.5±0.3, 5.6±0.3, 5.7±0.4µm)从三个细胞和纤毛略短(µmµm 5.4±0.3, 5.0±0.2, 5.0±0.3µm)暗示ciliogenesis可能在某些细胞持续的或不完整的。纤毛拍频的重要的是,分析表明,这是与使用标准的宠物阿里文化基质(图3 f)。最后,细胞的纤毛运动障碍得分decellularised真皮支架是在预期范围内纤毛阿里文化(图3 f)。
人类支气管上皮细胞(HBEC)分化decellularised真皮支架在气液界面(ALI)。)苏木精和伊红染色的部分成人气管黏膜。pseudostratified层与分泌粘液纤毛上皮杯状细胞基底膜上覆可以看到。固有层位于基底膜下面。b)苏木精和伊红染色部分呼吸道粘膜培养decellularised真皮。分化的上皮细胞层是沿着支架和细胞的分泌粘液的形态出现,杯状细胞和纤毛细胞。c)免疫荧光染色的部分生物工程呼吸道粘膜。4′,6-diamidino-2-phenylindole (DAPI)阳性细胞层彩色正面的上皮标记pan-keratin(绿色),相关联的mucosecretory细胞粘蛋白5 ac (MUC5AC)(红色),纤毛蛋白乙酰化微管蛋白(ACT)(红色),基底膜蛋白胶原IV(黄色),pan-laminin(蓝色)和整合素α2(红色)。d)自上而下的共焦显微镜上的分化标记decellularised dermis-based呼吸道粘膜显示(红色)和MUC5AC(黄色)积极性。e)的电子显微镜decellularised dermis-based呼吸道粘膜。 Cilia can be seen on the surface of the scaffold. f) High-speed digital video analysis of one donor HBEC culture differentiated on either standard positron emission tomography (PET) ALI substrates (controls; n=5 videos) or decellularised dermis scaffolds (n=10 videos). Analysis of ciliary beat frequency and dyskinesia demonstrated that on decellularised dermis cilia exhibited a comparable beat frequency to the control substrate. The dyskinesia score was slightly higher than in controls but remained within normal range. Scale bars=50 µm in (a)–(d) and 10 µm in (e).
移植的组织工程化呼吸道粘膜上小鸡绒毛膜尿囊的膜
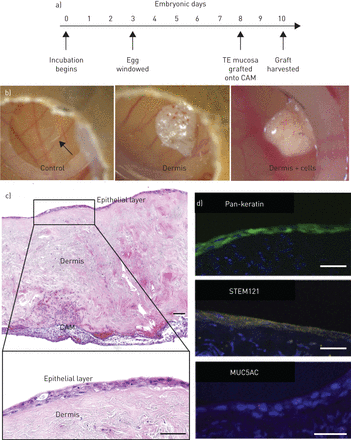
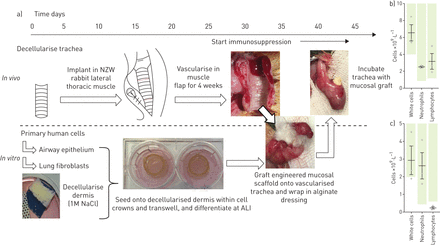
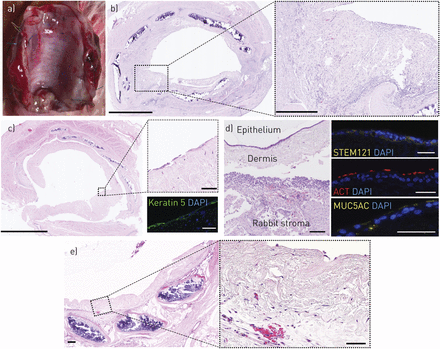
在确定decellularised真皮矩阵是支持呼吸道上皮细胞分化的能力在体外,我们下一个评估短期移植decellularised真皮支架播种HBECs和肺成纤维细胞在vascularised表面在一个小鸡凸轮试验(图4一)。凸轮检测免疫天真的优势,快速neo-vascularisation和接触道组织的空中接口。在48 h post-graft,自上而下的数码摄影显示小血管穿透脚手架,指示neo-vascularisation (图4 b),与此形成鲜明对比的是塑料-控制显示没有这样vascularisation (图4 b)。部分的非细胞decellularised真皮还演示了neo-vascularisation (图4 b),这表明这个过程不依赖于包括移植细胞。苏木精和伊红染色部分工程的呼吸道粘膜在这个时间点了保存的上皮细胞(图4 c)。此外,免疫荧光染色证实了他们的人类(STEM121) (图4 d)和上皮(pan-keratin) (图4 d)起源和显示稀有细胞表达mucosecretory细胞相关蛋白MUC5AC (图4 d)。然而,缺乏行动+纤毛表明上皮改造发生的在活的有机体内环境。
移植的decellularised dermis-based气道粘膜移植的小鸡绒毛膜尿囊的膜试验(CAM)。小鸡的时间轴凸轮化验。在胚胎蛋孵化,然后窗口的第三天,在脚手架嫁接在收获前胚胎第8天胚胎第十天。b)数码照片的凸轮化验后2天。c)呼吸道粘膜层的苏木精和伊红染色部分嫁接到凸轮检测胚胎第十天。演示了一个上皮细胞层表面的皮肤上覆凸轮。上皮细胞层的高放大显示保存的纤毛上皮但明显损失。d)免疫荧光染色的部分decellularised dermis-based呼吸道粘膜。4′,6-diamidino-2-phenylindole (DAPI)阳性细胞层彩色正面的上皮标记pan-keratin(绿色),人类细胞标记STEM121 mucosecretory细胞标记(黄色),很少粘蛋白5 ac (MUC5AC)(红色)。凸轮实验涉及epithelialised支架进行两次包括六个鸡蛋在每个实验小组在每个场合。 The decellularised dermis CAM experiment was performed once with six eggs in each experimental group. All scale bars=50 µm. TE: tissue-engineered.
移植的组织工程化呼吸道粘膜在活的有机体内
最后,我们调查了我们是否能够应用这些decellularised dermis-based呼吸道粘膜表pre-vascularised, decellularised气管的在活的有机体内兔子模型(47)(图5和补充表S2)。如果成功以这种方式实现了粘膜再生,构造可以旋转的血管蒂取代受损的部分气管和提供re-mucosalised和vascularised部分气道的移植。段decellularised兔气管5厘米的长度被植入肌肉皮瓣NZW兔子的脖子。我们允许为脚手架vascularisation 4周,并开始手术移植前免疫抑制。监控免疫抑制,静脉血液采样当天粘膜移植。在我们最初的实验中,免疫抑制由他克莫司和淋巴细胞数量均在正常范围内(图5 b)。7天之后,移植气管综合宏观上(图6),但没有显示保存上皮细胞层(两个的两个)(图6 b)。强烈的炎症反应是观察和随后的免疫抑制机制修改包括地塞米松。地塞米松和他克莫司造成淋巴球减少症(图5 c),导致没那么强烈的炎症反应在7天内植入皮肤层(图6 c)。能找到非常稀疏的区域keratin-positive上皮细胞在这些兔子(三分之二的)(图6 c)。来抵消机械剪切破坏的可能性道上皮细胞层,我们终于植入decellularised dermis-based气道黏膜保护层的床单柔软海藻酸敷料代替硅胶支架。在移植后24小时,上皮细胞层是保存在一个两只兔子(图6 d),证明适当的表达式与mucosecretory和纤毛分化相关的标记(图6 d)。然而,血管通道似乎并没有渗透到表面和粘膜层是脱离底层基质层加工、切片后,可能表明弱集成(图6 d)。5天之后,生物工程完整一些贪污的证据re-vascularisation (图6 e上皮细胞层),但已经失去了两个(两个)(图6 e)。血细胞和弥漫性炎性细胞浸润中观察到decellularised真皮在这个时间点(图6 e)。
时间表嫁接decellularised dermis-based气道粘膜移植到pre-vascularised段decellularised气管的兔子。)尸体兔气管decellularised使用一系列酶和洗涤剂洗涤。Decellularised气管pre-implanted在新西兰的侧胸肌白(NZW)促进vascularisation的兔子。此时,人类支气管上皮细胞(HBECs)和肺成纤维细胞被播种到decellularised真皮和培养在气液界面(ALI)。4周后,肌肉和气管综合开放和气管视觉评估vascularisation的迹象,感染和结构完整性的嫁接的呼吸道粘膜移植到支架表面。在一些兔子,藻酸盐敷料被粘膜支架保护上皮细胞然后支架腔内安全贪污。免疫抑制生物工程粘膜移植移植之前开始。b)免疫抑制效果与他克莫司在兔子(n = 3;0.3毫克·公斤−1皮下注射3天,然后隔天;血液采样7天),绿条指示正常范围。c)与他克莫司和地塞米松联合免疫抑制效果兔子模型(n = 3;0.3毫克·公斤−1他克莫司为3天,然后隔天皮下注射;三个剂量的2毫克公斤−1地塞米松肌内血液采样前24小时7天),绿条指示正常范围。
移植的decellularised dermis-based气道粘膜移植到pre-vascularised decellularised导管在兔子。一)数码照片的移植气管移植后7天生物工程气道粘膜。支架表面上的嫁接支架可以看到作为一种独特的层上覆软骨环。b)苏木精和伊红染色外植兔气管移植后7天,呼吸道粘膜组织工程(术语)硅胶支架使用他克莫司的免疫抑制。腔的表面接枝的术语可以看到强烈的炎性浸润和损失的上皮(放大部分)。规模酒吧= 1毫米(左)和250µm(右)。c)兔气管移植后7天,词在硅胶支架使用他克莫司和地塞米松免疫抑制。腔的表面接枝的术语可以看到用更少的炎性浸润和一些覆盖上皮不完整的大部分(放大的区域)。规模酒吧= 1毫米(左)和100µm(右上)。部分染色了角蛋白5(绿色)和4′,6-diamidino-2-phenylindole (DAPI)(蓝色)。 Keratin 5+ cells were found over small areas of the trachea (green). Scale bar=50 µm (lower right). d) Haematoxylin and eosin staining of an explanted rabbit trachea 24 h after grafting with an alginate dressing and dual immunosuppression. An epithelial layer was observed on the surface of one of the grafts but the grafts had detached from the underlying trachea, perhaps during processing. Immunofluorescence staining for the human cell marker STEM121 (yellow), mucin 5AC (MUC5AC) (yellow) and the ciliary protein acetylated tubulin (ACT) (red) is shown. Scale bars=50 µm. e) Haematoxylin and eosin staining of explanted trachea 5 days after grafting with an alginate dressing and dual immunosuppression. The epithelial layer had been lost from the decellularised dermis. The magnified image shows evidence of blood cells within the dermis layer and the presence of inflammatory cells. Scale bars=50 µm.
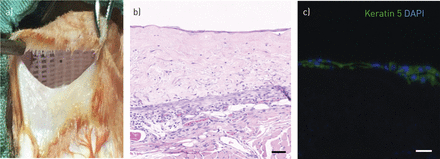
由于不完整的免疫抑制的可能性导致这些结果的兔子,我们进一步调查在活的有机体内集成在SCID小鼠点头。Decellularised dermis-based气道粘膜表被嫁接到背部肌肉和硅胶敷料覆盖保护上皮细胞层(图7)。7天之后,移植是检索和上皮细胞的组织学证实保留三(三)(图7 b),尽管覆盖支架不同的复制。保留上皮细胞基底细胞相关蛋白表达角蛋白5 (图7 c),这表明改造发生,也许是因为缺乏极性信号可用上皮细胞实验模型。
移植的decellularised dermis-based点头SCID小鼠气道粘膜移植。一个5厘米)横向切口是在三个点头SCID小鼠。皮下的口袋是发达国家和decellularised真皮支架,计划与人类支气管上皮细胞分化(HBECs)和肺成纤维细胞,被植入到vascularised肌肉和与硅树脂覆盖敷料(星号)。b)苏木精和伊红染色显示7天之后综合脚手架。连续的单层上皮分化被认为细胞可能是迷路了。c)免疫荧光染色证实,单层是角质5-expressing(绿色)。幻灯片和4′,复染色6-diamidino-2-phenylindole (DAPI)(蓝色)。所有酒吧= 50µm规模。
讨论
IV型胶原蛋白和层粘连锚多种上皮细胞,包括呼吸道、皮肤(21),小肠(48)和角膜(49),底层基质在活的有机体内(50]。在上皮改造支持他们的积极作用,胶原IV表达式是减少部分真皮厚度伤口上皮细胞迁移(51)和层粘连蛋白引导呼吸(52],表皮[53和角膜49)上皮细胞迁移。我们的研究表明,胶原IV是一个关键的中介的气道上皮细胞吸附和扩散的生物工程支架上,整合蛋白α2β1介质的这些过程,符合已知的整合素作用α2 /β1作为ECM蛋白质受体(54]。
我们相信胶原IV的存在(本地)和层粘连蛋白在生物工程气道结构和/或操作整合素α2介导粘附,可以改善上皮细胞附件效率并允许降低细胞播种密度达到支架覆盖(22]。的好处是多方面的整体细胞培养时间,人口的数量倍增细胞所经历的文化和生产成本可以降低。虽然这可以采取多种形式,我们确定了decellularised真皮是一种很有前途的气道支架材料再生IV型胶原蛋白和层粘连的基于其保留。胶原蛋白我支架相比,合成支架和decellularised气管支架,主要HBECs坚持decellularised真皮在体外。很可能整个气管所需的更广泛的decellularisation过程会破坏胶原蛋白IV-rich基底膜,从而限制上皮的依从性。进一步的研究可能的目标部署decellularisation方法保存关键矩阵腔的表面蛋白质或开发方法来取代这些通过decellularisation时丢失。
符合一个以前的报告46),我们生成的生物工程呼吸道粘膜纤毛跳动和粘液分泌的培养主要HBECs decellularised真皮阿里在体外。我们发现纤毛的长度是与那些在本土航空公司和纤毛拍频和人类鼻纤毛运动障碍得分与健康评估的高速视频显微镜直接(55)或在阿里文化后22]。这种支架可能操纵手术,可能意味着恢复黏膜纤毛的在呼吸道黏膜覆盖,已经丢失或损坏。为此,我们研究了在凸轮支架的性能分析,发现post-engraftment但纤毛上皮是保留2天不再存在。这些细胞的命运是未知的,但我们的数据表明,凸轮检测可能作为一个短期访问上皮改造试验在窗口前15天当免疫反应植入材料成为限制(56]。
在第二个在活的有机体内研究中,我们使用一个两阶段移植手术在兔子测试decellularised dermis-based生物工程呼吸道粘膜移植。他克莫司和地塞米松与中性粒细胞计数保存导致淋巴细胞减少,可能会限制免疫介导性改造支架的同时防止immunosuppression-associated机会性感染。我们看到与短期上皮移植保留但无法证明长期保留的分化上皮细胞层。延迟血管形成可能解释这个观察,作为新的血管通道的渗透率约1毫米到真皮支架可能需要好几天,在此期间上皮依赖于扩散的营养从底层移植床(57]。我们团队的经验生产三维组织工程皮肤和口腔黏膜,包括临床移植,表明移植放在差vascularised床常常无法生存(58]。的内皮细胞和血管生成生长因子已被证明neo-vascularisation缩短时间合成和生物支架和可能是一个潜在的战略,更迅速地恢复血液供应到上皮细胞层(59,60]。另外一个策略是区分一个薄支架,使呼吸道上皮细胞提供营养和氧气的上皮由扩散层与底层的毛细血管。扩散是有限的距离大约150µm从毛细管因此脚手架需要类似的厚度(61年- - - - - -63年]。是否采取了150µm刮胡子的真皮包括胶原和laminin-rich基底膜和底层固有层将缩短血管形成和增强上皮生存所花费的时间为未来的调查是一个明确的目标。
频繁的上皮细胞层的损失在活的有机体内实验突出了嫁接的技术挑战一个新的进入气道粘膜层。为了防止位移粘膜移植,支架部署,保留了嫁接移植床同时保持气道通畅。然而,气道的动态属性必然导致机械剪切的支架对道上皮细胞层可能会进一步导致上皮损失(64年]。未来的发展可能采用定制的支架和一个支持性的柔软外层包含营养供给,使移植并保持气道通畅,同时支持和保护上皮。另外,发展pro-angiogenic胶粘剂可能允许嫁接的呼吸道粘膜组织工程气管不需要支架。
结论
组织工程整体器官移植在航空公司,而且在膀胱和肠道,目前的限制无法再生黏膜衬里。我们的研究结果表明,ECM IV型胶原蛋白和层粘连蛋白对呼吸道上皮细胞粘附和扩张很重要在体外了解生物工程支架的发展,包含一个差异化的呼吸道粘膜层decellularised真皮支架。这些支架的交付是可行的在活的有机体内但是,上皮细胞在短期内保留,需要进一步的研究来提高长期在活的有机体内生存。我们的工作强调的重要性交付方法细胞在气道细胞疗法的研究和建议临床前研究的价值,直接比较分化细胞移植基底电池只方法(虽然前将恢复的成功迅速组织功能,未分化的基底干细胞移植可能是更健壮的)。
补充材料
补充材料
请注意:补充材料并不是由编辑部,编辑和上传已由作者提供。
补充视频。自顶向下、高速数字视频后三周的气液界面文化decellularised dermis-based生物工程粘膜。纤毛蠕动在支架表面可以观察到。erj - 01200 - 2019. -视频
可共享的PDF
确认
作者感谢霏欧纳瓦(英国伦敦国王学院)和罗宾McAnulty(英国伦敦大学学院)请提供3 t3-j2成纤维细胞和人肺成纤维细胞,用于这项工作。
脚注
可以从本文的补充材料www.qdcxjkg.com
利益冲突:N.J.I.汉密尔顿没有披露。
利益冲突:D.D.H.李没有披露。
利益冲突:K.H.C.高尔没有披露。
利益冲突:C.R.巴特勒没有披露。
利益冲突:E.F.莫恩没有披露。
利益冲突:b Jevans没有披露。
利益冲突:J.C.或者没有披露。
利益冲突:C.J.麦肯没有披露。
利益冲突:A.J.燃烧没有披露。
利益冲突:美国麦克尼尔没有披露。
利益冲突:硕士伯彻尔没有披露。
利益冲突:c .奥卡拉汉没有披露。
利益冲突:右眼Hynds没有披露。
利益冲突:克里琼斯没有披露。
支持声明:N.J.I.汉密尔顿是一个MRC临床训练的支持和NIHR临床讲师和皇家外科学院的泵启动格兰特和医学科学院起动器给予临床讲师。支持c .奥卡拉汉NIHR啊呀BRC。作者的观点是(s)和不一定NHS, NIHR或卫生部。克里琼斯是一个威康信托基金会高级研究员在临床科学(WT107963AIA)和右眼Hynds支持亨利爵士康博士后奖学金来自威康信托基金会(WT209199 / Z / 17)。右眼Hynds和克里琼斯获得资金作为英国成员再生医学平台(UKRMP2)工程细胞环境中心(MRC;先生/ R015635/1)和Longfonds呼吸肺再生财团。右眼Hynds和琼斯克里支持的罗伊琼斯城堡肺癌基础和克里也收到资金从UCLH Rosetrees信任和慈善基金会。资金信息,本文已沉积的Crossref资助者注册表。
- 收到了2018年5月21日。
- 接受2020年2月26日。
- 版权©2020人队
这个版本分布在Creative Commons归因执照的条款4.0。