抽象的
背景过敏性肺炎是一种免疫介导的疾病,其通过暴露于易感个体中的有机颗粒而引发。据报道,患有超敏肺炎患者的亚组,具有自身免疫疾病的临床表现或不具有自身免疫疾病的临床表现。然而,涉及该过程的机制和自身抗体对超敏肺炎临床过程的影响是未知的。我们评估了人白细胞抗原(HLA)II类等位基因和过敏肺炎患者的关联,患有和不含自身抗体的患者。
方法纳入170例过敏性肺炎患者。我们分析了诊断时存在的抗核抗体、类风湿因子、抗ssa /Ro、抗ssb /La和抗ccp。此外,在一组患者中,我们评估了抗scl -70、抗中性粒细胞胞浆抗体和抗dna。采用PCR序列特异性引物高分辨率进行HLA分型,包括HLA-DRB1和HLA-DQB1.位点。采用Epi-Info v7和SPSS v20进行统计学分析。
结果60个过敏肺炎患者显示血清自身抗体(HPABs+), 110例超敏性肺炎患者没有(habs-).等位基因的频率HLA-DRB1 * 03:01habs+组(10.8%与0.45%;或30.14,95%置信区间3.83-237.1;p = 1.65×10-4Bonferroni调整后)。同样,我们发现了单倍型DRB1 * 03:01-DQB1 * 02:01,这是8.1祖先单倍型的一部分,自身免疫性疾病的主要遗传决定因素,赋予培养自身抗体(或19.23,95%CI 2.37-155.9; P = 0.0088)的显着风险。除此之外HLA-DRB1 * 03:01等位基因与高敏感性肺炎患者的较高死亡率有关(调整为5.9,95%CI 1.05-33.05; P = 0.043)。
结论一种超敏肺炎患者的血栓炎患者呈循环自身抗体和较高的死亡率,与8.1祖型的一些等位基因相关。
抽象的
来自8.1祖先单倍型(#HLA-DRB1和DQB1位点)的等位基因与墨西哥混血患者队列中的#超敏性#肺炎中的#自身抗体产生相关https://bit.ly/3bprep.
介绍
过敏性肺炎是一种间质肺疾病(ILD),由基因易感个体对吸入多种有机颗粒的过度免疫反应引起[1- - - - - -5].急性过敏性肺炎的预后通常是有利的;然而,慢性纤维化超敏性肺炎往往进展,随后破坏肺结构[4,6].
免疫反应的异质性和疾病的临床差异表明,多种分子途径参与了疾病的发展和进展。
以前的研究已经描述了一些等位基因在过敏肺炎易感性中的主要组织相容性复合物中的参与。特别是,鸽子育种者疾病和夏季超敏肺炎患者中鉴定了人白细胞抗原(HLA)II类等位基因[7- - - - - -9],暗示位于HLA地区内的遗传因素有助于过敏肺炎发育。二等 -DRB1.和 -DQB1.涉及8.1祖先单倍型的等位基因似乎确定了特定的自身抗体的发展,有机特异性和非器官特异性[10.].
2016年,一组慢性过敏性肺炎患者接受了adegunsoye.等.[11.]确定自身免疫特征的患病率。他们发现,少数过敏肺炎患者(15%)显示出自身免疫特征,并且自身免疫的存在是增加死亡率的独立预测因素。
在患有超敏肺炎的患者评估过程中,经常检测到循环自身抗体的存在,而不满足结缔组织疾病的标准。迄今为止,与自身抗体阴性群相比,尚不清楚该超敏感性肺炎患者是否具有与HLA相关的不同遗传易感性。
在这种情况下,该研究旨在研究II类HLA等位基因的等位基因频率,以揭示具有和不含自身抗体的过敏肺炎之间的推定差异(HPABs+和HPAB-以及某些多态性是否与死亡率有关。
材料与方法
研究人群
回顾性研究的成人患者(年龄≥18年)称ILD诊所呼吸疾病研究所(墨西哥城,墨西哥),并有足够的DNA样本质量从170年确诊的患者过敏性肺炎期间2003 - 2018包括(图1).自2000年起,从ILD患者身上获取用于基因研究的DNA样本,并有明确的解释,并及时收集签署的知情同意书。
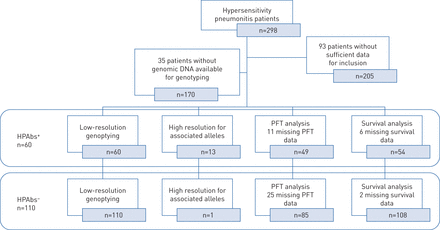
包含过敏肺炎,没有自身抗体(HPABs+和HPAB-)分别显示出不同分析的排除率。PFT:肺功能测试。
所有患者均有至少三代在墨西哥(父母和祖父母)中出生,被认为是墨西哥Mestizo。我们之前已经表明,这一标准是由祖先 - 信息标记评估的墨西哥血统的良好代理[12.].
根据先前描述的标准诊断过敏肺炎[13.,14.], 如下。1)症状和肺功能测试改变与ILD相容;2)高分辨率计算断层扫描(HRCT)显示出明确定义的结节,地面玻璃衰减和空气捕获到期(80%的HPABs+和54%的HPABs-还显示出与纤维化相容的改变,例如不规则的线性不透射率和牵引支气管扩张和偶尔囊性病变);3)支气管肺泡灌洗淋巴细胞增长> 30%;4)活组织检查(在30%的HPAB中进行+和28%的HPABs-)与过敏性肺炎兼容。一个多学科小组证实了诊断结果。
临床数据是从医疗记录获得的。收集的变量包括人口统计数据,合并症,烟草吸烟史,环境抗原暴露评估,临床实验室研究,肺功能试验(包括强迫致命能力,一氧化碳的肺部扩散容量(DLCO)和6分钟步行试验)以及1年随访时所有原因的死亡率。
我们考虑了血清学阳性的过敏性肺炎(habs)+)作为以下抗体中的至少一种的阳性:抗核抗体(ANAs)具有任何类型的结缔组织疾病的特异性图案(细胞质,核仁,CENTROMERE);ANA具有均匀图案,精细或粗糙的斑点;类风湿因子三个或更多次上正常限制(20 iu·ml−1);抗循环柑橘肽≥20ru·ml−1和/或Sjögren综合征自身免疫谱中至少一种抗体(anti-Ro (SSA), anti-La (SSB))。这些自身抗体在所有患者中进行了分析。此外,88%的habs检测了与系统性硬化(抗scl -70)、血管炎(抗中性粒细胞胞浆抗体(ANCA))和抗dna相关的自身抗体+55%的habs-.没有患者根据美国风湿病学院/欧洲联盟反对风湿病的结核组织疾病的分类标准[15.- - - - - -17.].
根据血清中自身抗体(habs)的存在情况对患者进行分类+与HPABs.-)(表格1).
道德声明
本研究由Instituto Nacional De Envermedadess Respiratorias IsmaelCosíovillegas(Iner;墨西哥城,墨西哥)的科学和伦理机构委员会批准(认证码:B20-15和C60-17)。
基因组DNA孤立
通过静脉穿刺获得外周血(7mL),并用EDTA收集在管中,作为抗凝血剂,用于随后的DNA提取。在诊断时获得样品,并且患者没有接受皮质类固醇或免疫抑制药物。
血液样本在INER的HLA实验室处理,使用商业试剂盒(BDtract基因组DNA分离试剂盒;马克西姆生物技术公司,旧金山,加州,美国)。使用NanoDrop 2000设备(Thermo Scientific, Waltham, MA, USA)用紫外分光光度法定量DNA。通过测量280nm和260nm处的吸光度比来确定有机物和蛋白质的污染。当这一比率达到~ 1.8时,被认为是高质量的样品。
HLA II类分子打字
DRB LOCI的分子打字DQB1.使用Micro SSP™HLA DNA键入托盘(一个Lambda,Canoga Park,Ca,USA)使用PCR序列特异性引物(PCR-SSP)技术进行了轨迹。与其他基于PCR的方法不同,SSP方法采用在PCR过程中不同等位基因之间的判别。扩增的DNA片段通过琼脂糖凝胶电泳分离,并通过染色和暴露于紫外光而可视化。PCR-SSP结果的解释基于特异性扩增的DNA片段的存在或不存在。由于PCR反应过程中的扩增可能受到诸如移液误差,DNA质量差和抑制剂存在的各种因素不利影响,因此在每个PCR反应中包括内部控制引物对。控制引物对放大人β-珠蛋白基因的保守区域,其存在于所有人DNA样品中,并用于验证PCR反应的完整性。
最初,HLA-DRB键入通过低分辨率模态进行,包括DRB1.,DRB3.,DRB4.和DRB5.24个独立反应的等位基因。DRB Loci Allele Group CoversDRB1 * 01.,* 03,* 04,* 07,* 08,* 11,* 12,* 13,* 14,* 15和* 16以及DRB3 * 02.,DRB3 * 03.,DRB4 * 01.和DRB5 * 01.特异性(DR51,DR52和DR53血清学等同物)。高分辨率HLA-DRB1 * 03用另一组16对引物来建立等位基因鉴别。为HLA-DQB1.用键入,使用八双,而HLA-DQB1.用于实现的高分辨率套件DQB1.扩增包括DQ6,DQ3,DQ4,DQ5和DQ2的55个等位基因。
所有扩增使用Kapa Taq HotStart PCR试剂盒(Kapa Biosystems,开普敦,南非)。PCR-SSP产品在3%琼脂糖凝胶中电泳,使用MIDORI Green Advanced DNA染色(Nippon Genetics Europe, Dueren, Germany)进行染色。利用HLA融合软件对分型结果进行解释与4.3(一个兰德)。
统计分析
统计程序SPSS(版本21; SPSS,Chicago,IL,USA)用于描述研究人群,并确定每个变量的中位数,最小值和最大值,并使用Mann-Whitney U-Test进行比较。将连续变量报告为平均值±SD.并使用T检验进行分析。分类变量被报告为计数和百分比,并使用Fisher精确测试对比。
通过直接计数确定HLA的等位基因和单倍型频率。使用传统的Fisher的确切测试,观察到的和预期的HLA二级等位基因(每个轨迹)用于硬性 - Weinberg平衡。通过Fisher的确切双尾试验评估关联,其统计显着性值为P <0.05。考虑到在整个人口中发现的22个单倍型中鉴定的20个等位基因进行了Bonferroni校正。使用2×2应急表计算的差距和95%的置信区间计算了通过使用EPI INFO V4.0.1的等位基因和单倍型进行了比较了两组和单倍型[18.].最后,单倍型被构造使用arlequin v3.1软件[19.]使用最大似然方法,具有迭代期望的最大化算法。
为了评估死亡率和风险等位基因之间关联的强度,我们首先使用单变量回归分析估计原始赔率比(COR);使用WALD测试估计p值,然后我们估计了调整后的赔率比(AOR),具有多变量的逻辑回归分析,其仅包括P <0.05的变量,由于小的样本大小。执行任何撤销程序以处理缺失数据。
结果
在298名患者中登录的过敏肺炎群组中,93次没有足够的纳入数据进行研究,包括缺乏自身抗体结果(2006年之前,ILD患者不经常进行自身抗衡性),或者因为我们的多学科团队没有确认过敏肺炎的诊断。由于没有足够的基因组DNA来进行基因分型,另外35被排除在外。包含170例过敏肺炎患者,60例循环自身抗体(HPABs+没有(HPABs-)(图1).大多数HPAB+患者(89%)对抗核抗体(> 1:320)呈阳性,偶尔将它们对另一种自身抗体的阳性阳性(参见方法部分)。12%(7名患者)对ANA阴性阴性,但表现出增加的其他自身抗体水平(例如类风湿性因子n = 2,ANCA n = 2,抗RO n = 2,抗LA n = 1)。HPABs.-患者对所有检查的自身抗体负阴性。
人口特征
habs之间没有差异+和HPAB-关于人口统计特征,包括年龄,性和吸烟(表格1).同样,两组间肺功能试验的比较(60例habs中49例进行)+患者和110名HPABs患者的85名患者显示出没有差异(表格1).但是,HPABS.+患者比HPAB更容易对HRCT进行慢性/纤维化变化-.相比之下,HPABs中无法识别抗原的患者的百分比显着高-团体 (表格1).
在1年的后续行动期间,六个HPABs+患者和两个HPABs-患者丢失了。12%的整个队列死亡,HPABs的比例显着更高+组(20%与8%,p = 0.02)。
HLA II类等位基因和单倍型
基于病例和对照的原产地,在人口分层中没有发现统计学上显着的差异。来自两组的每个轨迹的HLA等位基因对满足Hardy-Weinberg均衡(P> 0.05),占生产常见基因型的常见等位基因,即。杂合的(例如DQB1 * 02:01,DQB1 * 05:01)和纯合(例如DQB1 * 03:02)对。
分布的DRB1.和DQB1.等位基因列于表2和3..10.HLA-DRB1在HPABs中鉴定了等位基因+小组,其中七个,等位基因频率> 5%,最常见的是DRB1 * 08.(等位基因频率20.00)和DRB1 * 04.(等位基因频率为17.50)。标记的频率增加HLA-DRB1 * 03在habs+组(10.8%与0.45%;或30.14,95%置信区间3.83-237.1;p = 1.65×10-4经过Bonferroni对所有等位基因的校正后(两个位点共鉴定出20个等位基因)。所有DRB1 * 03.受试者是DRB1 * 03:01在高分辨率亚型分析中。等位基因DRB3.和DRB4.在habs中未发现基因+患者也没有HPAB-的病人,DRB5.在没有统计差异的患者中鉴定了等位基因。
七个等位基因被认可HLA-DQB1.洛杉矶,其中,DQB1 * 03:01,DQB1 * 03:02和DQB1 * 04:02两组中最常见的。等位基因的较高频率DQB1 * 02:01(等位基因频率15.00)在HPAB中检测到+与HPABS相比-(15.0%与6.364%, p = 0.007;或2.93,95%置信区间1.33-6.45);然而,在Bonferroni校正后,这种相关性消失了(p=0.14)。频率HLA-DQB1 * 06:01HPABs的等位基因也比高度较高+组(12.5%与4.5%, p = 0.006;OR 3.33, 95% CI 1.39-7.98),但Bonferroni校正显示,这种差异也不显著(p=0.12)。
另外,我们比较了单倍型频率DRB1.-DQB1.位点。如图所示表4.,在整个超敏肺炎组中鉴定了22个单倍型;有趣的是,在HPABS中+组(n = 60)有19个单倍型,而在HPAB中-组(n=110)仅确定了14个单倍型(22个中19个)与14分中为22,p = 0.08)。
我们观察到单倍型的显着较高频率DRB1 * 03:01-DQB1 * 02:01在HPABs的患者中+(7.5%与0.45%;或19.23,95%置信区间2.37-155.9;经Bonferroni校正后p=0.0088(应用在整个群体中鉴定的22个单倍型))。
物流回归
为了评估死亡率与风险等位基因之间关联的强度,我们估计了使用单变量逻辑回归分析的死亡率。风险等位基因HLA-DRB1 * 03:01与死亡率有关(Cor 4.5,95%CI 1.19-16.9; P = 0.026)。为了调整混淆,我们执行了三种多变量逻辑回归模型(表5.).在模型1中,通过单变量分析,我们纳入了四个与死亡率显著相关的变量:HLA-DRB1 * 03:01,DLCOc反应蛋白(CRP)和habs+.我们发现了DLCO和CRP保持重大。在模型2中我们排除了HPABS时+,等位基因HLA-DRB1 * 03:01与死亡率强烈有关(AOR 5.9,95%CI 1.05-33.0; P = 0.043)。相比之下,当我们排除等位基因时HLA-DRB1 * 03:01,HPAB+失去意义,支持与风险等位基因的强烈联系。重要的,HLA-DRB1 * 03:01和HPAB+显著相关(OR 9.52, 95% CI 1.85-92),表明两个变量之间存在共线性关系。
通过103名患者的数据获得多变量逻辑回归模型,模型2的适合度为P = 0.69,接收器下的面积工作特性曲线= 0.82(表5.).
讨论
关于过敏肺炎遗传易感性的研究有限,但HLA II类基因已被确定为有助于疾病发展的关键因素[8,9,20.].
在过去的几年里,越来越多的证据表明,患有超敏肺炎患者的亚组产生血清或甚至自身免疫的临床特征,尽管潜在的机制仍然未知。此外,除了提高死亡率外,该“表型”尚未表征。
同样,近年来,已经描述了患者的患者的子集,他具有特发性的间质肺炎(IIP)和自身免疫功能(IPAF),其不符合结缔组织疾病(CTD)的标准,但至少有一个标志或症状暗示CTD和至少一种血清学测试的自身免疫过程的反射[21.].这些患者的特征性更好,一些研究还表明,遇到IPAF标准的患者的存活率明显差,而没有自身免疫功能的患者[22.],尽管已报道结果有很大的差异[23.].与过敏性肺炎一样,触发自身免疫过程的机制和遗传易感性尚不清楚。
在这项研究中,我们发现大约三分之一的过敏肺炎患者可能存在自身抗体。这个比例高于a报道degunsoye.et al。[11.[我们知识唯一一个唯一一项展示这项协会的研究,虽然原因目前未知。
在这项研究中,我们旨在鉴定与HLA II类系统相关的推定遗传因素,这可能会增加高敏感性肺炎患者发育自身免疫特征的风险。我们的结果首次揭示了一些遗传等位基因赋予这些患者在这些患者中发育自身抗体的风险。因此,频率的显着增加HLA-DRB1 * 03:01等位基因以及单倍型DRB1 * 03:01-DQB1 * 02:01在没有他们的患者的患者中观察到患有自身抗体患者的患者。
有趣的是,已经在经典和罕见的自身免疫障碍中形成了自身抗体的描述。例如,等位基因HLA-DRB1 * 03:01和DQB1 * 06:01与Systemic Lupus红斑狼疮的自身抗体的发展有关[24.,25.].同样,发现抗-J-1或抗PM-SCL抗体的存在与强烈相关HLA-DRB1 * 03:01和DQA1 * 05:01成人和少年肌炎患者队列的等位基因[26.- - - - - -28.].这DQB1 * 02:01等位基因与遗传联系在一起DQA1 * 05:01在乳糜泻1型糖尿病和其他自身免疫性疾病中有典型的描述[29.].
单倍型分析显示频率显着增加HLA-DRB1 * 03:01-DQB1 * 02:01,常见于欧洲人口[30.]和若干自身免疫疾病相关,例如具有自身抗体生产的原发性Sjögren综合征[31.].这种单倍型含有两种主要等位基因,部分为8.1祖先单倍型。祖先的单倍型是一个非常长的(超过四个兆级)保守的等位基因组合:HLA-A1,CW7.,B8,TNFAB * A2B3,tnfn * s,C2 * C.,bf * s,C4a * Q0.,C4B * 1,DRB1 * 03:01,DRB3 * 01:01,DQA1 * 05:01和DQB1 * 02:01.它被认为是导致多种自身免疫性疾病风险的最关键的免疫决定因素[10.].此外,这种单倍型的健康载体均显示出高值的自身抗体,血液活化的T细胞和血液免疫复合物。因此,8.1祖先的单倍型增强免疫功能障碍和自身免疫疾病,我们的结果表明它也可能有助于在过敏肺炎的自身免疫发育。
过敏性肺炎是一种复杂的疾病,其中环境和遗传因素的相互作用影响了疾病的发展和表型,例如纤维化或非纤维化疾病[4].例如,已经证明的小等位基因频率MUC5B慢性超敏肺炎患者患者患者比健康对照患者均高,更重要的是,射线照相纤维化的程度与这种常见变种有关[32.].
我们的研究结果表明,HLA系统的特定等位基因和单倍型可能导致自身免疫特征的发展,改变过敏肺炎的课程和结果。此外,携带风险等位基因,HLA-DRB1 * 03:01与生存降低有关。有趣的是,与8.1祖先单体型相关的免疫功能障碍似乎是老年女性早期发病率和死亡率的一个因素[33.];在过敏的肺炎队队列中,女性显着频繁。
此外,我们发现habs组的死亡率+高于无自身抗体组,这与之前的一项研究一致,该研究发现自身免疫的存在与不良预后相关[11.].然而,经过等位基因的调整HLA-DRB1 * 03:01,Auto intibodies的存在失去了意义。令人惊讶的是,死亡率没有显示慢性纤维化和非凝血过敏肺炎患者之间的差异,可能是因为随访时间和小样本大小。
我们的研究有一些局限性,包括相对较小的样品大小。此外,我们排除了患有超敏肺炎的患者,并确认了结缔组织疾病或炎症疾病的历史。
需要进一步的研究来验证这些发现,并确定过敏性肺炎患者自身免疫过程的分子机制。
结论
在过敏性肺炎患者中,等位基因HLA-DRB1 * 03:01和单倍型DRB1 * 03:01-DQB1 * 02:01,8.1祖先单倍型的一部分是自身免疫疾病的主要遗传决定因素,与自身抗体的存在有关。HLA-DRB1 * 03:01还增加了过敏肺炎患者死亡率的风险。
可共享的PDF
脚注
利益冲突:I. Buendía-Roldán没有什么可披露的。
利益冲突:L. Santiago-Ruiz没有什么可披露的。
利益冲突:G.Pérez-rubio没有什么可披露的。
利益冲突:M. Mejía没有什么可披露的。
利益冲突:J. Rojas-Serrano无需披露。
利益冲突:E. Ambrocio-Ortiz没有什么可透露的。
利益冲突:G.Benítez-Valdez无需披露。
利益冲突:M. Selman没有披露。
利益冲突:R. Falfán-Valencia没有什么可披露的。
- 已收到2019年7月12日。
- 接受2020年4月13日。
- 版权所有©ers 2020
此版本在Creative Commons归因非商业许可证4.0的条款下分发。















