抽象的
Covid-19患者的一小部分对呼吸衰竭的严重疾病表现和机械通气的必要性。鉴定风险的患者对于优化的护理和早期治疗干预措施至关重要。我们调查了相对于疾病严重程度的严重急性呼吸综合征冠状病毒2(SARS-COV-2)的动态。
我们分析了92例COVID-19患者的鼻咽部和气管脱落情况。入院时采集标准化的鼻咽拭子或痰标本。如果患者采用机械通气,则额外获得气管内抽吸样本。实时荧光定量PCR检测SARS-CoV-2 RNA,定量检测病毒脱落。
45%(92例中41例)的COVID-19患者病程严重,需要机械通气(重症组)。在第1周,从鼻咽拭子确定的初始病毒脱落在非重症和重症病例之间没有显著差异。在第2周,可以观察到严重疾病患者的病毒脱落仍然升高。c反应蛋白、白细胞介素-6和降钙素原的时间进程显示,在重症患者病毒脱落负荷延迟下降后,炎症反应更为持久。显著比例(47.8%)的患者表现出延长的病毒脱落(>17天),这与严重的病程(73.2%)相关。
我们举报的是,在入院时严重和非耐性Covid-19案件之间的病毒脱落在患者之间没有显着差异。在第二周的住院中升高的SARS-COV-2脱落,第二和第三周之间的全身炎症反应,延长的病毒脱落与更严重的疾病课程有关。
抽象的
这项工作发现,在附加期间的第二周升高的SARS-COV-2脱落,在第二和第三周之间达到了全身炎症反应,延长的病毒脱落与更严重的Covid-19疾病课程有关https://bit.ly/3p544zr
介绍
在Covid-19中,经过初始症状稳定性后经常观察到快速肺化。先前报道了严重急性呼吸综合征冠状病毒2(SARS-COV-2)感染或Covid-19的临床特征[1-3.].有几份报告描述了病毒脱落会持续很长时间[4.那5.].完全评估病毒脱落可以对潜在的免疫机制有价值的洞察力[6.].通过PCR检测病毒RNA并不一定与传染性病毒有关,因为尽管存在SARS-CoV-2 RNA,但在较晚的时间点,传染性已被证明显著降低[7.-10.].
肺炎代表了Covid-19感染最重要的临床表现,是严重病患者预后的主要决定因素。在个体课程和疾病的严重程度中存在显着的异质性。因此,病毒的肺部间隙特别感兴趣[10.].某些患者反应过度或免疫依赖性病毒清除减少可加重肺部症状[11.]病毒倾向性、病毒脱落负荷、病毒脱落持续时间和病毒组织分布的个体差异可能在其中起作用。关于病毒脱落的组织分布和时间动力学的数据很少,需要进一步的临床特征描述。最近的研究揭示了与新冠病毒-19相关的纵向炎症反应[11.];将临床活性炎症参数与病毒脱落连接临床活性炎症参数仍然很高。
在我们的医院中,患有Covid-19的患者对来自呼吸道的材料中SARS-COV-2 RNA的证据,包括重复的气管插气(ETA),痰和鼻咽拭子(NPS)样品。
在这里,我们报告了描述由于Covid-19在2020年2月29日至5月29日之间的Covid-19,涉及到我们医院的92名患者的群组中病毒脱落动态的临床和病毒学结果。
方法
学习规划
本研究是一项回顾性队列研究,所有实验室证实的Covid-19患者,与2020年2月29日至5月17日,慕尼黑慕尼黑大学(慕尼黑慕尼黑)至17日,达成了连续。
耐心
所有疑似COVID-19的患者都被转诊或进入德国南部主要学术中心大学医院的急诊病房。这些患者经SARS-CoV-2 PCR阳性回顾性确诊为COVID-19病例。仅纳入成人(年龄≥18岁)。我们使用了一种简单的疾病严重程度分类:重症病例定义为需要机械通气的患者,如以前所使用的[12.].在我们的患者中,中度疾病被定义为没有机械通气和需要充氧,而两者都没有则定义为轻度病程。非严重疾病包括轻至中度疾病。
样本
NPS,Sputum或ETA(在入学患者中,在入学患者中,常规地获得当地指南进行的入场和程序。在Covid-19的临床怀疑上采样NPS样品。此外,当计算的断层摄影扫描显示Covid-19 - 典型的渗透和NPS样品为阴性或临床监测目的时,获得痰样品。在入院时,获得最多两个NPS样品(具有至少12-H间隙)和一个痰液样品(如果需要)。
对临床监测进行反复收集样品(NPS,Sputum或ETA)。当Covid-19症状回复并且两个连续的NPS样本(至少为期1天间隙)显示出阴性结果时,停止测试。
病毒载量分析
病毒载荷表示为SARS-COV-2基因组当量·mL-1痰液、ETA或拭子样本的运输介质。我院标准拭子含1ml Amies液体转运培养基(eSwab;COPAN Diagnostics, Murrieta, CA, USA)。
以下PCR分析用于马克斯·冯·佩滕科弗研究所(德国慕尼黑)经认可的常规诊断实验室的定量分析:核衣壳(N1)美国疾病控制和预防中心的反应(CDC)议定书[13.),信封(E)扩大Charité议定书[14.那15),核衣壳(N) Seegene Allplex 2019-nCoV试剂盒和Roche Cobas SARS-CoV-2试剂盒的扩增核衣壳(N) 反应。
标准曲线产生在多个稀释复制使用一个质粒含有核衣壳基因(2019-nCoV-N-PositiveControl;IDT,Coralville,IA,USA)或具有基于数字滴状PCR结果的拷贝数的临床样本,如前所述[16].为每个PCR测定导出不同的配方以转换阈值循环(CT./交叉点(CP.)的值来复制数字估计:80×1.95^(40.29−.CP.)为CDC (N1), 80×1.99^(39.34−CP.)对于Charité(e),80×2.00 ^(38.63-CT.)对于Seegene Allplex 2019 nCoV分析(N)和80×1.99^(39.34−CT.)适用于罗氏科巴斯SARS-CoV-2(N)。这些计算未考虑单独PCR运行、不同PCR化学品或不同核酸提取方法之间的差异。然而,由于这些变量适用于所有患者组,因此它们不会影响本研究结果的解释。
“病毒脱落”是指通过PCR在呼吸道物质中检测SARS-CoV-2 RNA。然而,我们量化的这个参数也可能包括亚病毒粒子或来自死亡细胞的RNA,并不等同于完全的病毒粒子排泄,甚至传染性。
血清炎症参数
在Cobas 8000平台(瑞士巴塞尔罗氏诊断公司)上测量降钙素原(PCT),在Cobas e801平台(罗氏诊断公司)上测量白细胞介素(IL)-6。在Cobas c702平台上通过Tina quant C-反应蛋白分析(罗氏诊断公司)测量C-反应蛋白(CRP)水平。
统计分析
根据需要检查参数连续变量,例如病毒载量的差异。临床特征的分布是由Mann-Whitney U-Test或Chi平方试验检查的临床特征。用具有四节的平滑花键进行曲线配件。进行Cox回归分析以研究病毒脱落持续时间与性别,年龄,动脉高血压,糖尿病,冠状动脉疾病和Charlson合并症指数等临床特征的关联[17].无重复阴性结果的患者在阳性的最后一天进行审查。p<0.05为差异有统计学意义。使用SPSS版本25 (IBM, Armonk, NY, USA)或Prism版本8.0.1 (GraphPad, San Diego, CA, USA)进行统计分析。
伦理声明
Ludwig Maximilian University of Munich的当地伦理委员会批准了这项研究(project 20-454)。
结果
入院后,所有患者都有NPS采样,ETA采样或两者。在所有92例中,通过实时PCR在呼吸样品中确认SARS-COV-2感染。患者特性显示在表1.回顾性地确定患者被证实的Covid-19案件于2020年2月29日入院。在入学上,大多数病例(92分中的85分)是自发呼吸的并且具有非疾病。7名患者被转移到我们院,已经接受机械通风。在入院的85名非耐心患者中,34例患者在住院期间发育了严重的疾病课程。其余51例(非耐温)患者中,20名患者开发了中度疾病课程。中位数(中位数(IQR)年龄为62(51-75)年。大量比例患者有几种具有平均(IQR)Charlson合并症指数分数2.5(1-4)的合并症;动脉高血压(49%)和糖尿病(17%)是最常见的合并症。额外的患者特性显示在补充表S1.检查共473个呼吸样品(245个NPS,228η和9个痰样品)。平均而言,每位患者收集5.3个样品,两组之间的测试频率相似(补充表S2).
ETA和NPS样品中SARS-COV-2病毒脱落的差异
对机械通气患者样本采集的评估显示,在同一时间点(n=13名患者)采集的ETA和NPS样本对彼此显著相关(r=0.499,p=0.041),但配对比率t检验显示ETA中的病毒脱落显著较高相对nps(p = 0.0041)(图1A).因此,在随后的测试中分别分别分析NPS和ETA。NPS的单独取样(r = 0.8231,p <0.0001;比率配对t检验:p = 0.2575)和eta(r = 0.7948,p <0.0001;比率配对t-test:p = 0.1436)显示每个采样的高再现性方法 (图1B.和c)。
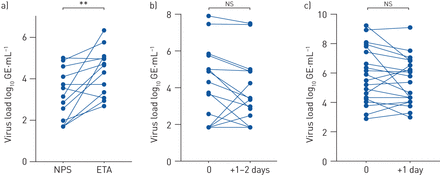
a)同一时间点采集的鼻咽拭子(NPS)和气管内抽吸(ETA)配对样本(n=13), b)同一患者连续的NPS样本(n=16), c)同一患者连续的ETA样本(n=20)。通用电气:基因组等价物。* *: p < 0.01;ns.:不重要的。
SARS-CoV-2病毒脱落和疾病严重程度
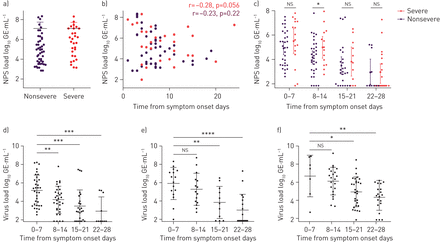
根据疾病严重程度的病毒脱落,如图所示图2.严重或非疾病患者的初始病毒脱落在患者中没有什么不同(图2a).我们排除了时间对病毒脱落负荷进行第一次测试的影响(图2b).对于后续的测试,我们计算每周患者的平均病毒脱落量,以减少样本时间和样本偏差的影响。根据疾病严重程度,直接比较重症患者在第2周时的病毒脱落量显著升高(图2c和补充表S2).
严重急性呼吸综合征冠状病毒2 (SARS-CoV-2)的病毒脱落动态按疾病严重程度、样本类型和症状出现时间划分。NPS:鼻咽拭子;通用电气:基因组等价物。a)根据疾病严重程度,在NPS样本中进行初始SARS-CoV-2病毒脱落负荷比较。b)初始病毒载量根据症状出现时间,Pearson相关。c)根据症状出现时间比较非重症和重症患者NPS标本中病毒脱落情况。d, e)有d)非重症(n=51)和e)重症(n=41)患者的NPS样本中的病毒脱落动态。f)仅在严重疾病患者的气管内吸入物中测量病毒脱落动力学(n=41)。非重度包括轻度和中度疗程。误差条表示平均值±sd.p值通过t检验计算。*: p < 0.05;* *: p < 0.01;* * *: p < 0.001;* * * *: p < 0.0001;ns.:不重要的。补充表S2显示相应的统计数据。
在非重症患者的NPS样本中,SARS-CoV-2病毒脱落在第2周(p=0.0098)、第3周(p=0.0003)和第4周(p=0.0004)较第1周(图2d).在重症患者中,病毒脱落在第2周无差异(p=0.3089),但在第3周(p=0.0056)和第4周(p<0.0001)下降(图2e).
在严重疾病患者的ETA样本中,与第1周相比,病毒脱落量在第3周(p=0.0358)和第4周(p=0.0022)显著下降(图2f).
SARS-CoV-2病毒脱落和全身炎症
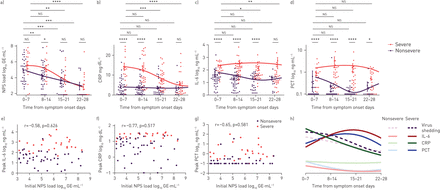
为了进一步表征对病毒脱落和疾病严重程度的纵向炎症反应,我们表征了CRP,IL-6和PCT的时间过程(图3A- d)。我们计算了CRP、IL-6和PCT的每周平均值,以防止抽样偏倚。接受托西珠单抗的患者被排除在CRP和IL-6分析之外(n=4)。统计分析显示,重度组CRP、IL-6、PCT在早期时间点(1-2周)显著升高。在随后的时间点(3-4周),CRP和IL-6下降,但PCT没有。最初的病毒脱落量与IL-6峰值、CRP峰值或PCT峰值无相关性(图3E.- g)。曲线拟合显示IL-6和PCT在2 - 3周达到峰值,而CRP在1 - 2周达到峰值,在2 - 3周下降(图3H.).患者严重疾病的患者显着增加了直接入院(PCT测量<48小时后的PCT水平)(补充图S2a;有关根据合并感染或继发感染进行的进一步分层,请参见补充表S4和补充图开通).
非耐旱性患者炎症反应的时间过程。NPS:鼻咽拭子;GE:基因组等同物;CRP:C-反应蛋白;IL:白细胞介素;PCT:procalcitonin。a)在NPS样品中的病毒脱落,B)CRP,C)IL-6和D)PCT随时间绘制并通过疾病严重程度进行分组。平均值±sd是表示。e - g)将初始病毒载量(仅在入院时自主呼吸患者的NPS样本)与e) IL-6、f) CRP和g) PCT的峰值进行对比,并计算Pearson相关性。h) NPS样本中炎症参数和病毒脱落的纵向过程的代表性概述。对于曲线拟合,计算了四节样条。误差条表示平均值±扫描电镜.t检验用于确定均值差异。*:p<0.05;***:p<0.01;***:p<0.001;***:p<0.0001;ns.:不重要的。补充表S3显示相应的统计数据。
SARS-COV-2病毒脱落持续时间
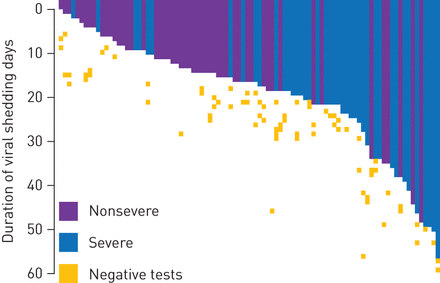
病毒脱落持续时间能够区分机械通气的需求(补充图S2),约登指数为0.467;临界值为17是最优的。92例患者中有34%的患者观察到持续性病毒脱落(>17天)。病毒脱落的持续时间因疾病严重程度而有显著差异(表1);这在图4.
根据疾病严重程度可视化病毒脱落的持续时间。彩色车道描绘了每位患者的病毒持续时间从第一次阳性测试中脱落,直到最后一次阳性测试。还指出了负测试。
为了纠正其他变量的影响,通过UNI和多元COX回归分析研究了延长的病毒脱落。为了验证定义“病毒脱落的持续时间”,COX回归分析也以“病毒脱落的持续时间”进行,定义为从症状到第一个负测试结果的暂停时间。结果之间的意义和解释基本上不变(补充图S1).多变量分析证实长时间的病毒脱落与严重疾病有关。此外,没有发现病毒脱落与免疫抑制之间的关联(表2).
讨论
我们的研究显示,在COVID-19重症患者的前两周内,病毒脱落量仍然升高,而在NPS样本中,非重症患者组的病毒脱落量较早下降。此外,我们发现持续性病毒脱落与疾病严重程度有关。SARS-CoV-2的时间进程和病毒脱落尚未在欧洲患者队列中进行调查。病毒脱落动力学的特征是高度感兴趣的,因为它可能指示潜在的免疫过程。
以往对SARS-CoV-2在呼吸道样本中的病毒脱落的调查显示,在更深的呼吸道样本中有更高的病毒脱落[10.那18].H独角仙等.[19[不同呼吸道样品(支气管和鼻咽)的SARS-COV-2病毒脱落,发现严重疗程的患者在深层呼吸道样品中表现出升高的病毒脱落。这些发现符合我们的研究,其中ETA和NPS测试在直接比较了两种样品类型时表现出高的可变性。因此,在随后的测试中,它们分别分析(图1).这种变异可能是由SARS-CoV-2病毒的不同趋向性解释的,但nps对鼻咽标本的技术限制可能会增加差异[20.].
调查SARS-COV-2病毒脱落和疾病严重程度的研究随着呼吸道样本作为支气管和鼻咽癌的研究[8.那21那22].如前所述,对下呼吸道样本和上呼吸道样本进行单独分析可以防止任何抽样偏差。当单独分析时,我们发现SARS-CoV-2鼻咽病毒脱落在重症患者组第2周仍然很高,而在非重症患者组第2周下降。在比较入院时的绝对病毒脱落时,我们没有发现根据疾病严重程度的显著差异。重度组在第2周的持续升高表明缺乏病毒清除是肺恶化的一种致病机制。最初的病毒载量没有因疾病严重程度而不同,这可能进一步表明,血管紧张素转换酶2受体结合饱和导致复制上限[23].最近的z研究恒等.[21]显示重症患者呼吸道标本中SARS-CoV-2病毒的脱落量高于轻症患者。在本研究中,呼吸道样本没有区分痰液和唾液,这可能解释了观察到的病毒脱落差异,因为在重症组中纳入更多的痰液样本也可能导致病毒脱落水平升高。
在分析炎症的全身标志物时,在初始升高和降低CRP(第2周)后,我们观察到IL-6和PCT的长期全身炎症反应。这些结果支持以前公布的数据表征严重患病患者的免疫应答[11.那24那25]有趣的是,尽管重症和非重症患者的初始病毒载量没有差异,但重症患者在第2周时的初始病毒载量保持升高,但有一小部分相关的新冠病毒-19患者出现了炎症性重症病程。这些发现与康复试验的报道效果一致,该试验表明类固醇治疗的免疫抑制可显著降低28天死亡率[26].可以与其他不平衡的高炎症综合征进行类比,如。只有一小部分患者在Epstein-Barr病毒感染后发育血糖淋巴管激尿剂[27].托西珠单抗IL-6受体阻滞剂在中度病情的COVID-19患者中缺乏疗效,表明参与这一炎症过程的其他潜在途径[28].
IL-6和CRP的不协调运动提示先天因素主导早期免疫反应。最近的研究表明,IL-6并非只与CRP对应(CRP通常由肝细胞在对IL-6反应时产生),尽管IL-6的某个(低)阈值是CRP产生所必需的[29-31].两项规模更大的研究表明,血清IL-6在预测COVID-19临床结局(如呼吸衰竭和死亡)方面优于CRP、铁蛋白、肝酶和其他简单的临床实验室指标,最佳临界值为80和86 pg·L-1, 分别 [32那33].
PCT值为0.2–0.5 ng·mL-1被认可对患有患者患者的患者敏感和特异性,患有较低呼吸道症状和肺浸润的患者[34那35].有趣的是,我们观察到具有和没有共感或二次感染的群体中高度升高的PCT水平,这可能表明存在亚临床细菌共感染(补充图开通).必须强调的是,痰/ ETA培养的时序可能在抗菌治疗之前,因此可能低估了阳性痰的患者的比例。有权进一步调查,解决Covid-19患者在Covid-19患者中的细菌有关,亚临床的共感和定植的重要性[36-38].
到目前为止,已经在几个选定的患者群体中调查了SARS-CoV-2病毒脱落的持续时间。在对191例中国COVID-19住院患者的早期综合临床特征的研究中,病毒长期脱落明显。然而,没有关于绝对拷贝数或采样点(痰、NPS或ETA)的数据[4.].另一项研究调查了病毒脱落和传播性,并且根据患者亚组分层了病毒脱落的时间模式[7.].在任何研究的亚组中未显示病毒脱落的持续时间增加。但是,在分析中,只有少数患者在非酿造和严重的亚组中,并且不可用这些亚组的定义。我们的研究表明,在患有严重疾病的患者中,在患者患者(n = 44岁的患者中的病毒脱落持续存在(n = 44.4.8%的患者的病毒脱落)更频繁地发生严重疾病的患者(表2).
持续升高的SARS-COV-2病毒脱落在呼吸标本中表明严重课程患者的免疫清除降低。在年轻时和少数合并症中,病毒间隙迅速,但在少数寡糖患者中观察到延长的病毒脱落[11.].导致这种现象的重要潜在因素可能是宿主因素或免疫反应的差异。有趣的是,男性与长期的病毒脱落有关(表2).男性患者的延迟病毒间隙可以通过免疫学和流行病学性别特异性差异来解释[39那40].
此外,症状出现50天后病毒RNA >的存在可能提示病毒持续复制,导致慢性局部炎症反应。这些发现可以解释COVID-19患者往往难以恢复和拖延,并伴有持续的局部免疫反应,对呼吸系统和其他器官产生不利影响[41那42].在SARS中观察到类似的病毒脱落图案[43].与SARS一样,尽管血清转化,但SARS- cov -2病毒脱落的缓慢减少表明,COVID-19中正在进行细胞清除,抗体介导的清除无效[10.那43].进一步研究免疫学因素对COVID-19病程和结局的影响。
本研究的局限性
我们的研究有几个局限性。首先,这是一项具有中等样本量的回顾性单中心队列研究。这可能导致在亚组分析中混杂因素的分布不平衡。由于非重症患者住院时间较短,检测的患者数量随着时间的推移而减少,而在我们进行分析时,其他患者仍在进行通气;当比较病毒脱落时,收集的样本可能不太具有代表性。PCR法测定病毒脱落量主要依赖于样本采集和分析前因素,影响测定的病毒脱落量。宿主因素如随着坏死/凋亡细胞的增加而增加的支气管易感性也可能影响病毒的脱落量。
结论
我们的研究结果表明,在第一周的严重Covid-19课程中,病毒脱落仍然升高,可能持续超过更长的持续时间。持续的和不平衡的炎症反应可能最终有助于疾病严重程度。进一步的研究应该调查与这些现象相关的个体宿主因素来阐明潜在机制。
补充材料
补充材料
请注意:编辑部没有编辑补充材料,并随着作者提供的,上传。
补充图S1。COX回归分析。erj - 02724 - 2020。Figure_S1
补充图S2.a)严重和非严重疾病入院时的PCT值(入院后<48小时测量的PCT);b)细菌合并感染和继发性细菌感染亚组的PCT水平。erj - 02724 - 2020。Figure_S2
补充表S1。延长病人的特点。ERJ-02724-2020.表1
补充表S2。根据时间点和疾病严重程度比较NPS的平均病毒载量。ERJ-02724-2020.表2
补充表S3。CRP、Il-6、PCT随时间点和病情严重程度的比较ERJ-02724-2020.表3
补充表S4。重症和非严重Covid-19患者中辛纤维,阳性ETA /痰样品和继发感染的分布。ERJ-02724-2020.表4
可分享的PDF.
脚注
这篇文章有补充资料可从www.qdcxjkg.com
作者贡献:D. Munker, A. Osterman和S. Munker对数据的设计、获取、分析和解释做出了贡献。所有作者的贡献是产生和分析数据,仔细修改工作,批准最终版本,并同意工作的所有方面。
利益冲突:D.芒克没有什么要披露的。
利益冲突:A.奥斯特曼没有什么可披露的。
利益冲突:H. Stubbe没什么可透露的。
利益冲突:穆恩霍夫先生没有什么可透露的。
利益冲突:维特没有什么可披露的。
利益冲突:T.温伯格没有什么可披露的。
利益冲突:巴尼克尔先生没有什么可透露的。
利益冲突:J-N.MUMM没有什么可披露的。
利益冲突:K. Milger没有什么可披露的。
利益冲突:E. Khatamzas没有什么可透露的。
利益冲突:S.克劳斯没有什么要披露的。
利益冲突:C.Scherer无需披露任何信息。
利益冲突:J.C. Hellmuth无需披露。
兴趣冲突:C. Giessen-Jung无需披露。
利益冲突:M. Zoller无需披露。
利益冲突:T.Herold无需披露任何信息。
利益冲突:S. SteCher无需披露。
利益冲突:E.N. De Toni没有什么可披露的。
利益冲突:C. Schulz无需披露。
利益冲突:N. Kneidinger没有什么可披露的。
利益冲突:O.T. Keppler没什么可透露的。
利益冲突:J. BEHR没有什么可披露的。
兴趣冲突:J. Mayerle没有披露。
利益冲突:S. MUNKER没有什么可披露的。
- 已收到2020年7月10日。
- 公认12月13日,2020年12月。
- 版权©2021人队。
这个版本是在知识共享署名非商业许可4.0的条款下发布的。有关商业复制权利和许可,请联系权限{exernet.org