摘要gydF4y2Ba
2019冠状病毒病(COVID-19)是2019年底出现的一种呼吸道急性感染gydF4y2Ba1gydF4y2Ba,gydF4y2Ba2gydF4y2Ba.中国最初的疫情涉及13.8%的重症病例和6.1%的重症病例gydF4y2Ba3.gydF4y2Ba.这种严重的表现可能是由于病毒使用主要在肺表达的病毒受体所致gydF4y2Ba2gydF4y2Ba,gydF4y2Ba4gydF4y2Ba;同样的受体趋向性被认为决定了2003年严重急性呼吸综合征(SARS)的致病性,但也有助于控制gydF4y2Ba5gydF4y2Ba.然而,有报告称,COVID-19病例中患者表现出轻微的上呼吸道症状,这表明有可能出现症状前或少症状传播gydF4y2Ba6gydF4y2Ba,gydF4y2Ba7gydF4y2Ba,gydF4y2Ba8gydF4y2Ba。迫切需要有关病毒复制、免疫力和身体特定部位传染性的信息。我们报告了9例新冠病毒-19病例的详细病毒学分析,证明病毒在上呼吸道组织中复制活跃。在感染的第一周,咽部病毒的脱落率非常高症状,峰值为7.11×10gydF4y2Ba8gydF4y2Ba第4天每个咽拭子的RNA拷贝数。传染性病毒很容易从喉咙或肺的样本中分离出来,但从粪便样本中分离不出来——尽管病毒RNA浓度很高。血液和尿液样本从未检测出病毒。喉部样本中存在的病毒复制RNA中间物证实了喉部的活跃复制。我们始终在一名患者的咽喉和肺部样本中检测到序列不同的病毒群体,证明了独立复制。病毒RNA从痰中脱落持续到症状结束。50%的患者在第7天发生血清转化(所有患者在第14天发生血清转化),但随后病毒载量没有迅速下降。COVID-19可表现为上呼吸道的一种轻微疾病。确认上呼吸道病毒活跃复制对遏制COVID-19具有重要意义。gydF4y2Ba
主要的gydF4y2Ba
SARS冠状病毒(SARS-CoV)与冠状病毒19、SARS-CoV-2的致病因子之间存在着密切的遗传关系。ACE2在下呼吸道的主要表达被认为决定了SARS作为下呼吸道感染的自然史gydF4y2Ba5gydF4y2Ba.虽然在上呼吸道临床标本中发现SARS-CoV-2呈阳性,但以前曾有过描述gydF4y2Ba9gydF4y2Ba,gydF4y2Ba10gydF4y2Ba,这些观察并没有解决SARS和COVID-19在临床病理方面的主要区别。在这里研究的患者之所以被登记,是因为他们是在与指示病例的已知密切接触中获得感染的,因此避免了基于症状的病例定义的代表性偏见。所有患者都在德国慕尼黑的一家医院接受治疗。病毒学检测是由两个密切合作的实验室进行的,它们使用了反转录聚合酶链反应(RT-PCR)和病毒分离的相同技术标准;这两个实验室几乎在所有的单个样本中都确认了彼此的结果。由于结果的高度一致性,除了血清学数据(仅基于一个实验室的结果)外,所有数据都被一起呈现。这些患者是2020年1月23日之后在慕尼黑发生的更大的流行病学相关病例群集的一部分,1月27日发现(参考文献)。gydF4y2Ba11gydF4y2Ba).本研究使用了在医院临床过程中采集的样本,以及入院前初步诊断检测的样本。在由其他实验室进行初步诊断检测的情况下,根据本研究的严格质量标准检索并重新检测原始样本。gydF4y2Ba
RT-PCR、复制位点和传染性gydF4y2Ba
为了首先了解所描述的临床表现是否仅由SARS-CoV-2感染引起,对所有患者的样本进行了呼吸道病毒感染的典型病原体的检测,包括人类冠状病毒(HCoV)-HKU1、HCoV-OC43、HCoV-NL63和HCoV-229E、流感病毒A、流感病毒B、非诺病毒、肠病毒、呼吸道合胞病毒、人类副流感病毒1-4、人类偏肺病毒、腺病毒和人类博卡病毒。未在任何患者中检测到共同感染。gydF4y2Ba
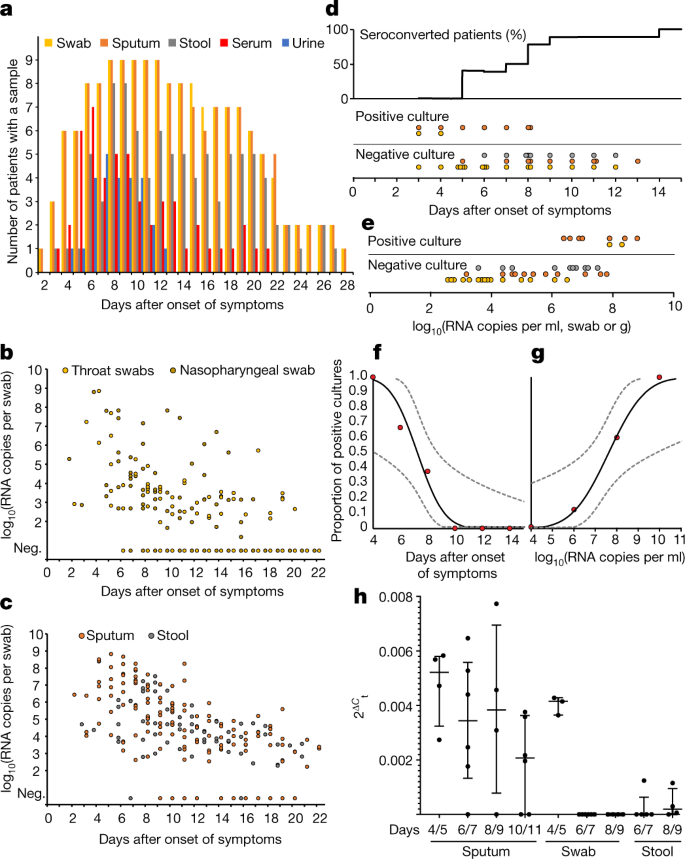
所有患者均通过鼻咽拭子标本的RT-PCR初步诊断gydF4y2Ba12gydF4y2Ba. 在所有患者的整个临床过程中都收集了这两种类型的标本。比较鼻拭子和口咽拭子时,病毒载量或检出率没有明显差异(图。gydF4y2Ba1bgydF4y2Ba).最早的拭子是在出现症状的第一天采集的,这些症状通常非常轻微或前驱症状。所有患者在第1天至第5天的拭子检测均呈阳性。平均病毒RNA载量为6.76 × 10gydF4y2Ba5gydF4y2Ba直到第5天,每根棉签的拷贝数最大为7.11 × 10gydF4y2Ba8gydF4y2Ba拷贝/拭子。第5天后采集的拭子样本的平均病毒载量为3.44 × 10gydF4y2Ba5gydF4y2Ba每个拭子的样本数,检出率为39.93%。最后一次检测呈阳性的拭子样本是在症状出现后第28天采集的。痰中的平均病毒载量为7.00×10gydF4y2Ba6gydF4y2Ba每毫升复制数,最大为2.35 × 10gydF4y2Ba9gydF4y2Ba拷贝/毫升。gydF4y2Ba
一个gydF4y2Ba,每天样本和样本类型。gydF4y2BabgydF4y2Ba,上呼吸道样本中的病毒RNA浓度。底片。,sample negative for RNA copies.cgydF4y2Ba,痰液和粪便样本中的病毒RNA浓度。gydF4y2BadgydF4y2Ba,血清转化和病毒分离的成功与否,取决于出现症状后的天数。第一,血清转化患者的比例。底部为病毒分离试验的汇总结果。gydF4y2BaegydF4y2Ba、病毒分离成功与否,取决于病毒载量。病毒载量预测为每毫升(痰样本)、每拭子(咽拭子样本)或每克(粪便样本)的RNA拷贝数。gydF4y2BafgydF4y2Ba,gydF4y2BaggydF4y2Ba,根据概率分布预测病毒分离成功率。内线为概率曲线(剂量-反应规则)。外虚线为95%置信区间。对于<5%的分离成功率,估计日数为9.78(95%置信区间8.45–21.78)症状出现后天,分离成功率<5%的估计RNA浓度估计为5.40 loggydF4y2Ba10gydF4y2Ba(每毫升RNA拷贝数)(95%可信区间- 4.11-6.51)。gydF4y2BahgydF4y2Ba,与病毒基因组RNA相关的亚基因组病毒RNA转录本。点代表从至少两次独立的患者样本实验中获得的RT-PCR数据的平均值。图中显示了四分位数范围的中值。gydF4y2Ba
因为拭子样本对SARS病例的初步诊断敏感性有限gydF4y2Ba13gydF4y2Ba,gydF4y2Ba14gydF4y2Ba,我们分析了7名患者在同一时间采集的第一对拭子和痰样本。所有样本均在症状出现后2至4天内采集。在两例患者中,拭子样本中的病毒浓度明显高于痰样本中的病毒浓度,如阈值周期中的差异>3所示(gydF4y2BaCgydF4y2BatgydF4y2Ba)值。另外两例的情况正好相反,其余三例的两种样本的浓度相似。gydF4y2Ba
27份尿液样本和31份血清样本均未检测出SARS-CoV2 RNA阳性。gydF4y2Ba
为了了解传染性,我们尝试在多个场合从临床样本中分离活病毒(图。gydF4y2Ba1dgydF4y2Ba).尽管在出现症状的第一周,从相当一部分样本(16.66%的拭子和83.33%的痰样本)中很容易分离出病毒,但在第8天的样本中没有分离出病毒,尽管病毒持续高负荷。gydF4y2Ba
从粪便样本中分离病毒从来没有成功过,不管病毒RNA浓度如何,根据从4名患者的第6天和第12天共采集的13个样本。病毒分离的成功还取决于病毒载量:包含<10的样本gydF4y2Ba6gydF4y2Ba每毫升拷贝数(或每样本拷贝数)从未产生分离物。对于痰样本,基于probit模型进行插值,以获得基于实验室的患者出院感染性标准(图。gydF4y2Ba1 f, ggydF4y2Ba).gydF4y2Ba
高病毒载量和早期咽拭子成功分离提示病毒可能在上呼吸道组织复制。为了在缺乏组织病理学的情况下获得病毒复制活跃的证据,我们进行了RT-PCR检测,在临床样本中直接识别病毒亚基因组mrna(扩展数据图)。gydF4y2Ba1gydF4y2Ba).病毒亚基因组mRNA仅在受感染细胞中转录,而不封装到病毒粒子中,因此表明样品中存在活跃的受感染细胞。比较同一样本中病毒亚基因组mRNA水平与病毒基因组RNA水平。在痰液样本9天4天,在此期间活跃复制在所有患者痰是显而易见的按纵向病毒载量课程(详见“病毒载量、抗体反应和临床课程”),意思是每个基因组规范化subgenomic mRNA的比率约为0.4%(图gydF4y2Ba1ggydF4y2Ba).从第10天到第11天出现下降。在咽拭子中,直到第5天的所有样本均在相同范围内,而此后在咽拭子中未检测到亚基因组mRNA。总之,这些数据表明,在出现症状后的头5天,SARS-CoV-2在喉咙中活跃复制。用同样的方法没有(或只有少量)大便复制的指征(图)。gydF4y2Ba1ggydF4y2Ba).gydF4y2Ba
在我们的研究中,我们对所有患者的全病毒基因组进行了测序。首先在一名患者中检测到G6446A交换,随后传播给群集中的其他患者gydF4y2Ba11gydF4y2Ba.在第一位患者中,在咽拭子中发现了这种突变,而同一天的痰样本显示了原始等位基因(G6446)。通过RT-PCR和Sanger测序分析该患者所有序列样本的单核苷酸多态性(见表)gydF4y2Ba1gydF4y2Ba).咽拭子和痰液中独立的基因型的存在有力地支持了我们的怀疑,即病毒在喉咙中独立复制,而不是从肺向喉咙被动脱落。gydF4y2Ba
病毒载量、抗体反应和临床病程gydF4y2Ba
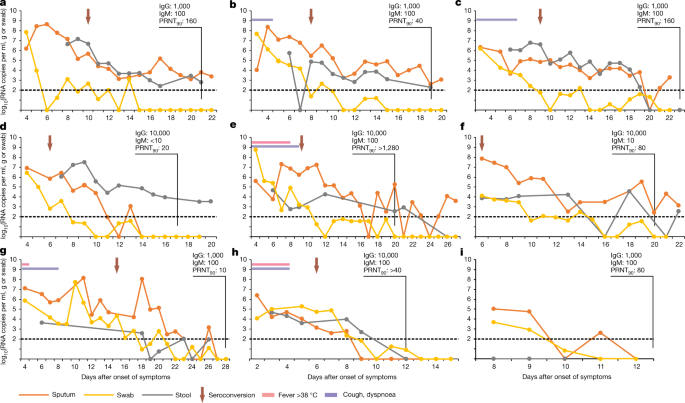
图中总结了痰液、咽拭子和粪便中病毒载量的日常测量。gydF4y2Ba2gydF4y2Ba。一般来说,初始样本中的病毒RNA浓度非常高。在除一名患者外的所有患者中,咽拭子中的病毒RNA浓度在首次出现时似乎已经在下降。痰中的病毒RNA浓度下降得更慢,其中三名患者在出现症状的第一周达到峰值ht患者。粪便中的病毒RNA浓度也很高。在许多情况下,粪便中病毒RNA浓度的过程似乎反映了痰中的过程(图。gydF4y2Ba2 a - cgydF4y2Ba).从粪便RNA排泄的过程来看,只有1例患者在肠道中进行了明显的独立复制(图1)。gydF4y2Ba二维gydF4y2Ba).而症状大多在第一周结束后消退(见表)gydF4y2Ba2gydF4y2Ba),直到第二周咽拭子中仍可检测到病毒RNA。在9名患者中,有6人的粪便和痰标本在3周内保持rna阳性,尽管症状完全缓解。gydF4y2Ba
一个gydF4y2Ba- - - - - -gydF4y2Ba我gydF4y2Ba这些小组对应的是病人。1 (gydF4y2Ba一个gydF4y2Ba), 2 (gydF4y2BabgydF4y2Ba), 3 (gydF4y2BacgydF4y2Ba), 4 (gydF4y2BadgydF4y2Ba), 7 (gydF4y2BaegydF4y2Ba)、8日(gydF4y2BafgydF4y2Ba), 10 (gydF4y2BaggydF4y2Ba)、14 (gydF4y2BahgydF4y2Ba)及16 (gydF4y2Ba我gydF4y2Ba)gydF4y2Ba11gydF4y2Ba.虚线,量化的限度。实验是重复进行的,所提供的数据是两个实验室独立获得的结果的平均值。PRNTgydF4y2Ba90gydF4y2Ba,血清稀释,可使病毒斑块减少90%。gydF4y2Ba
所有病例的病程相对较轻(表1)gydF4y2Ba2gydF4y2Ba).这两名有肺部感染迹象的患者是痰病毒载量在第10天或第11天出现晚高峰的唯一病例,而其他所有患者的痰病毒载量此时都在下降(图)。gydF4y2Ba2 f, ggydF4y2Ba).值得注意的是,九名患者中有四名表现出味觉和嗅觉的丧失,并描述这种丧失比普通感冒更强烈、更持久。gydF4y2Ba
用表达SARS-CoV-2刺突蛋白的细胞和用SARS-CoV-2病毒中和试验检测血清转化的IgG和IgM免疫荧光(表)gydF4y2Ba3.gydF4y2Ba,扩展数据图。gydF4y2Ba2gydF4y2Ba).50%的患者在第7天发生血清转化,所有患者在第14天发生血清转化(图。gydF4y2Ba1dgydF4y2Ba).第7天未分离出病毒。所有患者均有可检测到的中和抗体,其滴度并不表明与临床病程密切相关。请注意,病人没有。4组在第2周结束时病毒中和滴度最低,似乎病毒从粪便中流出的时间较长(图2)。gydF4y2Ba二维gydF4y2Ba).差异重组免疫荧光试验的结果表明,在几个患者中对四种地方性人类冠状病毒具有交叉反应或交叉刺激作用(扩展数据表)gydF4y2Ba1gydF4y2Ba).gydF4y2Ba
结论gydF4y2Ba
研究中的患者均为年轻至中年专业人士,没有明显的潜在疾病。除一名患者外,所有患者均在症状仍然轻微或处于前驱期时首次接受测试(大多数患者一旦普遍意识到一种流行性疾病,就会出现的时期)gydF4y2Ba5gydF4y2Ba诊断试验表明,简单的咽喉拭子在感染的这一阶段将提供足够的敏感性,这与SARS形成鲜明的对比;例如,98个鼻咽或鼻咽拭子样本中只有38个在香港的SARS患者中通过RT-PCR检测阳性。gydF4y2Ba15gydF4y2Ba.SARS和COVID-19之间的病毒载量也有很大差异。就SARS而言,症状出现后7至10天,RNA浓度达到峰值(高达5 × 10)gydF4y2Ba5gydF4y2Ba每个棉签的拷贝数)gydF4y2Ba13gydF4y2Ba,gydF4y2Ba14gydF4y2Ba.在目前的研究中,浓度在第5天之前达到峰值,并高出1000多倍。从咽拭子成功分离活病毒是COVID-19和SARS的另一个显著区别,这种分离很少成功gydF4y2Ba16gydF4y2Ba,gydF4y2Ba17gydF4y2Ba,gydF4y2Ba18gydF4y2Ba.这表明病毒在上呼吸道组织中活跃复制,尽管可检测到ACE2表达,但SARS-CoV不认为在上呼吸道组织中复制gydF4y2Ba19gydF4y2Ba,gydF4y2Ba20gydF4y2Ba.同时,ACE2同时作为SARS-CoV和SARS-CoV-2的受体,在痰中具有高度相似的排泄动力学,并在肺中积极复制。sars冠状病毒以前被发现gydF4y2Ba13gydF4y2Ba痰中的平均浓度为1.2–2.8×10gydF4y2Ba6gydF4y2Ba每毫升的拷贝数,与这里的观察结果一致。gydF4y2Ba
虽然组织病理学还未证实其复制,但我们对咽喉拭子样本中转录亚基因组mRNA的细胞的研究,特别是在症状的前5天,强烈支持了SARS-CoV-2在喉内复制的扩展组织趋近性。另一个值得注意的证据是喉部的独立复制,一个病人的序列发现,他一贯显示喉部有不同的病毒,而不是肺。此外,味觉和嗅觉的紊乱指向上呼吸道组织的感染。gydF4y2Ba
重要的是,在本研究中,大多数患者在第一次检测时上呼吸道样本的脱落高峰似乎已经超过,而在出现症状的第一周,痰中传染性病毒的脱落仍在持续。综上所述,这些发现表明SARS-CoV-2比SARS-CoV更有效地传播,在症状仍然轻微和典型上呼吸道感染的情况下,通过活跃的咽部病毒脱落。在疾病后期,COVID-19在下呼吸道复制方面类似于SARS。值得注意的是,有肺部感染症状的两名患者痰中病毒载量延长。我们的研究是有限的,因为没有观察到严重的病例。包括严重病例在内的未来研究应关注在第一周结束后病毒载量增加的预后价值,这可能表明症状的加重。gydF4y2Ba
一个最有趣的假说解释了向喉部的可能延伸,即在SARS-CoV-2刺突蛋白的S1-S2连接处存在一个多碱的furin型剪切位点,而该位点在SARS-CoV中不存在gydF4y2Ba17gydF4y2Ba.在SARS-CoV的S1-S2区域插入一个多碱基切割位点,此前已被证明会导致中度但可识别的融合获得活性,这可能导致病毒进入低密度ACE2表达的组织中增加gydF4y2Ba21gydF4y2Ba.gydF4y2Ba
高浓度的病毒RNA和偶尔在粪便中检测到的含有亚基因组mRNA的细胞表明在胃肠道中有活跃的复制。与中东呼吸系统冠状病毒(MERS-CoV)相比,该病毒的检出率高得多,这也表明其复制活跃。在沙特阿拉伯利雅得住院的37名患者的样本中,仅14.6%的样本中发现粪便相关RNA。gydF4y2Ba22gydF4y2Ba,gydF4y2Ba23gydF4y2Ba.如果SARS-CoV-2只是被动地出现在粪便中(如吞咽呼吸道分泌物后),预计其检出率将与MERS-CoV相似。胃肠道的复制也与SARS-CoV相似,SARS-CoV定期从粪便中排出(从粪便中可以在细胞培养中分离出来)gydF4y2Ba24gydF4y2Ba).我们未能从粪便中分离出活的SARS-CoV-2可能是因为病例病程较轻,只有一例出现间歇性腹泻。在中国,99例中只有2例出现腹泻gydF4y2Ba25gydF4y2Ba。因此,进一步的研究应该解决粪便中脱落的SARS-CoV-2是否通过与肠道环境接触而被视为非感染性。我们的初步结果表明,控制病毒传播的措施应该以液滴传播为目标,而不是以蚊虫传播为基础。gydF4y2Ba
痰中病毒的长期脱落不仅与医院感染的控制有关,也与出院管理有关。在传染病病房病床容量有限的情况下,有治疗后尽早出院的压力。根据目前的发现,对于症状超过第10天且每毫升痰中病毒RNA拷贝数少于10万的患者,可以选择早期出院并随后进行家庭隔离。这两个标准都预测,在细胞培养的基础上,几乎没有残留的感染风险。gydF4y2Ba
所有患者的血清学病程表明血清转化的时间与SARS-CoV感染类似或稍早gydF4y2Ba18gydF4y2Ba。大多数SARS病例的血清转化发生在症状出现的第二周。与SARS和MERS一样,在免疫荧光检测中,IgM的检测时间远早于IgG;这可能部分是由于技术原因,因为IgG抗体的高亲和力在检测中超过了IgM对病毒表位的竞争。IgG的消耗只能部分地进行缓解这种影响。由于免疫荧光分析是一种劳动密集型方法,因此应将酶联免疫吸附试验作为筛选试验。中和试验是必要的,以排除针对地方性人类冠状病毒的交叉反应抗体。基于中和抗体滴度通常较低在冠状病毒感染中观察到的sgydF4y2Ba26gydF4y2Ba,gydF4y2Ba27gydF4y2Ba,我们在这里开发了一种特别敏感的斑块减少中和试验。考虑到我们观察到的滴度,一种更简单的微中和试验形式可能在常规应用和人群研究中提供足够的敏感性。gydF4y2Ba
当与病毒载量进程相一致时,似乎在血清转化时没有突然的病毒消除。相反,血清转化在第2周早期与痰中病毒载量缓慢而稳定的下降同时发生。糖蛋白关键位点的糖基化模式等特性是否在中和抗体反应的衰减中起作用,还需要进一步澄清。在任何情况下,主要以诱导抗体反应为目标的疫苗方法应该以诱导特别强的抗体反应为目标,以达到有效。gydF4y2Ba
方法gydF4y2Ba
没有使用统计方法来预先确定样本量。实验不是随机的,研究人员在实验和结果评估过程中对分配也不盲目。gydF4y2Ba
临床样本和病毒载量转换gydF4y2Ba
痰液和粪便样本被采集并在当地条件下运输。鼻咽拭子和鼻咽拭子保存在3ml病毒转运培养基中。假设所有样本成分都悬浮在3ml病毒转运培养基中,将痰样本中的病毒载量推算为每毫升RNA拷贝数,粪便样本中的病毒载量推算为每克RNA拷贝数,咽拭子中的病毒载量推算为每3ml RNA拷贝数。对于悬浮在少于3ml病毒运输培养基中的拭子样品,这种转换适用于代表整个拭子的拷贝数。图中显示了所有患者发病后每天收到的样本的汇总概况。gydF4y2Ba1agydF4y2Ba.gydF4y2Ba
SARS-CoV-2和其他呼吸道病毒的RT-PCRgydF4y2Ba
RT-PCR使用的靶标gydF4y2BaEgydF4y2Ba和gydF4y2BaRdRpgydF4y2Ba如前所述的基因gydF4y2Ba12gydF4y2Ba.这两个实验室都使用了预先配制的寡核苷酸混合物(Tib-Molbiol),以使实验室程序更具可重复性。所有患者还使用LightMix-Modular Assays(罗氏)检测了其他呼吸道病毒,包括HCoV-HKU1、HCoV-OC43、HCoV-NL63和HCoV-229E、流感病毒A、流感病毒B、鼻病毒、肠道病毒、呼吸道合胞病毒、人副流感病毒1-4、人偏肺病毒、腺病毒和人博卡病毒。附加的技术细节在补充方法部分提供gydF4y2Ba1gydF4y2Ba.gydF4y2Ba
病毒分离gydF4y2Ba
在两个实验室对Vero E6细胞进行了病毒分离。简言之,将100 μl悬浮、清除、过滤的临床标本与等体积的细胞培养基混合。分别于0、1、3、5 d后收集上清,用于RT-PCR分析。附加的技术细节在补充方法部分提供gydF4y2Ba2agydF4y2Ba.gydF4y2Ba
血清学gydF4y2Ba
如前所述,我们进行了重组免疫荧光试验,以确定对VeroB4细胞中的重组刺突蛋白的特异性反应性gydF4y2Ba26gydF4y2Ba,gydF4y2Ba28gydF4y2Ba。本试验使用了从HCoV-229E、HCoV-NL63、HCoV-OC43、HCoV-HKU1或SARS-CoV-2克隆的冠状病毒棘突蛋白。筛选稀释度为1:10。斑块减少中和试验基本上按照之前对MERS-CoV的描述进行gydF4y2Ba26gydF4y2Ba.血清稀释导致斑块减少90%(PRNTgydF4y2Ba90gydF4y2Ba)和50% (PRNTgydF4y2Ba50gydF4y2Ba)记录为滴度。补充方法部分提供了其他技术细节gydF4y2Ba2b,cgydF4y2Ba.gydF4y2Ba
统计分析gydF4y2Ba
使用SPSS软件(第25版)或GrapPad Prism(第8版)进行统计分析。gydF4y2Ba
伦理批准声明gydF4y2Ba
所有患者均为本研究使用其数据和临床样本提供了知情同意。Ludwig Maximillians Universität Munich医学院伦理委员会已批准该治疗机构科学使用患者数据的机构审查委员会许可(投票20- 225kb)。gydF4y2Ba
报告摘要gydF4y2Ba
有关研究设计的进一步资料,请参阅gydF4y2Ba自然研究报告摘要gydF4y2Ba链接到本文。gydF4y2Ba
数据可用性gydF4y2Ba
序列数据可在Gisaid中获得,登录号为ep_isl_406862。如有合理要求,可向C.D.索取其他资料。gydF4y2Ba
改变历史gydF4y2Ba
2020年12月11日gydF4y2Ba
对本文的更正已发表:gydF4y2Bahttps://doi.org/10.1038/s41586-020-2984-3gydF4y2Ba
参考文献gydF4y2Ba
- 1.gydF4y2Ba
等。一种新型冠状病毒来自2019年中国肺炎患者。gydF4y2Ba英国医学院gydF4y2Ba.gydF4y2Ba382gydF4y2Ba, 727–733 (2020).gydF4y2Ba
- 2.gydF4y2Ba
国际病毒分类委员会冠状病毒科研究组。这个物种gydF4y2Ba严重急性呼吸综合征相关的冠状病毒gydF4y2Ba:将2019-nCoV分类并命名为SARS-CoV-2。gydF4y2BaMicrobiol Nat。gydF4y2Ba5gydF4y2Ba, 536–544 (2020).gydF4y2Ba
- 3.gydF4y2Ba
谁。gydF4y2Ba中国-世界卫生组织新冠肺炎联合考察团报告gydF4y2Bahttps://www.who.int/docs/default-source/coronaviruse/who-china-joint-mission-on-covid-19-final-report.pdfgydF4y2Ba(世卫组织,2020年)。gydF4y2Ba
- 4.gydF4y2Ba
霍夫曼,M.等。SARS-CoV-2细胞进入依赖于ACE2和TMPRSS2,并被临床证实的蛋白酶抑制剂阻断。gydF4y2Ba细胞gydF4y2Ba181gydF4y2Ba, 271–280 (2020).gydF4y2Ba
- 5.gydF4y2Ba
梁,g.m.等。2003年香港流行的严重急性呼吸系统综合症的流行病学:对所有1755名病人的分析。gydF4y2Ba安。实习生。地中海gydF4y2Ba.gydF4y2Ba141gydF4y2Ba, 662 - 673(2004)。gydF4y2Ba
- 6.gydF4y2Ba
Rothe等。德国无症状接触者传播新型冠状病毒gydF4y2Ba英国医学院gydF4y2Ba.gydF4y2Ba382gydF4y2Ba, 970 - 971(2020)。gydF4y2Ba
- 7.gydF4y2Ba
Holshue,M. L.等.美国2019例新型冠状病毒的首次报道gydF4y2Ba英国医学院gydF4y2Ba.gydF4y2Ba382gydF4y2Ba, 929 - 936(2020)。gydF4y2Ba
- 8.gydF4y2Ba
Hoehl,S.等人。从中国武汉返回的旅行者中SARS-CoV-2感染的证据。gydF4y2Ba英国医学院gydF4y2Ba.gydF4y2Ba382gydF4y2Ba, 1278 - 1280(2020)。gydF4y2Ba
- 9.gydF4y2Ba
Zou,L.等人。感染患者上呼吸道标本中的SARS-CoV-2病毒载量。gydF4y2Ba英国医学院gydF4y2Ba.gydF4y2Ba382gydF4y2Ba, 1177–1179 (2020).gydF4y2Ba
- 10gydF4y2Ba
杨,B. E.等。新加坡SARS-CoV-2患者的流行病学特征和临床病程gydF4y2Baj。医学协会。gydF4y2Ba.gydF4y2Ba323gydF4y2Ba, 1488 - 1494(2020)。gydF4y2Ba
- 11gydF4y2Ba
Böhmer, M.等。德国暴发的COVID-19是由一个与旅行有关的原发病例引起的。gydF4y2Ba柳叶刀感染.gydF4y2Bahttps://doi.org/10.1016/s1473 - 3099 (20) 30314 - 5gydF4y2Ba(2020).gydF4y2Ba
- 12gydF4y2Ba
Corman, V. M.等。实时RT-PCR检测2019新型冠状病毒(2019- ncov)gydF4y2Ba欧元监管gydF4y2Ba.gydF4y2Ba25gydF4y2Ba, 1 - 8(2020)。gydF4y2Ba
- 13gydF4y2Ba
等。严重急性呼吸综合征相关冠状病毒检测的先进逆转录- PCR检测和替代PCR靶区评估gydF4y2Baj .中国。MicrobiolgydF4y2Ba.gydF4y2Ba42gydF4y2Ba, 2043 - 2047(2004)。gydF4y2Ba
- 14gydF4y2Ba
王志强,王志强等。冠状病毒相关性SARS肺炎社区暴发的临床进展和病毒载量:一项前瞻性研究gydF4y2Ba《柳叶刀》gydF4y2Ba361gydF4y2Ba, 1767 - 1772(2003)。gydF4y2Ba
- 15gydF4y2Ba
潘立国等。常规和实时定量逆转录- pcr检测SARS冠状病毒gydF4y2Ba中国。化学gydF4y2Ba.gydF4y2Ba50gydF4y2Ba, 67 - 72(2004)。gydF4y2Ba
- 16gydF4y2Ba
Ksiazek, T. G.等。一种与严重急性呼吸综合征相关的新型冠状病毒。gydF4y2Ba英国医学院gydF4y2Ba.gydF4y2Ba348gydF4y2Ba, 1953 - 1966(2003)。gydF4y2Ba
- 17gydF4y2Ba
DrStin,C.等.一种新的冠状病毒在严重急性呼吸综合征患者中的鉴定gydF4y2Ba英国医学院gydF4y2Ba.gydF4y2Ba348gydF4y2Ba, 1967 - 1976(2003)。gydF4y2Ba
- 18gydF4y2Ba
Peiris,J.S.等人。冠状病毒是严重急性呼吸综合征的可能病因。gydF4y2Ba《柳叶刀》gydF4y2Ba361gydF4y2Ba, 1319–1325 (2003).gydF4y2Ba
- 19.gydF4y2Ba
Bertram, S.等。流感和sars冠状病毒激活蛋白酶TMPRSS2和HAT在人类呼吸道和胃肠道的多个位点表达。gydF4y2Ba公共科学图书馆一号gydF4y2Ba7gydF4y2Bae35876(2012)。gydF4y2Ba
- 20.gydF4y2Ba
徐华等。口腔黏膜上皮细胞高表达2019-nCoV ACE2受体gydF4y2BaInt。j .口腔科学gydF4y2Ba.gydF4y2Ba12gydF4y2Ba8(2020)。gydF4y2Ba
- 21.gydF4y2Ba
Belouzard,S.,Chu,V.C.和Whittaker,G.R.通过在两个不同位点的顺序蛋白水解裂解激活SARS冠状病毒棘突蛋白。gydF4y2Ba美国国家科学院学报。美国gydF4y2Ba106gydF4y2Ba, 5871 - 5876(2009)。gydF4y2Ba
- 22gydF4y2Ba
Corman, V. M.等。37例中东呼吸综合征冠状病毒感染患者的病毒脱落和抗体反应gydF4y2Ba中国。感染。说gydF4y2Ba.gydF4y2Ba62gydF4y2Ba, 477 - 483(2016)。gydF4y2Ba
- 23gydF4y2Ba
Zhou,J.等人。人类肠道是中东呼吸综合征冠状病毒的另一种感染途径。gydF4y2Ba科学。阿德gydF4y2Ba.gydF4y2Ba3.gydF4y2Baeaao4966(2017)。gydF4y2Ba
- 24gydF4y2Ba
梁,W. K.等。严重急性呼吸综合征相关冠状病毒感染的肠道累及gydF4y2Ba胃肠病学gydF4y2Ba125gydF4y2Ba, 1011–1017 (2003).gydF4y2Ba
- 25gydF4y2Ba
陈,N.等.中国武汉99例2019例冠状病毒肺炎的流行病学和临床特征:描述性研究gydF4y2Ba《柳叶刀》gydF4y2Ba395gydF4y2Ba, 507 - 513(2020)。gydF4y2Ba
- 26gydF4y2Ba
等。mers冠状病毒在家庭接触者中的传播。gydF4y2Ba英国医学院gydF4y2Ba.gydF4y2Ba371gydF4y2Ba, 828 - 835(2014)。gydF4y2Ba
- 27gydF4y2Ba
Müller, m.a.等。沙特阿拉伯存在中东呼吸综合征冠状病毒抗体:一项全国性、横断面、血清学研究gydF4y2Ba柳叶刀感染gydF4y2Ba.gydF4y2Ba15gydF4y2Ba, 559 - 564(2015)。gydF4y2Ba
- 28gydF4y2Ba
Corman, V. M.等。新型人冠状病毒(hCoV-EMC)感染的实验室确认方法gydF4y2Ba欧元监管gydF4y2Ba.gydF4y2Ba17gydF4y2Ba, 20334 (2012).gydF4y2Ba
致谢gydF4y2Ba
这项工作由德国研究部(01KI1723A)和欧盟(602525)的资助向C.D.以及德国联邦国防军医疗服务生物防御研究计划提供资助。资助者在研究设计、数据收集和分析或发表决定方面没有任何作用。我们感谢P.Mackeldanz、E.Möncke Buchner、A.Richter、M.Schmidt和J.Beheim Schwarzbach提供的技术援助。gydF4y2Ba
作者信息gydF4y2Ba
从属关系gydF4y2Ba
贡献gydF4y2Ba
R.W.和V.M.C.计划和监督实验室测试,并评估数据。W.G.和M.S.管理病人并评估临床资料。s.z.、t.b.、s.b.、j.s.、R.E.和K.Z.进行了实验室测试。M.A.M.管理血清学实验室检测。D.N.管理和进行病毒分离研究。T.C.J.分析了序列和群体特异性多态性。P.V.负责实验室检测。crr管理最初的病人接触。M.H.管理最初的病人接触和评估临床资料。C.D.设计并指导实验室研究,并撰写手稿。 C.W. designed and supervised clinical management and clinical data.
通讯作者gydF4y2Ba
道德宣言gydF4y2Ba
相互竞争的利益gydF4y2Ba
两位作者宣称没有相互竞争的利益。gydF4y2Ba
额外的信息gydF4y2Ba
同行评议信息gydF4y2Ba自然界gydF4y2Ba感谢彼得·奥彭肖和其他匿名审稿人对这项工作的同行评议做出的贡献。gydF4y2Ba
出版商的注意gydF4y2Ba施普林格《自然》杂志对已出版的地图和机构附属机构的管辖权要求保持中立。gydF4y2Ba
扩展数据图表gydF4y2Ba
图1序列分析gydF4y2BaEgydF4y2Ba基因亚基因组mRNA。gydF4y2Ba
前导序列(紫色)、推测的转录调节序列(TRS)(灰色)和编码5 ' -近端部分的核苷酸gydF4y2BaEgydF4y2Ba基因(黄色框)显示。绿色箭头为用于扩增和RT-PCR检测的PCR引物结合位点,红色箭头为5 ' -nuclease PCR探针。gydF4y2Ba
扩展数据图2重组SARS-CoV-2-spike免疫荧光试验显示4号患者血清转化。gydF4y2Ba
在症状出现后5天和17天,使用4号患者的血清稀释液1:10、1:100、1:1000和1:10000进行重组免疫荧光试验的代表性结果。通过使用标记有Alexa Fluor 488(绿色显示)的山羊抗人免疫球蛋白进行二次检测。试验一式两份。gydF4y2Ba
补充信息gydF4y2Ba
补充信息gydF4y2Ba
本文件包含补充方法,包括RNA提取和RT-PCR方法的描述,细胞培养和抗体检测方法的描述和补充参考。gydF4y2Ba
权利和权限gydF4y2Ba
关于这篇文章gydF4y2Ba
引用这篇文章gydF4y2Ba
Wölfel,R.,科尔曼,V.M.,古格莫斯,W。gydF4y2Baet al。gydF4y2BaCOVID-2019住院患者的病毒学评估。gydF4y2Ba自然界gydF4y2Ba581年,gydF4y2Ba465 - 469(2020)。https://doi.org/10.1038/s41586-020-2196-xgydF4y2Ba
收到了gydF4y2Ba:gydF4y2Ba
接受gydF4y2Ba:gydF4y2Ba
发表gydF4y2Ba:gydF4y2Ba
发行日期gydF4y2Ba:gydF4y2Ba
DOIgydF4y2Ba:gydF4y2Bahttps://doi.org/10.1038/s41586-020-2196-xgydF4y2Ba
进一步的阅读gydF4y2Ba
通过快速诊断免疫分析法检测COVID-19患者的sars - cov -2特异性抗体gydF4y2Ba
病毒学杂志gydF4y2Ba(2021)gydF4y2Ba
粪便中SARS-CoV-2检测的优化方案gydF4y2Ba
BMC微生物学gydF4y2Ba(2021)gydF4y2Ba
蝙蝠体内与严重急性呼吸综合征(SARS)相关的冠状病毒gydF4y2Ba
动物疾病gydF4y2Ba(2021)gydF4y2Ba
下呼吸道标本SARS-CoV-2肺炎的快速诊断gydF4y2Ba
BMC传染病gydF4y2Ba(2021)gydF4y2Ba
基于宿主细胞对SARS-CoV-2的转录反应的计算分析,以重新利用针对CoV-19的药物gydF4y2Ba
BMC医学信息学及决定gydF4y2Ba(2021)gydF4y2Ba
评论gydF4y2Ba
通过提交一个评论,你同意遵守我们的gydF4y2Ba条款gydF4y2Ba和gydF4y2Ba社区准则gydF4y2Ba.如果您发现一些辱骂或不符合我们的条款或指导方针,请标记为不适当。gydF4y2Ba