摘要
抗菌素耐药性是全球一个重大公共卫生问题。同样,对一线和二线结核病药物耐药的结核病形式对患者、卫生保健工作者和卫生保健服务构成重大挑战。2019年11月,世界卫生组织(世卫组织)召集了一个独立的国际专家小组,使用“建议分级评估、开发和评价”方法审查关于多药耐药结核病和耐利福平结核病治疗的新证据。
本次审查得出的世卫组织最新指南于2020年6月发布,建议对氟喹诺酮类药物不耐药的耐多药/耐多药结核病患者(9-11个月)采用更短的治疗方案,包括贝达喹啉而不是注射药物,使方案全部口服。对于耐多药结核病和氟喹诺酮耐药的患者,可在手术研究条件下(6-9个月)使用由贝达喹啉、pretomanid和利奈唑胺组成的方案。根据耐药情况、结核病的程度或疾病严重程度,可采用较长时间(18-20个月)的全口服、个体化治疗方案。此外,2019年对新数据的审查使世卫组织得出结论,在>6个月期间使用贝达喹啉、delamanid和贝达喹啉一起使用以及怀孕期间使用贝达喹啉没有重大安全问题,尽管没有就这些问题提出正式建议。
2020年修订版强调了对高质量证据的持续需求,并重申需要进行临床试验和其他研究,以促进循证政策的制定。
摘要
世卫组织关于耐药结核病治疗的新指南载有关于缩短或延长耐药结核病患者所有口服治疗方案的最新建议,包括使用的药物和其他支持性措施https://bit.ly/2UJeib7
简介
抗微生物药物耐药性是全球一个重大公共卫生问题,已成为全球卫生安全问题[1,2].耐药细菌感染在全球范围内呈上升趋势,这使耐药结核病(TB)及其诊断和治疗受到高度关注[3.].在过去20年里,很明显,耐药结核病的广泛传播将继续挑战全球治愈患者和实现终结结核病战略宏伟目标的努力[4]、可持续发展目标[5]以及《联合国结核病问题高级别会议政治宣言》提出的目标[6].
耐多药结核病(MDR -TB)是由结核分枝杆菌至少对异烟肼和利福平这两种用于治疗结核病的一线药物具有耐药性的菌株[7].世界卫生组织(世卫组织)估计,2019年世界范围内发生的新发结核病病例中3.3%(95%置信区间2.3-4.3%)和18%(95%置信区间9.7-27%)为耐多药/耐利福平结核病,这意味着近50万(范围为40万- 53.5万)新发耐多药/耐利福平结核病[8].在全球范围内,根据105个国家和地区报告的数据,耐多药结核病患者的平均比例结核分枝杆菌对其中一种氟喹诺酮类药物耐药的菌株为20.1%(95%置信区间15.5-25.0%)[8].尽管各国一直在扩大诊断能力,近年来检测出更多的利福平耐药患者,但2019年全球仅通报了206 030例患者(占估计总数的44%),这表明药物敏感性检测覆盖率严重不佳[8].一旦确诊,大多数已确诊的耐多药/耐多药结核病患者(86%)可获得治疗。
与药物敏感疾病患者相比,MDR/RR-TB患者需要更长时间的治疗方案,并且不良事件发生的可能性更高,这取决于所使用的二线药物。在过去几十年里,大多数耐多药结核方案设计的持续时间≥20个月[9];然而,较短的疗程(9-12个月)[10- - - - - -16]自2016年起由世卫组织推荐[17- - - - - -19].尽管有了这样的发展,由于这些方案的长度和安全性,以及与长时间治疗和护理相关的财务和社会限制,较长和较短方案的规划实施继续对患者和卫生系统提出挑战[20.- - - - - -22].
在全球范围内,国家结核病规划向世卫组织报告,根据2017年开始治疗的队列,只有57%的耐多药/耐多药结核病患者和47%的耐多药/耐多药结核病患者获得了成功的治疗结果[8].虽然这些数字近年来略有增加,但治疗成功率仍然低得令人无法接受。
制定结核病治疗规范指南是世卫组织在终止结核病战略背景下支持国家结核病规划以扩大获得护理的核心任务的一部分[4,23,24].自1996年以来,世卫组织全球结核病规划定期发布耐药结核病治疗指南和实施手册[17,19,25- - - - - -34].在此,我们描述了世卫组织于2020年发布的最新政策更新的过程和内容,并讨论了这些变化对参与耐药结核病临床和规划管理的执行者的影响[7].关于2020年之前存在的建议的其他信息不在此列出,但在[7].
指南制定过程
总的来说,世卫组织内部的指南制定由技术规划协调,确保这一过程是基于证据和透明的,坚定地依赖于科学中的最高道德标准。GRADE框架(建议分级、评估、制定和评价)为世卫组织指南制定过程提供信息[35,36].
2020年耐药结核病治疗指南的更新始于2019年,当时以人口、干预、比较指标、结果(PICO)格式确定了指南更新的范围以及研究问题(表1).通过世卫组织通过一个在线公众评论平台,分享了关于指南更新的目标和目的的信息,以及提出研究问题的新证据的来源,以及打算参加指南制定小组的专家名单。然后,世卫组织发出了一项公开呼吁,呼吁行业、研究人员、国家结核病规划和其他机构提供合适的数据集,以增加与研究问题相关的证据。在gg会议之前,世卫组织委托对不同治疗方案对患者结局影响的现有证据进行了系统审查和荟萃分析。
一个拥有广泛的耐药结核病技术知识并对任何利益冲突进行了仔细审查的国际专家小组组成了全球专家组。所有利益冲突及其处理,均载于指引的附件内[36,37].gg的成员代表了来自不同地理和卫生系统环境的人、指南的未来用户以及社区和患者代表。在日内瓦举行面对面会议之前,与全球政府举行了若干在线网络研讨会。
更新指南的范围
2020年指南更新的范围涵盖以下四个领域。1)持续9-12个月的含贝达喹啉的标准化口服方案治疗MDR/RR-TB患者的有效性和安全性;2)由贝达喹啉、pretomanid和利奈唑胺(BPaL)组成的6 - 9个月方案治疗耐多药结核病和额外氟喹诺酮耐药患者的有效性和安全性;3)使用贝达喹啉作为>6个月较长疗程的一部分;4)同时使用贝达喹啉和delamanid作为长期治疗方案的一部分。此外,关于怀孕期间使用贝达喹啉的新证据补充了四个PICO问题的评估证据。在GDG面对面会议之前,GDG成员对这些PICO问题的所有相关结果进行了评分(表2).2020年指南更新的范围不包括耐药结核病规划管理方面,自2019年发布上一版指南以来,这些方面没有出现实质性的新证据[7].
分析和审查证据
针对每个PICO问题的分析方法编制了详细的统计分析计划。进行了描述性分析,以确定人口特征,并提供有关匹配和调整所需变量的信息。然后,使用精确匹配和基于几个变量(协变量)的倾向分数匹配的组合来最小化偏差和混淆。评估干预组和比较组内匹配协变量的分布,以确定匹配过程的保真度。基于纳入研究和数据集的汇总数据的比较,使用逻辑回归和二项回归计算绝对和相对效应估计值及其95%置信区间。
根据分析结果,使用GRADEpro在线应用程序(www.gradepro.org).同样在GRADE证据概要中,使用以下标准评估证据质量:研究设计、偏倚风险、不精确性、不一致性、间接性、发表偏倚、效应量级、似是而非的混杂和剂量效应响应梯度[38].在制定“从证据到决策(EtD)”框架之前,GDG讨论了GRADE证据概况。这些框架记录了政府调查小组在与PICO问题有关的选定领域的判断以及所提供的证据,包括但不限于干预的理想和不理想效果;平衡:这些影响的平衡;证据:证据的确定性;干预对资源利用、公平性、可行性和可接受性的影响;以及人们对利益结果的评价。此外,EtD框架对GDG讨论的内容进行了叙述性总结,对GDG的判断进行了解释性注释,并对每项建议的措辞和强度进行了描述,以及任何随附备注[7].GRADE证据表和EtD框架全文载于指南附件[37].
证据和分析总结
PICO问题:在耐多药/耐多药结核病患者中,与符合世卫组织指南的其他方案相比,持续9-12个月并包括贝达喹啉的全口服治疗方案是否安全改善预后?
对较短的含贝达喹啉全口服方案进行审查的证据来自南非电子耐药结核病登记册(www.edrweb.net).2017年1月至6月期间,有152例MDR/RR-TB患者随时开始结核病治疗,其中891例接受含贝达喹啉的全口服短疗程治疗的患者被纳入初步分析。这些数据与987例接受较短方案(包括注射药物)治疗的患者进行了比较;1437例患者接受符合世卫组织2016年指南更新中先前建议的较长疗程治疗[19];474名患者接受了包括贝达喹啉和其他药物在内的较长疗程的治疗。比较数据来自个体患者数据集(IPD),其中包括来自38个国家55个不同研究/中心的13273个个体患者记录。
分析表明,在MDR/RR-TB患者中使用含贝达喹啉的全口服短疗程与更高的治疗成功率(73%)相关与与接受包括注射在内的标准化短期方案的组相比,降低了60%)。该比较的校正比值比(aOR)为2.1 (95% CI 1.1-4.0)与失败/复发的总和;1.6 (95% CI 1.2-2.1)为成功与死亡;1.7 (95% CI 1.3-2.2)表示成功与合并失败/复发和死亡;1.9 (95% CI 1.6-2.4)为成功与所有不利结果加在一起(即。失败/复发/死亡和失去随访)。在接受贝达喹啉作为短期治疗方案一部分的组中,随访损失率低于接受含有注射药物的短期治疗方案的组(9.9%)与17.3%;aOR 0.5, 95% CI 0.4-0.7)。
PICO问题:在广泛耐药结核病患者或治疗不耐受或耐多药结核病无反应的患者中,与符合世卫组织指南的其他方案相比,由贝达喹啉、pretomanid和利奈唑胺组成的持续6-9个月的治疗方案能否安全地改善预后?
支持这个PICO问题的证据来自于Nix-TB研究[39],该研究的总研究人群为109例患者。一名患者撤回参与研究的知情同意,此人被纳入安全性分析,但未纳入有效性分析。这些数据与来自IPD的数据子集进行了比较。对于主要分析,比较组包括接受较长治疗方案(平均治疗时间为21.0-25.5个月)的IPD患者,他们同时接受贝达喹啉和利奈唑胺作为方案的一部分(IPD中没有患者接受前托马尼)。该对照组包括研究中报告的456名患者的数据,包括来自白俄罗斯、印度、法国、俄罗斯、中国、韩国、菲律宾、泰国、俄罗斯和南非的患者。
总的来说,当比较治疗成功时与在失败或复发的情况下,Nix-TB研究的治疗成功率为97.0%,而比较组为91.7%。用于治疗成功的比较与在Nix-TB研究中,治疗成功率为93.2%,而比较组为91.9%。用于治疗成功的比较与失败,复发,死亡和治疗成功与在所有不利结果中,干预组和比较组中治疗成功的患者比例为90.5%与84.8%, 88.9%与82.2%,分别。基于这些数据,初步分析得出治疗成功的aORs为3.3与失败或复发(95% CI 0.8-13.7);成功1.0与死亡(95%可信区间0.1-8.2);1.8成功与失败或复发或死亡(95% CI 0.7-4.4);成功则是1.2与所有不良结果(95% CI 0.5-3.1)。干预组(BPaL)失去随访的患者比例(1.8%)低于对照组(3.1%)。
关于不良事件,在Nix-TB研究的109例患者中,28例(25.7%)经历了至少一次严重不良事件。这包括一例与急性出血性胰腺炎相关的死亡(0.9%),29例(26.6%)其他严重不良事件,包括住院和危及生命的事件,以及2例(1.8%)导致持续或严重残疾或丧失能力的不良事件。共有53例(49%)患者经历了至少一次被认为与研究药物相关的3-4级不良事件;其中包括25例周围神经病变(11例缓解),16例肝转氨酶升高(13例缓解),9例血液不良事件(全部缓解),8例胰酶升高(7例缓解),2例视神经炎(均缓解)。来自临床前和早期临床数据的独立审查的信息描述,在高于人类使用的暴露时观察到安全信号;然而,值得注意的安全信号包括肝毒性(在啮齿动物中观察到高剂量,在猴子中观察到低剂量时,肝细胞肥大、转氨酶升高和肝脏重量增加)和雄性的生殖毒性,在动物(小鼠和猿猴)模型中观察到,这似乎是时间和剂量依赖的。
PICO问题:在耐多药/耐多药结核病患者中,与贝达喹啉治疗>6个月相比,含有贝达喹啉治疗>6个月的治疗方案作为符合世卫组织指南的较长治疗方案的一部分,能否安全改善预后?
对于这个PICO问题,数据来自EndTB观察性研究[40],整体数据集包括来自13个国家的1094名患者[40].这些国家是亚美尼亚、孟加拉国、白俄罗斯、朝鲜民主主义人民共和国、埃塞俄比亚、格鲁吉亚、印度尼西亚、哈萨克斯坦、肯尼亚、莱索托、缅甸、巴基斯坦和秘鲁。在符合纳入标准的515份记录中,242例接受贝达喹啉治疗>203天的患者构成干预组。他们与来自EndTB观察研究的273名患者进行了比较,这些患者总共接受了168到203天的贝达喹啉治疗。在EndTB观察性研究中,所有患者使用贝达喹啉的联运低谷期为203天,因此选择203天作为截止日期。值得注意的是,截止日期不是确切的6个月,而是203天。
分析得出治疗成功的aORs为1.5 (95% CI 0.7-2.7)与失败;0.8 (95% CI 0.2-0.4)表示治疗成功与死亡;1.0 (95% CI 0.5-1.7)表示治疗成功与失败/死亡;0.8 (95% CI 0.5-1.2)表示治疗成功与都是不利的结果。由于无法应用预定义的分析方法,在用于评估>6个月贝达喹啉使用PICO问题的数据中有很大可能存在残留混淆。该研究中来自患者群体的现有数据不允许外推到所有MDR/RR-TB患者的常规使用。这就排除了对6个月以上使用贝达喹啉的疗效或有效性的正式建议。然而,证据支持6个月以上接受适当基线计划和后续药物不良反应监测和管理的患者使用贝达喹啉是安全的。
PICO问题:在耐多药/耐多药结核病患者中,与其他符合世卫组织指南的治疗方案相比,同时使用贝达喹啉和德拉马尼是否能安全地改善结果?
对于最后一个PICO问题,数据来自于EndTB观察研究中的同一队列患者[41],告知PICO关于6个月后贝达喹啉使用的问题。然而,在这个数据集中,只有92例患者在任何一段时间内同时使用这两种药物,更少的患者在治疗的第一个月结束时同时使用贝达喹啉和delamanid (n=38)。另一个数据来源包括100名在印度孟买接受贝达喹啉治疗的患者(来自Médecins Sans Frontières-supported项目)。因此,总干预人群包括84例患者;38例来自EndTB观察性研究队列,46例来自孟买数据集。主要对照组包括401例患者(n=302来自EndTB观察性研究),99例患者来自另外两个数据集(n=82来自白俄罗斯共和国提供的数据集,另外17例患者的数据来自乌兹别克斯坦共和国共享)。
分析得出治疗成功的aORs为1.6 (95% CI 0.5-5.4)与治疗失败;0.8 (95% CI 0.3-2.1)表示治疗成功与死亡;1.2 (95% CI 0.6-2.5)表示治疗成功与失败/死亡;治疗成功为0.6 (95% CI 0.3-1.1)与都是不利的结果。关于不良事件,在EndTB观察性研究中,在治疗期间接受贝达喹啉同时伴有delamanid的92例患者中(总暴露量为1095人-月),发生了2例贝达喹啉相关不良事件和3例delamanid相关不良事件(总暴露率为0.46 / 100人-月,其中2例为严重事件)。这一比率与单独接受贝达喹啉和单独接受德拉马尼的人的比率相当(分别为每100人-月接触0.41和0.68)。在同时接受贝达喹啉和德拉曼尼治疗的患者中,没有发生致命的药物相关不良事件,1例患者使用弗里德里西亚公式(QTcF)校正了3级QT间期延长。
提供的其他数据包括来自Delamanid Bedaquiline用于耐药结核病(DELIBERATE)试验的安全性数据(艾滋病临床试验组A5343) [42].在这项随机对照试验中,在随机使用贝达喹啉(n=28)、delamanid (n=27)或两种药物(n=27)的患者中,治疗时QTcF较基线的变化分别为11.9 ms、8.6 ms和20.7 ms [42].在接受两种药物治疗的27例患者中,10例(37.0%)发生了1级QT不良事件,而2例(7.4%)患者经历了2级QT不良事件,与贝达喹啉组和delamanid组的患者相当(分别有32.0%和41.0%的患者经历了1级QT不良事件,3.6%和7.4%的患者经历了2级QT不良事件)。在DELIBERATE试验中,1级QT不良事件被分为绝对QTcF >480 ms,≤500 ms,从基线到>0 ms, QTcF≤30 ms或绝对QTcF≤480 ms,从基线到>30 ms,≤60 ms。2级QT不良事件分为绝对QTcF >480 ms,≤500 ms,与基线相比,>30 ms,≤60 ms;或绝对QTcF≤480 ms,与基线相比,>60 ms。3级QT不良事件被分类为绝对QTcF >500 ms或绝对QTcF >480 ms, QTcF从基线>改变60 ms,而4级QT不良事件是危及生命的后果,例如尖扭转或其他相关的严重室性心律失常[42].QTcF延长>500 ms是罕见的,仅在1例患者中发生,没有患者出现3级或4级QT不良事件[42].
没有足够的证据来评估贝达喹啉和德拉马尼联合使用的疗效或有效性。这些数据并不有助于对次要比较器进行有意义的分析(仅扩展使用delamanid),因为种群差异太大,无法进行通常进行的匹配。这就排除了对贝达喹啉和德拉马尼合用的疗效或有效性的正式建议。然而,数据表明贝达喹啉和delamanid同时使用没有额外的安全问题。因此,贝达喹啉和德拉曼尼可以同时用于其他治疗选择有限的患者,即。对于在其治疗方案中包含少量其他有效药物的患者,可能是由于广泛的耐药情况或对其他二线结核病药物不耐受。对这些患者应制定适当的安全监测计划(在基线和整个治疗期间),包括心电图和电解质监测,临床医生应认识到方案中有可能延长QT间期或引起其他潜在不良事件的其他药物。
额外的操作问题:贝达喹啉在怀孕期间的使用
回顾了南非一项关于怀孕期间贝达喹啉使用的队列研究的其他数据[43].这项研究包括2013年1月至2017年12月期间从南非一家耐多药/耐多药结核病转诊医院招募的108名耐多药结核病孕妇的信息[43].58名妇女接受了贝达喹啉作为耐多药/耐多药结核病方案的一部分,并与50名没有服用贝达喹啉的妇女进行了比较。在这项研究中,妇女生下109名活婴,其中49名接触过贝达喹啉在子宫内60人没有接触贝达喹啉在子宫内.
关于怀孕期间接触贝大喹啉,队列研究的结果表明,比较宫内接触贝大喹啉的婴儿在出生或妊娠结局方面没有统计学上的显著差异与未接触此种物质者(出生结局p=0.741,妊娠结局p=0.312) [43].在所有评估的妊娠和婴儿结局中,只有低出生体重与贝达喹啉暴露有关在子宫内(45%与26%, p = 0.034)。然而,不可能最终将这种影响归因于贝达喹啉,需要更多的调查来探索这种关系[43].出生后婴儿生长没有显著差异(在对86名婴儿进行前瞻性随访的亚分析中(41名暴露于贝达喹啉在子宫内45个未暴露)[43].此外,贝达喹啉对孕妇的治疗效果有利与而不是那些暴露的人(治疗成功率71%与62%, p=0.349) [43].
阿米卡星,链霉素,原硫酰胺和乙硫酰胺在怀孕期间通常是禁忌的。根据南非提供的新证据,胎儿接触贝达喹啉在子宫内与低出生体重有关[43].然而,在婴儿结局、妊娠结局或产妇治疗结局(包括1岁前婴儿体重增加)方面没有其他显著差异[43].在这种情况下,建议对较长的方案进行个体化,以包括已经很好地建立了安全特性的成分。治疗和妊娠的结果,包括产后对先天性异常的监测数据应予以记录,以帮助为今后在妊娠期间治疗耐多药结核病的建议提供依据。
建议及备注
用于治疗耐多药/耐多药结核病和广泛耐药(XDR)结核病的药物分组作为较长治疗方案的一部分,此前已根据2018年全球药物专家组的讨论进行了修订,这一药物分组在当前更新中保持不变[7].这些药物及其分组载于表3[7].世卫组织认为,在规划条件下,只有本表中的药物与耐多药/耐多药结核病治疗方案相关。下文提供了针对耐多药/耐多药结核的较短的含贝达喹啉全口服方案和针对耐多药结核伴氟喹诺酮耐药的BPaL方案的新建议。其他关于在较长治疗方案中使用的药物、较长治疗方案的持续时间和监测、多药耐药/多药耐药结核病的手术使用、艾滋病毒感染者在结核病治疗期间使用抗逆转录病毒药物以及患者支持的建议保持不变,并在世卫组织2020年发布的最新指南中转载,以便世卫组织关于多药耐药/多药耐药结核病治疗的所有建议都在一份文件中[7].
2019年为解决含贝达喹啉的较短全口服方案和BPaL方案的PICO问题而审查的证据的确定性被评为非常低,GDG提出的两个新建议都被评为有条件的(表4).对于贝达喹啉的使用>6个月疗程,贝达喹啉和delamanid一起使用或怀孕期间使用贝达喹啉没有正式的建议;然而,GDG能够就它们的安全使用做出一些声明。
更短的耐多药/耐多药结核病全口服贝达喹啉方案
对于符合条件的确诊耐多药/耐多药结核病患者,建议采用为期9-12个月的更短的、全口服、含贝达喹啉的方案,这些患者未接受该方案中使用的二线结核病药物治疗1个月且已排除对氟喹诺酮类药物的耐药性(有条件推荐,证据的确定性非常低)。
该建议的证据回顾集中在较短的方案,其中注射药物被贝达喹啉(使用6个月)取代,联合左氧氟沙星或莫西沙星、乙硫胺、乙胺丁醇、异烟肼(高剂量)、吡嗪酰胺和氯法齐明4个月(如果患者在4个月结束时痰涂片仍呈阳性,则可能延长至6个月);随后用左氧氟沙星或莫西沙星、氯法齐明、乙胺丁醇和吡嗪酰胺治疗5个月。在考虑了患者的偏好和临床判断后,该方案可以成为以下所有患者的首选方案:确诊的MDR/RR-TB(至少确诊对利福平耐药),排除对氟喹诺酮类药物耐药,以前接受二线药物治疗不超过1个月,没有广泛的结核疾病和没有严重的肺外结核。广泛(或晚期)结核病的定义是胸片上存在双侧空腔疾病或广泛的实质损伤。在年龄<15岁的儿童中,晚期疾病通常通过胸片上的空洞或双侧疾病来定义。严重肺外结核的定义是存在粟粒性结核或结核性脑膜炎。在年龄<15岁的儿童中,除淋巴结病以外的肺外疾病(周围淋巴结或孤立的纵隔肿块,无压迫)被认为是严重的(改编自[44])。审查的证据支持在患者亚组中使用该方案,如艾滋病毒感染者(见[7])。实施该方案需要对氟喹诺酮类药物进行快速药敏试验(DST)。
BPaL方案用于耐多药结核病伴氟喹诺酮耐药
由贝达喹啉、普莱托马尼和利奈唑胺(BPaL)组成的持续6-9个月的治疗方案可在操作研究条件下用于耐氟喹诺酮类结核病的耐多药结核病患者,这些患者之前没有接触过贝达喹啉和利奈唑胺2周(有条件推荐,效果估计的确定性非常低)。
BPaL方案在南非广泛耐药结核病患者中使用时显示了较高的治疗成功率,与接受贝达喹啉和利奈唑胺较长时间方案的患者相比,使用该方案可获得显著的额外有利治疗结果。然而,对于不良事件的可能性和严重程度、临床前数据中可能的生殖毒性信号、研究设计的局限性以及证据的总体确定性非常低,仍存在重要的剩余担忧。
BPaL方案(用于Nix-TB研究)[39在获得更多关于有效性和安全性的证据之前,可能不会考虑在全球范围内进行常规规划使用。然而,对于无法根据现有世卫组织建议设计有效方案的个别患者,BPaL方案可作为现行伦理标准下的最后手段。
审查的证据支持在某些患者亚群中使用该方案,如艾滋病毒感染者(见[7])。
的所有建议的摘要世卫组织结核病综合指南,模块4:耐药结核病治疗与之前的指导方针相比,突出显示变化,包括在表5.
讨论
世卫组织耐药结核病治疗指南2020年修订版标志着全球参与耐药结核病患者治疗的国家结核病规划和其他组织将发生重大变化。标准化的全口服含贝达喹啉的短期方案是符合条件的患者的首选治疗方案。一些患者亚组,如结核病孕妇(对其禁用乙硫胺)、以前接触过该方案中使用的药物的患者或广泛结核病患者或严重肺外结核病患者不符合较短方案的条件,需要开始使用A、B和c组推荐药物的层次结构组成的全口服较长方案。这占全球所有耐多药/耐多药结核病患者的五分之一,除非他们参加了提供BPaL方案的运筹学研究,否则他们将需要更长的治疗方案。这两项新建议的证据的极低确定性加强了未来对耐多药结核病治疗方案的研究的重要性,不仅是对BPaL,而且对其他方案,包括对所推荐的短期方案的任何修改。
这些建议强调了国家结核病规划若干方面的重要性,这些规划需要良好运作,以便有效地诊断和治疗耐多药/耐多药结核病。其中包括可获得有质量保证的诊断、药物分级检测、获得耐药、交叉耐药、药物安全主动监测和管理以及对患者的社会支持[16,45].目前,为了诊断耐多药/耐多药结核病,世卫组织建议将快速分子检测作为诊断肺结核和同时检测利福平耐药的初步检测方法[46].世卫组织最新指南还支持在肺外结核和结核病儿童的诊断工作中使用分子诊断学(特别是在胃标本、鼻咽标本和粪便标本中)[46].此外,世卫组织建议,对于确诊的耐多药/耐多药结核病患者,可使用二线探针试验作为初步试验,而不是基于表型培养的DST,以检测对氟喹诺酮类药物的耐药性[47].检测氟喹诺酮类药物的耐药性对于推出较短的方案至关重要,因为它含有氟喹诺酮类药物,预防对该方案中其他药物的耐药性至关重要。此外,DST对于确保较长疗程由针对特定患者的最有效药物组成,以及防止扩大对其他有效的新型抗结核药物的耐药性也很重要。至关重要的是,患者能够获得正在使用的药物的可靠DST,各国将这些药物纳入其监测计划,最终,实验室能够对贝达喹啉和利奈唑胺等药物进行快速DST,从现在开始,这些药物可能在耐多药结核病治疗方案中更加突出。实验室进行DST能力不足的国家(特别是氟喹诺酮类药物)应优先加强这种能力。尽管需要进一步加强新推荐方案中某些药物的DST,但世卫组织2017年的一次技术磋商确定了氟喹诺酮类药物、贝达喹啉、德拉马尼、氯法齐明和利奈唑胺的敏感性试验临界浓度[48].一些国家可能有更先进的实验室方法,如下一代或全基因组测序,但并非全球所有国家结核病规划都能广泛使用。然而,关于某些药物耐药流行情况的国家数据,包括通过定向测序或全基因组测序获得的数据,可能有助于指导治疗政策。预防获得这种耐药也是至关重要的,同样重要的还有aDSM的实施[49].
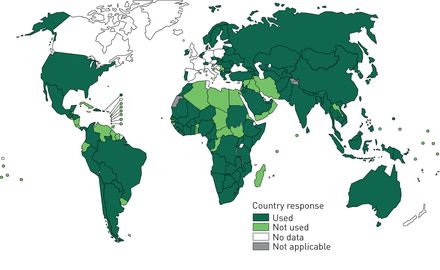
在将新的抗结核药物和新的耐多药结核病方案引入国家结核病规划的背景下,建议采用抗多药疗法。总体目标是“减少耐药结核病二线治疗患者的药物相关伤害风险,并生成标准化的aDSM数据,以便为未来有关使用此类药物的政策更新提供信息”[49].鼓励更多地采用aDSM,因为较短和较长的方案现在包含贝达喹啉[50].根据世卫组织可获得的最新数据(186个国家于2020年报告),截至2019年底,109个国家(占报告国家的59%)已将贝达喹啉用于耐多药/广泛耐药结核病的治疗,作为扩大获取、同情使用或在正常规划条件下的一部分(图1).患者支持一直是几种较短和较长方案的一个特点,并继续是耐多药结核病治疗的一个重要组成部分。关于患者社会支持的建议也是世卫组织新指南的一部分[7].
到2019年底,将贝达喹啉作为扩大获取、同情使用或在正常规划条件下用于耐多药/广泛耐药结核病治疗的国家。
GDG在2019年11月确定的研究差距反映了目前对较短方案和BPaL方案的知识差距(表6) [7].需要进一步研究更短的耐多药结核病治疗方案的变体的有效性和安全性,以及总治疗时间减少到≤6个月的情况。南非国家结核病规划最近进一步修改了较短的方案,包括利奈唑胺而不是乙硫胺[51],这种改良方案和其他正在研究的结果可能有助于为未来的政策提供信息。此外,比较短期方案的这些变体的有效性将有助于先前研究中排除的特定患者亚组,如儿童、额外耐药患者、肺外结核患者或广泛结核患者、孕妇和哺乳妇女或对氟喹诺酮类药物和二线注射药物以外的药物背景耐药较高的环境(如。吡嗪酰胺或高水平异烟肼抗性)。总的来说,仍然需要进行更多的高质量研究,包括操作研究和随机对照试验,以便比较全口服短时间方案和全口服长时间方案,并提供更多关于在南非以外地区使用全口服短时间方案的数据。贝达喹啉抗性获得的频率和机制是另一个重要的研究重点。对于BPaL方案,目前的建议以其在运筹学条件下的实施为条件。因此,南非以外的其他区域和国家将需要对BPaL方案的实施进行更多的研究。由于pretomanid是一种新的化合物[52],重要的是要描述瘤前耐药的机制和分子标记,并记录其完整的不良事件概况,重点是人类的肝毒性和生殖毒性。治疗后随访的更多数据有望获得,这对了解较短治疗方案的疗效很重要。此外,在Nix-TB研究中,近三分之一的患者由于不良事件而提前停用利奈唑胺,这强调了在耐药结核病方案中使用利奈唑胺的最佳剂量和持续时间需要进一步研究[39].ZeNix的研究目前正在解决这些问题,它将提供重要的新信息,以帮助指导利奈唑胺在未来的剂量(clinicaltrials.gov标识符号码NCT03086486).其中包括GDG确定的研究重点概要表5.
为了促进对耐多药/耐多药结核病治疗方案的进一步研究,热带病研究和培训特别规划和世卫组织启动了ShORRT(耐利福平结核病的全口服短期治疗方案),这是一项业务研究包,用于评估对耐多药/耐多药结核病成人和儿童使用全口服短期治疗方案的有效性、安全性、可行性、可接受性、成本和影响(包括对与健康相关的生活质量)[53].该一揽子方案促进对有无氟喹诺酮耐药的耐多药结核病患者的短期方案的研究,包括包含贝达喹啉和利奈唑胺的全口服短期方案和BPaL方案[53].
与实施这些新方案有关的其他问题对于国家结核病规划和参与耐药结核病规划管理的其他利益攸关方将是重要的。国家结核病规划应计划尽快过渡到新的方案,消除对注射药物的需要;它们还应努力改善贝达喹啉等新药的公平获得。通过全球基金为其国家结核病规划获得资金的国家将能够将这些更新的方案纳入资金申请,目前正在开展宣传工作,以降低贝达喹啉等某些药物的成本。贝达喹啉目前在较短和较长方案以及BPaL方案中均有使用。利益相关者还应意识到,随着新的证据的出现,未来可能会对方案进行进一步的改变。
此外,虽然将世卫组织耐药结核病治疗指南与美国胸科学会(ATS)/疾病控制和预防中心(CDC)/欧洲呼吸学会(ERS)/美国传染病学会(IDSA)发布的临床实践指南进行比较时,这些建议主要是一致的,但也存在一些差异[188bet官网地址54].这些差异并不显著,并在临床实践指南中进行了完整的总结,因此在此不进行复制[54].虽然两个指南使用了类似的方法、证据和GRADE应用,但差异可以解释为以下事实:世卫组织指南基于一个经过修改的数据集,该数据集扩展了用于ATS/CDC/ERS/IDSA临床实践指南的数据集,其中包括来自南非的一个相对较大的数据集[54].两份指南使用的数据集有很大重叠,但并不完全相同[54].此外,世卫组织准则的目标受众是全球性的,与ATS/疾控中心/ERS/IDSA和其他准则相比,适用于流行程度、资源和卫生基础设施不同的情况。
限制
世卫组织的建议基于现有的最新证据,使用旨在限制混淆影响的分析,并在GRADE过程的背景下提出;然而,局限性仍然存在。短时间方案和BPaL方案的新建议都是有条件的。从患者、临床医生和决策者的角度来看,有条件的建议具有不同的意义(表4).有条件的建议通常是在可取的影响超过不可取的影响时提出的,但根据EtD框架所作的判断,存在一些不确定性[55].此外,这两项建议都是基于非常低确定性的证据,这些证据是基于许多领域进行评估的,包括不一致性、间接性和不精确性[55].这突出表明需要更多关于耐药结核病治疗方案的高质量证据,包括来自试验和观察数据的证据。描述证据质量的GRADE表和概述为得出建议而作出的判断的EtD框架均载于指南附件[37].此外,虽然在为决策提供信息的数据分析中已尽一切努力限制混杂的影响,但仍有可能存在残余混杂。事实上,这也是2019年GDG会议上无法就两个PICO问题提出建议的原因之一。
结论
世卫组织2020年更新的耐药结核病治疗指南根据世卫组织可获得的最新证据,就耐多药/耐多药结核病的有效治疗方案提出了新的建议[7].国家结核病规划和参与耐多药/耐多药结核病治疗的其他利益攸关方应使国家政策与这些建议保持一致,同时也应开展解决已确定的研究重点所需的重要研究。通过新的和现有的建议,并在患者支持的情况下安全及时地实施这些建议,需要各国政府、私营部门、技术伙伴、民间社会和供资机构的参与下作出政治承诺。继续迫切需要进一步的高质量研究,包括运筹研究和随机对照试验,以改善全世界耐药结核病患者的治疗结果和生活质量。
可共享的PDF
确认
这篇文章主要是复制的建议和内容世卫组织结核病综合指南,模块4:耐药结核病治疗,是根据世卫组织指南审查委员会关于收集证据、评估和制定建议的要求制定的。所有作者都参与了这些指南的制作,并参与了这篇手稿写作的不同阶段。作者感谢为指南制定小组、外部审查小组、证据评审员、世卫组织指南指导小组、世卫组织指南审查委员会、世卫组织结核病区域顾问以及为证据审查提供数据的国家规划、技术机构和结核病联盟的许多人员(完整的个人名单可在世卫组织结核病综合指南,模块4:耐药结核病治疗).
脚注
利益冲突:f·米尔扎耶夫没什么可透露的。
利益冲突:K. Viney没有什么可透露的。
利益冲突:N.N. Linh没有什么可透露的。
利益冲突:L. Gonzalez-Angulo是世卫组织工作人员,所提交的手稿是世卫组织开展的规范工作的一部分。
利益冲突:M. Gegia没有什么可透露的。
利益冲突:E. Jaramillo没有什么可透露的。
利益冲突:M. Zignol没有什么可透露的。
利益冲突:T. Kasaeva没有什么可透露的。
支持声明:在美国国际开发署(USAID)、国际药品采购机制和俄罗斯联邦的资助下,准则得以修订。美国国际开发署也是向本文涉及的世卫组织作者提供薪金支持的主要机构。没有为文章的改编、写作和提交提供具体资金,这些工作是在有关作者的正常工作过程中完成的。本文的资助信息已存入交叉参考基金注册.
- 收到了2020年8月28日。
- 接受2020年11月13日。
- 版权所有©作者2021
本版本根据创作共用授权协议4.0发布。