摘要gydF4y2Ba
特发性肺纤维化患者下气道细菌负荷增加,导致疾病进展和死亡风险增加。然而,尚不清楚这种增加的细菌负担是否直接影响纤维化的进展或仅仅反映了潜在疾病的程度或严重程度。gydF4y2Ba
我们前瞻性地招募了193例接受支气管镜检查并接受特发性肺纤维化多学科诊断的患者。采用16S rRNA基因qPCR法定量测定支气管肺泡灌洗液细菌总负荷。影像学由两名阅读者独立评估,对影像学变化的程度、严重程度和地形进行定量评分,并评估这些特征与细菌负荷的关系。gydF4y2Ba
细菌负担增加与疾病进展显著相关(HR 2.1;95% ci 1.287-3.474;p = 0.0028)。多元逐步回归显示细菌负荷与放射学特征或疾病程度没有关系。当特别考虑明确或可能为常见性间质性肺炎的患者时,两组之间的细菌负担没有差异。尽管假定胸膜实质纤维弹性增生与临床感染之间存在关联,但胸膜实质纤维弹性增生的存在或程度与细菌负荷之间没有关系。gydF4y2Ba
我们证明,在特发性肺纤维化中,下气道的细菌负担不仅仅是继发于肺实质的潜在建筑破坏程度。这种关联的独立性支持了与潜在致病机制的关系,并强调了功能研究的迫切需要。gydF4y2Ba
摘要gydF4y2Ba
升高的细菌负担预示着IPF的死亡率,并且与放射学特征和疾病程度无关gydF4y2Bahttp://bit.ly/2RaDbdvgydF4y2Ba
介绍gydF4y2Ba
特发性肺纤维化(IPF)的发病率持续上升,相关死亡率的负担也在增加[gydF4y2Ba1gydF4y2Ba].虽然对其发病机制的精确理解仍然难以捉摸,但越来越多的人认识到肺和环境之间的相互作用在IPF发展中的重要性[gydF4y2Ba2gydF4y2Ba- - - - - -gydF4y2Ba4gydF4y2Ba].在过去的十年中,我们对下气道中动态和复杂的细菌群落(微生物组)及其在健康和疾病中的作用的了解急剧增加[gydF4y2Ba5gydF4y2Ba].虽然从历史上看,感染不被认为是IPF的主要驱动因素,但现在很清楚,感染发作与疾病急性加重具有相同的毁灭性死亡率[gydF4y2Ba3.gydF4y2Ba,gydF4y2Ba6gydF4y2Ba].此外,即使在诊断和没有感染的情况下,IPF患者下呼吸道的细菌负荷也会急剧增加,呼吸道微生物组的组成也会改变[gydF4y2Ba7gydF4y2Ba,gydF4y2Ba8gydF4y2Ba].gydF4y2Ba
我们和其他人在比较健康个体和IPF患者以及比较稳定或进行性IPF患者时,强调了微生物组多样性和个体细菌水平的差异。已经确定了微生物群落组成部分与细胞因子、外周血转录组谱和疾病行为之间的许多关联[gydF4y2Ba9gydF4y2Ba,gydF4y2Ba10gydF4y2Ba].最近,动物模型已经开始梳理出下气道生态失调导致纤维化的机制[gydF4y2Ba11gydF4y2Ba].IPF中最有效的微生物信号是下气道细菌负荷信号。在诊断时,IPF患者的细菌负担高于健康个体和慢性阻塞性肺疾病患者。重要的是,在IPF受试者中,细菌负荷水平与生存有关,并在培养阴性急性加重期间进一步增加[gydF4y2Ba12gydF4y2Ba].gydF4y2Ba
目前尚不清楚细菌负担是否直接影响纤维化的进展,或者细菌数量是否反映了其他潜在的疾病过程。虽然以前的研究使用生理参数(包括用力肺活量(FVC))和气体传递测量(肺对一氧化碳的扩散能力)来解释疾病的严重程度。gydF4y2BaDgydF4y2BaLCOgydF4y2Ba)),没有评估细菌负荷与肺纤维化变形的放射标志物或疾病程度或严重程度之间的关系。我们假设,如果细菌负荷是继发于肺实质的潜在建筑破坏,那么在IPF患者的下气道中,诸如蜂窝状或牵引性支气管扩张等影像学表现与细菌负荷之间可能存在明确的关联。gydF4y2Ba
方法gydF4y2Ba
病人招聘gydF4y2Ba
在2015年11月至2017年1月期间,前瞻性招募了疑似IPF的诊断性支气管镜检查和支气管肺泡灌洗(BAL)患者。仅纳入根据现行美国胸科协会(ATS)/欧洲呼吸学会(ERS)/日本呼吸学会(JRS)/拉丁美洲胸科协会(ALAT)指南定义接受IPF多学科团队诊断(MDT)的受试者[188bet官网地址gydF4y2Ba13gydF4y2Ba].如果受试者有自我报告的上呼吸道或下呼吸道感染史、前3个月使用过抗生素、IPF急性加重或其他呼吸系统疾病,则排除受试者。所有受试者都获得了书面知情同意,该研究得到了当地研究伦理委员会(10/HO720/12和15/SC/0101)的批准。gydF4y2Ba
支气管镜检查gydF4y2Ba
行纤维支气管镜BAL检查gydF4y2Ba通过gydF4y2Ba如前所述的口咽途径[gydF4y2Ba7gydF4y2Ba].简单地说,将60ml等分温盐水分别灌注到右中叶的一段,总容积为240ml。采集后,将部分未经过滤和处理的BAL立即放在冰上,快速冷冻并保存在- 80°C。阴性对照样本在使用前通过支气管镜吸入通道吸入缓冲盐水。巨噬细胞、淋巴细胞、中性粒细胞和嗜酸性粒细胞的细胞分化如前所述[gydF4y2Ba14gydF4y2Ba].gydF4y2Ba
放射学gydF4y2Ba
CT变量定义基于Fleischner术语表[gydF4y2Ba15gydF4y2Ba]和现行ATS/ERS/JRS/ALAT指南定义[gydF4y2Ba13gydF4y2Ba].计算机断层扫描(CT)数据使用以下评分标准进行评分:每肺叶最接近5%(纤维化,蜂窝状),在二元基础上(通常间质性肺炎(UIP)),在肺叶范围内将语言定义为第六肺叶(胸膜实质纤维弹性增生(PPFE)) [gydF4y2Ba16gydF4y2Ba]和18分制(牵引性支气管扩张)[gydF4y2Ba17gydF4y2Ba].gydF4y2Ba
细菌DNA提取gydF4y2Ba
BAL样品(2 mL)在21 000×下离心gydF4y2BaggydF4y2Ba使细胞碎片和细菌成粒30分钟。将微球重悬于100 μL上清液中,加入含有500 μL十六烷基三甲基溴化铵(CTAB)缓冲液(10% w/v CTAB在0.5 M磷酸盐缓冲NaCl中)和500 μL苯酚:氯仿:异戊醇(25:24:1)的裂解基质E管(MP Biomedicals, OH, USA),在FastPrep仪器(MP Biomedicals)中振荡5.5 msgydF4y2Ba−1gydF4y2Ba60年代。打珠后,用等体积的氯仿:异戊醇(24:1)提取样品,用2体积的沉淀液(30% w/v PEG6000在NaCl中)沉淀DNA,乙醇洗涤后用100 μL Tris-EDTA重悬。使用NanoDrop 1000分光光度计(Thermo Fisher Scientific, Hemel Hempstead, UK)测量分离DNA的质量和数量,并将DNA保存在- 80°C以待进一步使用。gydF4y2Ba
16S rRNA基因定量PCRgydF4y2Ba
建立了3个10 μL的定量pcr (qPCR),其中含有1 μL细菌DNA和9 μL Femto细菌qPCR预混物(Cambridge bioscience, Cambridge, UK)。每次运行包含10倍稀释系列gydF4y2Ba营养弧菌DSM 759gydF4y2Ba克隆到已知大小和非模板控制的质粒中的基因。数据采集采用以下循环参数:1次95℃循环10min;40次循环,95°C 30秒,50°C 30秒,72°C 1分钟;72°C 1次循环7分钟[gydF4y2Ba18gydF4y2Ba].gydF4y2Ba
统计分析gydF4y2Ba
连续变量以平均值±表示gydF4y2BasdgydF4y2Ba分类变量是比例。使用Kaplan-Meier方法计算时间-事件曲线,并与使用log-rank检验进行比较。使用连续变量的Mann-Whitney检验和分类变量的Fisher精确检验来评估受试者组之间的差异。斯皮尔曼的gydF4y2BaρgydF4y2Ba用于计算连续变量之间的相关性。用相关系数评价预测变量的共线性。发现细菌负荷数据偏斜,并进行对数变换。转化后的细菌负荷数据采用单变量和逐步多元线性回归模型对CT特征和细胞差异进行检验。所有分析均使用R [gydF4y2Ba19gydF4y2Ba].双侧p值<0.05认为具有统计学意义。gydF4y2Ba
结果gydF4y2Ba
研究对象和抽样gydF4y2Ba
在2014年至2017年期间,前瞻性招募了193名接受诊断性支气管镜检查的受试者,最终进行了IPF MDT。19名受试者接受了冷冻或手术肺活检,MDT在进行诊断时可以获得这些信息。反映IPF的人口统计数据,该队列主要是男性,平均年龄为70岁,有明显的吸烟史(gydF4y2Ba表1gydF4y2Ba).在本研究纳入的193例患者中,107例伴有胃食管反流(GORD)(定义为自我报告的症状或无症状使用质子泵抑制剂(PPI))。共97例患者接受抗反流治疗。36名受试者在支气管镜检查时接受吸入糖皮质激素治疗,21名受试者口服糖皮质激素治疗(<10 mg·d)gydF4y2Ba−1gydF4y2Ba) (gydF4y2Ba补充表S1gydF4y2Ba).gydF4y2Ba
特发性肺纤维化患者的临床和影像学特征gydF4y2Ba
细菌负担预测IPF的死亡率gydF4y2Ba
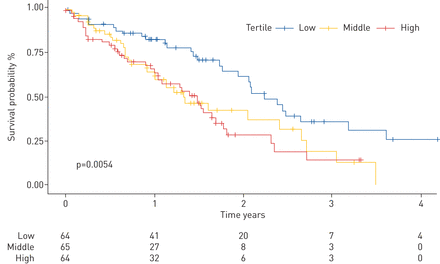
成功地从所有受试者中提取细菌DNA,并使用qPCR进行定量。平均细菌负荷为2.87×10gydF4y2Ba5gydF4y2Ba(±1.63×10gydF4y2Ba6gydF4y2Ba)每mL BAL中有16S rRNA基因拷贝数。与历史对照相比,这一数字有所上升,与之前公布的负担相似[gydF4y2Ba11gydF4y2Ba].技术对照(通过支气管镜工作通道冲洗生理盐水)如预期的那样,显示计数接近或低于qPCR定量下限(100拷贝·mL)gydF4y2Ba−1gydF4y2Ba) (gydF4y2Ba补充图S1gydF4y2Ba).为了证实细菌负担与疾病进展之间的关联,采用了第一年全因死亡率或12个月时FVC下降10%或更多的复合终点。102例患者符合进展性疾病的标准。使用未调整的Cox比例风险模型,细菌负担与疾病进展显著相关(HR 1.20;95% ci 1.06-1.35gydF4y2Ba;gydF4y2Bap = 0.0034)。在调整了年龄、性别、预测FVC的基线%和预测FVC的基线%后,这种关联仍然显著gydF4y2BaDgydF4y2BaLCOgydF4y2Ba多变量Cox比例风险模型(HR 1.16;95% ci 1.02-1.30;p = 0.0022)。一项生存分析证实,细菌负担最高的菌群中的受试者与最低菌群中的受试者相比,其危险性显著增加(HR 2.1;95% ci 1.287-3.474;p = 0.0028)。此外,与细菌负担最低的菌群相比,中等菌群的个体死亡风险也显著增加(HR 2.0;95% ci 1.197-3.307;p = 0.008) (gydF4y2Ba图1gydF4y2Ba).在细菌负荷的这些分类中,IPF患者在年龄、性别、吸烟史或疾病严重程度上没有显著差异。gydF4y2Ba
特发性肺纤维化在诊断时细菌负担增加,死亡率增加。由细菌负担分层的Cox比例风险模型生成的Kaplan-Meier曲线(低质量:4.15×10)gydF4y2Ba3.gydF4y2Ba-3.17×10gydF4y2Ba4gydF4y2Ba16S rRNA基因拷贝数·mLgydF4y2Ba−1gydF4y2Ba支气管肺泡灌洗液;中蘖:3.33×10gydF4y2Ba4gydF4y2Ba-1.90×10gydF4y2Ba5gydF4y2Ba16S rRNA基因拷贝数·mLgydF4y2Ba−1gydF4y2BaBAL流体;高质量:1.90×10gydF4y2Ba5gydF4y2Ba-5.44×10gydF4y2Ba6gydF4y2Ba16S rRNA基因拷贝数·mLgydF4y2Ba−1gydF4y2Ba拜尔港液体)。报告的Log rank p检验值。gydF4y2Ba
细菌负荷和BAL差异细胞计数gydF4y2Ba
接下来,我们研究了BAL差异细胞计数与细菌负荷的关系。正如预期的那样,这组IPF患者的BAL细胞差异显示肺泡巨噬细胞(71.3±10.86%)和中性粒细胞(9.86±7.78%)的优势(gydF4y2Ba补充图S2gydF4y2Ba).采用线性模型评估细菌负荷与BAL炎性差异细胞计数(gydF4y2Ba补充表S2gydF4y2Ba).有趣的是,细菌负荷与每mL BAL液中白细胞总数之间没有相关性(Spearman’s rho:−0.093,p=0.24)。gydF4y2Ba补充图S3gydF4y2Ba)或任何特定气道炎症细胞类型的比例(gydF4y2Ba图2gydF4y2Ba).gydF4y2Ba
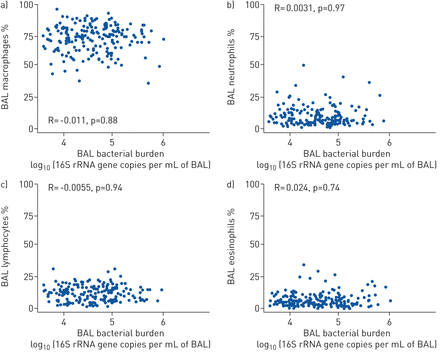
特发性肺纤维化(IPF)患者的支气管肺泡灌洗(BAL)差异细胞计数与细菌负荷无相关性。说明IPF患者BAL中细菌负荷与(a)巨噬细胞、(b)中性粒细胞、(c)淋巴细胞和(d)嗜酸性粒细胞百分比的相关性(n=193)。qPCR计算细菌负荷,以log10个16S rRNA基因拷贝数·mL表示gydF4y2Ba−1gydF4y2Ba落下帷幕。gydF4y2Ba
细菌负担与生理疾病严重程度gydF4y2Ba
然后,我们试图调查基线疾病严重程度(以FVC(预测百分比)衡量)与gydF4y2BaDgydF4y2BaLCOgydF4y2Ba(预测百分比)和细菌负荷。然而,没有相关性(FVC, %)预测:Spearman's rho: - 0.013, p=0.86;gydF4y2BaDgydF4y2BaLCOgydF4y2Ba, %预测:Spearman's rho: - 0.002 p=0.98)gydF4y2Ba补充图4gydF4y2Ba).虽然我们没有直接着手解决GORD或伴随用药的问题,但我们没有看到使用低剂量皮质类固醇、吸入类固醇或PPI对细菌负担的影响。gydF4y2Ba
细菌负担与放射疾病程度gydF4y2Ba
在整个队列中,140名受试者在支气管镜检查后4个月内进行了CT成像。从支气管镜检查到成像的中位(范围)时间为- 31(- 117-120)天。ct由两位独立的放射科医生评分[A]。Nair, B. Rawal],对所有临床数据视而不见。如果放射科医生之间b> 20%的差异(包括b>叶评分差异,牵引支气管扩张bbbb3评分或二元变量不一致),数据由第三位放射科医生仲裁[a]。Devaraj]。对于最接近5%的评分,全肺评分被定义为平均肺叶评分。在仲裁之后,放射科医生之间的平均得分被用作分析的最终得分。总体而言,放射科医生(gydF4y2Ba补充表S3gydF4y2Ba) [gydF4y2Ba20.gydF4y2Ba,gydF4y2Ba21gydF4y2Ba].根据目前的ATS/ERS/JRS/ALAT指南,超过一半的队列(57.7%)可能或明确患有UIP [gydF4y2Ba13gydF4y2Ba].21%(30 / 141)的受试者有PPFE的放射学证据,30%(43 / 141)的受试者有蜂窝(gydF4y2Ba表1gydF4y2Ba).采用多变量逐步回归方法探讨疾病严重程度的影像学指标与细菌负荷之间的关系。CT纤维化程度与CT牵引支气管扩张评分呈强共线(Spearman’s rho: 0.57),因此分别纳入模型。细菌负荷与疾病的放射程度或牵引性支气管扩张或蜂窝状程度无相关性(gydF4y2Ba表2gydF4y2Ba).当特别考虑明确或可能的UIP患者时,两组之间的细菌负担没有差异(gydF4y2Ba图3一gydF4y2Ba).此外,与不确定或可能/确定UIP的IPF患者相比,细菌负担没有差异(gydF4y2Ba补充图S5gydF4y2Ba).尽管假定PPFE与临床感染之间存在关联[gydF4y2Ba22gydF4y2Ba], PPFE的存在或程度与细菌负荷没有关系(gydF4y2Ba图3 bgydF4y2Ba).此外,当考虑到是否有蜂房时,细菌负荷没有差异(gydF4y2Ba图3 cgydF4y2Ba).gydF4y2Ba
支气管肺泡灌洗细菌负荷的影像学特征及其单因素预测gydF4y2Ba
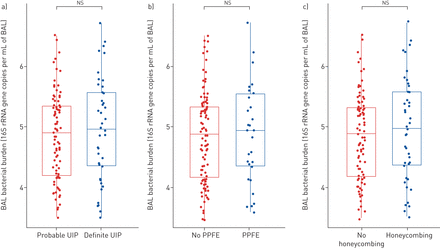
支气管肺泡灌洗(BAL)细菌负荷与影像学特征的关系。细菌负荷log10 (16S rRNA基因拷贝数·mL)无差异gydF4y2Ba−1gydF4y2Ba基于(a)通常间质性肺炎(UIP)的明确或可能的模式,(b)放射性胸膜实质纤维弹性增生(PPFE)的存在或不存在,或(c)蜂窝状的存在或不存在。采用Mann-Whitney检验进行统计学显著性检验。gydF4y2Ba
然后,我们将疾病严重程度的影像学特征纳入生存模型,以评估细菌负担是否独立于影像学特征预测生存。即使将影像学特征纳入生存模型,并对年龄、性别、预测FVC的基线百分比、预测FVC的基线百分比进行调整,细菌负担仍然是一个独立的预测因素gydF4y2BaDgydF4y2BaLCOgydF4y2Ba吸烟状况。同样,考虑到CT纤维化程度和CT牵引支气管扩张评分呈强共线(Spearman’s rho: 0.57),它们被纳入单独的模型。在这两种模型中,细菌负担仍可预测疾病进展(HR 1.16;95% ci 1.01-1.35;p = 0.04)。gydF4y2Ba
讨论gydF4y2Ba
这项研究证实了先前的发现,对于IPF患者,在诊断时增加的细菌负担会导致更差的生存率。然而,我们证明这种增加的细菌负担与疾病形态和严重程度的放射标志物无关。这项工作是迄今为止对IPF患者下气道细菌进行的最大的前瞻性研究,证实了气道细菌负担在IPF中的重要性。此外,与疾病严重程度和肺纤维化破坏的测量缺乏相关性表明,细菌负荷的变化与疾病有关,不太可能仅仅继发于结构扭曲。gydF4y2Ba
纤维化肺病的许多矛盾之一是,尽管经常存在广泛的牵引性支气管扩张,但支气管扩张所见的生产性症状很少出现[gydF4y2Ba23gydF4y2Ba].虽然IPF患者下气道的细菌负荷比囊性纤维化或支气管扩张患者低很多,但与健康患者相比却有所升高。呼吸道微生物群的数量和组成受到迁移率和清除率之间的平衡的影响。细菌的主要入境途径是微吸和吸入空气中的细菌,而消除是通过咳嗽反应、粘膜纤毛清除和先天和适应性免疫反应的结合来实现的。在疾病中,这两个相反因素之间的平衡失去,导致生态失调[gydF4y2Ba24gydF4y2Ba].考虑到与GORD和IPF的强烈关联,微吸可能是该队列患者的主要驱动因素[gydF4y2Ba25gydF4y2Ba].事实上,已经在呼吸道微生物群中发现了支持这一观点的胃细菌[gydF4y2Ba12gydF4y2Ba].然而,考虑到粘蛋白遗传结构中普遍存在的异常,IPF中可能出现异常的不仅仅是移民[gydF4y2Ba26gydF4y2Ba- - - - - -gydF4y2Ba28gydF4y2Ba].黏液蛋白糖蛋白是黏液屏障的主要结构成分,维持气道上皮的水合作用,并至关重要地包裹微粒以供黏液纤毛清除。在小鼠中,gydF4y2BaMUC5BgydF4y2Ba似乎是正常巨噬细胞功能和有效清除细菌所必需的[gydF4y2Ba29gydF4y2Ba].这就提出了一种假设,即细菌迁移和清除之间的平衡丧失导致下气道细菌负担增加,从而导致长时间和重复暴露,引发过度的间质损伤,最终导致纤维化的发展。gydF4y2Ba
尽管微生物负担增加,但在检查BAL差异细胞计数时,在细胞水平上没有看到宿主反应。关于BAL嗜中性粒细胞在IPF中的预后意义,有相互矛盾的数据。先前迄今为止最大规模的研究表明,BAL中性粒细胞计数增加会增加12个月时的死亡风险,但这种关联在一年后就消失了,这使得研究人员假设他们可能确定了一个具有更活跃疾病的个体亚群[gydF4y2Ba30.gydF4y2Ba].在这里,我们证明了IPF患者气道中中性粒细胞的增加,但与他们的计数和总体细菌负荷无关。我们还发现BAL细胞谱与气道中的细菌负荷之间没有关联,突出了稳定微生物组和感染期间之间的差异,在感染期间可以看到细胞反应。这与反复的上皮微损伤触发疾病的理论一致,你不会预料到如此大的细胞反应。因此,可能需要更细致的检测反应的方法,如上皮和气道转录组的表征,并且应该包括在任何未来的研究中。gydF4y2Ba
虽然牵引性支气管扩张和蜂窝状是明确定义和不同的实体,放射学上,它们可能代表IPF中发生的病理重构连续谱的两个方面。这两种特征都与疾病行为和临床结果相关,就像总体纤维化的程度一样[gydF4y2Ba31gydF4y2Ba].然而,蜂窝或牵引性支气管扩张的程度与细菌负荷之间没有相关性,即使考虑到这些因素,细菌负荷仍然是病情进展的预测因子。许多受试者的UIP放射学不确定,多学科会议可以获得临床数据、血清学和BAL细胞差异计数,以支持IPF的诊断。在我们的MDT IPF诊断队列中,CT UIP形态学(明确的、可能的、不确定的或不一致的)的相对比例与先前发表的比例相似[gydF4y2Ba32gydF4y2Ba].与纤维化或牵引性支气管扩张的程度没有联系,影像学诊断队列之间也没有差异gydF4y2Ba与gydF4y2Ba明确的摘要。我们还考虑了是否伴随疾病的共同发病者可能导致了这种负担,并考虑到PPFE与感染之间的临床关联,对此进行了特别的研究。几乎三分之一的队列有PPFE的放射学证据,并且在患病和未患病或仅考虑疾病程度时,细菌负担没有差异。虽然这是一个有趣的发现,但患有PPFE的受试者数量很少,这种缺乏关联的情况必须在更大的队列中得到验证,在更大的队列中,检查孤立PPFE受试者的微生物组也将是有趣的。gydF4y2Ba
最近,用生化标志物来估计IPF时间进展的相关结果(COMET)作者试图在68名IPF患者的亚组中检查微生物组与蜂群存在与否之间的关系[gydF4y2Ba33gydF4y2Ba].简单地根据是否有蜂房进行分组,他们发现与下呼吸道细菌负担没有关联。在这里进行的前瞻性和定量放射学分析使我们能够在他们的工作基础上建立和扩展。我们的研究设计特别允许我们回答有关放射变化与细菌负荷之间的分级关系的问题。这使我们能够进行更详细和细致的分析,并加强了我们的结论,即细菌负担的增加不仅仅与放射疾病的程度有关。gydF4y2Ba
我们的工作[gydF4y2Ba34gydF4y2Ba],以及O'DgydF4y2Ba王寅gydF4y2Baet al。gydF4y2Ba[gydF4y2Ba33gydF4y2Ba],也提出了一些与IPF抗菌治疗潜力相关的问题[gydF4y2Ba34gydF4y2Ba,gydF4y2Ba35gydF4y2Ba],其中一些已在试验中(gydF4y2BaNCT02759120gydF4y2Ba, 17464641)。虽然IPF患者的下气道中存在明显的微生物生态失调,但唯一一致的发现是细菌负担增加。目前还没有一种正在试验的治疗方法被证明对减少细菌负担有效。必须注意来自支气管扩张领域的警示故事,因为对抗生素的异质反应导致多项抗生素试验未能达到其主要终点。的确,最近S。gydF4y2BaibilagydF4y2Baet al。gydF4y2Ba[gydF4y2Ba36gydF4y2Ba已经证明,在gydF4y2Ba事后gydF4y2Ba对吸入抗生素的多项试验分析表明,细菌负担较高的患者一贯表现出临床反应并改善了生活质量。因此,可以想象,IPF患者可能还需要一种更有针对性的方法,而不是简单地不分青红皂白地治疗。然而,这项研究没有证据表明细菌负荷可以通过放射学或细胞计数的差异来预测。gydF4y2Ba
这项工作有一些局限性。首先,在右中叶进行BAL检查,同时对疾病的放射学范围进行全面评估。这一标准化方法是根据目前的诊断和研究标准采取的;然而,我们认为深入的多叶的地理调查可能会提供更多的信息,应该在任何未来的研究中加以考虑。这也将为评估纤维化肺疾病中细菌负担和微生物组成的区域差异提供完美的机会。本研究旨在调查细菌负荷与放射性疾病程度之间的关系,我们没有对细菌群落进行任何表征。虽然到目前为止,细菌负荷增加是IPF中最一致的微生物组相关发现,但与更复杂的16S扩增子分析相比,这可能只是反映了这种测量的易用性和可重复性。更大的队列和更标准化的测序/分析管道[gydF4y2Ba37gydF4y2Ba(允许荟萃分析)将需要揭示特定社区组成和临床结果之间更一致的关系。鉴于已知的rs35705950的单核苷酸多态性之间的关联gydF4y2BaMUC5BgydF4y2Ba粘蛋白基因[gydF4y2Ba38gydF4y2Ba],这些前瞻性研究还应考虑基因型对细菌负荷的影响。另一个限制是CT的放射学解释是MDT的关键部分,可能会混淆任何关于CT表现的研究。我们试图通过确保至少有一名评分放射科医生独立于MDT参与IPF的最终诊断,从而将这种影响降到最低。gydF4y2Ba
虽然我们的假设是建筑破坏充当了增加细菌负担的水库,但另一种可能性是,增加的细菌负担确实可能导致建筑破坏。我们的数据不支持这两种情况中的任何一种,但需要纵向和机制研究来支持这一点。已知GORD反流与IPF之间存在关联。许多患者服用PPI,这与肺炎风险增加有关[gydF4y2Ba21gydF4y2Ba,gydF4y2Ba39gydF4y2Ba].虽然我们没有前瞻性地着手解决这一问题,但我们证明GORD或PPI的使用与细菌负担之间没有关联。虽然更正式的前瞻性研究与客观测量的酸和非酸反流将需要直接回答这个问题。gydF4y2Ba
我们证明,细菌负荷升高可预测IPF的死亡率,但与放射学特征、细胞计数差异和疾病程度无关。我们认为,这种关联的独立性支持了与潜在发病机制的关系。然而,迫切需要功能性研究,特别是在介入研究已经开始的情况下,细菌负荷指导IPF患者抗生素治疗的潜力应该进行前瞻性测试。gydF4y2Ba
补充材料gydF4y2Ba
补充材料gydF4y2Ba
请注意:gydF4y2Ba补充材料不是由编辑部编辑的,而是由作者提供的。gydF4y2Ba
补充材料gydF4y2Baerj - 01519 - 2019。补充gydF4y2Ba
可共享的PDFgydF4y2Ba
脚注gydF4y2Ba
本文有一篇社论评论:gydF4y2Bahttps://doi.org/13993003.00318-2020gydF4y2Ba
本文的补充资料来自gydF4y2Bawww.qdcxjkg.comgydF4y2Ba
利益冲突:R. Invernizzi没有什么可透露的。gydF4y2Ba
利益冲突:J. Barnett没有什么可透露的。gydF4y2Ba
利益冲突:B. Rawal没有什么可透露的。gydF4y2Ba
利益冲突:A. Nair没有什么可透露的。gydF4y2Ba
利益冲突:P. Ghai没有什么可透露的。gydF4y2Ba
利益冲突:金斯顿没有什么可透露的。gydF4y2Ba
利益冲突:蔡美儿没有什么可透露的。gydF4y2Ba
利益冲突:Z. Wu没有什么可透露的。gydF4y2Ba
利益冲突:A.U. Wells报告了来自Intermune Roche、Boehringer Ingelheim和Bayer的演讲者和咨询费。gydF4y2Ba
利益冲突:E.R. Renzoni从BI、罗氏(Roche)和蒙迪制药(Mundipharma)获得了演讲费。gydF4y2Ba
利益冲突:A.G. Nicholson报告了医学定量图像分析和赛诺菲的个人咨询费用,勃林格殷格翰的个人咨询和讲座费用,罗氏的个人讲座费用,以及提交的工作之外的个人费用。gydF4y2Ba
利益冲突:a . Rice是辉瑞公司的股东。gydF4y2Ba
利益冲突:C.M.劳埃德没有什么可透露的。gydF4y2Ba
利益冲突:A.J.伯恩没有什么可透露的。gydF4y2Ba
利益冲突:T.M. Maher,gydF4y2Ba通过gydF4y2Ba他的机构获得了葛兰素史克研发和UCB的行业学术资助,并获得了来自Apellis, AstraZeneca, Bayer, Blade Therapeutics, Boehringer Ingelheim, Bristol-Myers Squibb, Galapagos,葛兰素史克研发,Indalo, Novartis, Pliant, prometics, Respivnat, Roche, Samumed和UCB的咨询或演讲费。gydF4y2Ba
利益冲突:A. Devaraj报告了GSK、罗氏和勃林格殷格翰在提交作品之外的个人费用。gydF4y2Ba
利益冲突:P.L. Molyneaux,gydF4y2Ba通过gydF4y2Ba他的研究所获得了来自罗氏、勃林格殷格翰和加拉帕戈斯的行业学术资助,并获得了罗氏的演讲费。gydF4y2Ba
支持声明:P.L. Molyneaux得到肺纤维化行动组织Mike Bray奖学金的支持。T.M. Maher是由国家健康研究所临床医师科学家奖学金(NIHR ref: CS-2013-13-017)支持的,是英国肺基金会呼吸研究主席(C17-3)。C.M. Lloyd由惠康基础生物医学高级奖学金(107059/Z/15/Z)资助。A.J. Byrne获得了Wellcome Trust奖(205949/Z/17/Z)和Asthma UK高级奖学金(AUK-SNF-2017-381)的支持。本文的资助信息已存入gydF4y2Ba交叉基金注册处gydF4y2Ba.gydF4y2Ba
- 收到了gydF4y2Ba2019年8月1日。gydF4y2Ba
- 接受gydF4y2Ba2019年12月29日。gydF4y2Ba
- 版权所有©ERS 2020gydF4y2Ba
本版本是根据gydF4y2Ba知识共享署名许可4.0gydF4y2Ba.gydF4y2Ba
参考文献gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba