摘要
来自美国和法国队列的肺动脉高压(PAH)的当代预后方程在英国可能不如当地衍生的评分方案执行得好。该研究的目的是开发和验证英国风险评分来预测PAH的预后。
182例PAH患者的多变量Cox分析确定的基线死亡率预测因子用于得出苏格兰综合评分(SCS)。在独立的英国队列中,使用Brier评分(BS)将其预后表现与法国注册表和肺动脉高压连接(PHC)注册表方程进行比较。
基于年龄、性别、病因、右房压、心输出量和6分钟步行距离的SCS预测验证队列的生存(风险比(HR)每增加一点1.7;p<0.001),并提供了世界卫生组织(WHO)功能III级患者的进一步预后分层(HR每增加一点1.8;p < 0.001)。在预测1年生存率方面,它比法国注册方程更准确(BS: 0.092)与0.146;P =0.001)和2年生存率(0.131)与0.255;p < 0.001)。SCS和PHC注册方程的BS无显著差异。
SCS预测生存,可作为WHO功能分级预测的补充。
肺动脉高压(PAH)仍然是一种无法治愈的疾病,尽管在过去十年中有效的药物治疗扩大了发病率和死亡率[1].由于准确的预后是疾病管理的一个组成部分,人们已经做出了相当大的努力来确定预后因素并开发算法来预测临床使用的患者预后。第一个基于肺血流动力学的预后方程(右心房压(P类风湿性关节炎)),平均肺动脉压(平均值P巴勒斯坦权力机构)和诊断时的心脏指数)来源于美国国立卫生研究院(NIH)对来自美国32个中心的194例原发性肺动脉高压(现在被分类为特发性、遗传性和厌氧性相关的PAH)患者的登记研究,这些患者20年前在PAH特异性药物治疗出现之前[2].它已经过时,但继续被用作没有靶向治疗干预的患者结果的基准。在芝加哥(IL, USA)的一个单一中心,对肺动脉高压连接(PHC)登记的当代PAH队列进行生存分析,包括人口统计学和功能测量,确定了与NIH方程相同的血流动力学变量,并使用这些变量基于类似的方法学方法推导出新的方程[3.].另一个基于性别、6分钟步行距离(6MWD)和心输出量(CO)的预后方程已从法国注册表中开发出来,包括在研究进入前3年诊断的事件和流行患者[4,5].这两个当代方程仅适用于特发性、家族性和厌食相关的多环芳烃患者,而从评估早期和长期肺动脉高压疾病管理登记处(REVEAL)开发的方程包括世界卫生组织(WHO) I组多环芳烃的所有患者[6].由于样本量大,与法国注册表和PHC注册表方程相比,预测模型中纳入的变量数量更多(13)与三个变量)。
这些当代预后算法利用基线变量来计算随访期间某个时间点的预测生存概率。迄今为止公布的这些方程的验证数据支持了它们的预测价值。REVEAL方程及其简化风险评分(22分评分系统)在新诊断PAH患者的前瞻性队列中具有良好的区分能力[7].当PHC登记和法国登记方程应用于四项随机对照临床试验及其扩展研究中PAH患者的前瞻性队列时,预测和观察到的生存率之间存在很好的一致性[8].由于这些公式是根据美国和法国的患者人群开发的,与英国的人口统计、医疗保健系统和治疗方法不同,因此它们在英国PAH人群中的表现可能不如当地衍生的评分方案好。本研究的目的是建立一个英国风险评分,以预测苏格兰一个定义明确的队列中PAH患者的预后,并在一个独立的英国PAH队列中验证其预后表现。
方法
研究设计
对2000年11月至2009年9月期间在苏格兰肺血管科(Glasgow, UK)诊断为WHO I组PAH的患者进行回顾性队列研究,得出苏格兰综合评分(SCS)。排除标准为PAH合并先天性心脏病(CHD-PAH)、长期钙通道阻滞剂(CCB)应答者、肺毛细血管楔压(P物理化学加工>15 mmHg和严重肺部疾病(以1 s的用力呼气量或根据欧洲煤钢共同体参考值预测的用力肺活量或总肺活量<60%来定义)[9].PAH的诊断是基于右心导管(RHC)根据当代指南[1,10].患者随后接受常规治疗(长期使用华法林、利尿剂或补充氧气)和pah特异性单药治疗(前列环素类似物、磷酸二酯酶-5抑制剂或内皮素受体拮抗剂)。根据临床指示开始序贯联合治疗。人口统计学、RHC、肺功能、WHO功能分类(FC)、6MWD、n -末端前脑钠肽(NT-pro-BNP)和剑桥肺动脉高压结局评价(CAMPHOR)评分的基线数据[11收集诊断性RHC 3个月内和开始pah特异性治疗前的记录。在多变量Cox分析中发现的独立死亡率预测变量被纳入SCS。对探索性分析确定的每个变量的阈值进行加权赋值。SCS通过对每个变量得分的总和获得,并在2001年1月至2009年12月期间在Papworth医院(Cambridge, UK)肺血管疾病部门治疗的突发和治疗初期特发性和遗传性PAH患者队列验证之前最终确定。有明显肺部疾病(由肺功能定义)的患者增加P物理化学加工排除长期CCB应答者。收集基线数据,应用SCS、法国注册表和PHC注册表方程。在整个队列和WHO FC III患者中,SCS预测随时间推移的生存和将患者分为预后组的能力进行了测试。使用法国注册和PHC注册方程计算诊断后1年和2年的生存估计。使用Brier评分(BS)将其预测准确性与SCS进行比较。有关机构的当地研究伦理委员会认为没有必要征得患者同意。
统计分析
采用Statview 5.0.1版本(SAS Institute, Cary, NC, USA)和Graphpad Prism 5.00版本(Graphpad Software, La Jolla, CA, USA)进行统计分析。使用D'Agostino和Pearson综合正态性检验检验连续变量的正态性。正态分布变量使用均值和标准差描述,并使用非配对t检验进行比较。非正态分布变量采用中位数和四分位间距描述,比较采用Mann-Whitney U检验。分类变量用数字(百分比)描述,并用卡方检验进行比较。
采用单因素Cox比例风险分析确定衍生队列中的基线死亡率预测因子。生存时间计算自RHC发生之日至数据截止日期(2010年5月1日)。接受肺移植或随访失败的患者根据手术日期或最后一次临床接触进行审查。使用探索性Cox分析中确定的阈值将显著连续变量转换为分类变量(参见在线补充数据),并使用反向选择程序在多变量Cox模型中使用相应的指标变量编码对缺失数据(“缺失”和“未缺失”)进行评估。指标变量的使用是为了在多变量分析中纳入数据缺失的患者。缺失数据的指标变量均不能预测生存率。性别在单因素Cox分析中不显着,但由于其预后意义已被既往研究证实,因此被纳入多因素模型。病因学分为两个亚组:结缔组织病相关的系统性硬化症肺动脉高压(CTD-PAH-SSc)和WHO I组PAH其他与特发性,遗传性,厌食相关和CTD-PAH非ssc(参考亚组)。厌食相关PAH被纳入参考亚组,因为这些患者被认为与特发性和遗传性PAH患者具有相似的结果。“WHO I组PAH其他”包括门脉性高血压、HIV和肺静脉闭塞性疾病患者。在最终的多变量Cox模型中保留p<0.1的变量。根据最终模型中各变量子组调整后的风险比(HR)给予加权分,如参考子组调整后的风险比为1,给予0分。对于其他分组,如果调整后的人力资源为2,则加1分,如果调整后的人力资源为3,则加2分,如果调整后的人力资源为4,则加3分。
生存率采用Kaplan-Meier分析,组间比较采用log-rank检验。在验证队列中,使用Cox分析来评估SCS预测生存的能力。BS [12,13]用于评估SCS、French registry和PHC registry方程在预测验证队列1年和2年生存率时的准确性,允许进行筛选。它测量预测概率与实际结果的均方差。BS为0表示预测完美。BS值为0.25表示预测结果等同于偶然发生的结果。较低的BS表示较高的预测精度。为了比较SCS与其他方程的性能,从200,000个bootstrap重新样本中获得SCS与每个方程之间BS差异的点估计及其95%置信区间。BS差异>0.02被认为具有临床相关性。p值<0.05为有统计学意义。
结果
标准说明的推导
衍生队列和病原学参考亚组的特征总结于表1。10%的患者接受前列环素类似物(7%静脉注射丙烯醇,2%吸入伊洛前列素,1%皮下注射曲前列素),47%磷酸二酯酶-5抑制剂(45%西地那非,45%他达拉非,2%)和44%内皮素受体拮抗剂(29%波生坦,7%西他森坦,8%氨布里森坦)。中位随访25个月(0.1-113个月)后,81例患者死于各种原因,2例患者接受肺移植,1例患者失去随访,2例患者转移到另一个中心治疗。整个队列的生存率估计为1年79%,2年68%,3年57%。在单变量Cox模型中考虑的17个基线变量中,年龄、病因、一氧化碳扩散能力% pred、P类风湿性关节炎、CO、WHO FC、6MWD、NT-pro-BNP和CAMPHOR评分是显著的死亡率预测因子(表2)。当这些变量被分为两到四个亚组,并在多变量Cox模型中进行评估时,诊断年龄、性别、病因、P类风湿性关节炎, CO和6MWD被保留为独立的死亡率预测因子,并用于构建SCS(0至8)(表3)。
《能力标准说明》的验证
在验证队列的119例患者中,99例患者有完整的数据来计算SCS (表4)。随访期间(中位29个月,0.3-102个月),38例死亡,4例接受肺移植。接受SCS治疗的患者的1年、2年和3年生存率分别为87%、74%和68%,与未接受SCS治疗的患者无显著差异(log-rank p=0.196)。死亡风险随着SCS的增加而增加(HR每增加1个点增加1.7个点,95% CI 1.4-2.1, p<0.001)。当患者被分为三个SCS危险组时(“高风险”:4-8 (n=23);“中等风险”:2-3 (n=44);“低风险”:0-1 (n=32)),组间生存率有显著差异(log-rank趋势检验p<0.001) (图1)。SCS进一步对WHO FC III患者进行分层(HR每增加1个点增加1.8,95% CI 1.4-2.4, p<0.001) (n=66, 30例死亡)。将这些患者分为3个SCS危险组(“高危”= 4-8,“中危”= 2-3,“低危”= 0-1),组间生存率差异有统计学意义(log-rank趋势检验p<0.001) (图2)。
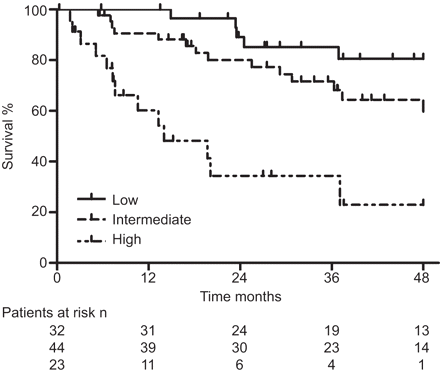
由三个苏格兰综合评分风险组分层的验证队列的Kaplan-Meier生存估计。
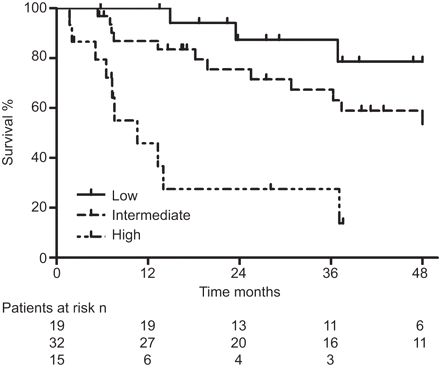
世界卫生组织功能III级患者在验证队列中的Kaplan-Meier生存估计,按三个苏格兰综合评分风险组分层。
讨论
本研究首次描述了基于英国数据预测PAH事件患者预后的风险评分的推导和验证。数据分析显示,SCS是一个基于年龄、性别、病因的8分简单评分系统,P类风湿性关节炎诊断时的CO和6MWD可用于将患者分为预后组,并为WHO FC III患者提供进一步的风险分层。当在独立的英国PAH队列中进行测试时,SCS的预测准确性与PHC注册方程相当,并且可能大于法国注册方程。先前的研究也证实了性别和病因对预后的影响。这些发现增加了越来越多关于PAH预测的文献,并为从其他登记研究中获得的当代预测方程的使用提供了进一步的见解。
法国注册表、PHC注册表和REVEAL方程的预测价值已在各自的验证研究中得到证实。然而,它们在其他患者群体中的适用性将受到研究人群特征、治疗途径和统计方法(表6)。SCS被设计为一个简单的基于点的风险评分,将患者分为预后组,而其他方程被开发用于计算诊断后特定时间点的预测生存概率。SCS衍生和验证队列均在单一三级中心进行治疗,这将确保完整的数据捕获和护理的均匀性。相比之下,法国登记和REVEAL包括来自选定中心的国家队列。这可能导致选择偏差,临床实践和患者结果的变化。SCS来源于严格意义上的事件和未接受治疗的患者队列,而法国注册、PHC注册和REVEAL方程来源于混合事件和流行队列。纳入流行患者可能会引入幸存者偏倚,因为这些患者存活时间足够长,可以被纳入研究,并且比那些因严重疾病或对多环芳烃治疗缺乏反应而早期死亡的患者预后更好。通过比较法国登记研究中事件队列和流行队列的生存率,这一点得到了清楚的证明[5].为了消除这种幸存者偏倚,法国注册方程的作者估计了从诊断时开始的生存率,而不是从入组时开始,并且只考虑患者从入组时开始的风险。在PHC登记或REVEAL方程的开发中,没有采用这种对流行患者诊断和研究进入之间的时间延迟的调整。初级保健登记处的研究期间跨越了前和后现代治疗时代。在此期间,由于治疗进展,患者预后可能发生变化,这可能影响了生存分析。这些因素,加上医疗系统和治疗方法的差异,会影响这些预后算法在不同临床环境中的表现。
众所周知,患者的预后因多环芳烃的病因而异。冠心病-多环芳烃患者被排除在本研究之外,因为他们与其他多环芳烃患者有不同的血液动力学特征和自然病史[14].肺动脉高压合并系统性硬化症的预后比特发性多环芳烃更差,尽管其血流动力学紊乱程度相似,但原因尚不完全清楚[15,16].当PAH与不同类型结缔组织疾病(包括混合性结缔组织疾病、重叠综合征和类风湿性关节炎)相关时,将其分组并与衍生队列中的CTD-PAH-SSc进行比较,CTD-PAH-SSc的预后更差。这与一项英国流行病学研究的结果一致[17].特发性、遗传性、厌食相关的多环芳烃患者被认为具有相似的结果,因为他们具有共同的临床和病理生理特征[18].因此,SCS的病因分组将与以前的研究结果一致。也有越来越多的证据支持患者预后的性别差异,本研究证实了这一点。受多环芳烃影响的女性多于男性,但她们的预后更好[4,19].最近对REVEAL项目患者的分析显示,男性的平均值更高P巴勒斯坦权力机构和平均P类风湿性关节炎诊断时年龄≥60岁的患者生存率低于年龄≥60岁的女性[20.].性激素被认为发挥了作用,但确切的机制仍有待阐明。其他研究也证实了SCS中其他组成变量的个体预后价值(年龄[3.,19], 6mwd [4,6,21- - - - - -25],P类风湿性关节炎(6,23- - - - - -27], co [4])。
目前多环芳烃管理指南所提倡的关于初始药物选择和联合治疗使用的建议算法主要基于WHO FC,因为其预后价值已得到牢固确立[1,28,29].然而,WHO FC可能不是一个足够可靠的功能状态测量,因为据报道临床医生的评估存在很大差异[30.].世卫组织FC I或II和IV之间的差异是明确的,但世卫组织FC III涵盖了具有广泛功能能力的患者。本研究结果表明,SCS可以为WHO FC III型患者提供进一步的风险分层,从而在临床评估中补充WHO FC。随访期间测量的变量可能比基线评估时测量的变量更能预测长期结果,因为它们可以捕获治疗反应和疾病进展对生存的影响。最近的一项研究证实了疾病过程中结果变量变化对预后的影响,并证明了将其纳入风险评估的重要性[31],但目前还没有专门针对这一问题开发的公开预测工具。我们建议,SCS可用于评估一到两年时间范围内的初始死亡风险,以建立一个包含死亡率预测因子随时间变化的风险评分,以便在随访期间重复使用。
这项研究有几个局限性。由于该研究的回顾性,数据缺失是不可避免的。由于NT-pro-BNP和CAMPHOR评分的测量直到2004年才被引入临床实践,与其他基线变量相比,数据较少,尽管进行了统计调整,但在多变量生存分析中可能会引入对它们的偏倚。衍生队列由不同病因的PAH患者组成,在一些亚组中数量相对较少。然而,这仅仅反映了现实生活中临床队列中不同病因的相对发病率。诊断时血管反应状态的数据不完整,因此无法评估血管扩张反应阳性对生存率的影响。只有一名患者表现出CCB的持续反应,并被排除在研究之外。这是基于长期CCB应答者的预后优于非CCB应答者的发现[32].由于数量很少,因此与此排除相关的偏差将是微不足道的。在推导或验证队列中,没有因血吸虫病或慢性溶血性贫血等较罕见原因导致WHO I组多环芳烃的患者,并且只有特发性和遗传性多环芳烃患者被纳入验证队列。因此,SCS在其他PAH亚组中的表现仍有待验证。在验证队列中,17%的患者不具备计算SCS所需的所有变量。与其他方程相比,不可能确定SCS在这些患者中的表现如何,但在有和没有SCS的患者之间的生存没有差异。在诊断时测量每位患者的心率(HR)和收缩压(SBP),但未记录在验证数据库中,因此无法用于本分析。由于HR和SBP数据的系统遗漏会导致其性能偏差,因此不能将REVEAL方程纳入比较。这是数据库分析的局限性,不能反映评估工具在临床实践中的潜在价值。
综上所述,SCS是一种简单的多维风险评分,结合了人口统计学、肺血流动力学和功能状态对PAH患者生存的影响。当在独立的英国特发性和遗传性PAH队列中验证时,它与死亡率相关,并为WHO FC III患者提供了进一步的风险分层。它在英国人群中的表现可能比从其他登记研究中得出的预后方程更好,但需要在更广泛的多环芳烃人群中进一步验证,才能对其临床应用得出明确的结论。
致谢
作者要感谢J. Alsop (Numerus Ltd, Northampton, UK)的统计建议和Actelion UK对这个项目的资助。
脚注
有关编辑评论,请参阅530页。
本文的补充资料来自www.www.qdcxjkg.com
利益声明书
wtn的利益声明。Lee, K. Sheares, J. Pepke-Zaba, A.J. Peacock, M.K. Johnson以及研究本身的资料可以在www.www.qdcxjkg.com/site/misc/statements.xhtml
- 收到了2011年11月11日。
- 接受2012年3月24日。
- ©2012人队















