摘要
健康的肺以前被认为是一个无菌器官,因为标准的微生物培养技术总是产生消极的结果。然而,不依赖培养的技术报告了大量微生物在肺中共存。该领域有许多未知的方面,但现有的报告表明:1)健康受试者的下呼吸道微生物群与口咽微生物群相似,以厚壁菌门、拟杆菌门和变形菌门的成员为主;2)显示吸烟者的变化和慢性呼吸道疾病的明确差异,尽管这些变化的时间和空间动力学仅部分了解;3)慢性阻塞性肺疾病、特发性肺纤维化、囊性纤维化和支气管扩张中不可培养细菌相对丰富,每种疾病均有特定的模式。在所有这些疾病中,多样性的丧失与变形菌门的过度代表(生态失调)并行,与疾病的严重程度和恶化有关。然而,目前尚不清楚生态失调是支气管肺泡表面损伤的原因还是后果。
最后,我们对细菌的功能以及病毒、真菌和细菌之间的相互作用知之甚少。预计未来在细菌基因表达、宏基因组纵向分析和宿主-微生物组动物模型方面的研究将有助于呼吸道疾病的靶向微生物组干预。
摘要
在慢性呼吸系统疾病中,呼吸系统细菌群落主要由特定的门所控制http://ow.ly/j68Z30967DB
简介
健康的肺传统上被认为是无菌器官,因为标准的微生物培养技术总是产生阴性结果[1].然而,在过去十年中,不依赖培养的分子技术的使用证明了这一教条是错误的,大量微生物有机体,包括细菌、真菌和病毒,合称为微生物组,共存于健康受试者和呼吸系统疾病患者的肺部[2,3.],挑战我们对呼吸内科微生物学的认识[3.].事实上,解决肺部微生物群与呼吸道上皮表面之间关系的本质似乎是呼吸医学中最有前途的研究领域之一[1].例如,现在有大量证据支持这一概念,即在不同器官和不同体表的宿主-微生物群相互对话的异常调节可能在几种慢性炎症性疾病中发挥重要的致病作用[4- - - - - -7].因此,人们对确定气道微生物组组成特征作为预后标志物或能够指导几种呼吸道疾病治疗的因素的潜在价值越来越感兴趣[3.].这份手稿反映了目前呼吸道微生物组的知识水平(见箱1对于目前的术语来说),其不特异性可能与目前使用的呼吸道疾病临床分层的异质性有关。考虑到这些因素,巴塞罗那呼吸网络于2016年6月3日组织了一次国际多学科研讨会,讨论和确定该领域的研究挑战、优先事项和差距,并研究未来的方向和对患者和医疗保健系统的影响。在那里进行的讨论以及讲习班的主要结论摘述如下。完整的报告均录成视频,并可在巴塞罗那呼吸网络网站(www.brn.cat microbiome2016).
专栏1一般术语
微生物群:微生物群落与特定栖息地相关的微生物群落成员,如人体
微生物:一个微生物群的基因产物的遗传信息(基因组)和推断的物理化学性质。
人类微生物组:在人体内部和外部栖息地中发现的微生物群。
宏基因组:使用序列数据库和计算工具对样本中总DNA(包括来自宿主和微生物的DNA)进行分析、组织和识别的鸟枪随机测序。
16S核糖体RNA (16S rRNA)基因:原核核糖体30S小亚基的组成部分。由于该基因的进化速度极慢,并且存在允许扩增的可变和恒定区域,因此被用于重建系统发育。
16S rRNA基因高变区:显示不同细菌种类多样性的DNA序列。
16S rRNA基因分析(或基因测序):一种常用的扩增子测序方法,用于识别和比较给定样本中存在的细菌。16S rRNA基因测序是一种完善的方法,用于研究来自复杂微生物组或难以或不可能研究的环境的样品的系统发育和分类。
扩增子:DNA扩增的产物通过PCR。
鸟枪测序:DNA测序的一种方法,其中DNA被分割成测序片段。
失调:微生物群组成的改变与局部生态条件的扰动有关,通常与宿主-微生物相互作用受损有关。
不同学科的挑战
生物信息学观点
16S rRNA基因有几个可变区域,可用于细菌和古生菌分类(即。分类法)[8- - - - - -10].此外,由于其测序速度快且相对便宜[11],常用于测定不同生态系统(如人类呼吸道)中细菌和古细菌的组成、丰度和多样性[12- - - - - -14].然而,这种方法有一些重要的局限性。首先,在任何研究活动中,研究人员必须确定正确的问题,并从一系列可用的生物信息学工具中选择适当的工作流程,以适当地解决问题[15,因为过多的分析会产生混乱,导致学习重点的丧失。其次,适当控制研究中潜在的变异来源,包括患者多样性、采样方法、DNA提取程序、扩增和测序批次,在微生物组研究中是必不可少的,因为它们都很容易引入不必要的变异和意想不到的偏差[16) (表1).正如下面所讨论的,尽量减少这些变化来源是克服这些障碍的最佳策略。第三,16S rRNA基因测序不提供关于病毒和真菌的信息,也不提供关于它们与细菌微生物群相互作用的信息,这些信息需要使用宏基因组学和/或内部转录间隔测序等替代方法进行研究。最后,从纯生物信息学的角度来看,下面讨论的一些与数据库不完整和方法学限制有关的问题(见框2对于当前的术语)也需要考虑。
专栏2生物信息学术语
OTU(操作分类单位):微生物群,按特定分类学标记基因的DNA序列相似性分组,如。16 s rRNA。OTUs被用作微生物“物种”在不同分类水平的代理:门、纲、目、科、属和种。基于相似度准则定义序列相似度;如。相似度97%的测序reads可以聚在一起,代表一个OTU,对于某些细菌可以达到种水平的等效。
多样性:样本或原始种群中不同OTUs的数量和分布。因此,所谓的alpha多样性估计描述了单个样本中的物种数量(或类似指标),而beta多样性估计描述了样本之间物种多样性的差异。一个广泛使用的多样性指数是香农-维纳多样性指数。
相对丰度:一个OTU相对于社区中其他OTU的常见或罕见程度,以OTU在人口中总数的百分比来衡量。因此,OTU丰度被视为细菌物种丰度的替代测量。
均匀度:测量种群中不同OTUs相对丰度的相似性。
分类:一个或多个被认为构成一个单位的有机体的群体。
数据库的约束
现有的16S rRNA基因数据库目前提供了170多万种细菌和古生菌的(部分或完整)基因序列[17],并详细地将细菌按不同的分类级别进行分类,从门(高分类级别)到属(低分类级别)(图1).然而,这些数据库包含一些序列的未解析信息,因此对一些微生物无法实现物种级别的鉴定[18].也有可能,由于物种之间16S序列的高度同源性,一个序列在数据库中两个或多个不同的记录中给出了多个具有相同分数的命中,这表明无法区分它们。为了解决这种情况,通常使用“最低共同祖先概念”[19].按照这种方法,分类单元的分配不是在种的水平上给出的,而对某些细菌仅达到属的水平。例如,这是链球菌属,普遍存在于呼吸系统,包括致病菌种类,如肺炎链球菌还有共生生物,比如绿球菌群。这种物种分配的限制明显地限制了鉴定归属于这些属的微生物的范围。由于所有这些原因,微生物组研究中使用的生物信息学工具通常使用一种通用方法,在通用术语操作分类单位(OTUs)下,在某种相似程度上进行聚类测序。因此,如果与16S rRNA序列的参考数据库的序列相似性至少为97%,则通常可以将所识别的OTUs视为相当于种水平,如果相似性仅达到94%,则可以将其视为属水平。
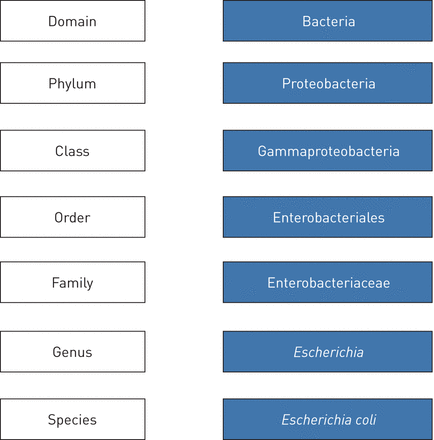
植物分类大肠杆菌.
方法论的问题
如上所述,16S rRNA基因有几个可用于细菌分类的可变区域(V1-V3或V3-V5) [3.,8,9].然而,目前尚不清楚其中哪一种提供了对呼吸道微生物群的最佳评估。此外,已经证明不同的测序平台,包括454、Illumina HiSeq和MiSeq,可以产生不同的结果[16].这部分是由于所用16S基因的特定可变区域、所用引物以及不同平台产生的扩增子的长度。为了减少测序错误,更长的读取是首选[16].另一个方法学问题是,使用不同的算法、假设和参数会导致不同的结果[13,19,20.].因此,认识到这些局限性是很重要的,如果可能的话,使用不同的测序和生物信息学工具(如.标记基因、鸟枪基因组或转录组测序)比较不同方法获得的结果。最后值得一提的是,16S测序提供的是定性而非定量的微生物组信息,建议采用定量PCR或数字PCR等辅助方法来完成通过分析16S rRNA基因获得的信息。
其他生物信息学挑战
其他需要考虑的生物信息学挑战包括以下内容。首先,到目前为止进行的大多数研究都是根据序列文库中恢复的16S rRNA基因拷贝数来估计每个分类单元的相对丰度[21].然而,基因丰度的变化可能是由实际细菌负荷的差异或特定细菌类群在分析过程中能够获得的基因组拷贝数造成的。这两个因素对微生物群落结构估计的相对权重尚不清楚,但在使用16S rRNA测序的研究中可能是系统偏倚的来源。有一些方法可以纠正16S rRNA基因的拷贝数,但这种纠正可用于<5%的已知细菌种类[22].同样值得注意的是,其他基因喜欢cpn06也可用于推断细菌群落多样性[23];因此,也应该考虑使用一个以上基因的可能性。第二个,为了比较在不同实验室进行的研究之间的结果,建议使用模拟社区在体外具有预定义的肺部微生物组特异性的细菌操纵子内容[24],但创建一个在单一中心执行所有分析的联盟可能会更方便。第三,DNA提取的差异[25]而PCR扩增方法也可引入方法相关的变异[26].
呼吸内科的观点
健康肺中的微生物群
对正常人类肺部微生物群的研究仍处于起步阶段,但现在很明显,健康的肺部拥有系统发育多样化的微生物群落[2,3.,27- - - - - -31].已发表的研究结果因其规模小和缺乏纵向采样而受到一定限制,但表明在健康受试者中,厚壁菌门、拟杆菌门和变形菌门是门水平上最常被识别的细菌[32].在属水平上,普氏菌、韦永氏球菌属而且链球菌是主要的微生物,常见的致病性变形杆菌的贡献很小,包括嗜血杆菌[32].健康的气道取样具有挑战性,因为健康的受试者不会产生自发的痰,因此取样需要支气管镜检查,并且在健康的个体中重复内窥镜检查过程很麻烦,限制了获得纵向数据的可能性。然而,最近的研究包括对近端和远端支气管树进行支气管镜取样,报告称健康个体口咽、支气管树和肺泡表面的微生物群组成相似[29].这种相似性归因于睡眠时口咽分泌物的吸入[33- - - - - -35].这种情况在呼吸道疾病中可能会改变,其中支气管树和肺实质的生长条件的扰动促进了微生物群落组成的变化,潜在的致病菌能够持续更长的时间[3.,29- - - - - -31) (图2).
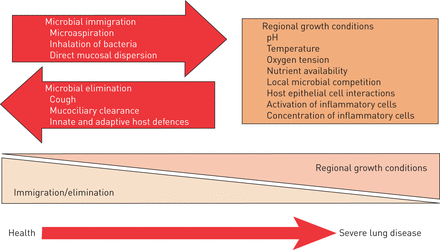
决定呼吸道微生物组的关键因素:微生物迁移,微生物消除及其成员的相对繁殖率。在健康受试者中,微生物群主要由迁移和清除决定。然而,在严重的肺部疾病中,区域生长条件是微生物组组成的主要决定因素。经允许转载自[102]。
在任何微生物组研究中,污染都是一个令人担忧的问题,口咽微生物群对下气道样本的潜在污染是呼吸道疾病中需要特别解决的一个主要问题[3.].与人体其他表面相比,呼吸系统的微生物数量更少,低生物量的样品,如保护标本刷(PSB)或支气管肺泡灌洗(BAL)获得的样品,可能无法提供足够的DNA,而试剂的背景信号可能被误解为真实信号[36].因此,为了区分信号和噪声,在基于序列的样本分析中,特别是在可能受到稀释效应的呼吸样本中,非常需要适当的技术控制。
关于吸烟对健康受试者呼吸道微生物组的长期影响的信息很少,显然需要进行研究。对吸烟者口咽菌群的初步研究报告了微生物组成的变化,主要影响厚壁菌门和奈瑟氏菌属重要到足以被视为生态失调的物种[37],变形菌门相对丰度下降;这些改变在戒烟后不会恢复[38].相比之下,对支气管分泌物中呼吸道微生物群的研究并没有发现吸烟者和非吸烟者之间的显著差异[37],以及戒烟后细菌多样性的相关变化[39],表明暴露于烟雾会导致近端微生物组的变化,至少在没有呼吸道疾病的情况下,这些变化不会在支气管树的相应下游变化中反映出来。目前口腔微生物群的差异与然而,有或没有呼吸道疾病的前吸烟者尚未得到适当的评估,目前还不可能从与慢性疾病相关的生态失调中正确辨别由暴露于刺激物和急性损伤引起的暂时性生态失调。
慢性阻塞性肺疾病
潜在致病微生物在慢性阻塞性肺疾病(COPD)中的支气管定植已在先前的几项研究中得到很好的证实[40,41],但这种定殖与气道炎症、气流限制、支气管和肺实质破坏之间的因果关系仍然不确定。有证据表明,急性加重症状的出现与新菌株的获得之间存在关系[40],但这种菌群的变化只是部分地证明了病情恶化的出现。
在临床稳定的COPD患者中,几项研究现在报告了丰富的肺部微生物群,这与健康对照组明显不同[2,27,30.,31,42- - - - - -46].这些患者常见门为变形菌门、拟杆菌门、放线菌门和厚壁菌门假单胞菌,链球菌,普氏菌而且嗜血杆菌是这些病人的常见属[2,27].
关于慢性阻塞性肺病的大多数数据来自活组织检查的样本[46],肺组织外植体[30.]、BAL或PSB [2,27,31,46]、痰液[43- - - - - -47].然而,不同的采样程序针对呼吸系统的不同区域,结果表明痰中含有不同于支气管肺泡样本中的微生物群落[46],并证实COPD患者的支气管和肺泡实际上含有不同的微生物群[3.)(见图3在迪克森et al。[3.])。
在病情加重期间,一些属的相对丰度增加,而其他属则没有显著变化[42,44,48,49].此外,加重似乎不仅与孤立属的过度代表有关,而且还与整个微生物组组成的附带变化有关,这反过来又似乎与BAL中炎症相关标记物的增加有关[41,50].此外,病毒感染与细菌群落组成之间似乎存在相互作用,实验鼻病毒感染后变形菌门的相对丰度增加[48].真菌和细菌之间也有类似的相互作用[51].此外,在病情加重期间,基于抗生素的治疗对呼吸道微生物组的影响是不同的,抗生素会减少细菌的丰度,主要是变形菌门,与口服类固醇,当全身给药时,不影响细菌的丰富度,但有利于特定类群的过度代表[40,52].
最后,在COPD微生物组研究的益处能够有意义地纳入临床实践之前,需要解决几个挑战:1)关于报道的支气管远端和近端呼吸道微生物组的差异,分别以BAL和痰为目标[46],需要确定有意义的阈值,以确定所有样本类型的临床显著细菌过度代表;2)通过微生物组研究确定的不可培养但具有潜在致病性的微生物的作用尚不清楚,需要进一步研究;3)细菌、病毒和真菌与宿主之间的相互作用需要有针对性。
总而言之,尽管存在这些重要的障碍,但肺微生物组研究有可能揭示COPD发病机制的新的相关见解,从而可能导致更好的COPD临床管理。具体来说,显然需要了解目前标准的COPD治疗方法,特别是吸入糖皮质激素对COPD气道微生物群的影响,因为这些药物已被证明可以减少急性发作的频率,但同时也会增加肺炎的风险,可能是通过直接调节气道微生物群。最终,微生物组的变化可能成为重要的机制(即。不同临床表现的内在型(即。COPD的表型)。
囊性纤维化和支气管扩张
气道细菌感染是我们了解囊性纤维化(CF)和(非CF)支气管扩张的病理生理学的中心。传统的微生物培养技术揭示了众所周知的病原体的重要性,如流感嗜血杆菌,铜绿假单胞菌而且莫拉克斯氏菌属复活支气管扩张症[53],另外金黄色葡萄球菌而且伯克不过在CF中[54].微生物组的研究正在推动我们对这两种疾病的认识。例如,在一些患者中,以前未被识别的生物体丰富,无论是在CF [55,56]和支气管扩张症[57,58].此外,对抗生素治疗后气道微生物组特征的研究表明,这些患者的细菌群落随着时间的推移具有显著的耐药性[57,59,60];抗生素治疗主要导致细菌多样性减少,但这种影响在几周后消失,恢复了以前的微生物组成[57].使用Shannon-Wiener多样性指数等综合指数测量的总体细菌多样性与CF和支气管扩张中存在的气流限制水平和疾病严重程度的其他标志物有关。此外,澳大利亚一项针对非cf型支气管扩张患者的随机临床试验表明,来自支气管的潜在致病微生物的相对丰度假单胞菌接受大环内酯类慢性治疗的患者属增加[60],但微生物组的变化在多大程度上可归因于抗生素制度尚不清楚。真菌,病毒和分枝杆菌(未被标准细菌16S rRNA测序识别)在CF和支气管扩张中都不清楚,需要未来的研究[61].同样,在这种临床环境中需要检查的其他重要问题包括:16S rRNA基因测序在多大程度上提供了培养之外的有用临床信息、与宿主的相互作用、基于微生物组谱选择抗生素治疗的可能性、微生物组结果对评估治疗反应的有用性、微生物组分析的预后意义以及抗生素对新病原体出现的影响。在这些患者群体中容易获得痰有利于在未来几年进行大规模研究。
间质性肺疾病
传统上,间质性肺疾病(ILD)被认为是非传染性肺实质疾病。然而,最近特发性肺纤维化(IPF)中呼吸道微生物组的特征显示了特定生物的过度代表,如链球菌,普氏菌而且葡萄球菌这些患者与健康对照组相比62,63) (图3).它们是否能推动疾病进展是一个值得未来研究的假设[63].
细菌载量(16S拷贝数·mL−1在特发性肺纤维化(IPF)、慢性阻塞性肺疾病(COPD)患者和健康对照组中进行支气管肺泡灌洗(BAL)。IPF患者(红色;n=64)的细菌负担明显高于COPD受试者(绿色;N =17)和健康对照组(蓝色;N =27) (p=0.006和p=0.0007)。方框表示第25和第75百分位,中位数由方框内的一条短线表示。经允许转载自[53]。
IPF急性加重的存在已日益被认为是这些患者死亡的主要原因[64].这些发作的确切发病机制尚不清楚,目前的诊断标准特别要求排除任何感染诱因[65].尽管如此,仍有证据支持IPF加重的感染性假设:1)一项随机对照试验显示,接受预防性复方新诺明的患者死亡率降低[66], 2)免疫抑制与急性加重率增加有关[67], 3)冬季加重的比例较高,4)感染发作与非感染加重的死亡率相同[63].因此,使用不依赖培养的分子技术来探索感染在IPF急性加重中的作用引起了极大的兴趣,尽管这些事件的不可预测性质和采样困难一直是解决这一问题的限制因素。
在不同ild的整个范围内进行微生物组研究应确定:1)肺部微生物组成是否在其发生和进化中起任何作用;2)考虑到这些实质性疾病可能不适合用痰等支气管样本来代表,这些患者的最佳采样方式是什么。
肺移植
由于长期使用预防和/或治疗性免疫抑制药物和抗生素,肺移植受者的下气道为常住菌群提供了一个特殊的生态位[68,69].事实上,移植后最初几个月局部条件的改变容易引起机会性细菌病原体引起的下气道感染。移植后6至12个月,炎症状态普遍减弱,这与口咽菌群中常见的细菌的强大优势有关[70].肺移植环境中呼吸道微生物群组成的改变足以被认为是生态失调,并通过特定OTUs的过度代表表现出来,包括下面列出的那些,这些OTUs与异常的潜在宿主炎症特征的持续存在有关[70,71].此外,移植后闭塞性细支气管炎综合征的发病也与宿主-微生物相互作用有关,通过病原体驱动的炎症触发和/或受损的宿主先天反应影响细菌清除[72,73].
使用不依赖培养技术鉴定肺移植患者中微生物群失调的研究报告,变形菌门和/或厚壁菌门经常明显占优势,与来自肺移植患者的微生物有关假单胞菌而且葡萄球菌属(68,74],以及柏氏科[75].这些细菌可能代表BAL微生物群落的70%以上,通常与促炎反应有关,而拟杆菌门的过度代表数量相似,主要是由于丰富的普氏菌,而是与重构宿主基因表达谱有关[70].这些发现表明,微生物群-宿主相互作用影响移植肺内的先天免疫过程。未来的研究应尝试将这些模式与长期同种异体移植结果和移植排斥反应发生的风险联系起来。
从其他人体器官系统吸取的教训:肠道
肠道微生物组的研究是微生物组研究领域的先驱,远比呼吸道微生物组的研究先进。首先,它现在正在使用下一代测序技术,通过研究微生物基因或全基因组,可以更深入地了解微生物群落[76]和元转录组学,其中包括RNA测序(见中术语盒3).第二,人类微生物组[77]和MetaHIT [78由美国国立卫生研究院(National Institutes of Health, USA)和欧盟委员会(European Commission)分别赞助的项目,已经允许对健康和疾病状态下的人类肠道微生物群进行深入描述。因此,我们现在知道,人类胃肠道(GI)拥有超过100万亿个微生物,是现有微生物群落中最复杂和最丰富的微生物群落之一,微生物基因的数量超过人类GI细胞数量的约100倍。虽然肠道微生物组的组成和功能在不同年龄之间是稳定的,但它受到许多因素的影响,包括遗传和出生时与分娩、年龄、地理位置、饮食、吸烟和医疗有关的接触[79].第三,虽然也有许多潜在的可变性来源可以显著影响胃肠道菌群研究的结果,但全球已经努力确定最佳实践和方案,以比较不同的胃肠道菌群研究,对其进行荟萃分析并提取新知识。这项工作的协议,国际人类微生物组标准项目,可在网上(www.microbiome-standards.org).第四,肠道菌群不仅影响胃肠道,还会影响身体的许多功能,从饮食中营养物质的加工和收获,到先天和适应性免疫系统反应的形成[80,81].因此,胃肠道微生物群的变化可以促进胃肠道以及非胃肠道疾病的发展。例如,大量文献现在将功能性和代谢性胃肠道疾病,如炎症性肠病、肠易激综合征或肥胖,与肠道微生物组的改变联系起来[82- - - - - -85],但也有报告称肠道微生物群的变化与神经系统疾病之间存在关系(如。自闭症)[86- - - - - -89]和呼吸系统疾病(如感染性休克患者发生的急性呼吸窘迫综合征[90])。第五,艾滋病毒的流行告诉我们,同性恋男性的粪便微生物群通常具有独特的组成,微生物的丰富度和多样性增加,以及在细菌中富集普氏菌肠型,与他们的HIV感染情况无关[91].HIV-1感染与细菌丰富度降低有关,特别是在接受抗逆转录病毒治疗的CD4+ T细胞计数不理想的受试者中[91].最后,旨在改变肠道微生物组组成的干预措施在特定的胃肠道疾病中已经成功。粪便菌群移植作为一种有效和安全的干预越来越被接受艰难梭状芽胞杆菌感染,不同的中心报告了这种治疗的成功率>90% [92].这种方法在炎症性肠病中要复杂得多,在炎症性肠病中,粪便移植的成功率约为13% [93].肠道菌群的细菌修饰对健康受试者和各种呼吸道疾病患者呼吸道微生物群的影响,以及潜在的间接影响通过宿主免疫反应的改变(及其对粪便移植的反应)迄今尚未得到适当的解决。目前的知识,包括早期肠道微生物群的有益和有害的改变,及其与过敏性呼吸道疾病的关系,最近已被回顾[94],而肠肺轴现在提供了广泛的研究可能性,如下所述。
专栏3其他系统术语
国际人体微生物组标准:旨在优化人类微生物组领域数据质量和可比性的标准操作程序。
粪便移植:将健康个体的粪便细菌移植到受者体内的过程。
未来呼吸道微生物组研究
通过上述讨论,研讨会的参与者就以下九个具体方面达成了一致,这是未来呼吸道微生物组研究需要特别解决的问题:
正常模式:到目前为止,在健康受试者中进行的研究清楚地表明,呼吸系统中存在丰富的微生物群,包括厚壁菌门、拟杆菌门和变形菌门的微生物,并显示出与口咽微生物群的密切相似性。然而,病毒和真菌的正常模式仍然需要定义。慢性呼吸道疾病中呼吸道微生物群的微生物组成发生变化,但这些变化的时间和分布仅部分已知。
抽样程序的多样性:有一个广泛的共识,最好的样本程序取决于所要解决的问题。痰可能是研究具有显著支气管成分的呼吸系统疾病的合适方法,因为痰可以从广泛的患者中获得,不需要侵入性手术,但更可靠的外周支气管树和肺泡表面信息需要侵入性样本(即。BAL, PSB,支气管或肺活检)。同样,在胃肠道研究中,现在收集粪便用于大型研究,局部活检用于回答有限数量患者的特定问题。在任何情况下,这些测量仍然需要与传统的微生物学研究相平行,因为尽管测序提供了细菌群落组成的总体情况,但微生物培养提供了关于呼吸道病原体作用的临床有意义的信息嗜血杆菌而且假单胞菌在微生物组分析中还没有相应的方法。
标准化:目前迫切需要标准化用于分析呼吸道微生物组的方案,包括采样、处理和生物信息学方法。建立关于这一主题的研究联盟和网络将促进这一标准化,从而有可能分享来自不同群组的结果。
不可培养和/或非致病菌:16S rRNA基因分析显示,在COPD、IPF、CF和支气管扩张患者的支气管和肺部样本中,不可培养微生物的相对丰度较高,且具有特异性(变形菌属普遍过度代表)。以前认为非致病性的特定物种的作用需要在这些不同的临床条件下得到解决。
多样性丧失:在COPD、IPF和CF中,多样性的丧失与疾病严重程度有关,在这些疾病恶化期间也有描述。在肠道中也报道了类似的观察结果,这表明在人类疾病中可能出现与特定OTUs过度代表相关的微生物组成多样性下降的一般模式,但这些微生物变化的时间动态尚不清楚。是什么导致了细菌多样性的丧失,包括种间竞争、抗生素暴露和宿主免疫反应的影响,必须加以定义。
与主持人的互动:在肠道疾病中,关于微生物群-宿主相互作用的数据不完整,在呼吸道疾病中几乎不存在。未来的研究应该同时解决微生物群落的局部和系统影响,因为重要的远程影响可以通过释放血液中的介质来实现。因此,解剖不同身体部位(如肺、肠道和皮肤)宿主-微生物相互作用的复杂相互作用,是未来微生物组研究的主要挑战,但有可能有助于阐明几种慢性呼吸道疾病进展的决定因素。为了正确地评估这一点,新的研究应该包括对同一宿主在几个地点的微生物群落多样性的研究;有纵向的尺寸;评估宿主的局部和全身免疫;最后通过动物模型的微生物组移植,证明微生物组模式对呼吸道疾病发病机制的影响。
细菌RNA和宏基因组学:在16S rRNA基因分析之后,微生物组研究的一个新阶段开始了DNA霰弹枪测序和RNA分析。这些技术需要应用于呼吸道微生物组的研究,因为它们将提供16S rRNA基因分析所缺乏的功能信息。此外,16S rRNA基因不能区分活细菌和死细菌,死细菌的DNA在呼吸样本中存在多久还不知道。
病毒和真菌:病毒(包括感染细菌的大量噬菌体)和真菌在呼吸道健康和疾病中的作用不能通过16S rRNA基因分析来确定,需要进一步研究。到目前为止,病毒、真菌和细菌之间的相互作用只得到了粗略的评估,但初步结果表明,非细菌微生物群对变形菌门丰度的影响是明确的。
干预措施:通过益生菌及其等价物对微生物群的细菌补充和调节尚未在呼吸道疾病中进行探索,但这是一个潜在的富有成果的研究领域。益生菌是否直接针对肺实质,或恢复正常的上呼吸道或肠道菌群,对呼吸系统疾病产生有益作用,仍有待研究。
披露的信息
确认
作者感谢Momentum®为研讨会的组织提供后勤支持。
脚注
利益冲突:可以在本文旁边的网站上找到信息披露www.qdcxjkg.com
本文是2016年6月3日在巴塞罗那举行的巴塞罗那呼吸网络研讨会的摘要。研讨会得到了美纳里尼、阿斯利康、基耶西、葛兰素史克和诺华的无限制资助,部分资金由Fundació Ramón Pla Armengol、Fondo de Investigación Sanitaria 15/00167和PI15/02042提供。
- 收到了2016年10月25日。
- 接受2017年2月8日。
- 版权所有©ERS 2017