抽象
致癌驱动器的改变的标识,要小抑制剂背后灵敏度,导致生长在非小细胞肺癌识别额外靶向癌基因的兴趣。虽然这些改变的发现的治疗作用目前已被广泛证实的,与这些生物标记物相关的流行病学数据保持充分研究。在这次审查中,我们讨论用来发现这些候选癌基因的技术,其在非小细胞肺癌,并简单介绍一下主要的致癌基因和方法,使他们的身份能够确定治疗策略的流行病学特点盛行。
抽象
流行病学和非小细胞肺癌的预后和治疗反应的影响在很大程度上取决于分子的个人资料http://ow.ly/QCGP3094HLZ
介绍
米echanisms of oncogenesis in lung cancer have been largely deciphered over the past 20 years. The concept of “oncogene addiction” refers to tumour-cell dependence on the specific activity of an activated or overexpressed oncogene. The main oncogenic drivers in the field of thoracic oncology are mutations of表皮生长因子受体,KRAS和ALK重排。它们大多数腺癌的报道。然而,新的分子靶标被最近强调:即BRAF突变,HER2和PIK3CA和新的易位,如ROS1和RET。治疗策略被设计来抑制这些信号通路,其中包括单克隆抗体和酪氨酸激酶抑制剂。
现在肿瘤根据其分子的个人资料,这是新的人口数据赞同分类。肺腺癌现在可以被认为是离散的分子亚型集群,其中大部分是由单个的改变的致癌驱动程序定义。多重基因分型,并通过下一代测序的高通量基因组分析(NGS)已经越来越多地改进分子诊断。
在这次审查中,我们讨论用来发现这些候选癌基因,其在非小细胞肺癌患病率(NSCLC),其相关的流行病学特点,以及如何使他们的身份可以告知治疗策略的技术。
肿瘤取样方法
目前存在一个悖论,一方面需要为越来越多的分子生物标记物进行多次分析获取大量样本,另一方面需要开发微创或非侵入性技术,从而获得DNA含量极低的小组织样本。从福尔马林固定和石蜡包埋(FFPE)肿瘤样本中提取的DNA的初始分子谱使用了各种技术(如下所述)。
细胞学标本通常被认为不足以详尽的分子检测。然而,最近的数据表明,组织的数量非常有限,就足以对这种类型的分析。Only 10 ng of DNA is sufficient to analyse 22 genes using NGS [1]。同样地,对50个细胞激光显微切割可有助于分析表皮生长因子受体和KRAS用焦磷酸测序[2]。具有更高灵敏度的测试组合新的采样程序有助于肺病以获得来自不同样品的分子量分布。每个技术的主要优点和缺陷报告于表格1。
支气管内超声支气管针吸活检
多项研究已经证明了通过在非小细胞肺癌和echobronchoscopy分子检测淋巴结的超声引导cytopuncture获得细胞样品的有用性。在用B的研究oulangeret al。(3.],屏幕为KRAS和表皮生长因子受体突变95.1%和的情况下,97.6%分别为可能的(N = 82)。最近,Casadioet al。(4]测试NSCLC的306个样本表皮生长因子受体和KRAS(Sanger和RT-PCR)ALK重排(FISH),具有非常好的诊断准确性(样品的96.9%是适合于分子谱,相比于组织数据非常相似的结果)。在这种情况下,焦磷酸测序和高分辨率熔解产生同样优异的结果:97%和箱子93%,分别[5]。
经胸细针穿刺
年代CARPAet al。(1] demonstrated the feasibility of obtaining the mutational status of the main genes potentially involved in thoracic oncogenesis using just a small amount of DNA (10 ng) and NGS. In this study, 22 genes were examined in cytological samples obtained by transthoracic fine-needle aspiration. A mutation of at least one of these genes was found in 67% of patients, which included 28%KRAS突变和16%表皮生长因子受体突变。
生物液体
支气管肺泡和支气管涂片冲洗液
很少有研究评估分子分析对肺泡灌洗液的可行性。将PCR变性梯度凝胶电泳(DGGE)技术提供低灵敏度(43%)和只有33%的一致性与原发肿瘤(N = 36),用于KRAS突变[6]。在最近的研究中,通过支气管镜刷收集测序细胞激活突变只采样的77名患者中的一个被发现[7]。36例支气管肺泡灌洗阳性(0.3-9%的肿瘤细胞)表皮生长因子受体突变,在只有16%采用Sanger测序箱子中检测到相同的突变,但是在使用NGS箱子81%。NGS甚至可以检测表皮生长因子受体突变在细胞样品的42%,无肿瘤的证据[8]。EGFR,KRAS和ALK状态也可以从支气管内超声(EBUS)具有良好的诊断准确性(95.2%)和一致性与其它样品[外围结节引导下刷洗建立9]。
循环肿瘤细胞
各种方法允许循环肿瘤细胞,其中CellSearch上,基于细胞角蛋白染色的间接方法,和ISET(由上皮肿瘤细胞的大小分离),基于小区大小的直接方法,是最广泛使用的分离。除了它的预后价值和细胞形态学分析的可能性,ISET可以检测NSCLC一些分子改变,如表皮生长因子受体通过PCR [突变12], 要么ALK重组鱼和免疫细胞化学,与原始组织具有良好的一致性[13]。
一项研究报告检测的可行性KRAS100名患者携带:使用PCR突变的循环肿瘤细胞KRAS原发肿瘤的突变被列入(32和结肠直肠癌,51个乳腺癌和17个肺癌)。该研究报告的90.2%的敏感性和94.9%的特异性[14]。最近,为78%的灵敏度KRAS分析报道用冷-PCR(共扩增在较低的变性温度-PCR)/用于DNA高分辨率熔解从循环在一个大小选择的测定法(ScreenCell)分离的肿瘤细胞中提取[15]。
循环血浆中游离DNA
循环肿瘤DNA(小牛胸腺DNA)对应于由肿瘤细胞主动地或被动释放的片段化的DNA,细胞凋亡或坏死[期间16]。在肺癌患者[无细胞DNA增加17]。高水平与预后不良相关[18]和治疗期间的变化可以帮助监测肿瘤负荷[19]。尽管如此,无细胞DNA由于其特异性低一些限制,因为正常细胞或多种炎症感染性良性病症可以增加其电平[20]。可以通过靶向突变的肿瘤特异性DNA,可以避免此问题。因此,检测几个基因组改变的,包括那些的表皮生长因子受体,BRAF和KRAS在循环DNA是可能具有良好的诊断准确度和优异的特异性和敏感性,尤其是当使用数字微滴PCR(ddPCR)21- - - - - -23]。
我们最近表明,监测突变叶绿体DNA与ddPCR是后续的突变的非小细胞肺癌突变克隆一种非侵入性的方式,如与明显BRAF-mutated肺腺癌[24]。另一个非常令人兴奋的应用是抵抗的靶向治疗过程中机制的早期发现。的检测表皮生长因子受体- t790m突变的ctDNA,例如,在放射学进展之前EGFR-突变肺腺癌[21]。NGS允许的突变DNA的非常小的量(0.4%)的检测(KRAS,EGFR,BRAF,等),以及其他基因组改变(HER2插入,cMET的扩增和ALK,ROS1和RET重排)在血浆中具有100%的特异性和灵敏度,类似于ddPCR(77%)[25]。
肿瘤采样技术的决策树算法
初始基因分型,组织仍然应该是肿瘤的分子谱的第一选择。活检确实是必需的组织学诊断,并可能在一审中被使用。然而,微创技术应当优选在可能的情况。常规支气管活检是优选的的情况下,近端支气管肿瘤和线性EBUS-TBNA优选用于支气管周围的肿瘤或纵隔淋巴结[3.- - - - - -5]。
新的工具已经开发访问远端肿瘤,避免与计算机断层扫描(CT)相关的并发症引导下经胸活检(出血和气胸)26]。经仔细分析CT扫描后,可通过受累支气管引入放射状EBUS微型探头(rEBUS-MP)。当小探头到达肿瘤时,正常的肺“暴风雪”样貌被局灶性周向低回声代替,然后用活检钳代替小探头。一项荟萃分析报告称,对直径小于20毫米的结核,78%的总灵敏度为20毫米,56%的总灵敏度为20毫米[27]。然而,对于在CT扫描上显示支气管征的患者,必须保留这一步骤[28]。
虚拟支气管镜导航使用磁场,磁传感器探头和三维集成,以使CT扫描重建,并指示支气管镜的位置。该diagnostic yield of this technology is good (73.8%), even for lesions <20 mm in diameter (67.4%). This procedure is expansive and seems to be particularly suited for the upper lobes and peripheral third of the lung field [29]。
然而,如果分子表征不能对这些样品进行评估,液体活检是优选的,以避免第二侵入性采样过程。叶绿体DNA的测序被批准用于分析的唯一技术表皮生长因子受体突变状态和应作为在这种情况下的第一行方法。其特异性强,促进表皮生长因子受体酪氨酸的处方激酶根据其结果抑制剂(EGFR-TKI的)。然而,这种方法的灵敏度是不完美[三十]和否定结果必须由组织活检,这将使更宽的基因分型,包括重排(ALK,ROS1来确认等等。)[31]。
在进展,液体活检构成分析耐药机制的最佳选择。在EGFR突变的肿瘤的情况下,叶绿体DNA构成检测T790M突变,发生在超过一半的病人的一个非常有用的工具。这种技术的特异性高。此外,由于肿瘤的异质性和所使用的技术的改进的检测灵敏度时,T790M突变甚至可以在考虑T790M阴性患者基于组织分析来检测,使得叶绿体DNA的互补工具。美国食品和药物管理局(FDA)提出了一种新的模式来检测病情进展的T790M突变。等离子体基因分型应被提出作为第一线的技术,作为其高特异性促进了第三代EGFR-TKI的处方。然而,它的灵敏度是不完善的和负的结果必须由组织分析,这使得电阻的其它机制(小细胞癌转化,MET或HER2扩增,PIK3CA突变的检测来确认等等。)[32]。
决策树算法中提出图1。
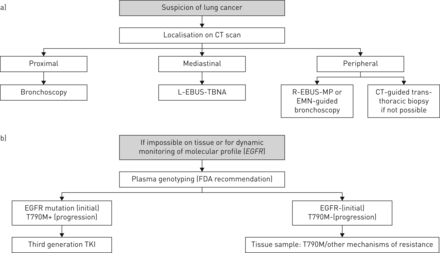
用于初始诊断(a)和病程进展(b)的肿瘤采样和分子分析的决策树算法。L-EBUS-TBNA:线性支气管内超声经支气管针吸;R-EBUS-MP:支气管内超声小探头;人物:电磁导航;美国食品和药物管理局;表皮生长因子受体;酪氨酸激酶抑制剂。
使用的方法来检测的分子改变
不同的方法可用于鉴别可在非小细胞肺癌中遇到从FFPE样品或材料的其他可获得的来源,例如细胞学标本或循环DNA获得的多样体细胞基因组畸变(点突变,插入或缺失和基因重排)。有些技术使基因突变进行甄别和感兴趣的区域测序,而另一些分析具体的和已知突变。
由于实体癌症的细胞异质性,主要的技术挑战是在肿瘤活检中检测体细胞变异。在野生型序列升高的背景下,体细胞突变的数量可能较少,因此需要比那些用于生殖系变异的更敏感的检测方法。此外,所面临的挑战是为小型活组织检查和液体活组织检查开发更敏感的技术。特别是,循环突变DNA只占总循环DNA的很小一部分[33]。继推出第一代毛细管的Sanger测序仪(1995年),提高技术的数字现在已经可用,包括实时PCR平台,数字PCR和NGS。
筛选试验
Sanger测序
直到最近,的Sanger测序被认为是所有突变的鉴定的金标准。这种技术使用测序根据上的PCR产物进行的终止,其生成由尺寸使用毛细管电泳[分离荧光标记的DNA片段34]。然而,Sanger测序具有非常低的敏感性。所述突变的变体应代表总的肿瘤DNA的至少15-20%待检测[35]。
焦磷酸测序
焦磷酸测序是通过合成进行测序,通过一系列酶促反应,利用生物荧光法检测核苷酸与DNA链结合过程中焦磷酸的释放情况。焦磷酸测序可以在预定位置识别单个碱基或短链核酸序列。等位基因的检测限为5% [36]。
高分辨率熔解
高分辨率熔解用于屏幕中的测序分析之前,感兴趣的基因突变。它是基于检测的PCR的解链曲线的图案的小差异后-PCR方法中,通过所述过渡从双到单链中的荧光染料的存在下产生的地嵌入从双链DNA和区分野生型序列纯合子或杂合子变种。在较低的变性温度提高从一系列2-10%该测定的检测限于与野生型DNA共扩增的突变体的混合物的0.1-1%,PCR(COLD-PCR),其允许少数等位基因的优先扩增可以用高分辨率熔解组合[36]。
新一代测序
NGS是一种高通量,在浓度低至5%检测肿瘤样品中的体细胞突变的测序方法。几种化学和分析方法是可用的。Illumina公司平台基于上形成簇,其然后通过重复循环测序上使用四种荧光标记的核苷酸的混合物的单碱基延伸,然后成像的固体支持物使用桥式PCR的DNA片段的制备。与此相反,离子洪流平台依赖于使用乳液PCR模板制备。特定的核苷酸的掺入的氢离子的释放下面检测。
治疗诊断的生物标志物和相关联的靶向疗法的数量正在迅速增加,和组织样本通常可以限定于非常少量的DNA。NGS可迅速同时评估肿瘤的完整基因组景观。在上组织样品初步诊断NGS促进肿瘤的基因型的鉴定。目标板包括参与肺癌的肿瘤发生的基因是优选的。一整个外显子组的方法将显著增加周转,生物信息学分析和成本,以及非靶向基因组异常的风险。当基因型是不可能的组织,血浆针对性NGS可能是大有裨益[25]即使这种方法还没有被验证常规使用。循环的游离DNA的基因分型可克服在同一肿瘤(空间异质性)的不同区域之间存在的肿瘤内的异质性的双重问题,原发肿瘤和局部或远处复发在同一病人之间(时间异质性)的技术。对血浆样品NGS也可能成为下靶向治疗肿瘤生物学的后续分析一个有吸引力的技术。如果像ddPCR靶向测定是在耐EGFR-TKI患者的首选方法,在其中T790M抗性突变是监测电阻的主要机制,多重测定应在其他TKI故障情形大有裨益。例如,在间变性淋巴瘤激酶(ALK)的患者阻力而与克里唑替尼处理的更趋于不均匀的。众多ALK抗性突变已报道和活性谱与不同的第二代和第三代ALK酪氨酸激酶抑制剂(ALK-TKI中)不相似[相关联37]。一种等离子体多路复用NGS从而测定将是这样的情况下是非常有用的。
有针对性的测定
大多数用于检测特定突变的方法是使用等位基因特异性PCR探针基于多重实时PCR;然而,他们只能检测已知突变。在肺腺癌的情况下,这种有针对性的方法似乎特别适合于检测频繁和定位的变化,如EGFR del19,L858R,KRAS G12X或EGFR T790M突变。
等位基因特异性竞争的TaqMan®PCR
竞争等位基因特异性PCR的TaqMan®(castPCR™)技术(Life Technologies公司)联合等位基因特异性的TaqMan®定量PCR与等位基因特异性的小沟结合受体阻滞剂来抑制由野生型等位基因特异性扩增。CastPCR™技术提供在检测大量野生型DNA(0.1%)的中少见的突变等位基因的高灵敏度和特异性。
Therascreen®突变套件
Therascreen®突变试剂盒(Qiagen公司)是组合的扩增阻滞突变系统(ARMS),这是一种等位基因特异性扩增的方法,与蝎PCR引物,其被连接到探针(荧光团和淬灭剂的实时PCR测定)。
COBAS?套件
在COBAS?试剂盒(罗氏分子系统)使用实时PCR特异性TaqMan探针(每个具有不同的荧光强度,由荧光团淬灭剂对产生的)来扩增和分析突变。
肽核酸钳技术
肽核酸钳技术包括使用特定的肽的核酸,其抑制野生型序列的扩增的突变等位基因的选择性扩增的。
聚束
整经(珠,乳液,放大和磁)是基于乳液数字PCR结合DNA于磁珠,使用流式细胞仪[促进分离和检测的过程38]。
分子生物学方法来检测基因重排
荧光原位杂交
荧光原位杂交(FISH)是用于检测ALK或ROS1重排的金标准,但不识别该融合伙伴。此细胞遗传学技术使用耦合到是与基因的5'和3'末端互补的荧光分子的两个小的DNA链。由于在荧光显微镜下观察到的,野生型细胞中的两个探针彼此非常靠近和它们的荧光可以融合;而在突变体细胞中,这两种颜色被很好地分离,或仅一个被检测到。一些认证ALK和ROS1破开的荧光原位杂交测定是可用[41]。FISH分析被认为是ALK NSCLC突变检测的金标准。2011年,FDA批准了Abbot Vysis ALK Break Apart FISH探针试剂盒用于分子诊断测试。
生物标志物靶向治疗
非小细胞肺癌的主要生物标志物的发生率和特征总结表2。其地理分布在呈现图2。
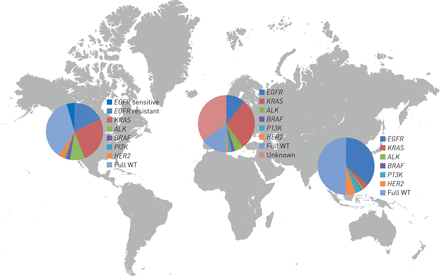
根据地理起源非小细胞肺癌的分子流行病学。亚洲:从L-我et al。[46],S韩et al。[47]和Z豪et al。[48]。欧洲 - 来自Barlesiet al。[49],Maziereset al。[50]和Maziereset al。[51]。美国:给K里斯et al。[52]。
表皮生长因子受体
流行病学
表皮生长因子受体(EGFR;erbB-1;HER1)属于酪氨酸激酶受体的ERBB家族[53]。该表皮生长因子受体基因位于第(7p11.2)染色体7和编码一个170 kDa的跨膜糖蛋白具有酪氨酸激酶活性。在结合于特定配体,表皮生长因子受体经历构象变化和磷酸化,从而导致参与细胞存活和增殖的几个途径,如PI3K / AKT,RAS / ERK和JAK / STAT,等等[活化54]。80年代以来,一些临床研究已经报道增加EGFR表达水平或在肺癌增加基因拷贝数,特别是在鳞状细胞癌,腺癌和大细胞癌[55- - - - - -58]。虽然EGFR的预后协会还讨论了,因为临床报告出现不一致[中57- - - - - -61],选择性抑制剂对EGFR酪氨酸激酶活性的发展(例如吉非替尼和厄洛替尼)已经允许特定突变的鉴定(2004年)表皮生长因子受体存在于对这些抑制剂有显著临床反应的患者亚组中的基因[61- - - - - -63]。自2004年以来,许多努力已经取得了识别和描述这些突变,从而产生的数据量大现在允许的患病率相对准确的概述表皮生长因子受体该人群中的突变。
在非小细胞肺癌中表皮生长因子受体外显子18至21,内被发现,其编码为周围设酶的ATP结合口袋的酪氨酸激酶结构域,其也结合位点的一部分表皮生长因子受体-TKi。最常见的表皮生长因子受体突变是外显子19(主要是delE746-A750)的符合读框的缺失,其占全部的约45%表皮生长因子受体突变,随后L858R取代在外显子21,在所有的40-45%中发现表皮生长因子受体突变[64]。对于剩下的10%,其他罕见表皮生长因子受体已报道的突变包括(分别为1%和4%),外显子19和20的插入和点突变外显子21(L861,大多L861Q:1-2%)和外显子18(主要是G719X:3%)[65- - - - - -68]。治疗方案的选择可能会为患者窝藏常见和罕见的基因突变不同,因为不是所有的表皮生长因子受体突变赋予相同程度的对EGFR-TKI的灵敏度的(见下文)。
表皮生长因子受体突变几乎完全与腺癌或细支气管肺泡组织学亚型相关,并且在很大程度上与腺癌的突变相互排斥KRAS要么ALK重排(在下面描述)[69]。他们是在非吸烟者和女性更经常观察。频率表皮生长因子受体突变是比在西欧(10-15%)和北美(15%-20%)的个人亚裔(45-50%)的人要高得多。值得注意的是,高可变性已经患病率被报道表皮生长因子受体亚太群体中的突变,在越南(64.2%),泰国(53.8%)和中国(50.2%)比印度(22.2%)和孟加拉国(23%)更高的频率[70,71]。这种变化也已在南美观察,用比例较高表皮生长因子受体相较于白种人(阿根廷,19.3%)美洲印第安人亚群之间的突变(主要是秘鲁,67%,但也墨西哥,31.2%,和哥伦比亚,24.8%)72]。代表世界地图表皮生长因子受体在NSCLC患者因国家的突变频率已经从151项研究中刚刚建成的全球[73]。
治疗
靶向治疗仍然是谁心怀治疗肺癌患者的最佳策略表皮生长因子受体激活突变。目前在美国和欧洲有三种药物(吉非替尼、厄洛替尼和阿法替尼)。对EGFR- tkis的敏感性似乎高度依赖于EGFR突变的类型。最佳反应率(RR)是观察到的患者包藏两个主要表皮生长因子受体改变(外显子19个缺失和L858R突变),具有更高的易感性在患者中观察到与外显子19缺失的治疗(70%-100%RR与对于那些与L858R突变20-67%)[65,66,74,75]。虽然罕见表皮生长因子受体突变通常与EGFR-TKI的较差的效率相关联相比于常见的突变,患者L861Q或G719X突变可以受益于这种类型的治疗,而在20外显子插入更可能于TKI治疗赋予抗性[61,74]。法国的一项多中心研究证实了这一点,该研究分析了10 117个样本,其中1047个样本(10%)发生egfr突变(102个发生罕见突变),外显子20插入与EGFR-TKI耐药有关,而外显子18突变对治疗表现出更好的敏感性[66]。EGFR-TKI的治疗具有罕见的突变也可能是很重要的选择;例如,阿法应在患者G719X和L861Q突变[青睐64,76]。对于患有非常罕见的或复杂的突变(一个以上的突变)(高于G719X和L861Q等)表皮生长因子受体基因,EGFR-TKI治疗的效率并没有得到明确因为少数患者证明。然而,比例表皮生长因子受体突变对EGFR-TKI治疗赋予灵敏度似乎是比其赋予阻力大[74,77]。我们认为一线EGFR-TKI治疗应该是治疗特发性肺损伤患者最合适的策略表皮生长因子受体突变,除非该数据表明在这个特定背景下靶向治疗一个明显的缺点。
Despite a high global response rate (∼60–70%), all patients usually relapse within a median delay of 12 months. In the majority of cases, this is due to the existence of theT790M患者50-60%,和时常要少得多把关突变引起的放大HER2和MET原癌基因中,上皮至间质转变,或更少见小小区组织学转化[78- - - - - -81]。一些第三代EGFR抑制剂最近已开发(例如osimertinib和rociletinib)的临床疗效T790M突变[82,83]。
Osimertinib(AZD9291,Tagrisso)最近收到加速审批通过FDA批准用于治疗的患者进行确诊T790M突变。然而,自适应耐药机制已经在患者的一个小的子集的第三代EGFR抑制剂治疗,其中包括那些与谁后复发描述表皮生长因子受体C797S突变[84]。虽然最初egfr激活突变(主要是exon-19缺失和L858R点突变)通常保存在erlotinib或gefitinib处理产生的抗性克隆中,但抗性克隆来自osimertinib或rociletinib处理T790M阳性肿瘤是很少的正面T790M突变。这是因为T790M抗性肿瘤往往伴有T790M阴性抗性克隆,它们可能对第三代EGFR抑制剂赋予抗性[85]。因此,这种内部tumoural异质性被认为是靶向治疗的致命弱点,并研究这种克隆多样性的起源可以提供线索,以促进更持久的缓解。
ALK
ALK,胰岛素受体酪氨酸激酶家族的一个成员[86],被编码的ALK基因2号染色体上。ALK首次鉴定为NPM-ALK(核酸蛋白-间变性淋巴瘤激酶)的一部分,由2号染色体和5号染色体之间的易位导致的致癌融合蛋白(t[2;5] [p23;q35])与间变性大细胞淋巴瘤相关[87]。同样的易位也已经在霍奇金淋巴瘤描述88]。随后,在融合基因的形成染色体2P结果内的小反转包含棘皮动物微管相关蛋白样4的部分(EML4)基因ALK基因,这是在一个切除标本腺癌鉴定从62岁男性吸烟者[89]。几个变种ALK-EML4已经确定[90]和其他合作伙伴的融合已经报道了非小细胞肺癌,其中包括KIF5B(91]。
ALK重排发生在NSCLC患者的3-5%,且当中更加普遍,年轻患者有轻度吸烟史,腺癌组织学和肿瘤是野生型表皮生长因子受体和KRAS(92,93]。这些因素可以帮助医生识别高危人群,可以进行ALK测试时,即使这些标准还不够强大,选择基于流行病学特征的患者。根据这些调查结果,国际协会肺癌的研究和欧洲肿瘤医学学会的指导方针一致的两个建议筛选所有患者的晚期肺腺癌,不论临床特点。
克里唑蒂尼是被批准用于ALK +非小细胞肺癌的药物。它是口服的,小分子抑制剂,其目标ALK,ROS1和MET受体酪氨酸激酶[94- - - - - -96]。它已经显示出显著(〜60%)总体反应中的单臂相-I研究率[95],导致其在美国的批准。最近III期临床试验的结果,已经证实克里唑替尼的优越性相比在二线化疗[97]和一线[98对于设置ALK +非小细胞肺癌。Unfortunately, the majority of patients also develop resistance within the first 12 months of therapy [99]。
在分子生物学和耐药机制的认识发展ALK +非小细胞肺癌已经取得了过去几年。Alectinib和ceritinib,双方第二代ALK抑制剂,具有比克里唑蒂尼颅内高活性,用于治疗脑膜癌病,最近获得批准,治疗患者谁是难治性,或不耐受,克里唑蒂尼的形式。连续使用ALK抑制剂导致提高成活率,一些ALK +patients reaching an overall survival of 5 years.
Lorlatinib(PF06463922),第三代ALK / ROS1抑制剂可以克服某些耐ALK突变(与ALK L1198F除外),现在是在相II期临床试验,其包括ALK +和ROS1 +NSCLC患者。ALK I1171X和ALK F1174X抗性突变有不同的敏感性alectinib和ceritinib,这可能会确定两个抑制剂应选择。等耐ALK已报道的突变。在一个案例报告,S山楂等。(100]近日报道,C1156Y-L1198F突变可能赋予lorlatinib,ceritinib,alectinib和brigatinib,但再使细胞对克里唑蒂尼性。
KRAS
在突变KRAS基因(V-KI-RAS2 Kirsten大鼠肉瘤病毒癌基因同源物)通过高频和特定流行病学特征。改建为KRAS基因最常定位于密码子12和更罕见的密码子上13和61 [101]。改建为KRAS基因原因GTPase活性的丧失,从而影响它的反馈调节。KRAS然后不断促进细胞增殖通过的MAP激酶(BRAF / MEK / ERK)和磷酸肌醇3-激酶(PI3K)途径[102]。G12C替代是最常见的改变,代表所有的52%KRAS突变。G12V、G12D、G12A和G12S的突变分别占11.6%、7.2%、2.9%和1.5%。在从不吸烟的腺癌患者中,50%的病例中发现G12D替代[103,104]。KRAS基因突变可以在腺癌的18-32%可以发现,大细胞癌12.8%,腺鳞癌的10%,在高加索人患者鳞状细胞癌[的1.6-7.1%49,105- - - - - -108]。之间的关联KRAS突变和烟草不可否认[108- - - - - -110],和已经以两种荟萃分析[被清楚地识别110,111]。尽管如此,KRAS突变也可在非吸烟者[5-15%发现112- - - - - -114]。KRAS突变的非洲裔患者更频繁相比白种人(OR 2.4; P = 0.048)115],并远在亚洲患者不太频繁,有11.2%的发病率[110]。
KRAS基因突变通常在患者描述为不利的生物标志物与切除肺腺癌[116,117],为1.40(N = 5216,P = 0.01)中由M的荟萃分析风险比ascaux等。(105]。然而,对预后的影响KRAS突变仍在争论。在用V研究illaruzet al。(106],其重点是九百八十八分之三百十八例腺癌窝藏一个的KRAS突变,多变量分析(与调整其他预后因素,特别是吸烟状态)显示的无预后影响KRAS。在另一起涉及1935年一组患者最近的一项研究,KRAS突变似乎与较短的总生存期相关,但不影响无进展生存期(PFS)111]。
矛盾的研究结果对于替代的不同亚型的影响报告;我HLEet al。(104]报道G12V的不利影响,而C则serepes等。(109]观察到类似患者对化疗和更长的PFS更好的反应。没有具体亚型KRAS突变表明在另一项研究中任何预后值,该值评价辅助化疗[118]。
上一页回顾性研究还报告的不利影响[119- - - - - -121],这似乎主要发生在位于13号密码子上的突变患者身上[118,122]。检测的KRAS在叶绿体DNA突变与基于铂的化疗[不良应答相关23]。然而,这些结果并没有一贯遵守[122- - - - - -124]。因为KRAS突变导致前面提到的信号通路的持续激活,与EGFR的激活无关,EGFR- tki的低效率似乎是一个逻辑推论。大多数回顾性分析与这些结果一致,应答率通常<3% [125- - - - - -130]。不过,一些临床试验未能显示出任何生存的区别[131,132]。与大肠癌的情况下,KRAS突变状态不影响肺腺癌单克隆抗EGFR抗体的响应[133]。
BRAF
在RAS蛋白激活后,BRAF另外两个激酶蛋白,MEK和ERK的诱导磷酸化。ERK的活化形式可以易位到核中并磷酸转录因子来调节分化,增殖,血管生成和细胞凋亡[134]。多数的BRAF突变定位于激酶结构域,增加激酶活性BRAFMEK。BRAF突变在1.6%和在吸烟者和非吸烟者,非小细胞肺癌病例的1.8%分别实测值[49]。
胸苷腺苷颠换在核苷酸T1799A在外显子15,这导致缬氨酸密码子600(V600E)谷氨酸取代,是最常见的突变,占所有病例的一半。其他两个最频繁观察到的突变是在G469A突变(箱子39%)和D594G突变(箱子11%)[135]。然而,许多非V600E突变只显示中间和低激酶活性;因此,他们作为司机癌基因的作用仍然[不清楚136]。在916名NSCLC患者,BRAF突变1.9%,其中主要包含腺癌(88%),女性患者(64.7%)和吸烟者(70.6%)被确定[137]。对1046例患者的回顾性分析显示,腺癌和鳞状细胞癌的患病率分别为4.9%和0.3%,V600E为56.8% [138]。
的预后影响BRAF突变保持在非小细胞肺癌争议。PAIKet al。(135]和Cardarellaet al。(139]表现出的无显著影响BRAF晚期患者生存的突变。然而,BRAFV600E亚型与侵袭性组织学(微乳头特征在80%的患者)相关联,并且降低的无病生存率和总生存率[139,140]。35例患者接受的BRAF靶向性治疗(威罗菲尼,dabrafenib或索拉非尼),用于BRAF-mutated lung adenocarcinoma in the European cohort, 83% had a V600E mutation, which appeared to be associated with a better prognosis than other subtypes of mutations (median survival 25.3 months与11。8 months, respectively) [141]。在一系列广泛的63名治疗的患者的另一项研究发现,V600突变的一个良好的预后比非V600突变(24%3年生存率与分别为0%)。吸烟似乎与非v600突变有更强的相关性(11%的非吸烟者与具有V600突变吸烟者)的42%142]。
PI3K / AKT / mTOR通路
PI3K/AKT/mTOR信号通路具有多种功能,包括调节细胞存活、分化和显示干细胞样特性、生长、增殖、代谢、迁移和血管生成等[143,144]。它在下游信号传导中起关键作用通过几种效应的磷酸化和活化,包括丝氨酸/苏氨酸激酶,AKT和mTOR(雷帕霉素的哺乳动物靶标),细胞生长和代谢的主要调节剂。通过PI3K / AKT途径的信号被负由肿瘤抑制基因调控PTEN(磷酸酶和张力同源物)[145]。
虽然在PI3K途径像差在某些癌症(包括浸润性乳腺癌,头颈部癌,结肠癌,子宫颈癌和卵巢癌)特别普遍,它们在肺癌罕见。最常见的改变是基因突变PIK3CA和损失PTEN功能(突变或缺失)。这些改变是在鳞状细胞癌更普遍(10-16%PI3KCA突变,15%的损失PTEN)中比在腺癌(3-4%PI3KCA突变,3%的损失PTEN,经常与相关KRAS要么表皮生长因子受体肺的突变)[146- - - - - -149]。PI3K像差与预后不良相关联,转移性疾病的更高负担和脑转移的发生率较高[150]。
的影响PIK3CA对预后和响应标准疗法突变仍下落不明。一项回顾性研究报告指出,伴随PIK3CA突变导致总存活率降低表皮生长因子受体-mutant肺腺癌(18与33 months, p=0.006), although the authors found no evidence that a concurrentPIK3CA突变影响EGFR-TKI治疗的结果[151- - - - - -155]。
HER2
人表皮生长因子2(HER2,ERBB-2 / neu基因)是erbB受体酪氨酸激酶家族的一个成员。该ERBB2基因,其编码HER2,是一个重要的增殖驱动程序,通过PI3K-AKT和MEK-ERK途径的激活下游信号传导。无配体已用于该受体,它是由同型二聚化或杂二聚化激活与所述erbB家族的其他成员进行了描述。HER2突变包括在帧插入的外显子到20,导致受体和下游AKT和MEK途径的组成型活化。一个的诱导型表达HER2突变体(HER2YVMA)在小鼠肺上皮细胞,导致侵入性腺鳞癌的出现,与肿瘤的维护需要驾驶员的连续表达,如在证实表皮生长因子受体驱动的癌症[156]。HER2突变已确定在约NSCLC患者的2-4%[50,157],但在法国国家数据库的不到1%85]。
该突变是在女性中,非吸烟者和在腺癌亚型,其类似于主要观察到表皮生长因子受体-mutated NSCLC [50,157]。HER2基因突变可能是更相关的肺癌发生比HER2扩增或过表达,这反映了是相反的那些乳腺癌的条件。最近的研究表明,HER2突变可能在肺癌HER2靶向疗法,例如HER2-TKI [可预测158]和her2抗体[159]。
ROS1
与c-ROS癌基因1(ROS1)是一种相对较新的肺癌目标。这对从胰岛素受体家族酪氨酸激酶受体。涉及的染色体重排ROS1基因最初在胶质母细胞瘤中被描述ROS1(染色体6q22)融合至图基因和结果在转基因小鼠已经显示变换[160,161]。在NSCLC细胞系和原发性肿瘤,ROS1融合已经被识别为驾驶员突变[162]。ROS1融合伙伴包括SLC34A2-,CD74-,TPM3-,SDC4-,EZR-,LRIG3,KDELR2和CCDC6(163]。ROS1重排在非小细胞肺癌[1-2%发生94]。激酶结构域总是全部保留在ROS1融合蛋白,并在mRNA水平接合点总是发生在外显子32-36 [5'端164]。该ROS1激酶结构域具有与ALK激酶结构域显著的同源性。ROS1阳性患者共享类似的特征ALK阳性患者,如腺癌组织学,形态学,低龄化和非吸烟者的患病率较高[94]。ROS1在2014年和2015年分别确定了四个新的融合伙伴(CLTC,LIMA1,MSN和TMEM106B),并且发病率和临床病理特征ROS1 +NSCLC患者已全面荟萃分析中描述165]。克里唑蒂尼是一个非常好的反应率和PFS [相关51,166]。目前正在评估其他药物。
新兴的分子靶标
该RET基因是一种原癌基因[167,168]。可发生致癌激活通过它的突变或重排。在非小细胞肺癌,RET重排发生在未选择的情况下,1-2%。这些都是在不吸烟腺癌[常见169]。相反对甲状腺癌,其中CCDC6和NCOA4是比较常见的上游伙伴基因,KIF5B是最常见的上游融合伴侣RET非小细胞肺癌[170]。卡博替尼和凡德他尼表现出效率患者RET-rearranged肺癌在三个II期试验[171- - - - - -173]。其他RET抑制剂,包括已被批准用于治疗晚期甲状腺癌的卡波赞替尼、万德丹尼、索拉非尼和伦瓦替尼,以及已被批准用于其他适应症的波纳替尼、阿立替尼和舒尼替尼,尚未在临床试验中进行测试。
MET外显子14个突变表示在非鳞状非小细胞肺癌的3%的其它新的目标分子改变。这些突变在不吸烟者更容易检测到,并且对MET抑制剂响应必须在临床试验中进行评估,作为少数病例报告和有限的系列已经证明有利的结果[174,175]。
结论
总之,许多治疗诊断分子标志物的非小细胞肺癌的发现极大地改变了肺癌的分类,因而其管理。流行病学,对预后的影响和应对传统和靶向治疗是非常不同的,这取决于基因组改变。
脚注
利益冲突:未申报。
- 收到2016年8月31日。
- 接受2016年12月28日。
- 版权©2017人队















