摘要
以前的研究通过固定地点测量或有限数量的个人测量(通常针对一种污染物和短时间)来调查空气污染对慢性阻塞性肺疾病(COPD)患者的影响。这些限制可能会造成偏见并歪曲流行病学的联系,因为它们没有考虑到所有潜在的污染源或污染的时间变异性。
我们使用在精细时空尺度上测量的个人暴露于各种污染物的详细信息,以获得更可靠的效果估计。研究人员对115名患者进行了平均连续128天的随访,他们携带了专门为该项目设计的个人监测仪,测量温度、二氧化氮(NO2)、臭氧(O3.)、一氧化氮(NO)、一氧化碳(CO)和空气动力学直径<2.5和<10 μm的颗粒物,时间分辨率为1分钟。每位患者记录每日呼吸症状信息并测量呼气峰值流量(PEF)。一位肺科医生结合相关数据定义了一个表示“加重”的二元变量。使用混合效应模型评估暴露-反应相关性。
我们发现气态污染物与患者健康的恶化有关。我们观察到增长16.4%(95%CI 8.6-24.6%),9.4%(95%CI 5.4-13.6%)和7.6%(95%CI 3.0-12.4%),其在狭隘的范围内增加不,2,否和co。获得类似的结果用于咳嗽和痰。O3.发现与PEF和呼吸困难有不良关联。没有观察到颗粒物与任何结果之间的关联。
我们的研究结果表明,考虑到个人对空气污染物的总暴露,影响COPD患者健康的主要是气态污染物。
摘要
研究发现,COPD患者的呼吸健康与他们6个月以上使用便携式传感器测量的气态污染物暴露之间存在显著的不良关联。颗粒污染物没有发现明显的关联。https://bit.ly/3aqMT6O
介绍
慢性阻塞性肺疾病(COPD)是全球第三大死亡原因,除非采取紧急行动减少潜在的危险因素,否则死亡人数预计将进一步增加[1,2].COPD患者有急性恶化(“恶化”)发作的风险,通常定义为呼吸系统症状的突然恶化。COPD急性加重是英国成人急诊住院的第二大原因,与死亡率增加和生活质量下降有关[3.].
在严重空气污染时期,慢性阻塞性肺病住院和死亡率增加,而空气污染物水平即使在当前指南范围内也可能增加恶化风险[4- - - - - -6].污染物可能引发气道炎症,从而导致病情恶化,或可能增加对病毒/细菌感染的易感性,增加发作的严重性和频率[7].空气污染的极端情况或迅速变化的影响并没有很好地描述,部分原因是研究中对个别环境接触估计不够详细[8].
在城市环境中,人类对环境压力的暴露程度取决于一系列影响因素,如活动、环境、地理、源的邻近和气象。一个人的暴露水平是不断变化的,因为他们的日常生活和移动的环境。传统上,流行病学研究的短期接触评估是基于固定的监测地点,如果没有许多假设,就无法用这些地点准确描述包括室内和室外产生的污染的人类接触,这可能会引入偏差[9].主动移动传感器已用于微环境(如运输模式或室内)暴露的“快照”研究[10.].它们也被用来测量小组研究中的暴露程度[11.].然而,在每种情况下,监测周期都被限制在几个小时或几天内,而且受试者的数量也很少。测量、材料和计算技术的进步意味着实际限制正在变得不那么严格,为个人暴露评估提供了新的机会[12.].这一发展为环境暴露与急性健康结果之间的关联提供了可能,可在日常环境中进行大型预选小组或队列评估,而不是在室内或小型小组研究中。此外,这些传感器现在可以在更长的时间内部署,允许在患者的正常日常活动和行为可能发生变化的季节之间捕捉关联。
COPE研究(www.erg.ic.ac.uk /研究/ home /项目/ COPE-Characterisation-of-COPD-Exacerbations-using-Environmental-Exposure-Modelling.html)旨在描述个人空气污染暴露与肺功能、慢性阻塞性肺病症状和加重之间的关系,该队列由115名慢性阻塞性肺病患者组成。首次对多种污染物采用了直接个人暴露测量,而不是替代测量或模型,方法是将多参数个人传感器部署到所有患者身上,每个传感器使用时间长达6个月。通过延长个人接触监测的时间,可以在广泛的条件和活动下调查罕见的健康信号和症状。
方法
用于曝光数据收集的完整研究协议可用oore.等.[13.].研究招募方法和结果的描述见Q使用uint等.[14.].这里描述了关键细节。
参与者的样本
总共通过临床实践研究DataLink招募了130例,通过临床实践研究(CPRD;www.cprd.com)在英国的大伦敦内,其中115人提供了曝光和健康数据;15名参与研究<2周的患者被排除在外。选择基于先前的医学史,并没有储存患者。招聘后,患者填写了一个基本的问卷,包括居住类型,烹饪和加热燃料,汽车所有权和家庭吸烟者的存在,并提供个人空气质量监测器(PAM)。在招聘中使用峰值流量计(PFM)和日记卡的研究生理治疗师培训的参与者,随访每月电话。这种相互作用水平最小化了辍学率,以及最大化的有效数据捕获和日志卡使用。
个人空气质量显示器
专门设计,制造和测试了PAM。它是一种自主单元,包括多个传感器,用于活动和物理和化学参数。测量的时间分辨率设定为20秒。气态污染物(二氧化氮(没有2)、臭氧(O3.)、一氧化氮(NO)和一氧化碳(CO)均用电化学传感器定量。空气动力学直径<2.5和<10 μm (PM2.5和点10.)是由光学粒子计数器获取的粒子计数得来的。PAM还能记录温度、湿度、噪音水平、三维加速度计和全球定位系统的位置。测量值聚合为1分钟平均值,并存储在关系数据库中。用C语言描述了PAM的操作和性能hatzidiakou等.[15.].
所有传感器都在冬季和夏季进行了校准,在使用参考仪器部署到室外的参与者之前和之后都进行了校准。NO、NO的均方根误差小于4 ppb2和O3.,CO,0.03ppm,9和2μg·m−3在冬季和夏季分别为颗粒物。
参与者不需要与PAM单元进行交互,只需要每晚将其置于其充电器中。当患者离开家时,要求他们连续佩戴PAM 6个月。在家时,PAM被放在客厅里。
健康状况
每天晚上,参与者填写一张日记卡,记录症状的恶化、药物治疗的变化(包括口服类固醇或抗生素的使用)以及睡眠模式的中断。16.].日记卡还询问病人是否离开过家,是否携带了PAM。此外,患者每天在同一时间使用PFM记录他们的每日呼气流量峰值(PEF)。
实地工作完成后,由一名呼吸系统临床医生核实日记卡,并记录每天的“恶化”事件。急性加重定义为症状(呼吸、咳嗽或痰量/颜色)在正常变化之外持续恶化至少2天[17.].也考虑了无记录症状的治疗或保健利用的变化。
最初确定每个参与者加剧的确认通过根据日记卡上所写的内容,通过电话跟进,然后在去诊所时再进行一次。然后,A.L.和J.K.Q.通过对日记数据的独立审查再次确认病情加重,然后讨论临床意见中的差异。基于家庭邮编与2015年英国人口普查数据的交叉引用,对每位患者进行多重剥夺指数(IMD)排名[18.].
统计分析
污染物浓度汇总到每日手段(CO,NO,NO)2,PM2.5和点10.)或每日最大8小时(o3.).我们应用了预定义的混合效果模型分析[19.].使用线性回归分析PEF测量值,而急性加重和日常症状的出现(编码为二元变量)则使用逻辑回归进行检查。随机截取模型被用来对健康结果的预期变化提供条件估计,考虑到每个参与者重复测量之间的相关性[20.].我们的核心模型是以下形式: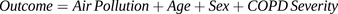 在哪里空气污染指个体每天依次接触到的每种污染物。为了考虑潜在的混杂效应,整个模型包括IMD作为参与者社会经济地位的指标和吸入皮质类固醇药物使用的二元变量。引入了限制的四自由度三次样条时间来解释数据中潜在的长期模式。温度也包括作为一个自然样条与三个自由度。
在哪里空气污染指个体每天依次接触到的每种污染物。为了考虑潜在的混杂效应,整个模型包括IMD作为参与者社会经济地位的指标和吸入皮质类固醇药物使用的二元变量。引入了限制的四自由度三次样条时间来解释数据中潜在的长期模式。温度也包括作为一个自然样条与三个自由度。
为了量化空气污染对患者健康的潜在长期影响,我们评估了滞后1、2和3天的影响估计,以及平均滞后0-3天的影响估计。双污染物模型还与除PM以外的所有污染物的成对组合进行了拟合2.5点10.,因为前者是后者的子集,以说明污染物之间潜在的协同或混淆效应。作为敏感性分析,完整的模型拟合排除了患者离开家而不携带PAM的人日。我们调查了不同季节和COPD严重程度的潜在影响修正。对于前者,我们将完整模型分为四类,IE。冬季、春季、夏季和秋季,而对于后者,我们将一个交互术语编码为两类,IE。轻微/中度和严重/非常严重。最后,我们比较了使用中央监测仪的环境测量值作为暴露指标时产生的效应估计值。
回归估计表达为预期PEF的变化,或者在除CO的所有污染物中的单位增加的情况下的加剧和症状的差异比例,其增加0.01ppm。还报道了每间条款范围(IQR)的估计。缺少数据被排除在分析之外。STATA版本15(Statacorp,College Station,TX,USA)用于所有分析。
伦理
卡姆登和伊斯灵顿的研究伦理委员会为该研究提供了伦理批准(14/LO/2216)。NHS研发部门也批准了CPRD GOLD数据的使用,CPRD独立科学咨询委员会也批准了该数据。
结果
描述性统计
招募时平均年龄为70.5岁,大多数患者(73%)患有中度或重度COPD (表1).所有患者报告他们的主要地址在大伦敦地区。
我们的数据库包括从2015年5月到2017年10月的14 740人日,每个参与者的平均随访时间和中位随访时间分别为128天和145天(最小-最大值为14 - 208天)。15%的人日观察到病情加重,18%的人日观察到呼吸困难,16%的人日观察到咳嗽,10%的人日观察到睡眠障碍和喘息,8%的人日观察到痰。数据丢失最常见的原因是参与者退出研究。其他原因包括参与者离家休假期间、PAM故障、未能向PAM收费以及未能记录健康数据。
均值±SD.24-h平均个人曝光测量为13.8±6.3 ppb2,NO,9.0±6.5 ppb,CO,15.8±18.0μg·m的0.2±0.1ppm−3对点2.5和16.8±20.6µg·m−3对点10.,而平均值±SD.8-h最大为O3.为6.5±5.3 ppb (表2).在污染物浓度下观察到季节性差异(补充表S2).在队列中,温度相对稳定,反映了大多数参与者在温度控制的建筑内花费大部分时间的事实。
除PM外,大气污染物之间的两两相关系数均较低(r<0.4)2.5和点10,r = 0.8(补充表S1).未携带PAM离家的人日为4083人(占总人日的28%)。
流行病学分析
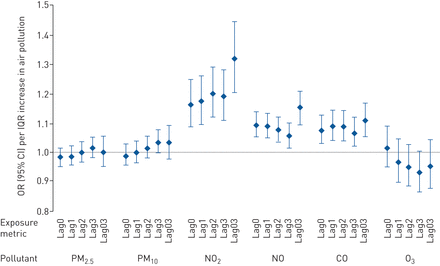
在我们对恶化发生情况的分析中,发现气体污染物与COPD患者的健康恶化有关,每增加一次一氧化氮IQR, COPD患者的健康恶化几率增加16.4% (95% CI 8.6-24.6%)、9.4% (95% CI 5.4-13.6%)和7.6% (95% CI 3.0-12.4%)2,不和co,分别(图1).除了“LAG3”的边缘协会外,涵盖整个研究期的主要或敏感性分析中,没有观察到颗粒物质的显着关联。IE。3.6% (95% CI 0.0-7.6%)。没有显著的,但始终是负相关,与O3.在完全调整的模型中。
与每种污染物在相同(Lag0)或以前(Lag1、Lag2和Lag3)天或相同和以前3天的平均值(Lag03)四分位区间(IQR)增加相关的恶化发生的优势比(95%置信区间)。点2.5:空气动力直径<2.5 μm的颗粒物;点10.:空气动力直径<10 μm的颗粒物;没有2: 二氧化氮;不:一氧化氮;CO:一氧化碳;O3.:臭氧。根据年龄、性别、慢性阻塞性肺疾病严重程度、多重剥夺指数、吸入皮质类固醇药物使用、温度和时间调整的随机拦截模型差:点2.510.8μg·m−3,PM10.12.0μg·m−3,没有2NO 7.2 ppb, CO 0.08 ppm, O3.十亿分之5.0。
当肺功能以PEF作为指标时,很少发现有显著的相关性(表3).我们观察到o的不利影响3.,IE。0.5升·分钟−1随着污染物IQR的增加而降低,并且在滞后暴露响应分析中对NO具有保护作用。
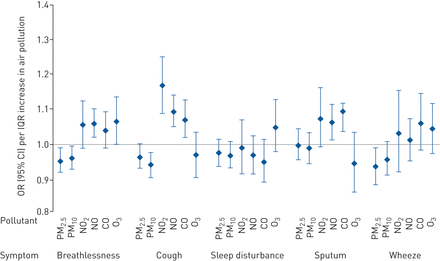
在自我报告的呼吸道症状中,气体污染物通常对参与者的健康有负面影响(图2).特别地,呼吸困难与NO(或1.060(95%(95%CI 1.019-1.102)相关)和o3.(OR 1.065 (95% CI 1.000-1.135)每个IQR);咳嗽不2(或1.167(95%CI 1.088-1.251),每IQR(或1.094(95%CI 1.052-1.1.139),CO(或1.071(每IQR1.071(95%CI 1.019-1.125));和痰,没有(或1.060(95%(95%CI 1.012-1.112),每个IQR的CO(或1.094(95%CI 1.035-1.115))。然而,颗粒物质与呼吸困难,咳嗽和喘息呈负相关。睡眠障碍与任何污染物无关。
对于与每个污染物的同一天(LAG0)相比,呼吸症状(IQR)增加的呼吸道症状(LAG0)增加的呼吸道症状的可能性比率的差异比率(具有95%的置信区间)。点2.5:空气动力直径<2.5 μm的颗粒物;点10.:空气动力直径<10 μm的颗粒物;没有2: 二氧化氮;不:一氧化氮;CO:一氧化碳;O3.:臭氧。根据年龄、性别、慢性阻塞性肺疾病严重程度、多重剥夺指数、吸入皮质类固醇药物使用、温度和时间调整的随机拦截模型差:点2.510.8μg·m−3,PM10.12.0μg·m−3,没有2NO 7.2 ppb, CO 0.08 ppm, O3.十亿分之5.0。
我们在冬季亚组分析中观察到显著的关系,IE。0.5%(95%CI 0.1-0.9%),0.8%(95%CI 0.2-1.3%)和3.0%(95%CI 0.1-5.8%)下午减少了每单位增长的加剧风险2.5,PM10.也没有2分别,但也分别为o和o的否定负(不利)关联的负(不利)协会3.OR分别为1.009 (95% CI 1.001-1.017)和1.149 (95% CI 1.074-1.229) /单位(表4).研究发现,在夏季,颗粒物与PEF的减少在统计学上显著相关,IE。−0.122 (95% CI 0.186 - 0.058−−)和−0.063 (95% CI 0.113 - 0.014−−)L·分钟−1每单位PM增加2.5和点10., 分别。O3.是积极的,总理2.5与春季的病情恶化呈负相关所有其他关联在统计学上都不显著。
当我们将分析限制在患者出门并携带监测器的人-天(表3和补充图S1),只有NO与PEF之间的正(保护性)关联没有统计学意义,且NO加重的优势比略有下降2, NO和CO,它们不影响估计的统计显著性。
对两种污染物模型的分析表明,除O的影响外,当我们对任何其他共污染物进行调整时,对所有污染物的估计的统计显著性没有变化3.在恶化时,在调整后为空(表5).没有加剧的差异2, NO和CO在两种污染物模型中降低,表明这些气体污染物之间存在潜在的混杂效应。O的负相关3.并且PEF保持不变。当我们对季节特定的两污染模型进行分析时,每个季节的发现几乎与之相同表4(结果未显示)。
观察NO随COPD严重程度的影响2CO和PEF组合,NO, CO和O3.和加剧协会(补充表S6).除了后者,所有这些显著的交互项被发现支持轻度/中度严重组的不良影响和严重/非常严重组的保护作用。然而,并不是所有的关联都具有统计学意义。当使用环境测量作为暴露指标时,我们发现恶化与个人暴露于NO和CO之间具有统计学意义的关联变为无效,而NO2比率几乎保持不变(补充表S7).对于PEF,我们观察了估计统计意义的一些变化(PM2.5也没有2效果在具有环境浓度的模型中显着,没有个人曝光;但是,所有的效果都与预期的方向相反(IE。更多接触环境PM2.5也没有2与PEF的增加有关)。O3.联想几乎翻了一番。
讨论
改善我们对环境应激与COPD症状和加重之间关联的认识,通过预测患者何时处于加重风险增加的状态,有可能促进更好的患者护理。这些关联也可用于警告患者高危期,从而防止病情恶化,从而改善生活质量,降低死亡率。
在本研究中,我们调查了慢性阻塞性肺病患者的呼吸健康与他们个人暴露于空气污染(包括环境(室外)和室内环境)之间的关系。研究人员使用了115名参与者的独特数据库,对其进行了长达6个月的集中跟踪。收集了个人接触各种空气污染物的情况,以及健康数据和潜在混杂因素的信息,结果进行了超过14700人日的观察。我们观察到呼吸道症状、IE。加剧,呼吸,咳嗽和痰,和气态污染物,如没有2, NO和CO. O3.与PEF呈负相关。没有发现颗粒物与对患者健康的任何不良影响有关联。
我们评估了我们各种敏感性分析的调查结果的稳健性。我们适合两种污染模型,以解释污染物之间的潜在混淆效果,我们排除在分析人员之外 - 患者在没有监视器的情况下出去的日子,我们检查了季节是否是一种效果改性剂。o之间的庞大积极关联3.和冬季的加剧可以解释为冬季O均匀低的组合3.在室内浓度(21.],通过滴定与NO反比[22.].另外,对于颗粒物质而言,观察到一些明显的保护作用和没有2在同一个季节。这些发现不能用两种污染物模型来解释,在该模型中估计数保持不变。
我们还比较了使用环境(中央监测仪)测量而不是个人暴露时的健康影响估计值。在估计中观察到一些差异,无论是在质量上还是在数量上,但我们预期可能是这样。流行病学研究通常使用中央监测点数据,或近年来更常见的环境模型来估计个人对环境空气污染的个人暴露,而我们直接测量个人总暴露。因此,必须谨慎地解释这种比较:一种方法评估环境空气污染暴露的影响,另一种方法评估总空气污染暴露。此外,这些研究使用环境浓度作为个人接触的代理。在大多数情况下,这将代表一个过高的估计,因为小于100%的环境污染通常渗透到建筑物,而个人花大部分时间在那里。因此,单位增长代表了代理度量,而个人度量不是代理度量。因此,不能使用这两种方法直接比较单位增长的流行病学估计值,因此,我们在本研究中表达了单位IQR增长的相关性。我们目前正在开发统计方法,以允许直接比较暴露方法,包括分离室内和室外源暴露,这将有助于估计偏差和绝对值与接触的代理措施。应该指出的是,我们的受试者比较古老,患有慢性呼吸状况,并且与其他同一人群相比,在家里可能花了更多的时间。
尽管如此,我们的发现与Peacock.等.[23.谁在伦敦与COPD患者进行了大型小组研究。结果类似于匹配污染物和健康结果之间的关联,尽管他们的研究仅评估了环境污染物的暴露。类似地,缺乏颗粒质量和PEF之间的显着关联,其其他具有COPD患者的研究[24.- - - - - -26.].测量绝对暴露的腔室研究可能更适合与我们的结果进行比较。在两个“牛津街”自然分庭研究[11.,27.]在呼吸功能和超细颗粒物质中发现哮喘和COPD患者的一致不良缔酶(在我们的研究中未测量的污染物),但不是PM2.5.实验室研究结果对所有污染物混合[28.- - - - - -30.].
COPE研究得益于从相对大量的参与者获得的过多的个人接触和健康结果测量数据。此前类似的个人接触研究要么只关注一种或两种污染物[31.,32.]和/或限制他们的后续时间或几周[25.,33.].使用专为本研究设计的显示器,我们能够收集六种不同污染物的测量。此外,我们每位参与者达到145天的中位随访,涵盖了长期,代表性的混合季节。
然而,COPE研究的主要优势在于收集了持续的个人暴露测量数据,尽管这对患者来说是一项艰巨的任务,但患者的依从性很高。坊间证据表明,这是因为慢性阻塞性肺病患者习惯于长期的临床监测,可以看到对他们自己的直接好处。之前的研究使用了类似大小的数据集,但他们使用的是环境污染的测量,而不是个人暴露[23.,34.].由于多种原因,这种暴露指标可能与患者的实际暴露有很大的不同,包括暴露于环境和室内污染源、建筑物的不同渗透因素、个人的时间-活动模式、不同微环境中的浓度和空间聚集[35.].这可能由于暴露测量误差而导致有偏差的流行病学估计[36.- - - - - -38.].在这项研究中,我们收集了个人曝光数据,以准确地代表参与者呼吸的空气质量,而不是代理估计。
我们的研究有一定的局限性。首先,COPE研究是在伦敦进行的,尽管伦敦是一个种族高度多元化的大都市,但不能提供全球范围内具有代表性的COPD患者样本。尽管如此,这些发现似乎与其他地方使用不同方法进行的一些研究是一致的[26.,33.,39.].
由于这项研究的长度和要求,一些参与者在离开家时并不总是随身携带显示器。然而,我们的结果没有改变,因为我们的分析仅限于那些携带显示器的人。值得注意的是,与其他人群相比,慢性阻塞性肺病患者的流动性更低,更习惯于携带/使用医疗设备。
最后,我们已经表演了许多辅助分析,其中一些可能导致统计上的重要协会偶然。然而,寻找各种健康结果的气态污染物的一致关联使得这不太可能。然而,我们观察到颗粒物质暴露和呼吸症状之间的一些意想不到的负联想,这难以在生物学上解释。潜在的理由可能是使用总个人暴露作为利息的公制,因为它反映了实际呼吸的患者,室外和室外产生的污染包括不同的来源,构成和行为[35.].假阳性关联可能是平等对待不同来源的污染的结果,而没有考虑到潜在的不同健康影响[40.].将通过将全部个人暴露分开进入室内和室外产生的污染,并在将来的工作中重新应用模型来进一步调查此问题,以及在曝光估计中的影响。本分区对于政策制定对室内污染的规定和缓解行动与环境空气的规定和减缓行为引起的政策制定非常重要,IE。交通,工业和农业排放与国内烹饪,供暖和清洁排放。这种分区还将有助于鉴定室内和室外环境中每种污染物的主导来源[15.].
结论
这项研究表明,在COPD患者队列中收集长期可靠的多污染物个人暴露测量值是可行的。通过使用个人测量,可以对总暴露量进行前所未有的详细评估。研究发现,个人暴露于气态污染物与呼吸健康之间存在显著关联,但与颗粒污染物无关。虽然这一发现对于确认个人污染物接触与患者健康之间的联系非常重要,但还需要进一步的工作来确定是哪些来源导致了这种联系,以及这些来源是室内还是室外。
补充材料
可共享的PDF
致谢
我们感谢Liz Moore和Adam Lewis(伦敦帝国理工学院,伦敦,英国),他们招募了这些患者,并成为他们的主要接触点,以及同意参与的130名参与者。
脚注
这篇文章有补充资料可从www.qdcxjkg.com.
作者贡献:D. Evangelopoulos:统计方法,统计分析和写作(原稿草案,审查和编辑)。L. Chatzidiakou:数据采集,方法和写作(审查和编辑)。H. Walton:概念化和写作(审查和编辑)。K. Katsouyanni:概念化,统计方法和写作(审查和编辑)。F.J.Kelly:方法和写作(审查和编辑)。J.K.Quint:招聘,数据采集,方法,临床建议和写作(审查和编辑)。R.L. Jones:方法和写作(审查和编辑)。B. Barratt:概念化,数据采集,方法,写作(原稿草案,审查和编辑)和监督。
利益冲突:D. Evangelopoulos没有什么可披露的。
利益冲突:L. Chatzidiakou无需披露。
利益冲突:沃顿没有什么可披露的。
兴趣冲突:K. Katsouyanni无需披露。
利益冲突:F.J.凯利没有什么可披露的。
利益冲突:J.K.Quint报告了医学研究委员会(MRC)的授予,在该研究期间;来自Asthma,Chiesi,MRC和Health Coupless的Asthnenca,Boehringer Ingelheim和Bayer的赠送和个人费用,在提交的工作之外。
利益冲突:R.L.琼斯没有什么可披露的。
利益冲突:B. Barratt没有什么可披露的。
支持声明:这项工作由医学研究理事会资助(MR/L019744/1)。该项目是英国国家卫生研究所(NIHR)英国临床研究网络(CRN)采用的一个组合。英国国家卫生研究所环境暴露与健康健康保护研究单位提供了额外支助,该单位是英国公共卫生部和伦敦帝国理工学院之间的一个伙伴关系。所表达的观点是作者的观点,不一定是英国国家卫生研究院、英格兰公共卫生部或卫生和社会保障部的观点。本文的资金信息已存入CrossRef Resder注册表.
- 收到了2020年9月8日。
- 接受2020年12月12日。
- 版权所有©ers 2021。
此版本在Creative Commons归因许可证4.0的条款下分发。