抽象
吸入皮质类固醇(ICS)被广泛处方用于治疗慢性阻塞性肺疾病(COPD),但具有可变的结果和不良反应,其可以是由遗传决定的。的primary aim of the study was to identify the genetic determinants for forced expiratory volume in 1 s (FEV1)与ICS治疗相关的变化。
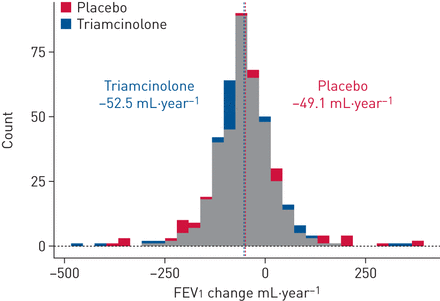
我n the Lung Health Study (LHS)-2, 1116 COPD patients were randomised to the ICS triamcinolone acetonide (n=559) or placebo (n=557) with spirometry performed every 6 months for 3 years. We performed a pharmacogenomic genome-wide association study for the genotype-by-ICS treatment effect on 3 years of FEV1802基因型LHS-2参与者的变化(估计为斜率)。199例慢性阻塞性肺病患者随机分为ICS组、氟替卡松组和安慰剂组。
总共5个基因座的表现出在p <5×10基因型逐ICS相互作用−6;其中,7号染色体rs111720447的单核苷酸多态性(SNP)被重复(discovery p=4.8×10)−6,复制p=5.9×10−5)用的交互效果相同的方向。ENCODE(DNA元件的百科全书)数据表明,糖皮质激素处理的(地塞米松)A549肺泡细胞系,糖皮质激素受体结合位点位于靠近SNP rs111720447。在LHS-2的分层分析,基因型在SNP rs111720447被显著与FEV的速率相关联的1ICS患者的下降(C等位基因β56.36 mL·年−1,95% CI 29.96–82.76 mL·year−1)和分配给安慰剂的患者,虽然较弱的关系和相反的方向,ICS组(C等位基因β−27.57毫升·−195% CI - 53.27 - 1.87 mL·年−1)。
与FEV相关的研究发现遗传因素1COPD患者,这可能提供关于COPD类固醇反应的潜在生物学新的见解与ICS改变。
抽象
遗传变异与吸入糖皮质激素对慢性阻塞性肺病患者长期肺功能下降的影响有关。这些变异可能为COPD类固醇反应的潜在生物学机制提供新的见解。http://bit.ly/2Ua7n9F
介绍
Chronic obstructive pulmonary disease (COPD) affects 384 million people and is the third leading cause of death worldwide [1]。吸入糖皮质激素(ICS)是世界上最常用的吸入抗炎药物对COPD患者[2,3.]。虽然目前,国际和国内的指南推荐使用ICS的只针对谁遇到频繁发作的患者(定义为每年两个或两个以上病情加重或前一年内住院)4]在临床实践中,大多数没有明显恶化史的患者都会服用这些药物。令人不安的是,长期使用含ICS的化合物与肺炎发病率增加有关[5]和加速骨脱矿质[6]。虽然平均ICS不修改COPD的长期“自然”的历史[7,有些人可能得到好处,而另一些人可能只得到坏处。有迫切需要了解生物学基础类固醇反应在慢性阻塞性肺病为了超越“平均”病人在临床实践(不存在)个性化治疗最重要的是使设计未来的干预措施,可以克服类固醇不敏感在慢性阻塞性肺病8]。
有强有力的证据支持遗传学在病人对ICS反应中的作用。首先,慢性阻塞性肺病的ICS临床试验的结果存在广泛的可变性[9,10]。早期对眼压的研究表明,患者对糖皮质激素治疗的反应方式既有家族隔离又有遗传性[11,12]。另外,在哮喘研究(其中ICS是最广泛处方药物)已经表明对ICS中的响应的特征在于高的个体内重复性[13]和高的个体差异[14],高达40%的哮喘病人对治疗没有反应[15]。综上所述,这些数据表明遗传变异在慢性阻塞性肺病的ICS反应中起重要作用。
在目前的研究中,我们的主要目的是通过测定1 s (FEV)用力呼气量的变化来发现改变ICS对肺功能影响的基因位点1)慢性阻塞性肺病患者随时间推移。我们首先使用了肺健康研究(LHS)-2的数据[7]以确定修订于FEV的速率ICS的效应的潜在遗传变型1decline over 3 years. We then externally validated these variants in a completely independent cohort, Advair, Biomarkers in COPD (ABC) trial [16]。
方法
肺部健康研究(LHS-1和LHS-2)
LHS-2的细节已先前公布[7]。短暂,LHS-2是一个多中心随机对照试验(RCT)来确定吸入型皮质类固醇激素的影响(1200µg去炎松)FEV1decline over 3 years [7]。LHS-2招募的研究对象为吸烟或最近戒烟(<2年),且之前参与过LHS-1。招募时,所有受试者的年龄均在40至69岁之间,均表现出经FEV诊断的气流障碍130-90%的预测值,在FEV存在的情况下1/支气管扩张术后用力肺活量比值<0.70。LHS-2排除了前一年经常使用支气管扩张剂或口服或吸入皮质类固醇的受试者。共有1116名受试者随机接受曲安奈德(1200微克/天,n=559)或匹配的安慰剂(n=557)。在基线时进行肺活量测定,然后每6个月进行一次,持续3年。所有的肺活量测量都是根据美国胸科学会的指南进行的。在这项研究中,我们只使用支气管扩张术后的数值。LHS在ClinicalTrials.gov标识符下注册NCT00000569,而目前的分析是英属哥伦比亚大学的伦理证书H16-01201下进行。
LHS基因分型
采用参与LHS-1的4251名欧洲裔美国人的buffy coat样本进行基因分型。基因分型和质量控制的细节以前已经描述过了[17]。简而言之,样本使用Illumina Human660WQuad v进行基因分型。1_A BeadChip(美国加州圣地亚哥)。利用单体型参考联盟小组与密歇根估算服务器进行估算。如果归责质量(r2)为<0.5,如果次要等位基因频率为<1%。对于1018(从1116)LHS-2名受试者谁参加LHS-1,818个具有基因型数据可用的(N = 410曲安西龙和n = 408安慰剂组)。这些参与者中,完整的表型信息是在802名受试者(n = 401曲安西龙和n = 401安慰剂臂)可用。LHS基因型健康数据库的国家机构数据可用于正在研究加入phs000335.v3.p2基因型和表现型(dbGaP)。
全基因组关联测试
我们对FEV进行了全基因组关联研究(GWAS)1变化率(毫升·年−1)使用具有基因型逐ICS(曲安西龙的添加剂遗传模型与安慰剂)交互项和基线FEV调整1以mL为单位,年龄、性别、体重指数、吸烟状况和前5位遗传主成分(PCs)按以下公式计算: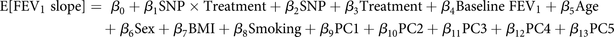 个别FEV1用FEV线性模型估计变化率1(基线、6个月、12个月、24个月和36个月的测量)。全基因组显著性阈值设定为传统的p<5×10−8。鉴于发现群的相对小的样本大小(LHS-2)中,我们定义一个次级组标准,以确定基因座可能滋生复制类固醇反应的真实信号。其中包括基因位点曾与FEV的关联1P的下降<5×10−6in LHS-2 and region plots demonstrating genetic support from surrounding single nucleotide polymorphisms (SNPs) within 500 kb of the sentinel SNP.
个别FEV1用FEV线性模型估计变化率1(基线、6个月、12个月、24个月和36个月的测量)。全基因组显著性阈值设定为传统的p<5×10−8。鉴于发现群的相对小的样本大小(LHS-2)中,我们定义一个次级组标准,以确定基因座可能滋生复制类固醇反应的真实信号。其中包括基因位点曾与FEV的关联1P的下降<5×10−6in LHS-2 and region plots demonstrating genetic support from surrounding single nucleotide polymorphisms (SNPs) within 500 kb of the sentinel SNP.
我们对根据吸烟状况(当前吸烟者)分层确定的位点进行了敏感性分析与以及根据慢性阻塞性肺病全球倡议(GOLD)肺活量分级得出的COPD严重程度。此外,我们只在那些被随机分配到ICS组的参与者中评估这些位点,而在安慰剂组中分别评估这些位点。
候选基因的方法:肺癌表达数量性状基因座的SNP为糖皮质激素受体基因NR3C1
的NR3C1基因编码糖皮质激素受体(GR),其是用于ICS靶受体蛋白质。除了不可知GWAS方法,我们使用的候选基因的方法,以确定在编码GR改性ICS应答的基因是否(或不)的变化。要或GR基因附近选择种候选SNP,我们使用生物测定基因调控方法,确定了与相关的基因变异NR3C1利用肺表达定量性状位点(eQTL)研究数据,研究基因在肺组织中的表达。有关的研究详情已于先前公布[18- - - - - -20]。简单地说,SNP和mRNA表达之间的关联调整了年龄的荟萃分析,性别,吸烟状况进行nontumour肺组织样本中的1111例患者谁接受肺切除手术进行。所发现的eQTLs要么独联体(从基因转录起始位点1mb)或事务处理(>1 Mb away or on a different chromosome). For the purpose of this study, we evaluated the lung eQTL dataset for SNPs that were significantly associated with the expression of probesets mapping toNR3C1在错误发现率(FDR) <5%时,选择发现GWAS中基因型p值最低的SNP来代表NR3C1在复制队列中对表型感兴趣的基因。
复制队列中的基因分型
我们尝试通过从参与ABC研究的COPD患者血液样本中获得的基因分型DNA,复制在LHS-2中识别的选择性SNPs。有关ABC队列的详情已于先前公布[16]。美国广播公司的研究是多中心的临床试验,评估吸入氟替卡松,一个ICS,单独或与沙美特罗组合,长效β的影响2-激动剂(LABA),减少慢性阻塞性肺病患者的全身炎症。所有招募的参与者年龄≥40岁,有≥10包年的吸烟史和FEV1<80%具有FEV预解码值1/支气管扩张后的<0.70 FVC比值。年代tudy participants underwent a run-in phase (visit 1: enrolment), during which they received fluticasone propionate (500 μg twice daily) for 4 weeks (visit 2: run-in phase). This was followed by a medication-withdrawal phase wherein ICS and long-acting bronchodilators were withdrawn for 4 weeks (visit 3: withdrawal phase). Participants were then randomly assigned to one of three arms: placebo, inhaled fluticasone (500 μg twice daily) or inhaled fluticasone/salmeterol combination (500/50 μg twice daily) for 4 weeks (visit 4: RCT phase). The lung function of each subject was measured at each visit. There were 212 participants who completed all four visits, of these 199 were successfully genotyped and our analyses were based on these subjects [16]。的ABC审判下ClinicalTrials.gov标识符注册NCT00120978表型数据可根据作者的要求提供。
Genotyping was performed at Genome Quebec using a multiplex PCR performed on 20 ng of template genomic DNA. Additional details on genotyping are available in the补充材料。质量控制过程包括基因分型强度簇(基因型的明确的分离),并从Hardy-Weinberg平衡偏差的检查。
复制队列的表型为FEV1change (in mL) over 4 weeks using data from visits 3 and 4 (即紧接4周的RCT阶段之后)。类似的线性模型来发现GWAS装配了六个单核苷酸多态性。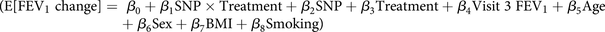 Bonferroni调整后的p值为0.008(6个snp的多次检测),以此作为具有统计学意义的复制的截止点。
Bonferroni调整后的p值为0.008(6个snp的多次检测),以此作为具有统计学意义的复制的截止点。
Phenome范围内的相关性研究
对于显著复制的snp,我们确定它们是否与其他疾病或表型相关。开放基因靶标平台用于评估复制snp的全表型相关性(PheWAS) [21],并辅以使用GWAS目录的查找[22]。
DNA元件的百科全书(ENCODE)数据
为了确定GR结合位点是否在靠近鉴定的SNP,我们利用DNA元件(ENCODE)染色质免疫沉淀(ChIP)与测序测定法(芯片SEQ)的数据集[的可公开获得的百科全书23]。年代pecifically, we investigated the GR binding scores with or without dexamethasone in varying concentrations (0–100 nM) and treatment times (GSM803358 and GSM803395) in the alveolar cell line A549.
摘要流程图显示的研究设计和人数包括的个人和主要结果显示在补充图S1。
结果
全基因组关联结果
在GWAS中,我们纳入了6 559 489个具有小等位基因频率>2%和归算质量>0.7的变异。共纳入802名没有缺失协变量的受试者。一个曼哈顿的阴谋显示图2。分位数,位数图中呈现补充图S2。基因组膨胀系数为0.991,说明关联统计无系统性偏差。全基因组未见明显位点(p<5×10)−8);然而,我们确定了使用二次标准中的p值5个基因座的5×10截止−6;他们的GWAS汇总统计数据显示在表2。使用一个额外的候选基因的方法,我们进行了查询对于已经显著与探针映射到表达相关eQTLsNR3C1。在FDR 195个显著eQTLs的<5%,SNP rs10057473具有的p = 4.16×10的eQTL p值−7对于问题集100122984,它映射到NR3C1基因在肺组织中,并且是具有最低基因型逐ICS相互作用p值的SNP。因此,使用SNP rs10057473表示NR3C1基因与在发现和复制队列的表型的关联。在发现药物基因LHS-2的GWAS中,GR eQTL rs10057473名义上与FEV相关联1下降(p = 0.02)。
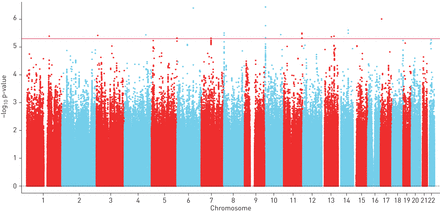
全基因组关联研究的曼哈顿情节基因型通过吸入的肺部健康研究-2在皮质激素的相互作用。该图显示的p值(-log10刻度)上的y轴和跨22条常染色体上的x轴的单核苷酸多态性的位置。横线表示p值截断5×10−6。
除了共同作用的结果,我们在报告表2单核苷酸多态性与治疗的主要作用。已知FEV的整体斜率1变化是负的,对于SNPs的主要作用,一个正的估计表明下降较慢,一个负的估计表明下降较快(加速)。
该协会结果六个与单核苷酸多态性FEV1每次随访的变化率(与GWAS使用的整体坡度相反)见表补充表S1。
敏感性和分层分析
对6个单核苷酸多态性的额外检测是在分层分析中进行的,该分析只包括ICS使用者、安慰剂组和当前吸烟者与前吸烟者以及由疾病的严重程度。分层分析的结果示于表3。结果表明,7号染色体上的SNP显著为rs111720447强烈FEV相关1decline in ICS users (C allele β 56.36 mL·year−1,95%CI 29.96-82.76;P = 3.35×10−5) and to a lesser extent in the placebo group, but in an opposite direction (C allele β −27.57 mL·year−1,95%置信区间-53.27–-1.87;p=0.036),如ICS组所观察到的。rs111720447的C等位基因在ICS与FEV的互作效应中表现出较强的基因型1changes in current smokers (β 72.74 mL·year−1,95%CI 32.47-113.00;p值= 0.0004)与former smokers (β 145.04 mL·year−1,95%CI 20.61-269.46;p=0.023) and in COPD GOLD II patients (β 85.97 mL·year−1,95%CI 38.32-133.63;p值= 0.0004),than in GOLD III and IV patients (β 116.33 mL·year−1,95%CI 8.24-224.42;P = 0.036)。该SNP没有表现出对FEV的交互影响1下滑GOLD I期患者(P = 0.38)。
在ABC队列复制
LHS-2和eQTL SNP中GWAS的5个显著位点NR3C1直接基因型在ABC队列。美国广播公司研究设计所示补充图S3. 出于分析目的,我们将两个治疗组(氟替卡松和氟替卡松/沙美特罗)归为一类(治疗)。共有199名参与者成功地对所有6个snp进行了基因分型。复制研究中199名受试者的人口统计数据如下表格1。
复制GWAS结果,我们计算了FEV1changes (in mL) over 4 weeks using data from visits 3 and 4 (即紧接4周的RCT阶段之后)。使用这种FEV1改变作为响应变量,类似的线性模型来发现然后GWAS拟合为六组的SNP。
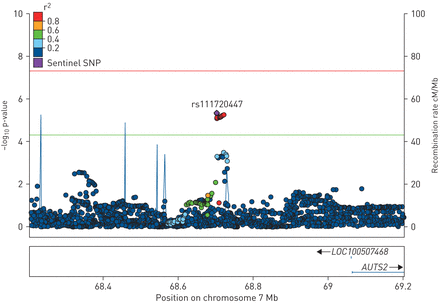
在复制队列中,两个snp在FEV之间有显著的相关性(p<0.05)1改变和基因型之间的相互作用与发现队列中观察到的作用方向相同。7号染色体上的SNP rs111720447具有很强的复制能力,p=5.98×10−5。SNP rs10057473是eQTL SNP基因NR3C1并以名义p=0.042进行了复制。将bonferroni校正的p值应用于6个SNP的复制(p=0.008),只有7号染色体上的SNP rs111720447的复制具有统计学意义。所有6个snp的结果显示在表4并在第7号染色体的复制的SNP的区域图显示在图3。的SNP rs111720447和rs10057473没有显示出从Hardy-Weinberg平衡(P = 0.92和p = 0.36,用于分别SNP rs111720447和rs10057473,),并且强度聚类图(偏差补充图S4),用于复制的单核苷酸多态性基因型显示出簇明确分开,说明高品质的基因分型。
Region plot of the inhaled corticosteroid pharmacogenomics loci associated with forced expiratory volume in 1 s decline in the Lung Health Study (LHS)-2 and replicated in Advair, Biomarkers in COPD (ABC) cohort. The y-axis represents the p-values (–log10x轴是基因组的位置。图中显示了基因名称及其对应的坐标。单核苷酸多态性(SNPs)的颜色编码反映了与哨点SNP结合不平衡的程度。横线表示p值截断5×108。水平绿线表示p值截断5×105。
FEV的差异1LHS-2和ABC试验中rs111720447和rs10057473基因分型与ICS治疗相关的变化
补充图S5示出了在FEV的变化1根据rs111720447和rs10057473的基因型,以及在LHS-2和ABC试验中,在ICS组和安慰剂组之间。在这两个队列中,在7号染色体上具有SNP rs111720447等位基因的个体显示出平均较低的FEV1在研究结束时,如果他们被分配到ics为基础的治疗与安慰剂。对于糖皮质激素受体SNP rs10057473, G等位基因,这与GR编码基因表达增加有关NR3C1肺组织中,与较高的FEV相关联1在那些谁被分配到ICS治疗与安慰剂相比。
ENCODE结果
我们利用ChIP-Seq数据对SNP rs111720447周围可能存在的连锁不平衡块进行了评估(使用r2> 0.5)和确定了两个GR结合位点(图4) in A549 alveolar cell lines treated with 100 nM dexamethasone for 1 h. These GR binding sites did not map to any known genes, but were in close proximity to the activator of transcription and developmental regulator (AUTS2)吉恩。
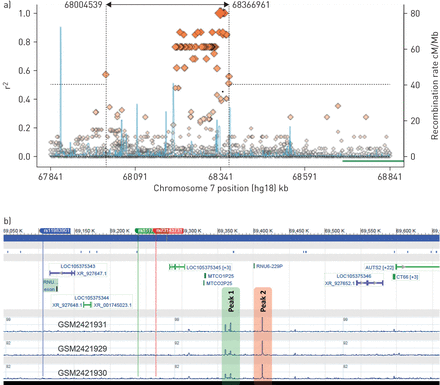
糖皮质激素受体(GR)在rs111720447附近结合。a) rs111720447周边联动不平衡块(r2基于1000个基因组的>0.5);b)对经100 nM地塞米松处理1 h的肺细胞(A549)进行GR染色质免疫沉淀测序。
PheWAS结果
SNPs rs111720447和rs10057473的PheWAS图如图所示补充图S6。有与用于SNP rs111720447测试表型的数量满足进行Bonferroni校正的P值的任何疾病或表型的共同用于该SNP没有显著关联。在GWAS目录中,没有被报道rs111720447该协会。对于GR eQTL SNP rs10057473,在PheWAS分析显示C等位基因与房颤风险增加显著协会以及减少“比较的机身尺寸为10岁。”
讨论
“一个尺寸适合所有”历史方法已被广泛应用于药物研发和批准的药品的临床试验。在现实中,发生的反应的光谱,“平均”的疗效和副作用在任何给定的临床试验的平均值两者的有益和平均响应的有害反应观察到。尽管他们的有争议的效果和患者的回应大量异质性,ICS被广泛用于慢性阻塞性肺病。支配病人响应ICS药物基因因素的识别是在临床实践中正确使用至关重要[24]。最重要的是,这些因素也可能会提供在COPD激素的反应(和nonresponses),可能会导致新的疗法和/或生物标志物在COPD众志成城激素不敏感的生物学关键见解。
在目前的研究中,我们进行了GWAS对FEV基因型逐ICS互动效应1从LHS-2在802名受试者下降。没有满足的SNP的全基因组显着性(P <5×10−8)。然而,通过使用二级定义的标准来发现p<5×10−6,我们确定了在染色体7(rs111720447,第一个基因间SNP = 4.81×10−6), p=5.98×10−5)在199名COPD受试者的独立队列中,他们要么单独使用氟替卡松,要么联合使用沙美特罗与安慰剂。使用候选基因的方法,我们发现,与GR-编码基因的肺组织中的表达水平相关的监管变种(rs10057473)NR3C1也改变了FEV的比率1拒绝与ICS治疗。然而,尽管该变型表明名义p值显着性(P = 0.02和0.04用于发现和复制,和分别用效果相同的方向),该协会没有生存多重检验(在p <0.008)的校正。编码数据表明,糖皮质激素处理的(地塞米松)A549肺泡细胞系,GR结合位点位于接近新颖ICS变体;rs111720447,这是在目前的研究中确定。在分层分析,我们发现7号染色体上的SNP显著为rs111720447强烈FEV相关1decline in the ICS group (C allele β 56.36 mL·year−1,95%CI 29.96-82.76;P = 3.35×10−5)安慰剂组(C等位基因β-27.57 mL·year−1,95%CI -1.87 -53.27-;P = 0.036)。该SNP表现出与FEV更强的基因型通过-ICS互动效应1减少吸烟者(β72.74毫升·−1,95%CI 32.47-113.00;p值= 0.0004)与former smokers (β 145.04 mL·year−1,95%CI 20.61-269.46;p=0.023) and in COPD GOLD II patients (β 85.97 mL·year−1,95%CI 38.32-133.63;p值= 0.0004),than in GOLD III and IV patients (β 116.33 mL·year−1,95%置信区间8.24–224.42;p=0.036)。GOLDⅠ组疗效不显著(p=0.38)。后一个数据与观察到的SNP和FEV之间的强相关性一致1变化在农行复制队列,其中没有任何GOLD我的患者和主要地是GOLDⅡ期患者。这些意见所依据的确切机制尚不清楚,并均超出了目前的研究范围。
迄今为止,ICS响应的数量GWAS已经报道,但所有的哮喘患者。在一个研究中,作者集成的药物反应的药效学性质与GWAS数据,然后仿照基于在多个剂量的药物反应的重复测量通过数学方程药效剂量的关系[25]。作者发现有多个ICS响应相关的snp映射到多个基因和基因间区域[25]。另一项研究报告在糖皮质激素诱导的转录物1基因变异rs37973 ICS响应的药理学作用(GLCCI1)[15]。有趣的是,在COPD患者中,其试图复制rs37973的药理学作用,研究得出了相互矛盾的结果。虽然462个的白种人一项研究未能确定关联[26],另一项对204名中国慢性阻塞性肺病患者的研究表明,ICS反应与慢性阻塞性肺病有显著的相关性[27]。在COPD这些相互矛盾的数据背后的原因rs37973尚不清楚,但可能是由于在潜在的疾病的严重程度的差异,样品的尺寸(低功率),即进行了评价,包括ICS的不同效力和使用组合药物而不是ICS药物单药治疗和各研究微分随访时间。在目前的研究中,SNP rs37973不与FEV相关1与ICS使用相关的下降(p>0.05)。这可能表明这种SNP对COPD患者ICS反应没有影响,或者与长期FEV无关1响应。
揭开GWAS相关变异的机制是一项艰巨的任务。的新颖变体,我们7号染色体上具有报告肺组织中的基因表达没有影响,但靠近气道肺泡细胞系A549与地塞米松处理后GR结合位点。这提供了一个潜在的机制的遗传关联底层。所述变体可能会改变GR复合物的结构或电荷且因此修改其下游的效果。最近的基因相关的SNP和GR结合位点是AUTS2基因,据报道与多种神经系统疾病有关,包括自闭症和神经元发育,以及非神经系统疾病,如急性淋巴细胞白血病[28]。
没有任何额外的信息,它是具有挑战性的从GWAS真正的生物信号不符合全基因组截止噪音区分开来。在分子水平,的驱动治疗反应到吸入器的药物的最重要的因素之一,是在肺组织上或浸润免疫细胞穿透气道和编排局部炎症反应的受体的变异和/或表达。为皮质类固醇,所述目标是GR,这是由核受体3C1编码(NR3C1)基因29]。因此,生物合理,在遗传变异体NR3C1基因可以调节ICS对FEV的影响1下降。在目前的研究中,这种基因的变异起着调节作用NR3C1表达与差FEV相关联1这是名义上在ABC队列(p值= 0.04)复制曲安西龙和安慰剂组(P = 0.02)之间的下降,但没有达到多重检验的Bonferroni校正的P值。的效果的方向是与相关联的遗传变异体降低NRC31表达与加速FEV相关联1拒绝去炎松小组。
目前的研究有一些局限性。首先,由于该研究的样本量相对较小,因此有可能出现2型错误,即忽略了基因型对FEV可能产生的显著交互作用1下降。然而,通过GWAS发现的候选位点的直接基因分型,我们发现了与COPD患者对ICS反应相关的新位点。其次,尽管编码数据表明该变异位于使用地塞米松(皮质类固醇)治疗的相关肺泡细胞系中GR结合位点附近,但其机制尚不清楚。第三,虽然临床试验设置有许多重要的方法学优势,包括缓解指征偏差和对不符合的治疗反应的混淆,但找到一个“理想的”外部队列进行复制是极具挑战性的。在本研究中,我们使用ABC队列进行复制,它与LHS-2相比有一些显著的差异,包括年龄、吸烟状况和气流受限的严重程度。ABC试验使用了一种更有效的脂溶性ICS(氟替卡松),并包含了ICS-LABA臂,而LHS-2使用的是不含LABA的曲安奈德。此外,ABC试验的RCT成分超过4周(主要评估ICS停用对FEV的影响1), while LHS-2 had ≥3 years of follow-up (and largely evaluated the effects of ICS addition to standard therapy on FEV1)。在通过后续年度LHS-2(分层分析补充表S1), the genetic effect became stronger for the reported SNPs at 24 and 36 months follow-up, arguing against a concentrated “early” effect that can explain the replication of chromosome 7 locus in the ABC trial, which had only a 4-week RCT duration. A more likely explanation is the inclusion of GOLD II and III patients in whom the association of chromosome 7 SNP was much stronger compared to GOLD I patients, who made up a significant proportion of LHS-2. The findings encourage the use of genetics for recent RCTs with various follow-up durations and treatment regimens (例如三重吸入疗法)。最后,虽然发现的变异可能为慢性阻塞性肺病ICS反应的生物学和生物标记物提供潜在的新见解,但其临床转译是不确定的,超出了目前研究的范围。临床转化将需要对生物标志物参数和表型进行微调,并在现实生活中进行额外的复制。
综上所述,本研究发现了一种新的与ICS对FEV的长期影响相关的遗传变异1慢性阻塞性肺病患者的下降,应在未来的生物学和临床翻译研究中进行评估。这一观察可能为慢性阻塞性肺病ICS反应的生物学提供新的见解,也为设计和验证新的治疗方法以克服慢性阻塞性肺病类固醇不敏感的挑战提供新的思路。
补充材料
可共享的PDF
致谢
Ma'en奥贝达特是迈克尔史密斯基金会健康研究和帕克乙弗朗西斯基金会的研究员的学者和唐仙是一级加拿大研究主席在COPD并持有德拉扎家庭主席在中心的心肺创新。
脚注
这篇文章有提供补充材料www.qdcxjkg.com
本研究是对临床试验标识符的完整研究的重新分析NCT00000569和NCT00120978。
作者贡献:构思和设计的研究:M. Obeidat, P.D. Pare和D.D. Sin。肺eQTL的数据收集与分析:M. Obeidat, M. van den Berge, P. Joubert, K. Hao, C-A。布兰德斯马和S.F.P.曼。肺健康研究数据和基因分型:M. Obeidat, X. Li, N.N. Hansel, N. Rafaels, R. Mathias, I. Ruczinski, T.H. Beaty和K.C. Barnes。研究数据分析:M. Obeidat, X. Li和A. Faiz。原稿:M. Obeidat和D.D. Sin。讨论了结果和含义,并评论了手稿的各个阶段:所有共同作者。
利益冲突:M. Obeidat没有要披露的内容。
利益冲突:A.法伊兹没有什么要披露的。
利益冲突:X. Li还没有透露。
利益冲突:M.范登贝格报告由葛兰素史克公司,基耶西,Teva公司和阿斯利康公司支付给学校,提交作品外津贴。
利益冲突:N.N. Hansel报告了来自阿斯利康(AstraZeneca)和葛兰素史克(GSK)咨询委员会工作的拨款和个人费用,来自勃林格殷格翰(Boehringer Ingelheim)、美国国立卫生研究院(NIH)和慢性阻塞性肺病基金会(COPD Foundation)的拨款,来自迈兰(Mylan)咨询委员会工作的个人费用,不包括提交的工作。
利益冲突:P.茹贝尔有没有透露。
利益冲突:K. Hao没有任何需要披露的信息。
利益冲突:C-A。布兰斯马没有什么要透露的。
利益冲突:N.Rafaels没有什么要披露的。
利益冲突:R.马蒂亚斯有没有透露。
利益冲突:一,Ruczinski有没有透露。
利益冲突:T.H. Beaty报告了国家心肺血液研究所在进行研究期间提供的资助。
利益冲突:K.C.巴恩斯有没有透露。
利益冲突:S.F.P. Man没有什么要披露的。
利益冲突:P.D. Pare没有什么要披露的。
利益冲突:D.D。仙报告默克补助,个人费用从赛诺菲 - 安万特和Regeneron公司,赠款和来自勃林格殷格翰,从阿斯利康,为咨询委员会工作的个人费用和顾问委员会的工作和讲座补助和个人收费的临床试验工作的个人费用咨询会议从诺华,外面提交作品的讲座。
支持声明:这项工作由加拿大政府、加拿大卫生研究所资助。本文的资助信息已存入交叉引用出资者注册。
- 收到了2019年3月13日。
- 接受2019年8月22日。
- 版权©2019人队
这篇文章是开放存取并根据知识共享188滚球软件署名非商业许可证4.0的条款分发。