摘要
白细胞介素(IL)-1家族细胞因子与系统性硬化(SSc)和肺受累密切相关,但其分子机制尚不清楚。本研究的目的是评估的角色IL-1α和肺血管和间质重塑IL-1βSSc的小鼠模型。
IL-1α和IL-1β中的SSc患者的肺和硬皮病的Fos相关抗原-2(FRA-2)的转基因(TG)小鼠模型中本地化。lung function, haemodynamic parameters and pulmonary inflammation were measured in Fra-2 TG mice with or without 8 weeks of treatment with the IL-1 receptor antagonist anakinra (25 mg·kg−1·天−1)。IL-1对肺动脉平滑肌细胞(肺动脉平滑肌细胞)和成纤维细胞实质直接影响进行了研究体外。
TG小鼠肺内胶原沉积增加,肺功能受限,血管肌肉化增强,伴发肺动脉高压,使人联想到SSc患者的变化。免疫反应性IL-1α和IL-1β增加Fra-2 TG老鼠和SSc患者。IL-1的刺激降低了PASMCs和实质成纤维细胞中胶原的表达通过不同的信号通路。阻断fr -2 TG中的IL-1信号会加重肺纤维化和限制,增强t -辅助性细胞2型(Th2)炎症,增加促纤维化、交替活化的巨噬细胞数量。
我们的数据表明,目前在几项临床研究中研究的阻断IL-1信号可能会加重特定患者亚群的肺纤维化,因为Th2扭曲了免疫反应,并形成了选择性激活的前成纤维巨噬细胞。
摘要
IL-1抑制肺结构细胞的胶原蛋白生成,平衡免疫系统的促纤维化作用。阻断fra2 TG小鼠IL-1信号通路可使肺组织Th2炎症反应和胶原蛋白生成增加,从而使肺功能恶化。http://bit.ly/2IVUGLX
介绍
系统性硬化症(SSC)是一种罕见的进行性纤维化疾病,影响皮肤和内脏器官[1]。50%的患者肺受累,肺实质和血管间室分别表现为纤维化和血管重构。血管重构可能导致肺动脉高压的发生,而肺动脉纤维化与不良预后密切相关[2]。南南合作相关肺纤维化的治疗选择是有限的和疾病管理大多局限在非选择性免疫抑制剂[3.]。最近一项对EUSTAR组亮点研究有必要进一步调查并找出更有效的治疗策略[4]。
尽管自身免疫中起着重要的作用,硬皮病引起的肺损伤的潜在的分子机制知之甚少。各种细胞因子和炎性介质有牵连硬皮病[的发展和进展5]。白介素(IL) 1家人IL-1αIL-1β强烈增加SSc患者的血清(6,7]。IL-1β水平也增加在支气管肺泡灌洗液(BALF) SSc病人和消极与肺功能(6]。此外,IL-1受体(IL-1R)信号传导途径与硬皮病易感性和硬皮病相关纤维化肺泡炎[相关联8]。缺乏IL-1R,或其下游信号小鼠中,是针对肺动脉高压保护[9和纤维化[10]。这导致了假设,即IL-1有助于肺纤维化和血管重构。因此,重组IL-1R拮抗剂阿那白滞改良后的博来霉素诱导的肺纤维化小鼠[10]以及缺氧或野百合碱诱发的肺动脉高压[9,11],并被认为是一种可能的治疗方案,可治疗与超临界水肺疾病有关的肺疾病[12]。
小鼠过表达激活蛋白(AP)-1转录因子家族成员Fos相关抗原-2(FRA-2)表示用于硬皮病相关性肺纤维化和高血压[鼠模型13,14]。FRA-2转基因(TG)小鼠自发肺部炎症以及血管和实质重塑,非常类似于硬皮病患者的临床表现为肺部受累[13,15]。然而,这种表型背后的分子病理机制仍然未知。在本研究中,我们使用fra2 TG小鼠模型来研究IL-1在肺纤维化和肺动脉高压中的作用,并评估靶向IL-1治疗SSc肺表现的可能的治疗潜力。
材料和方法
方法的详细描述载于补充材料。
研究人群
年代amples of SSc lungs were obtained from archival, anonymised lung tissue samples removed as part of patients’ medical care or post-mortem examination (Dept of Pathology, University of Pittsburgh Medical Center, Pittsburgh, PA, USA) or from SSc patients undergoing lung transplantation (Division of Thoracic Surgery, Medical University of Vienna, Vienna, Austria). Downsized nontransplanted donor lungs served as controls. The protocol and tissue usage was approved by the local authorities (Vienna: Institutional Ethics Committee (976/2010); Pittsburgh: Institutional Review Board (PRO1110204)). Patient consent was obtained before lung transplantation. Scleroderma patients met American College of Rheumatology diagnostic criteria or LeRoy and Medsger criteria for SSc [16,17]。病人的特点中列出补充表S1。
动物实验
雌性fra2 TG小鼠和野生型(WT)同窝小鼠在特定的无致病性条件下,在隔离的通风笼中进行12 h的光/暗循环。所有动物实验均符合欧盟指导方针(2010/63/EU),并获得了地方当局(奥地利教育、科学和文化部,维也纳,奥地利)的批准。20周龄的fra2 TG和WT小鼠进行了血流动力学和肺功能的表征。25 mg·公斤−1阿那白滞素(Kineret;瑞典孤儿Biovitrum公司,斯德哥尔摩,瑞典)给予通过daily intraperitoneal injection for a total of 8 weeks as previously described [18]。对照组接受注射用等体积的无菌生理盐水溶液。米ice were sacrificed at 18–19 weeks of age. Anakinra treatment was performed in two independent experiments with n=5–7 mice per group.
统计数据
在棱镜5版进行统计分析(的GraphPad,拉霍亚,CA,USA)。在数字数据表示为单一数据点位,如果不是另有说明。两组具有相等方差之间的比较采用非配对t检验来完成。两组显著不同的方差使用Mann-Whitney检验进行比较。阿那白滞对WT和TG小鼠的治疗效果是通过双因素方差分析和Bonferroni氏事后检验。细胞培养和蛋白表达数据的多组比较采用与邓恩后检验多重比较秩和检验检验。用于特定的数据集的所有统计检验的图例表示。p值<0.05被认为是统计学显著。
结果
在FRA-2 TG小鼠模型的特点是肺动脉高压和限制性肺功能
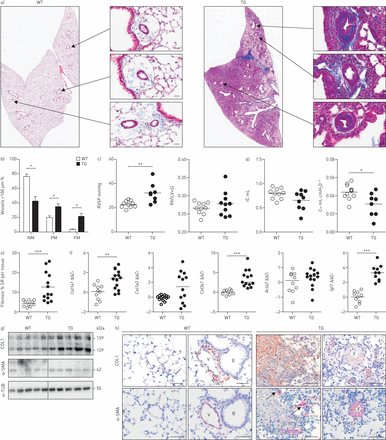
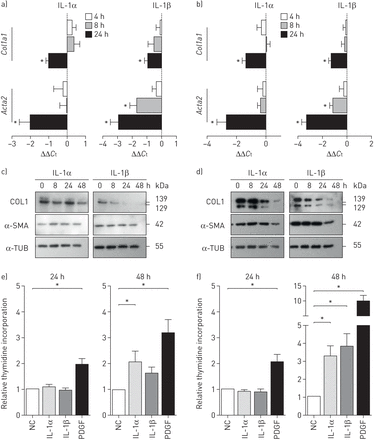
在小鼠中导致年龄依赖性重塑皮肤和肺FRA-2的表达(图1一个)[13,15]。一个ssessment of pulmonary vascular remodelling revealed increased muscularisation of pulmonary vessels (10–100 µm diameter;图1 b和补充图S1a)和右室收缩压(RVSP)升高,提示肺动脉高压(图1 c)在FRA-2 TG小鼠。TG小鼠的肺功能受损,具有降低的吸气量和顺应性(图1 d)。在肺中的胶原沉积,通过使用形态天狼胶原定量确定染成红色的左肺的部分(被显著增加图1 e和补充图印地)。因此,增加胶原蛋白但不是α-smooth肌肉肌动蛋白(α-SMA (ACTA2在mRNA和蛋白水平上的表达(图1 f和g)。此外,促纤维化因子胰岛素样生长因子1(Igf1)被高度上调(图1 f)。在fra2 TG小鼠中,胶原蛋白1在远端小血管周围和壁内及薄壁组织(图1 h)。α-SMA免疫反应主要是见于重塑的血管,在脑实质纤维化区域(箭头)进一步染色,这表明肌纤维母细胞的存在(图1 h)。
fos2相关抗原-2 (fra2)过表达(转基因(TG))小鼠发生血管重构和实质纤维化。WT:野生型;RVSP:右心室收缩压;房车:右心室;LV:左心室;S:隔;IC:吸气能力;Crs:呼吸系统的合规性;SR:天狼星红;Ct:循环阈值;COL1:胶原蛋白1;α-SMA:α-smooth肌肉肌动蛋白;α-TUB:α微管蛋白。a)用马松和20周龄WT改建船舶的放大倍率和FRA-2 TG小鼠染色全肺幻灯片的代表图像。年代cale bar: 20 µm. Collagen is stained in blue. b) Percentage of nonmuscularised (NM), partially muscularised (PM) and fully muscularised (FM) vessels <100 µm in diameter. n=10; mean±sd。c)按照权利心脏导管插入术和在WT富尔顿指数(RV /(LV + S))和FRA-2 TG小鼠中测定RVSP。d)肺功能测量(IC和Crs)。e)天狼星红染色WT及fra2 TG肺载玻片上胶原的形态定量。f)实时荧光定量PCR分析Col1a1,Col1a2,Col3a1,ACTA2和Igf1在WT和FRA-2的Tg小鼠的表达。ΔCt值正常化WT组(ΔΔ的均值Ct)。B2m(β2微球蛋白),hmb(羟甲基双酚a合成酶)作为参考基因。克)COL1的Western印迹分析和α-SMA的水平在WT和FRA-2 TG小鼠肺匀浆。α-TUB作为加载控制。1H)COL1(棕色)和α-SMA的免疫组织化学染色(红/粉红色)。B:支气管;五:容器。年代cale bar: 50 µm. *: p<0.05; **: p<0.01; ***: p<0.001.
FRA-2的过度表达导致增加的IL-1水平通过增强启动子结合
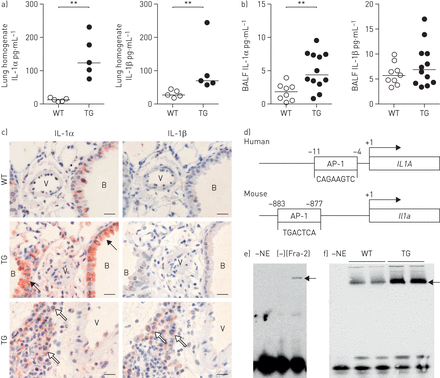
炎性细胞因子如IL-1α和IL-1β是已知与硬皮病[相关19]及特发性肺动脉高压[9,20.,可能是SSc中实质与血管重构之间的常见病理联系。在Fra-2 TG小鼠肺匀浆,蛋白质含量IL-1α和IL-1β明显升高(图2一个)。在BALF,IL-1α水平也增加,而IL-1β水平没有改变(图2 b)。因此,免疫组织化学染色对IL-1α强烈增加Fra-2 TG老鼠和位于支气管上皮细胞(黑色箭头),结构和炎症细胞(白色箭头)周围血管和薄壁组织(图1 c,左图)。IL-1β染色是不是在WT小鼠或FRA-2 TG小鼠的结构细胞可检测的和仅在炎性浸润(白色箭头)观察到(图2 c右面板)。
增加白细胞介素(IL)-1α和IL-1β水平在Fos相关抗原-2(FRA-2)-overexpressing(转基因(TG))小鼠。支气管肺泡灌洗液:支气管肺泡灌洗液;AP-1:活化蛋白-1。A,B)IL-1α和IL-1β蛋白水平在一个)肺匀浆和b)20周龄WT的BALF和FRA-2 TG小鼠。c)中的免疫组织化学上FRA-2 TG和WT小鼠的肺切片的IL-1α和IL-1β的染色。B:支气管,V:容器;黑箭头:支气管上皮细胞;白色箭头:结构和炎性细胞。年代cale bar: 20 µm. d) Schematic representation of the humanIL1A和鼠标IL1A启动子序列包括ap -1结合位点。e, f) e)过表达原始人实质成纤维细胞或细胞转染空白对照质粒(-)和f)来自WT或fra2 TG小鼠的肺匀浆的核提取物进行电泳迁移转移分析。-NE:不含核提取物的结合反应的阴性对照。有关加载和超表达式控件,请参阅补充图S1。* *:p < 0.01。
启动子分析IL-1α和IL-1β基因位点透露潜在AP-1-binding网站的启动子区域里人类和小鼠IL-1α基因(图2 d),但不存在于IL-1β的基因。为了进一步证实FRA-2对IL-1α启动子的直接的影响,我们对从原代人成纤维细胞实质的核提取物进行电泳迁移率变动分析过表达FRA-2(图2 e),从fra2 TG和WT小鼠的肺匀浆(图2 f)。核提取物的等量装载通过Western印迹证实(补充图S2)。在实验设置中,FRA-2的过表达导致增加的结合IL-1α的AP-1启动子区(图2 e和f)。因此,增加的IL-1α水平可能是异常FRA-2的表达的直接后果。
FRA-2和IL-1的表达的细胞定位在人的肺部硬皮病被改变
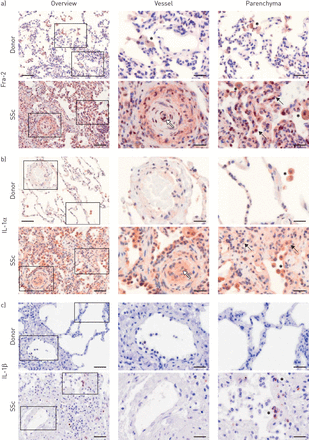
对供体和SSc肺中fra2定位的分析显示,在供体肺中,fra2阳性染色主要见于肺泡巨噬细胞(asterisks),而在SSc肺中,它也定位于重构血管(白色箭头),包括内皮细胞、炎性细胞(asterisks)和实质细胞(黑色箭头)(图3a)。此外,在SSc肺中,fra2的染色强度增加,已有报道[13,21]。IL-1α染色观察类似的模式,IL-1α本地化供体肺的肺泡巨噬细胞(星号),而在SSc肺,IL-1α染色也在改建中发现血管(白色箭头),内皮细胞,通常在改建实质区域(黑色箭头)图3b)。IL-1β是表达单一炎症细胞(星号),而不是其他细胞类型的SSc肺;没有IL-1β染色检测到供体肺(图3c)。
的Fos相关抗原-2(FRA-2),白细胞介素(IL)-1α和IL-1β在健康供体和全身性硬化症(硬皮病)肺定位。的免疫组织化学染色(褐色))FRA-2,B)IL-1α和c)IL-1β。左图:概述;右图:放大插图。星号:炎症细胞/肺泡巨噬细胞;黑箭头:实质细胞;白色箭头:内皮细胞。年代cale bar: 100 µm (overview)/20 µm (insets). n=3–4; representative images are shown.
在FRA-2 TG小鼠IL-1信号传导的阻断恶化肺功能
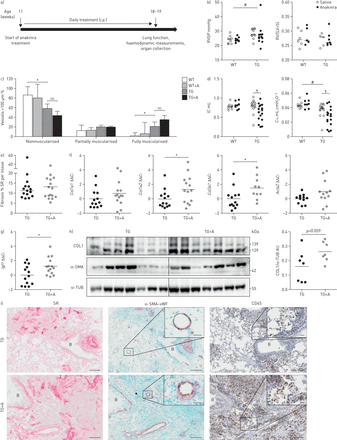
为了评估IL-1信号在fra2 TG小鼠模型中肺重建中的作用,我们用重组IL-1R拮抗剂anakinra处理小鼠8周以阻断IL-1R信号(图4一)。与阿那白滞治疗没有改变RVSP,富尔顿指数(图4 b)或肺小血管肌肉化(图4 c,但进一步恶化了fra2 TG小鼠的限制性肺功能(图4 d)。虽然天狼星胶原蛋白定量染成红色的肺切片并没有表现出检测的差异(图4 e的表达水平Col1a2和Col3a1在阿那白滞治疗均增加(图4 f)。促纤维化因子的水平Igf1(22],在anakinra治疗后进一步增加(图4 g)。与未处理的对照组(p=0.059)相比,经阿纳金拉处理的fra2 TG小鼠肺匀浆中的胶原蛋白水平略有升高(p=0.059)。图4 h)。胶原沉积和α-SMA免疫反应性的位置是与未处理的对照FRA-2的Tg小鼠一致(图4I)。另外,阿那白滞导致多种炎性细胞浸润在FRA-2 TG小鼠的肺中,通过明显增加了与炎性细胞标记物CD45染色(图4I)。
阻断白细胞介素(IL)-1信号可使fos2相关抗原-2 (fra2)过表达(转基因(TG))小鼠的肺功能恶化,并增加细胞外基质的产生。RSVP:右心室收缩压;右心室,左心室;S:隔;ns:不显着;IC:吸气能力;Crs:呼吸系统的合规性;SR:天狼星红;Ct:循环阈值;COL1:胶原蛋白1;α-SMA:α-smooth肌肉肌动蛋白;α-TUB:α-tubulin;盟:任意单位;vWF: von Willebrand因子。a) anakinra治疗概况:fra2 TG小鼠给予25 mg·kg−1腹腔注射8周,18-19周时处死。b) RVSP:采用右心导管和富尔顿指数(RV/(LV+S))测定,采用阿纳金拉治疗或对照(生理盐水)的fra2 TG和WT小鼠RV/(LV+S)。#: p<0.05,双因素方差分析确定基因型效应的显著性。c)的百分比nonmuscularised,部分肌和完全肌血管直径< 100µm。WT为n=3, TG为n=9;平均值±sd。*: p<0.05,无配对t检验。d)肺功能测量(IC和Crs)FRA-2 TG和WT小鼠用阿那白滞治疗或载体对照(盐水)的。#:P <0.05,通过双向ANOVA确定基因型效应的显着;¶: p<0.05,经Bonferroni’s后测双因素方差分析(two-way ANOVA)确定有无anakinra处理的fra2 TG差异有统计学意义(p<0.05)。e)使用(TG+A)和(TG)不使用(TG) anakinra处理的fr -2 TG和WT小鼠肺载玻片上的胶原形态定量分析。f, g) f的实时荧光定量PCR分析Col1a1,Cola1a2,Col3a1和ACTA2和g)Igf1在FRA-2的Tg小鼠的表达。ΔCt值是正常的意思是未经处理的Fra-2 TG集团(ΔΔCt)。B2m(β2微球蛋白),hmb(羟甲基双酚a合成酶)作为参考基因。*: p<0.05,无配对t检验。h)免疫印迹分析和量化的COL1和α-SMA水平Fra-2 TG和TG +一个小鼠肺匀浆。α-TUB作为加载控制。我)胶原染色SR(红色)胶原蛋白,免疫组织化学双染色的船只对α-SMA(紫色)和内皮标记vWF(浅棕色)和免疫组织化学染色法对炎症细胞CD45标记。B:支气管。酒吧规模:100µm(主要)/ 20µm(小图)。
IL-1α和IL-1β抑制胶原1和α-SMA的表达通过细胞类型特异性不同的信号传导途径
要确定哪些机制可能会导致肺功能的恶化在活的有机体内,我们讨论了IL-1的潜在影响体外,并研究了如何IL-1α和关于增殖,α-SMA的表达和胶原蛋白的产生IL-1β影响重要常驻肺细胞。IL-1α和肺动脉平滑肌细胞(肺动脉平滑肌细胞)和成纤维细胞实质导致减少的IL-1β刺激Col1a1和ACTA2信使rna (图5一个和b)。因此,胶原1和α-SMA蛋白水平减少(图5 c和d),建议直接anti-fibrotic行动IL-1α和IL-1β居民肺细胞。刺激与IL-1α或IL-1β没有改变细胞增殖后24 h,但只有48 h后(图5 ef),指出IL-1对细胞增殖的间接影响。有趣的是,PASMCs和薄壁组织的成纤维细胞显示不同的监管和细胞特定类型通路IL-1α和IL-1β刺激(补充图S3)。
白细胞介素(IL)-1下调胶原在肺动脉平滑肌细胞(肺动脉平滑肌细胞)和成纤维细胞实质1(COL1)和α平滑肌肌动蛋白(α-SMA)的表达。IL:白细胞介素;Ct:循环阈值;α-TUB:α-tubulin;PDGF:血小板衍生生长因子;NC:消极的控制。a, b)相对表达水平Col1a1和ACTA2后4、8和24小时IL-1αng(1毫升−1) and IL-1β (10 ng·mL−1刺激a) PASMCs和b)实质成纤维细胞(细胞外基质的产生)。来自六个独立实验的数据从不同的供体肺分离的细胞被描述。B2m(β2微球蛋白),hmb(羟甲基双酚a合成酶)作为参考基因。c, d)代表西方滴COL1和α-SMA c) PASMCs和d)薄壁组织的成纤维细胞治疗IL-1αIL-1β4、8、24 h。e, f)增殖e) PASMCs和f)实质成纤维细胞3.H-thymidine 24 h公司在与IL-1α刺激,IL-1βPDGF-BB。来自5个不同供体的10个独立细胞实验的数据;平均值±sd。*: p<0.05, Kruskal-Wallis检验与Dunn’s post-test进行多重比较。
Anakinra治疗加重了fra2 TG小鼠的t辅助细胞2型炎症
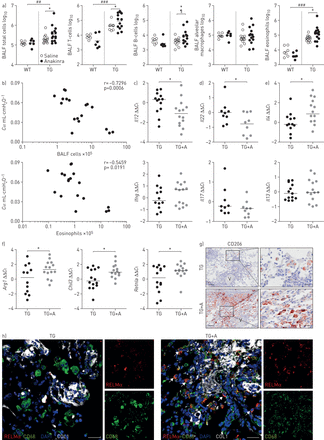
因为我们观察到在FRA-2 TG小鼠增加炎性浸润与阿那白滞处理(图4I),进行炎性细胞群和介体的详细分析。首先,组织学评分显示,在间质和周围的支气管显著更多的炎性浸润,嗜酸细胞和淋巴细胞作为最丰富的细胞群体(补充表S6)。在下一步骤中,炎性细胞在小鼠的BALF进行定量,并通过流式细胞术分析。如前所述,FRA-2 TG已经在BALF增加炎症细胞的数量,主要是由嗜酸性粒细胞,T淋巴细胞和B淋巴细胞(图6)[23]。尽管阿那白滞治疗并未导致在WT小鼠中的炎症细胞数量的变化,增加的T细胞,B细胞和嗜酸性粒细胞的量与阿那白滞处理FRA-2 TG小鼠中观察到(图6)。双向方差分析表明,b细胞(p=0.0329)和嗜酸性粒细胞(p<0.0001)的基因型和处理之间存在相互作用。BALF中总炎性细胞数量和嗜酸性粒细胞数量与fra2 TG小鼠肺顺应性呈负相关(图6 b),表明在阿那白滞的治疗,恶化肺功能不仅是由于增加的胶原蛋白产生,但在FRA-2 TG小鼠的肺中也增加了炎症。
阻断白细胞介素(IL)-1信令增加炎症Fos相关抗原-2(FRA-2)-overexpressing(转基因(TG))小鼠。支气管肺泡灌洗液:支气管肺泡灌洗液;WT:野生型;C圣:准静态肺顺应性;Ct:循环阈值;RELMα:resistin-like molecule-α;COL1:胶原蛋白1;DAPI: 4′, 6-diamidino-2-phenylindole;qRT:定量实时。a)流式细胞术分析经anakinra或vehicle control (saline)处理的fra2 TG和WT小鼠BALF的炎性细胞群。# #:p < 0.01;# # #: p<0.001,双因素方差分析确定基因型效应的显著性;¶: p<0.05,经Bonferroni后测双因素方差分析确定有无anakinra处理的fra2 TG差异有统计学意义;*: p<0.05,无配对t检验。b)相关图C圣与BALF总细胞数或BALF嗜酸性粒细胞。c-e)关键炎症介质qRT-PCR检测anakinra处理后fra2 TG小鼠肺匀浆中关键炎症介质的相对表达水平。ΔCt值是正常的意思是未经处理的Fra-2 TG集团(ΔΔCt)。B2m(β2微球蛋白),hmb(羟甲基双酚a合成酶)作为参考基因。*: p<0.05,无配对t检验。f)选择性巨噬细胞极化标记物的qRT-PCR分析。ΔCt值是正常的意思是未经治疗的对照组(ΔΔCt)。*: p<0.05,无配对t检验。克)上的肺切片CD206(棕色)的免疫组织化学染色从FRA-2 TG小鼠(TG + A)和不具有(TG)阿那白滞治疗。五:容器。酒吧规模:100µm(主要)/ 20µm(小图)。F)免疫荧光RELMα(红色),CD68(绿色),COL1(白色)和DAPI染色(核;蓝色)。箭头:CD68+/ RELMα+double-positive细胞。比例尺:25µm。
由于anakinra对WT小鼠炎症反应无影响,我们进一步研究了anakinra处理后,fra2 TG小鼠t -辅助性细胞1、2、17 (Th1、Th2、Th17)免疫应答细胞因子表达水平(图6 c-e)。Th1细胞诱导的细胞因子IL-12是表达强烈降低,而γ干扰素是不变(图6 c)。Th17细胞因子IL-17和IL-22减少或未改变(图6 d)。尽管IL-13的表达不受anakinra治疗的影响,但作为Th2免疫的关键中介的IL-4却显著增加(图6 e)。两者合计,这些结果表明IL朝-1信号的阻断之后Th2细胞驱动的免疫应答的转变。由于IL-4是参与伤口愈合并显示诱导成纤维细胞纤维化应答[或者活化巨噬细胞的有效诱导24],我们分析的替代性活化的巨噬细胞标志物的表达水平。精氨酸酶1(__arg1),几丁质酶样3(Chil3)和resistin-like molecule-α(RELMα(Retnla)),与车用甘油三酯小鼠(图6 f)。经anakinra处理后,fra2 TG小鼠肺组织中促纤维化巨噬细胞标记物CD206的免疫反应性明显增强(图6克)。三重CD68免疫荧光,RELMα和胶原蛋白1突出显示CD68的积累+/ RELMα+周围的胶原蛋白阳性纤维化区双阳性的巨噬细胞(图6 f)。这些数据表明,阻断IL-1信号引线到促纤维化的巨噬细胞的数量增加在FRA-2 TG小鼠。
讨论
肺部并发症是SSc患者死亡的主要原因[2]。肺实质可表现为肺纤维化,血管系统可表现为肺动脉高压。我们和其他人已经表明,异位超表达AP-1转录因子家族的成员Fra-2鼠标导致纤维化改变皮肤和肺结构变化观察到类似SSc的病人,如血管重塑的肺动脉闭塞,异常的细胞外基质(ECM)沉积与纤维化和炎症(13,15,25]。这些结构上的变化表现为严重的功能损害,其特征是肺功能受限和肺压力升高,这在SSc患者中可以看到,这使得fra2 TG小鼠成为研究SSc患者肺部病变的病理生理方面和进行临床前概念验证研究的一个有价值的工具。
到目前为止,还不确定是哪些因素导致了SSc患者的肺重构。几项研究表明,SSc与促炎细胞因子(如IL-1)有关[5]。IL-1α和IL-1β水平都显著增加的血清SSc [6,7]及特发性肺动脉高压[20.)患者。IL-1α基因多态性提高IL-1α蛋白表达与易感性增加有关SSc [26),而IL-1β多态性与肺癌患者参与有关SSc [27]。在这项研究中,我们描述了一种新的机制,导致通过直接FRA-2启动子结合增加IL-1α在硬皮病。在硬皮病患者中,FRA-2过表达和在细胞核中积聚[21,它可以结合激活IL1A启动子和导致IL-1α表达式。因此,IL-1α免疫反应性增加肺的实质和血管隔间SSc病人和Fra-2 TG老鼠,而IL-1β主要是炎症细胞中观察到。增加IL-1β可能因此次生效应由于增加炎症(IL-1α相比,直接受Fra-2)。
此前有研究表明,IL-1R信号缺陷或IL-1R拮抗剂anakinra阻断可保护肺动脉高压和纤维化[9- - - - - -11]。此外,一项使用阿纳金拉治疗的矽肺诱导肺纤维化患者的病例研究报告了呼吸道症状的改善和炎症参数的正常化[28]。因此,我们推测,由于异常的fra2活性导致的IL-1水平升高可能是肺表型的驱动因素,而anakinra治疗可以改善肺动脉高压和纤维化。出乎意料,在活的有机体内阿那白滞的应用进一步恶化FRA-2的Tg小鼠的肺功能在这项研究中,并导致的Th2 /促纤维化细胞巨噬细胞轴的活化增加,因此胶原蛋白合成。作为转录因子,FRA-2编排炎症介质和其他靶基因的阵列,除了IL-1。因此FRA-2 TG小鼠的表型不是由于一个单因子的上调,但是几个反作用途径失调。在这里,我们表明,阻断IL-1信号的有害影响可以具有两种解释:1)的IL-1对居民结构细胞和2)炎症的朝向的Th2为主的进一步的移位直接抗纤维化作用的损失炎症反应。
尽管IL-1细胞因子的硬皮病的明确的关联,它仍然是未知的,如果和如何这些细胞因子促进组织重建和ECM生产。IL-1α和IL-1β对结构细胞的直接影响已被广泛研究,但透露有关其促纤维化性质有争议的结果。以下成纤维细胞的IL-1刺激,下调以及胶原蛋白的上调已经观察到[29- - - - - -32]。此外,两个IL-1α和IL-1β被报道抑制转化生长因子(TGF)-β诱导胶原蛋白的产生[30.,33]。我们表明,在肺结构的细胞,如肺动脉平滑肌或实质的成纤维细胞,无论是IL-1α和IL-1β胶原浸湿无任何促纤维化刺激的在先申请的表达,这一效果是介导的通过在每种细胞类型不同的信号传导途径。因此缺乏IL-1信号的可能是夸大的胶原产生的驻地肺细胞的原因,并在FRA-2 TG小鼠中阿那白滞治疗肺功能下降。然而,IL-1的操作是非常复杂的,并且它不能排除了IL-1可通过次级介质和促存活因子,如IL-6的诱导起到肺纤维化的最初发展中发挥作用。增加PASMC,并用IL-1α和IL-1β长期治疗后实质成纤维细胞增殖已经观察到。However, the lack of proliferation after 24 h speaks against a direct proliferative effect of IL-1, and in combination with the suppression of collagen and α-SMA expression it points towards a direct anti-fibrotic activity of IL-1 on mesenchymal cells.
另一个混杂因素是IL-1对小鼠炎症的影响。我们之前报道过,fra2 TG小鼠的炎症反应主要是Th2与强嗜酸性粒细胞驱动[23]。经anakinra处理后,fra2 TG小鼠产生了更高的嗜酸性粒细胞(Th2反应),而WT小鼠未见任何反应,表明IL-1的复杂免疫调节作用强烈依赖于炎症微环境。阿纳金拉处理的fra2 TG小鼠的Th2细胞因子IL-4也升高。IL-4具有强大的促纤维化作用[34,35],其在SSc患者血清中的含量显著升高[36]。SSc患者BALF中嗜酸性粒细胞的数量也明显增加,有研究表明与间质性肺病及皮肤纤维化相关[37,38]。除了直接的促纤维化作用,IL-4可导致巨噬细胞的替代激活,如在我们的研究中。或者激活的巨噬细胞参与纤维化的发展[39],而SSc患者皮肤中的数量有所增加[40]以及在fra2 TG小鼠中[41]。SSc病理的成功治疗与fra2 TG小鼠中选择性活化巨噬细胞数量的减少有关[41]。
IL-1信号传导阻断可以如何诱导朝向Th2细胞介导的免疫的移位的问题是难以回答。IL-1对T辅助子集分化的影响是复杂的[42]。即使Th1细胞不表达IL-1R,既Th2和Th17细胞可以以IL-1 [响应43]。例如,无限制的IL-1信号(在IL-1R拮抗剂缺陷小鼠)导致增加的Th17应答[44]。关于Th2炎症反应,IL-1主要报道有利于Th2的分化[45,46]。然而,它也表明,增加IL-1β表达抑制胸腺基质淋巴细胞生成素的生产,一个关键的Th2细胞因子与特应性皮炎和哮喘(47],和激活的脾细胞从IL-1R1缺陷型小鼠中分离,缺乏IL-1信号传导,具有增加的产量的IL-4 [48]。结合我们的数据,这表明在某些情况下,IL-1可能是IL-4的负调控因子。更复杂的是,Th17和Th2的反应紧密交织,可以相互抵消[49]。因此,需要对IL-1对T辅助细胞亚组中的SSc的上下文效果的进一步调查。
值得注意的是,我们不能完全排除观测到的影响是由于IL-1R信号的封锁。虽然目前还没有关于肺或炎症的研究,但有少数研究报道了IL-1R拮抗剂的IL-1R非依赖性作用,例如在海马体,它可以作为一种兴奋剂模仿IL-1β效应(50或在肝脏中产生胰岛素抵抗[51]。尽管他们的相似之处,IL-1α和IL-1β具有不同的表达模式,功能,我们这里,下游信号通路:虽然IL-1α持续表达的各种细胞内稳态下,IL-1β只是诱导炎症期间(52,53]。因此IL-1R1的一般封锁可能会掩盖或覆盖特定的IL-1β中和有益的作用。此外,我们的研究是由人的小样本量和移植的终末期肺标本用于研究人体组织硬皮病病机变化的事实限制。因此,对疾病的发生和发展得出结论可能是有限的,必须依靠从动物模型收集的数据。然而,我们的研究结果可能有重要的临床意义,因为IL-1封锁属于那些在临床研究中涉及的概念。例如,IL-1使用rilonacept封锁(IL-1-阱)中的I / II期临床试验中进行测试;然而,观察到皮肤的病理或IL-1活性的任何改变的指标[54]。本研究观察到的不良反应表明,阻断IL-1R1信号通路的阳性抗炎作用可能被IL-1R1拮抗剂/IL-1阻滞剂治疗的患者纤维化/Th2炎症的增加所覆盖。例如,类风湿性关节炎患者,新的生物疗法治疗如白介素受体或肿瘤坏死factor-α封锁似乎恶化已有的间质性肺病(55]。因此,必须仔细考虑生物药物的益处及其风险,特别是易于发生炎症或感染的患者或Th1/Th2混合炎症的患者,在这些患者中,炎症平衡失调可能会导致严重的不良反应。
总之,我们已经证明IL-1在肺纤维化的发展中具有复杂的调节作用,通过抑制胶原蛋白的产生作用于结构细胞,进而平衡免疫系统的促纤维化和促炎作用。以肺部炎症、血管重构和纤维化为特征的fra2 TG小鼠IL-1信号通路的阻断,通过增加Th2炎症和肺内胶原蛋白的生成而使肺功能恶化。这些数据对寻找新的针对SSc特异性炎症通路的干预策略具有重要意义。
补充材料
补充材料
请注意:补充材料不是由编辑部编辑,因为它已经由作者提供的上传。
补充图S1。: Fra2过表达(TG)时的实质和血管重构。(A) 3只不同的fra2 TG小鼠和1只同窝物对照小鼠的天狼星红染色全肺切片代表性图像;规模酒吧1毫米。(B)代表图像对α-smooth肌肉肌动蛋白免疫组织化学双染色法(α-sma、紫)和内皮标记血管性血友病因子(vWF、浅棕色)野生型(WT)或Fra-2 TG老鼠。上面板:小实质血管,下面板:支气管周动脉;酒吧规模:20μm;B:支气管。erj - 00154 - 2019. - figure_s1
补充图S2。加载控制用于电泳迁移率变动分析转染实质成纤维细胞(PF)(在图2E-F提交)FRA-2的过度表达质粒(+)或空对照质粒( - )和从FRA-2过表达的肺匀浆(TG)或野生型对照(WT)小鼠。CE:胞质提取物;NE:核提取物。erj - 00154 - 2019. - figure_s2
补充图S3。信令在IL-1α和IL-1β的刺激调节的途径。(A)代表性蛋白质印迹图片磷酸化和总JNK,p38的,ERK,化cjun,FRA2和后用IL 5和15分钟的刺激从肺动脉平滑肌细胞(PASMC)和实质的成纤维细胞(PF)细胞质和核提取物的p65的-1α(1纳克/毫升)或IL-1β(10纳克/毫升)。拉明和α微管蛋白充当细胞核和细胞质加载控制。(B,C)在IL-1αCOL1A1表达(1纳克/毫升)和IL-1β(10纳克/毫升)和ERK的抑制肺动脉平滑肌信令(B)和NFκB的PFS(C)的信令。U0:ERK抑制剂U0126;PS:IκB抑制剂PS1145。DMSO:二甲基亚砜 - 车辆控制。* P <0.05。ERJ-00154-2019.Figure_S3
可共享的PDF
致谢
我们要感谢Verena Braunschmid、Julia Schittl、Bettina Schrenk和Thomas Fuchs (Ludwig Boltzmann肺血管研究所,奥地利格拉茨)提供的技术支持。我们感谢Latifa Bakiri和Erwin Wagner(西班牙国家癌症研究中心,马德里,西班牙)慷慨地提供了cmv -hu- fra2质粒结构。我们非常感谢奥地利维也纳的分子病理学研究所(Research Institute for Molecular Pathology)和奥地利的Erwin Wagner对fra2 TG小鼠的研究。
脚注
这篇文章有补充资料www.qdcxjkg.com
支持声明:A. Birnhuber由奥地利国家银行Jubilee基金会(赠款16187给G. Kwapiszewska)资助,并在格拉茨医科大学(奥地利格拉茨)的博士课程“分子医学”框架内接受培训。A. Sahu-Osen由奥地利科学基金(FWF)资助:P27848-B28 (G. Kwapiszewska)。R. Eferl获得了奥地利科学基金(FWF) doktoratskollegplus资助的“炎症和免疫”:FWF资助P26908-B20和P29222-B28。S. Crnkovic、V. Biasin、L. Brcic、N. Cikes、A. Olschewski和G. Kwapiszewska获得了奥地利教育与研究国际合作署(OAD)的支持(WTZ HR14/2012)。本文的资助信息已存入交叉引用出资者注册。
利益冲突:A. Birnhuber报道了来自奥地利国家银行Jubilee基金会在研究期间的资助情况。
利益冲突:S. Crnkovic没有什么要披露的。
利益冲突:V. Biasin没有什么要披露的。
利益冲突:马什没有什么要披露的。
利益冲突:B. Odler有没有透露。
利益冲突:A.萨胡-OSEN有没有透露。
利益冲突:E. Stacher-Priehse有没有透露。
利益冲突:L. Brcic报告赠款和个人的费用由阿斯利康,罗氏奥地利,从MSD奥地利和辉瑞奥地利,外面提交作品非金融支持的个人费用。
利益冲突:施耐德没有什么要披露的。
利益冲突:N. Cikes有没有透露。
利益冲突:B.加尼姆有没有透露。
利益冲突:克雷佩特科没有什么要披露的。
利益冲突:W. Graninger有没有透露。
利益冲突:Y. Allanore有没有透露。
利益冲突:R. Eferl没有什么要披露的。
利益冲突:A. Olschewski没有什么要披露的。
利益冲突:H. Olschewski报告来自拜耳、MSD、辉瑞和诺华的个人费用和非财务支持,来自Actelion的个人费用和非财务支持,来自Inventiva的资助,来自Bellerophon的个人费用,在提交的作品之外;他是奥地利格拉茨路德维希·玻尔兹曼肺血管研究所的兼职雇员。
利益冲突:G. Kwapiszewska报告从奥地利国家银行的银禧基金(批准16187),奥地利科学基金会(FWF)(P27848-B28)和奥地利机构在教育国际合作与研究(WTZ HR14 / 2012)的赠款,在研究进行期间。
- 收到2019年1月22日。
- 接受2019年6月23日。
- 版权所有©ERS 2019
这篇文章是开放存取并根据知识共享188滚球软件署名非商业许可证4.0的条款分发。