文摘
改造的机制和细胞球员导致慢性阻塞性肺病持续气流限制在很大程度上仍难以捉摸。我们最近表明,循环纤维细胞,这是一种罕见的人口产生的纤维母细胞骨髓基质,增加慢性阻塞性肺病患者在恶化。我们旨在量化纤维细胞密度原位在支气管标本对照组和慢性阻塞性肺病患者,定义关联与相关临床、功能和计算机断层扫描(CT)参数,并调查上皮在纤维细胞生存的微环境的影响在体外(“Fibrochir”研究)。
总共17 COPD患者和25对照组,所有需要胸外科,招募了。使用co-immunostaining和图像分析,我们确定了CD45+FSP1+细胞组织纤维细胞,并量化其密度在远端和近端支气管标本。纤维细胞,培养从六名慢性阻塞性肺病患者的血液样本,暴露在主支气管上皮细胞分泌物从对照组或慢性阻塞性肺病患者。
我们表明,纤维细胞增加远端和近端组织标本的慢性阻塞性肺病患者。纤维细胞的密度是负相关与肺功能参数和与支气管壁厚呈正相关评估CT扫描。远端支气管纤维细胞的高密度预测存在的慢性阻塞性肺病的敏感性为83%,特异性为70%。暴露慢性阻塞性肺病的纤维细胞上皮细胞上层的支持细胞的生存。
我们的结果从而证明纤维细胞密度增加慢性阻塞性肺病患者的支气管内,这可能是由epithelial-derived survival-mediating因素。
文摘
高组织纤维细胞的密度与减少肺功能和气道壁厚的增加bit . ly / 2 jo71dq
介绍
慢性阻塞性肺病的特点是慢性炎症和重塑导致进步的气流限制(1,2]。这种慢性疾病的演变是由急性加重恶化,经常由病毒或细菌感染3]。这些发作死亡率(被认为是一个独立的预后因素4]。目前药物治疗慢性阻塞性肺病患者减少恶化频率只有29%与安慰剂比较单独或组合,但是他们对死亡率没有显著的影响(5- - - - - -9]。慢性阻塞性肺病患者表现出改造过程导致永久性的组织结构的变化,如上皮粘膜化生,实质破坏(即。肺气肿)和结缔组织沉积在小气道壁(1]。后者,也叫做peribronchiolar纤维化,已经观察到即使在年轻吸烟者(10),因此这可能一个初始事件在慢性阻塞性肺病的病理生理学。这些过程不抑制或逆转目前的药物治疗。
纤维细胞纤维母细胞由骨髓基质和释放的末梢循环(11]。循环纤维细胞,定义为CD45+胶原蛋白我+细胞,增加慢性阻塞性肺病患者的恶化,而不是只在一个稳定的状态,而在对照组(12,13]。高血纤维细胞浓度在恶化是与死亡风险增加有关12),表明纤维细胞在慢性阻塞性肺病进化的有害作用。相比之下,myeloid-derived抑制细胞样的纤维细胞,循环纤维细胞的亚群,增加稳定的慢性阻塞性肺病患者的血液中,这些细胞可能发挥保护作用[13]。纤维细胞的存在和作用在肺部的慢性阻塞性肺病患者仍存在争议,需要澄清(13]。确实,定义为组织纤维细胞CD34+胶原蛋白我+细胞,没有发现在慢性阻塞性肺病患者的远端航空公司和已发现的近端航空公司只有< 50%的慢性阻塞性肺病患者13]。然而,众所周知,纤维细胞表达下调CD34表达当微分(14]。因此,coexpression CD34和胶原蛋白,作为组织纤维细胞的定义标准,可能会导致纤维细胞低估(13]。因此,我们将纤维细胞定义为细胞阳性CD45和fibroblast-specific蛋白1 (FSP1),从人类和小鼠的肺与先前的报告相一致15- - - - - -18]。
因此,本研究的目的是确定组织纤维细胞的密度(即。CD45+FSP1+细胞)在远端和近端慢性阻塞性肺病患者的呼吸道标本的价格相比对照组。然后我们评估组织纤维细胞的密度和参数之间的关系来源于肺功能测试和定量计算机断层扫描(CT)以及与血纤维细胞的关系。功能在体外实验评估上皮细胞微环境的影响也表现在纤维细胞的生存。
方法
更详细的描述中提供的方法补充材料。
研究人群
主题> 40岁都有资格报名,如果他们需要胸肺叶切除手术对癌症(pN0),肺移植或肺减容(见表E1对个人的迹象)。总共17 COPD患者的临床诊断慢性阻塞性肺病根据全球倡议对慢性阻塞性肺疾病指南(2)和25 non-COPD科目(对照组)与正常肺功能测试(即。用力呼气量在1 s (FEV1)/用力肺活量(FVC) > 0.70)和慢性症状(咳嗽或吐痰)招募大学医院的波尔多葡萄酒(法国波尔多)。
研究纤维细胞在体外、血液样本来自一个单独的队列的COPD患者:眼镜蛇队列(Cohorte阻塞Bronchique et Asthme(支气管阻塞和哮喘组),由法国国家健康与医学研究INSERM) (表E4和E6)。
研究设计
这个临床试验是由波尔多的大学医院。这项研究是在注册ClinicalTrials.gov与标识符NCT01692444(“Fibrochir”研究)。研究当地的研究伦理委员会批准的协议是5月30日,2012年,法国国家机构药品和保健品安全5月22日,2012年。所有科目提供书面知情同意。研究设计的总结图E1。四个访问计划:pre-inclusion访问解释研究和手术,包括访问当天手术,手术后1个月±15天的访问,和最后一个访问1年±手术后15天。
支气管纤维细胞识别
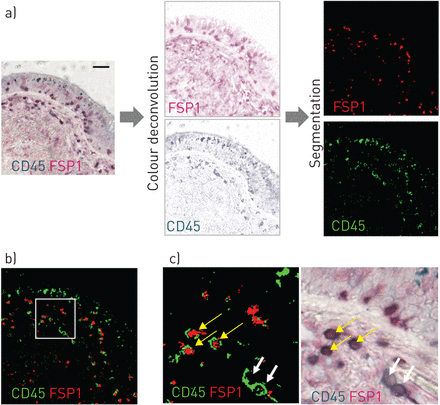
subsegmental支气管样本(近端组织)和远端软组织的碎片从肺切除材料获得距离肿瘤的癌症。额外的上部叶和下部叶的近端样本取自四移植患者(患者48,49岁的51、52个;表E1)测试潜在的在不同的叶纤维细胞密度的差异。在石蜡样本嵌入,厚2.5µm部分被削减和沾染了一只兔子anti-FSP1多克隆抗体(安捷伦,Les乌里,法国)和一只老鼠anti-CD45单克隆抗体(美国BD生物科学,圣何塞,CA)或鼠标anti-CD3单克隆抗体(安捷伦),鼠标anti-CD19单克隆抗体(安捷伦)和一只老鼠anti-CD34单克隆抗体(安捷伦)。部分是使用Nanozoomer 2.0 ht滑动扫描成像(滨松光子学、厚重的、法国)。量化FSP1和CD45 double-positive细胞进行了描述图1。FSP1的密度+CD45+细胞比值定义的固有层double-positive细胞的数量除以固有层区域。量化的double-positive FSP1和CD3, FSP1 CD19和FSP1和CD34细胞进行一些修改(见如前所述补充材料)。组织区域和细胞测量都是蒙蔽的方式执行。
检测CD45+fibroblast-specific蛋白1 (FSP1)+细胞。一)左栏:CD45(绿色)和FSP1(红色)染色;中间列:图像CD45和FSP1染色颜色反褶积后获得;右列:分割图像获得CD45和FSP1染色后由一个二进制的阈值分割。酒吧规模:50μm。b)合并分割图像。c)更高的分割图像的放大(b)。黄色和白色箭头指示CD45+FSP1+细胞和CD45+细胞,分别。
循环纤维细胞识别
不依从non-T (NANT)细胞纯化从外周血单核细胞(PBMCs)从全血中分离出来,和循环纤维细胞被当成CD45双阳性细胞表面标志和细胞内胶原蛋白标志我通过流式细胞术,如前所述[12]。
纤维细胞分化和生存
NANT细胞从血液样本中纯化的COPD患者(表E4和E6)在DMEM培养1周(费舍尔科学、伊利柯克奇、法国)补充20% FCS(擤鼻涕河滨分校密苏里州,美国),其次是1周无血清培养系统在无血清培养基或基底上层清液含有50%。2周后在文化、CD45的细胞被固定和染色,FSP1,纤连蛋白、波形蛋白,α-smooth肌肉肌动蛋白(α-SMA)和胶原蛋白我表达或分离accutase(费舍尔科学)和固定在一夜之间Cytofix / Cytoperm和染色评估相同的蛋白质的表达或直接由propidium碘染色(PI)评估死细胞的百分比(π+流式细胞仪细胞)。
统计分析
值提出了均值与标准差或中位数(95%置信区间)。统计学意义,定义为p < 0.05,被确切概率法分析了比例的比较,通过双边独立研究变量参数分布,Wilcoxon测试,Mann-Whitney u测验和斯皮尔曼相关系数为变量的非参数分布。关于相关性的分析,没有数学校正为多个比较,正如前面推荐(24]。接受者操作特征(ROC)分析和单变量逻辑回归分析进行评估之间的联系组织纤维细胞的慢性阻塞性肺病和高密度。
结果
研究人群
病人的数量登记、排除或手术后随访1年所示图E1。临床和功能特征与定量CT评估参数与组织纤维细胞的所有科目中所示表1。控制和慢性阻塞性肺病患者的组织匹配对年龄和身体质量指数。正如所料,慢性阻塞性肺病患者显著不同控制吸烟习惯,肺功能(FEV1FVC, FEV1/ FVC率和残余体积(RV)),扩散能力(肺的转移因子一氧化碳(TLCO))和CT参数,包括壁厚、肺气肿程度(低密度区),空气滞留(平均肺衰减值在过期),肺血管截面积和数量(表1),性别比例也不同,有更多的男性COPD组。
慢性阻塞性肺病患者的支气管纤维细胞数量增加
作为方法论的控制,我们首先培养纤维细胞从血液样本从一个单独的队列的COPD患者(表E4),我们表明,几乎所有CD45+FSP1+细胞(99.7±0.5%,n = 9)净化后循环PBMCs也表达胶原蛋白我14天的分化在体外(图E2)。同样,CD45的87.5±6.2%+胶原蛋白我+细胞阳性FSP1染色在相同的培养条件(n = 9)。CD45+FSP1+细胞自发表达间充质细胞的标记,如波形蛋白(99.9±0.1%,n = 6),纤连蛋白(73.3±0.1%,n = 2)和α-SMA (100±0%, n = 6) (图E2)。这允许我们定义和CD45组织纤维细胞+FSP1+细胞。通过免疫组织化学方法确定这些细胞所示图1,他们在远端组织标本中发现11种慢性阻塞性肺病患者(92%)和13的20对照组(65%)(图2),以及在近端组织标本14的14名慢性阻塞性肺病患者(100%)和16的21对照组(76%)(图3)。
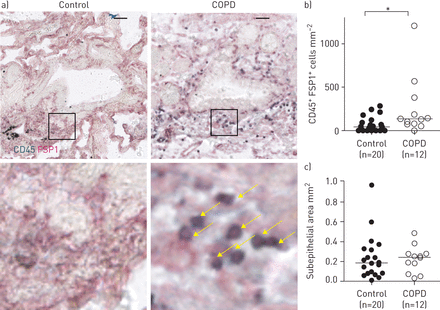
在远端气道的慢性阻塞性肺病患者纤维细胞密度增加。FSP1: fibroblast-specific蛋白1。CD45)代表染色(绿色)和FSP1(红色)在远端支气管组织标本控制主体和慢性阻塞性肺病患者。黄色箭头表示纤维细胞,定义为CD45+FSP1+细胞。更高的放大图像底部行所示。酒吧规模:50μm。b)量化的纤维细胞密度(正常的牙龈区)在一个标本/病人。*:p < 0.05, Mann-Whitney测试。c)牙龈的地区比较对照组和慢性阻塞性肺病患者。b, c)中位数表示为水平线。
纤维细胞密度增加的近端气道慢性阻塞性肺病患者。FSP1: fibroblast-specific蛋白1。CD45)代表染色(绿色)和FSP1(红色)在近端支气管组织标本控制主体和慢性阻塞性肺病患者。黄色箭头表示纤维细胞,定义为CD45+FSP1+细胞。更高的放大图像底部行所示。酒吧规模:50μm。b)量化的纤维细胞密度(正常的牙龈区)在一个标本/病人。*:p < 0.05, Mann-Whitney测试。c)牙龈的地区比较对照组和慢性阻塞性肺病患者。b, c)中位数表示为水平线。
这些纤维细胞是位于牙龈的远端和近端地区航空公司(图2一个和3),偶尔在上皮细胞层。没有CD45+FSP1+在气管平滑肌层细胞明显。一些组织纤维细胞被发现在支气管旁区域外的平滑肌层(图E3)。然而,纤维细胞密度的分析在这一地区不能系统地执行,因为这个区域不能确定在每个组织标本。支气管纤维细胞的密度更高的牙龈地区远端气道的慢性阻塞性肺病患者(平均133个细胞·毫米−2(95% CI 40 - 469细胞·毫米−2),n = 12)比对照组(平均42·mm细胞−231 (95% CI - 114细胞·毫米−2);p < 0.05, n = 20) (图2 b)。同样,纤维细胞密度也增加了近端气道的慢性阻塞性肺病患者(平均73个细胞·毫米−2(95% CI 47 - 139细胞·毫米−2),n = 14)与对照组(平均21细胞·毫米−2(95% CI 60细胞·毫米−2);p < 0.05, n = 21) (图3 b)。远端和近端,没有差别在牙龈领域考虑组织纤维细胞COPD患者和对照组之间的量化(图2 c和3 c)。不足为奇的是,然而,在牙龈纤维细胞的密度区域的近端组织积极和显著相关,在远端测量航空公司(图E4)。慢性阻塞性肺病以来称为异构子组上部叶主要疾病的患者(2),我们想知道是否专门积累上叶纤维细胞。远端和近端组织标本,在纤维细胞密度这两个网站之间无显著差异(图E5a和b)。利用样本网站的各种位置移植患者(n = 4),我们也观察到纤维细胞密度没有明显不同于上降低这些患者的叶(图E5c)。在近端和远端标本,纤维细胞密度显著增加在慢性阻塞性肺病患者相比,控制吸烟当never-smoker控制受试者从分析(图E6)。占慢性阻塞性肺病患者和对照组之间的性别差异,我们执行另一个性别和年龄患者的亚组分析。因此,性别比例是相同的子组(50%)。纤维细胞密度在近端,但不是远,组织匹配在慢性阻塞性肺病患者仍显著高于对照组(图E7a和b)。
为了进一步证实了我们的结论,我们co-stained FSP1 CD3或CD19确定FSP1+分别t淋巴球或b淋巴球细胞可以。除了一个控制主题,CD3很少+细胞也表达了FSP1 (图E8a),在CD3的密度无显著差异+FSP1+牙龈细胞远端区域航空公司之间的控制和慢性阻塞性肺病患者(图E8b和c)。同样,这个密度之间的近端航空公司没有明显不同的组(图E8d和e)。淋巴球CD19标记co-localised FSP1+细胞都在远端(图E9a)和近端(图E9b)组织标本。我们还co-immunostained CD34和FSP1。CD34+FSP1+细胞被发现在远端组织标本中只有两个12 COPD患者(17%)和四个对照组(20%)(图E10汽油)。CD34+FSP1+细胞被发现在近端组织标本13的COPD患者(69%)和11个21对照组(52%)(图E11),但是这些细胞的密度在慢性阻塞性肺病患者(平均0.5细胞·毫米−2(95% CI 0.1 - -1.7细胞·毫米−2),n = 13)与CD45相比很低+FSP1+细胞(平均73毫米−2(95% CI 47 - 139细胞·毫米−2),n = 14) (图2 b)。远端和近端,CD34的密度没有差别+FSP1+慢性阻塞性肺病患者和对照组之间的细胞(图E10汽油和E11)。
支气管纤维细胞密度和功能之间的关系和CT参数
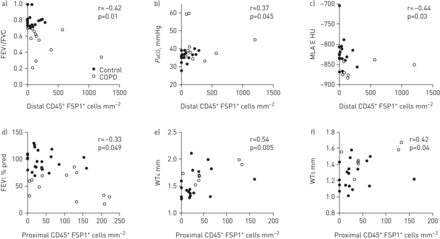
我们确定了单变量之间的相关系数在牙龈组织纤维细胞的密度地区的远端和近端航空公司和各种功能和CT参数,没有纠正多个测试(表E2和E3)。远端组织标本,纤维细胞的密度与FEV负相关1/ FVC比(图4一)和动脉二氧化碳张力呈正相关(P华2)(图4 b)。组织纤维细胞的密度也显著相关的是肺呼气时衰减值(图4 c)。近端组织标本,纤维细胞的密度与FEV负相关1(图4 d)和FVC (表E2),与RV呈正相关(表E2),在第四和第五代(壁厚图4 e和f),墙面积百分比在第四代(表E2)。此外,我们观察到相同的关键相关性never-smoker控制受试者的分析(图E12汽油)。再次,考虑慢性阻塞性肺病患者和对照组之间的性别差异,我们确定关键相关系数性别和年龄患者的亚组分析。所有关键相关性之前发现在整个人口仍然重要,除了远端纤维细胞密度和之间的关系P华2(图E7c-h)。
纤维细胞密度之间的关系,肺功能参数和计算机断层扫描参数。FSP1: fibroblast-specific蛋白1;FEV1:在1 s用力呼气量;FVC:用力肺活量;P华2:动脉二氧化碳张力;MLA E:是指肺衰减值在过期;WT4/5:壁厚在第四和第五代。FEV两者之间的关系)1/ FVC, b)P华2和c) MLA E和CD45的密度+FSP1+细胞远端航空测量对照组和慢性阻塞性肺病患者。d-f) d) FEV之间的关系1,e)4和f) WT5和CD45的密度+FSP1+在近端航空测量细胞对照组和慢性阻塞性肺病患者。相关系数(r)和显著性水平(p)是通过使用非参数分析枪兵。
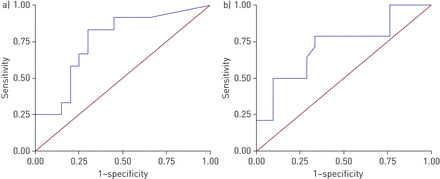
ROC曲线建立的所有主题组织纤维细胞的密度是评估在远端(n = 12 COPD患者和20对照组;图5一个)和近端(n = 14名慢性阻塞性肺病患者和21对照组;图5 b)组织标本和曲线下面积显著(表2)。预测慢性阻塞性肺病,纤维细胞的密度远航空的敏感性为83%,特异性为70%,而这个密度的敏感性为79%,特异性67%,近端航空公司(表2)。此外,消除慢性阻塞性肺病为97.5%,阴性预测值为96.6%,远端和近端,分别使用普通人群的COPD的患病率为10% (25]。ROC分析允许我们选择纤维细胞密度(截止值的最优值72和32 CD45+FSP1+细胞·毫米−2分别为远端和近端组织)对患者进行分类组织纤维细胞的高或低的水平(表2)。慢性阻塞性肺病是一种高密度的纤维细胞远端(或11.7 (95% CI 1.9 - -70.2);p < 0.05)和近端(或7.3 (95% CI 1.5 - -35.1);p < 0.05)。因此,高组织纤维细胞密度与慢性阻塞性肺病的风险增加相关。
慢性慢性阻塞性肺病的诊断准确性高纤维细胞密度:接受者操作特征曲线为对照组和慢性阻塞性肺病患者纤维细胞密度测量在一个远端或b)近端组织标本建立预测慢性阻塞性肺病。
循环纤维细胞在慢性阻塞性肺病稳定不变
血纤维细胞(CD45的百分比+胶原蛋白我+细胞)在PBMCs没有明显不同的稳定的慢性阻塞性肺病患者之间(平均10.3% (95% CI 4.6 - -16.5%)的PBMCs, n = 12)和对照组(中位数7.9% (95% CI 4.1 - -11.6%)的PBMCs, n = 22) (图E13a)。获得了类似的结果表示成纤维细胞浓度时的绝对计数每毫升血液(数据未显示)。最后,血纤维细胞的比例(即。CD45+胶原蛋白我+细胞)在PBMCs与支气管纤维细胞的密度显著相关(即。CD45+FSP1+细胞)的远端航空公司(图E13b)。
慢性阻塞性肺病上皮上层清液有利于纤维细胞的生存
我们下一个调查是否分泌物从bec控制或慢性阻塞性肺病患者可能会影响纤维细胞的可行性在体外化验。我们评估这种影响使用bec从肺切除材料取样在对照组(n = 2)或慢性阻塞性肺病患者(n = 2) (表E5),在气液界面培养。纤维细胞从血液样本单独培养的六名慢性阻塞性肺病患者(表E6)。7 - 10天后血液取样,细胞,几乎所有CD45+FSP1+(94.9±3.6%),暴露了7天的混合物完全分化BEC上层的派生从对照组或慢性阻塞性肺病患者。在最初接触后7天,CD45的水平+FSP1+细胞仍然很高(92.9±3.9%和93.4±3.3%控制和慢性阻塞性肺病条件,分别)。然而,暴露慢性阻塞性肺病的纤维细胞上皮上层清液明显减少的百分比死细胞(图E14灯头)。
讨论
在目前的研究中,我们已经表明,组织纤维细胞的密度(即。CD45+FSP1+细胞)明显更大的远端和近端呼吸道标本的COPD患者与对照组相比。我们还发现这个组织纤维细胞密度和血液之间的显著相关性纤维细胞以及气道阻塞,增加壁厚或空气滞留。使用ROC曲线分析和单变量逻辑回归分析,我们发现高组织纤维细胞的密度增加了慢性阻塞性肺病的可能性。最后,纤维细胞生存似乎是增加上皮细胞分泌物COPD患者,一种机制,可能导致牙龈纤维细胞密度升高的慢性阻塞性肺病患者。
目前的结果之间存在的差异和之前获得的W正确的et al。(13),这值得一些方法论的讨论。W正确的et al。(13)没有发现增加COPD患者的组织纤维细胞的水平。他们甚至不遵守任何纤维细胞远端航空公司。然而,组织纤维细胞的方法评估和最终纤维细胞不同的定义在目前的研究和W正确的et al。(13]。W正确的et al。的(13)方法依赖于识别CD34和胶原蛋白我在连续染色,而不是相同的,部分,这可能导致错误的纤维细胞识别因为明显coexpression密切不是但不相同的细胞或纤维细胞低估,因为没有coexpression只在一个部分细胞存在。我们有认真解决这个问题通过抗体和发色体兼容co-immunostaining相同的部分。因此我们开发了一个图像分析技术,明确标识纤维细胞。此外,定义组织纤维细胞CD34+胶原蛋白我+细胞(13)可能会导致纤维细胞低估,CD34表达差别符合之前的数据显示对这些纤维细胞分化在文化(14]。关于连接,目前的数据证实CD34的密度很低+FSP1+支气管细胞标本因此一致与W正确的et al。(13]。胶原蛋白纤维细胞通常定义为细胞共同表达CD45和我26]。造血的标记的表达,比如CD45,是最低标准纤维细胞识别和使用在目前的研究26]。然而,由于对胶原蛋白免疫组织化学我未能明确确定胶原蛋白+细胞实验(数据未显示),以及在另一份报告27),我们因此FSP1标记与CD45 co-marker用于纤维细胞识别,正如前面广泛描述(15- - - - - -18]。也称为S100A4 FSP1是用来标记肺成纤维细胞(27,28]。大多数肺FSP1+胶原蛋白细胞表达我和FSP1的数量+细胞与肺纤维化的程度在纤维化小鼠模型,表明这些细胞有助于胶原蛋白沉积(27,29日]。此外,我们表明,几乎所有的CD45+FSP1+细胞从循环PBMCs也表达纯化胶原蛋白,以及间充质细胞标记,如波形蛋白、纤连蛋白和α-SMA,经过14天的分化在体外(图E2),这是符合纤维细胞的定义myofibroblast前体,如前所述[11,14,30.]。看来这个术语组织纤维细胞更准确CD45和FSP1 double-positive细胞。因为FSP1表达式最初发现在成纤维细胞(28特征),但随后在T -淋巴细胞等免疫细胞(15),我们特别关注co-immunostaining FSP1 CD3或CD19。在这一过程中,我们表明,t淋巴球共同表达CD3和FSP1代表CD45的唯一的一个小子集+FSP1+细胞的密度在慢性阻塞性肺病患者并没有改变。我们还表明,没有细胞共同表达CD19和FSP1在场在人类支气管远或近端对照组和慢性阻塞性肺病患者。最后,FSP1表达式也被描述在巨噬细胞29日]。然而,大量的巨噬细胞标记,如CD68、CD163, CD204, CD206 CD209,由纤维细胞也表达了(31日- - - - - -33]。因此无法正确区分纤维细胞和巨噬细胞使用免疫组织化学即使我胶原蛋白+CD45+双染色法是合适的。
我们的研究结果可能支持组织纤维细胞在慢性阻塞性肺病的潜在作用。事实上,支气管纤维细胞的密度越大,FEV越低1值或FEV1/ FVC比率。同样,支气管纤维细胞的密度越大,支气管壁厚越大或肺部空气滞留。虽然纤维细胞之间的关系存在和肺功能与解剖相结合的变更修改显示纤维细胞的有害影响,我们想强调的是,协会并不表明这些细胞中发挥决定性作用。我们之前指出潜在的血纤维细胞的有害作用,因为高浓度的纤维细胞在慢性阻塞性肺病患者的末梢循环急性恶化与更高的死亡率(12]。此外,血纤维细胞经常加剧病人参加高水平(12]。因为小航空公司的主要网站在COPD气道阻塞(34- - - - - -37),观察到组织纤维细胞密度,评估在目前的研究中,在近端在远高于航空公司是有意义的。循环纤维细胞的浓度之间的相关性和远端支气管纤维细胞的密度可能表明,纤维细胞,这是血液中招募在急性加重(12),随后迁移到航空公司,可能参与组织修复和改造的过程。事实上,一旦招募到肺部,纤维细胞可能扮演不同的角色,包括基质分泌和退化,pro-fibrotic细胞因子生产、收缩力和激活(38]。肺纤维细胞的存在与哮喘和特发性肺纤维化患者的影响表明生理修复反应在几种类型的肺损伤14,39,40,41]。一方面,这个修复过程应该自发解决时间和烟草戒烟应该消失。另一方面,一个开关异常修复或过度降解异常可能参与改造过程,如支气管旁纤维化和肺气肿。减少细胞死亡在纤维细胞培养与bec COPD患者,检测到的单π+方法,结合纤维细胞密度升高的邻近上皮组织样本中慢性阻塞性肺病患者,表明分泌物上皮细胞在慢性阻塞性肺病组织纤维细胞微环境提供pro-survival信号,可以解释,至少部分,纤维细胞在慢性阻塞性肺病患者的支气管积累。纤维细胞是否存在慢性阻塞性肺病患者参与异常修复过程和慢性炎症仍在调查之中。纤维细胞的特定角色COPD发病机理仍然是另一个开放的问题。特定的物理和化学信号来自微环境可能会扮演一个关键的角色在调节纤维细胞最终的本地化,分化和功能在组织(38]。
根据观察到的重要的性别差异在慢性阻塞性肺病患者42),以及在慢性阻塞性肺病小鼠模型43),我们测试我们的结果是否反映出性别差异。匹配的患者性暗示,我们的结果是与性有关的特性。纤维细胞参与的问题与性有关的慢性阻塞性肺病的临床表现差异的男性和女性在以后的研究中还有待妥善解决,适当性分析。
本研究有一定的局限性,这值得进一步评论。需要更多的研究来探索细胞和分子机制参与epithelium-dependent纤维细胞的生存。不断努力是必要的澄清纤维细胞的细胞机制参与阻碍发展。纤维细胞检测的标本从诊断为肺癌患者42例37。作为FSP1通常是在恶性肿瘤细胞中表达44,45),一个可能表明,它可能会影响纤维细胞密度测量在我们的研究中。自1)支气管标本进行纤维细胞分析从宏观上选择正常的肺切除材料,2)分期不同于pN0证实手术后患者被排除在外,恶性肿瘤是不太可能足以解释纤维细胞密度的增加我们观察慢性阻塞性肺病患者。
总之,利用明确由co-immunostaining纤维细胞识别和图像分析,我们表明,慢性阻塞性肺病患者表现出更大的纤维细胞密度比对照组远端和近端航空。组织纤维细胞的高密度与低肺功能有关,气道结构改变与慢性阻塞性肺病的风险更高,基础需要进一步研究探讨纤维细胞的生理和病理生理功能。
补充材料
补充材料
请注意:补充材料并不是由编辑部,编辑和上传已由作者提供。
erj - 02173 - 2018 _online增刊材料erj - 02173 - 2018 - _online_supp_material
可共享的PDF
确认
确认:我们感谢研究参与者和胸外科的员工,放射学,病理学、呼吸道和肺功能测试部门大学医院的波尔多葡萄酒(法国波尔多),小薇吉妮•尼尔(中投1401年波尔多,法国)技术援助,和波尔多成像中心(BIC;法国波尔多)成像和图像分析提供帮助。显微镜在BIC CNRS-INSERM和波尔多大学的服务单位,法国国家BioImaging成员基础设施支持的法国国家研究机构(ANR-10-INBS-04)。的帮助下Christel Poujol Sebastien Marais说,Fabrice Cordelieres (BIC)成像,穆里尔的帮助Cario-Andre(大学健康U1035波尔多,波尔多,法国),免疫组织化学的帮助和皮埃尔Vallois(大学德洛林研究所Elie嘉当德洛林UMR 7502年Vandoeuvre-les-Nancy,法国)被公认为统计数据。
脚注
可以从本文的补充材料www.qdcxjkg.com
这项研究是在注册ClinicalTrials.gov标识号NCT01692444。
利益冲突:即杜宾报告从波尔多大学基金会赠款,在进行这项研究的。此外,她有一个专利(EP 15152886.6:新成分和方法治疗和/或预防慢性阻塞性肺疾病)悬而未决。
利益冲突:m . Thumerel没有披露。
利益冲突:大肠Maurat没有披露。
利益冲突:f . Coste没有披露。
利益冲突:大肠Eyraud没有披露。
利益冲突:h . Begueret没有披露。
利益冲突:t·特里没有披露。
利益冲突:m .蒙陶顿没有披露。
利益冲突:r . Marthan没有披露。
利益冲突:P-O。Girodet报告诺华的个人费用,基耶西,勃林格殷格翰集团,阿斯利康、葛兰素史克在提交工作。此外,他有一个专利(EP 15152886.6:新成分和方法治疗和/或预防慢性阻塞性肺疾病)悬而未决。
利益冲突:p·伯杰报告从奈科明赠款,武田和基金会du Souffle-Fonds de赠与矫揉造作的en桑特Respiratoire,期间进行的研究;赠款和诺华的个人费用,个人费用和非金融支持阿斯利康,赛诺菲,基耶西,资助,个人费用和非金融勃林格殷格翰集团的支持,和个人费用从Menarinni Teva,外提交的工作。此外,他有一个专利(EP 15152886.6:新成分和方法治疗和/或预防慢性阻塞性肺疾病)悬而未决。
支持声明:本研究赞助和支持由波尔多大学医院(CHU de波尔多)。本研究由波尔多大学基金会的资助,资金援助Ventilatoire住所(AVAD)和联合Girondine de Lutte靠les疾病Respiratoires (FGLMR)。资金信息,本文已沉积的Crossref资助者注册表。
- 收到了2018年11月14日。
- 接受2019年5月28日。
- 版权©2019人队