摘要
虽然靶向非小细胞肺癌(NSCLC)治疗已经改善了明确的疾病亚型的预后,但大多数患者的预后仍然较差。我们发现在278例NSCLC肿瘤样本中,AAA+ ATPase Reptin呈高表达。因此,本研究的目的是评估雷普汀在NSCLC中的作用。
1145例NSCLC患者的生存分析显示,高水平的RNA表达与不良预后相关。在人非小细胞肺癌细胞中,雷普汀的表达降低影响了细胞的生长离体消除异种移植模型中的移植。Reptin与组蛋白去乙酰化酶1 (histone deacetylase 1, HDAC1)直接相互作用,是NSCLC肿瘤进展的关键机制。药物干扰了Reptin/HDAC1复合物,导致NSCLC细胞增殖大幅减少,对顺铂明显敏感。
我们的研究结果表明,雷普汀是一种新的独立预后因子,是介导NSCLC细胞增殖和克隆生长的关键调控因子离体和在活的有机体内。我们推出了一个Reptin / HDAC1蛋白复合物,其药理中断敏感于非小细胞肺癌细胞对顺铂,这表明这种方法用于临床试验申请。
摘要
在AAA + ATP酶Reptin赋予肿瘤进展,耐NSCLC患者化疗和预后不良http://ow.ly/dLxW30kaUVu
介绍
多种致癌驱动突变的鉴定[1]的和不同的膜蛋白调节免疫系统的高表达的证据已经启用了强大靶向非小细胞肺癌的(NSCLC)的疗法的发展[2-4]。尽管有这些突破性发现的,最标准的非小细胞肺癌治疗的反应仍然是穷人和/或短暂的。迄今为止,肺癌占全世界癌症死亡的主要原因,且预后,尤其是NSCLC患者的晚期或转移性疾病仍然[可怜五]。确定预测早期转移或预后不良的参数可能有助于确定需要替代治疗策略的患者。此外,潜在的致癌和肿瘤进展的分子机制需要被阐明,以便设计出更多针对NSCLC的特异性和有效物质。
NSCLC在很大程度上是由基于多种遗传和表观遗传事件的转录调控调控决定的。转录程序的改变导致细胞转化和/或肿瘤的进展和维持[6]。在过去的几年中,AAA + ATP酶家族成员Reptin已牵涉各种生理过程,包括转录调控,DNA损伤的染色质和修复的重塑[7,8],即在非小细胞肺癌细胞经常恶化的机制。因此,我们试图确定Reptin在肺癌并作为未来非小细胞肺癌治疗的一个潜在的新靶点的作用。
材料与方法
肺癌组织芯片
肿瘤材料和临床随访数据来自德国Ostercappeln胸科的321名NSCLC患者(研究小组I;n=265例NSCLC组织样本)和德国美因茨(study collective II;56例NSCLC组织标本(中位年龄66岁)行根治性切除。收集石蜡包埋的组织样本用于生物标志物检测,获得了临床随访信息和Muenster和Mainz伦理委员会的研究批准。由于回顾性分析的匿名性,不需要病人的书面同意。临床TNM分期(包括临床检查、计算机断层扫描、超声、内窥镜、磁共振成像和骨扫描)基于国际癌症控制联盟/美国癌症建议联合委员会。对于明确的肿瘤分期,术后进行病理探查。根据世界卫生组织2004年指南,对原发性肺部病变进行病理分类;149例为鳞状细胞癌(SCC), 125例为腺癌(AC), 47例为大细胞癌。IV期、新辅助治疗、R1或R2切除状态或肿瘤组织学不明确的患者(如。非小细胞肺癌除非另有说明)被排除在我们的研究中。因此,278的患者样品保持用于分析。[Regular follow-up was performed for all patients, including systemic re-staging after 3, 6, 12, 18, 24, 36, 48 months等。或更早,如果临床需要。生存时间的计算从组织学诊断之日起至死亡或最后一次接触之日止。非小细胞肺癌患者的基线资料见补充表S1。组织微阵列(TMA中)购自福尔马林固定,石蜡包埋的组织标本产生并如先前所述[9]。应用抗人雷普丁抗体(ab号)。612482年,克隆42 / TIP49b;BD生物科学,海德堡,德国)。免疫反应用生物素化二抗(LSAB/AP, #K5005;(丹麦,格洛斯特鲁普)包括红色增色剂,并根据制造商的说明。免疫组化评价采用定量的H-score作为连续值,主要依据H提出的参数进行染色强度评价arvey等。[10],以及染色的细胞的百分比。的四个不同的染色强度(0 =无,1 =弱,2 =中度,3 =高)典型的例子是通过被染色的样本集的初始屏幕组装到建立一个参考框架(补充的方法)。每个肿瘤样本的染色强度是根据参考框架确定的。如果至少有10%的肿瘤细胞符合标准,则通过将不同颜色的肿瘤分配到更高强度的类别来整合比例信息。四个调查人员(J.-H.M。诗人书,讲述,中号。F.A.) independently analysed TMA slides. Samples with discordant assessment results were re-evaluated and a consensus was reached. The H-score was calculated as intensity × % stained cells. Optimal cut-off for overall survival was assessed using maximally selected log-rank statistics in R version 3.4.3. The association of clinico-pathological parameters with Reptin expression was tested using two-sided Fisher's exact test. Univariate overall survival analysis was performed using the Kaplan–Meier method and log-rank tests. A multivariable Cox proportional hazards model was fitted using a forward step-wise variable selection (inclusion criteria: p-value of the likelihood ratio test ≤0.05) to identify independent prognostic factors for overall survival. Patients with missing values in the cofactors were excluded from the analysis. All statistical tests were performed as exploratory analyses on a local significance level of 0.05. SPSS (SPSS Statistics, Version 22.0 released 2013, IBM Corp., Armonk, NY, USA) was used for all statistical analyses.
质粒,抗体和引物
人类的雷普丁短发针rna (shRNAs)是来自C. Abraham(美国科罗拉多大学博尔德分校)的礼物。序列为:Reptin TRCN0000051563, pLKO shRNA #1: CCGTGATGTAACAAGGATTGA;和TRCN0000051564, pLKO shRNA #2: cgagaaagacacgaagagat [11]。以雷普汀为靶点的单导rna (sgRNAs)序列载于补充图S2E。
HDAC1-的pcDNA3质粒从K.格拉塞(Abbott实验室,芝加哥,IL,USA)惠赠。我们用下面的抗体在这项研究中:旗M2(A8592)和抗β肌动蛋白(A5441;既有Sigma-Aldrich公司,圣路易斯,密苏里州,美国);Reptin抗体(抗TIP49b; 612482; BD Biosciences公司,海德堡,德国);抗CK7(SP52)兔单克隆和DAB的OptiView IHC检测试剂盒(790-4462;既有文塔纳医疗系统奥罗瓦利,AZ,USA);和山羊抗 - 小鼠(115-036-062)和山羊抗 - 兔(111-036-045;二者Dianova,汉堡,德国)。
细胞培养和试剂
人NSCLC细胞系A549,LUDLU 1和HOP62购自Sigma-Aldrich公司(梳,UK)和Charles River实验室(科隆,德国),分别获得。
一个五49和HOP62 cells were maintained in D10 medium (DMEM, 10% fetal calf serum (FCS), 100 U·mL-1青霉素和100µg·毫升-1链霉素)。大号UDLU 1 cells were maintained in R10 medium (RPMI, 10% FCS, 100 U·mL-1青霉素和100µg·毫升-1链霉素)。的DMEM(D5796),RPMI(R8758),青霉素/链霉素(P0781-100ML)和INT对碘硝基四唑紫((INT)I8377)自Sigma-Aldrich(圣路易斯,MO,USA)获得。FCS(S0115)从Biochrom(英国剑桥)获得和胰蛋白酶(BE02-007E)从龙沙(巴塞尔,瑞士)。Entinostat(MS-275,SC-279455)来自Santa Cruz Biotechnology(Santa Cruz公司,CA,USA),顺铂(PZN 06559665)从TEVA(德国Ulm),并从SERVA电泳GmbH的二甲亚砜((DMSO)20385.01)(来德国海德堡)。
慢病毒转导,集落形成和增殖测定
大号entiviral transduction was performed on NSCLC cells, adding 6 mL of D10 containing virus and 6 µg·mL-1聚凝胺(107689);西格玛,圣路易斯,密苏里州,美国)。使用合适的抗生素选择转导细胞。
为了敲除人类的雷普汀,细胞被pLKO转导。1puromycin plasmids containing shRNAs targeting human Reptin. Scrambled sequences were used as controls (sequences are available upon request). After antibiotic selection, cells were plated into methylcellulose medium containing specific drug treatment. Colonies were scored after 7–10 days of culture and labelled with INT overnight.
增殖试验采用CellTiter 96®水非放射性细胞增殖试验(G54301;Promega,麦迪逊,美国)。
免疫沉淀和免疫印迹分析
For generic immunoprecipitation, cells were lysed in NP-40 lysis buffer (0.5% NP-40, 50 mM Tris-base pH 7.5, 5 mM EDTA, 150 mM NaCl, 0.2 µM dithiothreitol, 10% glycerol, protease inhibitors) for 1 h at 4°C. Protein concentration was measured by the PerkinElmer VictorX3 spectrophotometer (Baesweiler, Germany) using the Bio-Rad protein assay reagent (Pierce, Rockford, IL, USA). Equal amounts of total protein were incubated with the respective antibody overnight, precipitated with protein A/G Dynal beads (Invitrogen, Carlsbad, CA, USA) at 4°C for 1 h and then the Dynal beads were washed with 0.5% NP-40 washing buffer. Eluted proteins were resolved by SDS–PAGE. Membranes were probed with antibodies described above. For immunoblotting, samples were lysed with radioimmunoprecipitation assay buffer (150 mmol·L-1NaCl, 1% Triton-X-100, 0.5% Na-deoxycholate, 0.1% SDS, 50 mmol·L-1的Tris·HCl的,pH为8.0)。Ëqual amount of proteins were resolved in NuPAGE Novex 4–12% Bis-Tris Gel 1.0 mm, 10-well (NP0321Box; Invitrogen, Carlsbad, CA, USA). Polyvinylidene fluoride membranes (Merck Millipore, Burlington, MA, USA) were blotted with indicated antibodies and detected by Western Lightning ECL reagent (PerkinElmer, Baesweiler, Germany). Density quantification of the bands was analysed using Image J software.
鼠标异种移植
NOD.Cg-Prkdcscid IL2rgtmWjl/Sz (NSG)小鼠用于移植实验。小鼠静脉注射1×106测试单元。所有的实验程序经批准“Landesamt献给NATUR,UMWELT UND Verbraucherschutz NRW”(GEZ 84-02.04.2014.A508),并按照规定执行。
流式细胞术分析人类细胞系
和PE小鼠IgG1k(同种型对照; 555749;用荧光染料缀合的单克隆抗体,PE抗人CD326(上皮细胞粘附分子)(; 324205 BD Biosciences公司,海德堡,德国小鼠IgG2b)通过流式细胞术分析进行免疫表型分析BD生物科学,海德堡,德国)。
染色一般在悬浮液(SM) (PBS, 0.2% FCS)中进行,在冰上孵育30分钟,洗涤两次,在SM中重悬,然后使用BD LSR II系统(BD Biosciences, Heidelberg, Germany)进行分析。
结果
Reptin在绝大多数非小细胞肺癌肿瘤组织中过表达
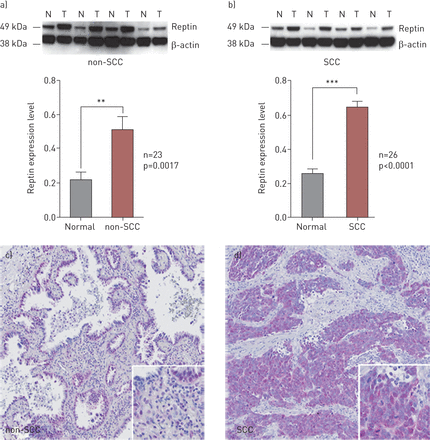
为了评估雷普汀在NSCLC中的作用,我们对49例NSCLC和278例NSCLC组织标本进行了蛋白表达的免疫组化分析。Western blot分析显示,Reptin在肿瘤组织中明显过表达与在绝大多数的NSCLC患者的相邻正常肺组织(图1a,B)。Reptin表达显著更高的患者的肿瘤组织与两个肺SCC和非SCC。在SCC患者的92%有一个在肿瘤Reptin的表达比在邻近的正常组织时(n = 26)和非SCC患者(n = 23)65%(图1a,B)。上免疫组织化学,肿瘤细胞在两个非SCC SCC和肺癌的肿瘤中显示的核染色模式为Reptin(图1c,D)。
雷普汀在大多数人非小细胞肺癌(NSCLC)中均有高表达。a, b)免疫印迹分析及肿瘤组织中Reptin表达的定量(T)与相邻的正常肺组织的患者的肺一(N))的非鳞状细胞癌(非SCC)和b)SCC。误差条代表SD至少有三个独立的实验。C,d c)中Reptin的免疫组织化学染色)非SCC和d)SCC NSCLC肿瘤组织。**:P <0.01;***:P <0.001。
在非小细胞肺癌患者中,雷普汀的预后较差
为了确定Reptin的过表达是否影响NSCLC患者的预后,我们从278名NSCLC患者TMA样品进行免疫组织化学,包括150例肺非SCC和128例SCC(补充表S1)。
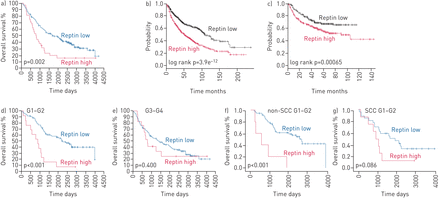
由H-评分> 160具有低Reptin表达肿瘤组织是由一个定义的H-得分≤160和高Reptin表达。低患者Reptin表达显示显著更好总体存活(P = 0.002)(图2a)。作为验证队列,我们使用了1145例NSCLC患者的生存数据,这些数据来自一个公开的数据集[12]来证实与低水平的患者相比,高水平的Reptin mRNA表达患者的总生存期(p<0.0001)明显降低(p<0.0001) (图2b, C)。间596周的患者记录的临床进展的数据,进展时间也显著患者减少了与Reptin的高表达(P = 0.00065)(图2b, C)。多变量分析使用相同的数据库确认Reptin作为整体和无进展生存期的独立差组织学和疾病阶段的(P <0.0001和p = 0.0089,分别地)的危险因素。
在非小细胞肺癌(NSCLC)患者中,雷普汀表达的预后价值表明其预后不良。a)所有患者的总生存期。b)总体和c)从公开数据中获得的更大患者队列中NSCLC患者的无进展生存期。d, e) NSCLC高分化(G1-2) (d)和低分化(g1 - 4) (e)肿瘤患者的总生存期。f, g)非鳞状细胞癌(非鳞状细胞癌)患者G1-2肿瘤(f)和SCC患者G1-2肿瘤(g)的总生存期。采用非配对t检验来确定总生存期和无进展生存期的概率的统计学意义。
与高度分化NSCLC肿瘤(G1-G2)的患者是已知的具有改善的长期结果[13]。因此,我们通过免疫组化分析,非小细胞肺癌的肿瘤样本的队列中,我们能够确定对更好的整体生存强劲走势患者的G1-G2肿瘤(N = 102),比患者更低分化(G3-G4)肿瘤(N = 170,p = 0.063)(补充图S1a)。患者高度分化的肿瘤显示出高表达Reptin已显著恶化总体存活的病人相比,来自相同子组具有低Reptin表达(P <0.001)(图2d,E)。这种差异并不患者低分化肿瘤(中看到图2d、e和补充图S1b中,C)。我们证实显著改善患者的高度分化的NSCLC表示非SCC患者低表达Reptin(P <0.001)的总生存。SCC患者与高Reptin表达G1-G2肿瘤代表了我们的研究更小群,但显示对患者总生存期的强烈趋势(P = 0.086)(图2F, G)。因此,生存分析结果显示,NSCLC患者Reptin高表达的显著预后的影响。
雷普汀的抑制抑制了非小细胞肺癌细胞的生长离体并且阻断它们的植入在活的有机体内
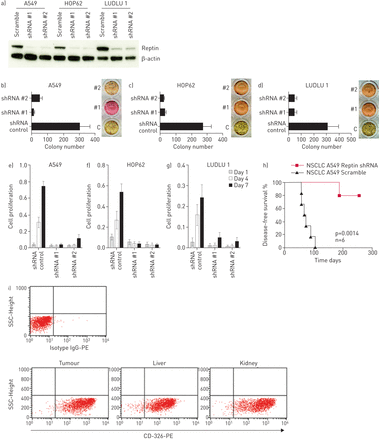
为了评估Reptin在NSCLC细胞生长和增殖中的作用,我们使用两种经过验证的针对人Reptin的shRNAs进行了慢病毒转导[11A549和HOP62人AC细胞以及LUDLU 1人肺SCC细胞。所有细胞系的雷普汀的稳定表达均与置乱对照(图3a)。Reptin的抑制显著受损的所有细胞系的克隆扩增,如甲基纤维素电镀(后通过集落数进行评估图3b-d)。此外,所有三种细胞系中表现出增殖的减少显著拦截时的Reptin(图3E-G)。要排除的shRNA介导的脱靶效应,我们设计sgRNAs靶向人Reptin不同的外显子(补充图S2E并将其克隆到慢病毒CRISPR-Cas9载体中。再次,在A549、HOP62和LUDLU 1细胞中实现了对雷普汀的稳定抑制通过我们构建的慢病毒转导(补充图S2a中和数据未显示)。我们证实在两种肺AC和SCC细胞Reptin表达水平的克隆形成能力和增殖依赖性(补充图S2b中-d和数据未显示)。
Reptin的敲低抑制克隆扩增和人非小细胞肺癌(NSCLC)细胞的增殖离体和损害移植在异种移植模型。一)(Reptin人肺腺癌细胞A549和HOP62)和鳞状细胞癌(SCC)的细胞的敲低(LUDLU 1)通过验证的shRNAs #1和#2与置乱对照组相比,评估通过免疫印迹。B-d)集落的数目A549,HOP62和LUDLU 1个肺癌细胞,分别在时Reptin击倒甲基纤维素和相比于加扰控制(C)和e-g)作为评估由MTS测定这些细胞的增殖。误差条代表SD至少有三个独立的实验。h)与对照组相比,shrna介导的Reptin表达下调后,NSG小鼠的无病生存。使用log-rank (Mantel-Cox)检验比较生存曲线。p值<0.05为差异有统计学意义。i)对照组小鼠转移组织细胞经人抗cd -326- pe染色后进行代表性流式细胞术分析。搞笑:免疫球蛋白。
A549细胞中雷普丁的下调也能够阻断6只NSG小鼠中的5只的移植,而所有移植了相同细胞的小鼠(经过干扰转导的对照组)在70-110天内发生转移性肺癌(n=6) (图3H)。流式细胞术检测到的人上皮细胞粘附分子CD326的强表达在从转移病灶分离的细胞,这表明患病小鼠的器官被很大程度上受人NSCLC细胞浸润(图3I)。此外,组织学分析证实了人类侵入AC鼠器官的浸润与人类CK7的强表达(补充图S3a, b)。因此,人非小细胞肺癌细胞的生长离体和植入在活的有机体内基本上依赖于Reptin的存在。
一个Reptin / HDAC1在NSCLC细胞复合物的药理学干扰显著降低克隆生长
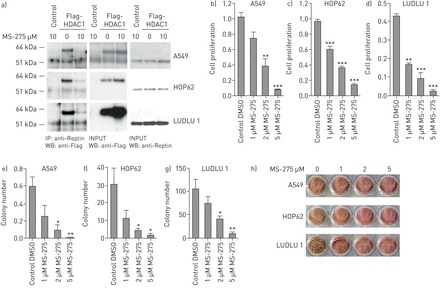
我们能够证实,Reptin直接与HDAC1,为转录抑制其涉嫌伙伴之一相互作用,在人类HEK-293细胞(补充图S4)14]。在肺AC,HDAC1与相关因素的患者预后较差的表达[15]。为了评估是否Reptin和HDAC1也非小细胞肺癌细胞联营,我们进行了进一步的免疫共沉淀实验。我们能够探测到在所有三个测试的肺癌细胞株Reptin和HDAC1之间的直接互动(A549,HOP62,LUDLU 1)。有趣的是,当我们暴露NSCLC细胞对MS-275(entinostat),1类HDAC抑制剂与HDAC1特殊的亲和力,这种蛋白质 - 蛋白质相互作用在两个肺AC和SCC细胞显著减少(图4a)。下一步,我们用不同浓度的MS-275处理A549、HOP62和LUDLU 1细胞。三种细胞系在MS-275的作用下增殖能力和集落形成能力均显著降低(图4b- h)。因此,药物抑制Reptin/HDAC1蛋白复合物可能是未来NSCLC治疗方法的一个有前途的新策略。
药物干扰Reptin/HDAC1复合物可显著抑制人非小细胞肺癌(NSCLC)细胞的集落形成和增殖。a)人A549、HOP62和LUDLU 1细胞在有无标记HDAC1的情况下共免疫沉淀分析,并在MS-275存在或不存在的情况下按指示浓度培养。b-d)增殖分析,e-g)集落形成分析,h) INT染色,这三种方法都表明无论MS-275的存在与否,NSCLC细胞系都存在。7天后进行菌落计数。采用单因素方差分析(one-way ANOVA)检验,确定MS-275处理后所有代表细胞增殖和集落形成测定的柱状图的统计学意义。误差条代表SD。DMSO:二甲亚砜。*:P <0.05;**:P <0.01;***:P <0.001。
破坏NSCLC细胞对顺铂的Reptin / HDAC1复合增强灵敏度
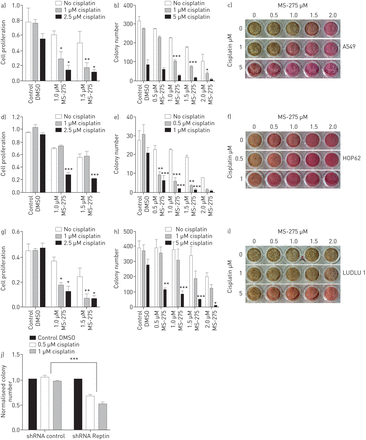
迄今为止,铂双药化疗仍然是(新)辅助治疗和姑息治疗的设置对于大多数小细胞肺癌患者的中坚力量。不幸的是,大多数NSCLC患者要么表明前期铂电阻或将发展初始治疗响应后复发或病情恶化。因此,我们评估是否顺铂与MS-275组合可以提高化疗的治疗效果。肺AC和SCC细胞暴露于甚至低剂量的MS-275的深刻增加顺铂对这些细胞的作用。低剂量的顺铂诱导的轻度至中度减少集落形成能力和A549,HOP62和LUDLU 1个细胞的增殖二者的;添加低剂量的MS-275显著增强其效果的(图5a-一世)。为了证实Reptin在这个复杂的角色对肺癌细胞致敏治疗与顺铂,我们暴露人类非小细胞肺癌细胞与Reptin的低剂量顺铂的shRNA介导的击倒。再次,相对于该加扰控制的化疗效果是显著更深刻(图5J)。因此,针对Reptin / HDAC1复杂的可能,以改善未来的铂类化疗方案的NSCLC患者的效果的有效选项。
Reptin / HDAC1蛋白通过MS-275敏感于非小细胞肺癌(NSCLC)细胞对顺铂复合物的破坏。联合治疗A-C的人NSCLC细胞)A549,d-f)中HOP62和g-i)的LUDLU 1使用顺铂和MS-275在所指示的浓度:增殖测定(一,d,g)中,集落形成测定(b,E,H)和INT染色(C,F,I)被显示。双向ANOVA检验用于确定所有条形图下组合治疗细胞增殖和集落形成测定统计显着性。j)的Reptin敏感于人NSCLC细胞对用顺铂治疗的敲低。的shRNA介导的Reptin的敲低提高了顺铂处理对人A549 NSCLC细胞的克隆扩增的影响离体相对于混乱控制。误差条代表SD至少有三个独立的实验。DMSO:二甲亚砜。*:P <0.05;**:P <0.01;***:P <0.001。
讨论
预防,诊断和治疗[:在过去的几年中,显著的进步已经在非小细胞肺癌管理的三大支柱制成2,16]。However, with >1.5 million deaths per year, lung cancer remains one of the major causes of cancer deaths worldwide [五]。对于成功的肺癌治疗包括诊断的主要障碍在疾病早期复发和/或转移,和患有转移性肺癌到可利用的疗法差响应的后期阶段。在NSCLC识别和靶向分子改变可以大大扩大医师的剧目用于治疗肺癌[最近的临床试验提供了证据2,4]。然而,目前还没有一种物质可以治愈大多数晚期NSCLC患者。因此,揭示导致肺癌的转录和表观遗传机制仍然是肺癌研究的主要目标。
我们揭示AAA + ATP酶Reptin的新功能,如在非小细胞肺癌的关键角色。我们能够证明,Reptin在绝大多数NSCLC肿瘤,不论其组织学类型的高表达和Reptin的高表达水平与受影响的患者的预后不良有关。此外,非小细胞肺癌的患者的预后差相当分化良好的肿瘤和高Reptin表达表明该蛋白是早期转移的在该亚组的预测值。我们提供的证据几行Reptin作为非小细胞肺癌细胞增殖和克隆生长的关键调节器。重要的是,在NSCLC细胞Reptin击倒显著损害它们诱导转移性肺癌在鼠异种移植物模型的能力。
因此,我们的数据呈现Reptin作为用于NSCLC患者预后的预测,以及用于治疗非小细胞肺癌未来治疗目标的潜在的新的分子标记。
然而,直接针对雷普汀还不适用。因此,靶向雷普汀的关键相互作用伙伴可能是一个合理的替代方法,以削弱雷普汀的信号通路。事实上,雷普汀可能是不同的多蛋白复合物的一部分,这意味着它在各种细胞过程中的功能,包括那些与肿瘤发生和肿瘤进展相关的过程。在-连环蛋白的协同作用下,一种雷普汀染色质重组复合物定向转录调控被证明是下调的KAI1[17]。然而,在非小细胞肺癌细胞中敲除Reptin并不影响表达水平KAI1(数据没有显示)。因此,我们的数据暗示了一种新的途径通过特别是在非小细胞肺癌中,一种Reptin/HDAC1的相互作用。有趣的是,在AC肺癌患者中,HDAC1的高表达会导致预后不良[15]。在我们的研究中,我们能够表明,在非小细胞肺癌细胞Reptin新兵HDAC1成复杂的蛋白质,而这种复合物可在暴露被打乱到MS-275是一种有效的HDAC1抑制剂,导致肺癌细胞生长的实质性抑制。
HDAC的主要贡献发生和癌症进展[18]。因此,HDAC的抑制已经成为肿瘤靶向治疗具有高度吸引力。使用HDAC抑制剂的多个临床试验已经结束,正在进行评估不同类型的癌症,这些药物的潜力,第一HDAC抑制剂最近已批准了几个恶性疾病。然而,单一药剂HDAC抑制可能不是作为用于治疗非小细胞肺癌的治疗方法是可行的,考虑到各种临床试验在内的一些非小细胞肺癌大多不能示出了使用HDAC抑制剂作为单一疗法突破作用[19],和高剂量的HDAC抑制剂的赋予相当大的毒性,以患者[20]。然而,从不同的临床试验结果显示,联合治疗包括HDAC抑制是更加有前途的肿瘤治疗策略[19]。因此,在我们的研究中,我们暴露肺交流和SCC细胞联合顺铂低剂量的MS-275。MS-275显著增强顺铂的细胞响应,显示出即使在顺铂的浓度不具有相关功效作为单一药剂显着的效果。
由于多数患者的局部晚期或转移性非小细胞肺癌不怀有致癌司机直接听话通过特异性抑制剂,它们仍然收到具体新辅助,辅助和姑息治疗设置铂类化疗两倍。此外,许多患者最初分子疗法治疗需要化疗在他们的治疗过程的后期阶段。实质毒性以及从这些细胞毒性疗法导致响应的有限速率和持续时间带动改善治疗反应和毒性特征的新物质的需要。上一页肺癌试验与联合治疗包括在大多数亚组未能显著改善患者的预后HDAC抑制剂。然而,更具体的和选择性HDAC抑制剂MS-275应该仍然被认为是一种有前途的药物NSCLC患者,更是如此鉴于其作用似乎是在除了对正常细胞转化的更深刻的[21]。它可能只需要与合适的合作伙伴一起应用。HDAC的作用非小细胞肺癌中需要的机制,以精确的理解,其抑制,应尽可能地具有针对性。在这里,作为一个原则研究证明,我们能够表现出与顺铂和entinostat,联合治疗可以成功地用于显著增强铂类为基础的治疗非小细胞肺癌细胞的反应。为了揭示的影响此组合治疗的细胞机制的光谱,未来蛋白质组学和表观遗传分析集中于Reptin / HDAC1相互作用可能有助于阐明信令这种复杂及其在NSCLC细胞抑制驱动路径的动态。
总之,我们的研究结果描述Reptin作为一种新型的稳压器,介导细胞增殖和人类非小细胞肺癌细胞的克隆生长离体和在活的有机体内。我们发现在肺癌患者高Reptin表达赋予预后不良,我们提出一个Reptin / HDAC1蛋白复合物,其药理中断敏感于非小细胞肺癌细胞对顺铂。这些结果揭示在非小细胞肺癌发生和可能有助于在早期疾病进展或复发和那些不太可能令人满意铂类为基础的化疗反应的风险较高,以确定病人。最后,我们的研究可能铺平了道路新的治疗策略HDAC1酶抑制剂与目前的标准治疗方案相结合。
补充材料
补充材料
请注意:补充材料不是由编辑部编辑,因为它已经由作者提供的上传。
补充方法:得分erj - 01637 - 2017 - _supplementary_methods
补充表S1。研究人群的基线特征。erj - 01637 - 2017 - _supplementary_table_s1
补充图S1。肿瘤分级和reptin的表达在NSCLC患者的预后值。erj - 01637 - 2017 - _supplementary_figure_s1
补充图S2。敲reptin的向下抑制人NSCLC细胞的克隆扩增和增殖离体。erj - 01637 - 2017 - _supplementary_figure_s2
补充图S3。血红蛋白和伊红染色及免疫组化分析显示转移性组织浸润。erj - 01637 - 2017 - _supplementary_figure_s3
补充图S4。在HEK-293细胞中,雷普汀与HDAC1在蛋白复合物中结合。erj - 01637 - 2017 - _supplementary_figure_s4
致谢
我们要感谢i Buchroth (Gerhard Domagk病理学研究所,大学中自得其乐,卓德国)求助与实验工作,和k·格拉泽(美国雅培公司,芝加哥,IL)和c·亚伯拉罕(部门的分子、细胞和发育生物学,科罗拉多大学博尔德分校,有限公司,美国),请提供我们与质粒含有HDAC1和人类Reptin shrna目标,分别。
脚注
这篇文章有提供补充材料www.qdcxjkg.com
利益冲突:无申报。
支持声明:我们的工作是慷慨否则克朗,费森尤斯基金会(第2015_A112)资助。我们。精益求精,明斯特,德国的集群 - Berdel的实验室是由德意志研究联合会,DFG EXC在运动1003个细胞的支持。本文资金的信息已交存Crossref资助者注册表。
- 收到2017年8月10日。
- 公认2018年5月19日。
- 版权©2018人队