摘要
慢性阻塞性肺疾病(COPD)的气道重塑部分源于吸烟引起的气道基底干/祖细胞(BCs)的改变。基于骨形态发生蛋白4(BMP4)影响发育中和成年小鼠肺上皮祖细胞功能的知识,我们假设BMP4信号可能调节与COPD相关的成年人气道BCs的生物学。
在mRNA和蛋白质水平上分析人气道上皮中的BMP4信号成分,并在没有/存在BMP4、BMP受体抑制剂和/或针对BMP受体和下游信号的小干扰RNA的情况下,使用BC扩增和气液界面模型评估BCs的分化。
数据表明,在香烟吸烟者中,BMP4在纤维化和中间未分化的细胞中上调,并且BMP4受体BMPR1A的表达富集在BCS中。BMP4诱导BCS获取吸烟相关的异常表型在体外由BMPR1A / SMAD信号介导的,其特征在于分化成正常粘膜上皮的能力下降,同时产生鳞状细胞癌。
夸大的BMP4信号通过诱导人类气道BCs的异常表型促进与吸烟相关的气道上皮重塑。靶向BMP4信号在气道BCs中可能是预防/治疗copd相关气道疾病的新靶点。
摘要
COPD发病机制是由BMP4重编程的人气道干/祖细胞介导的http://ow.ly/iWAI30nuWor
介绍
人气道上皮是一种伪分层柱状上皮,由基底干/祖细胞(BCs)、中间未分化细胞、纤毛细胞和分泌细胞组成[1-3.].BCS,驻留在气道基底膜上的小型立方体电池用作人气道上皮的茎/祖细胞,能够区分为物理屏障的纤毛和分泌细胞,宿主防御和粘液覆膜[1那2].中间细胞是bc来源的前体,可分化为纤毛细胞和分泌细胞[4.那5.].
吸烟是慢性阻塞性肺疾病(COPD)的主要病因,与气道上皮细胞形态的显著改变有关,包括BC和中间细胞增生、粘液细胞增生、鳞状细胞化生、纤毛细胞缺失和纤毛缩短[5.-13]. 越来越多的证据支持气道BCs的重新编程是吸烟引起气道上皮紊乱的早期发病机制的核心这一概念[14那15].与非吸烟者分离的bc相比,吸烟者分离的bc具有显著的转录组差异,包括与慢性阻塞性肺病遗传风险相关的基因重编程[16].吸烟通过抑制气道上皮细胞分化和紧密连接形成而使BCs的正常功能发生倾斜[12那17],部分通过BCS和其他细胞类型之间的串扰[5.那18].例如,BCs中表皮生长因子(EGF)受体(EGFR)的激活改变了BCs向鳞状和上皮-间充质转化(EMT)样表型的分化程序,这是吸烟诱导气道上皮变化的特征在活的有机体内[5.].
在评估健康非吸烟者、无症状吸烟者和COPD吸烟者的气道上皮时,我们观察到无症状吸烟者和COPD吸烟者的气道上皮中骨形态发生蛋白4(BMP4)表达上调。BMP4是一种分泌型转化生长因子(TGF)-β家族成员,通过调节早期中胚层的形成,控制发育中和成年小鼠肺的上皮祖细胞功能[19,气道分支形态发生[20.]促进近端气道分化[21]并诱导人类气道上皮细胞系中的EMT样变量[22,我们假设过量的BMP4信号可能在与吸烟和慢性阻塞性肺病相关的成人气道BCs生物学失调中发挥功能作用。数据表明,在吸烟者中,BMP4在纤毛细胞和中间未分化细胞中表达上调,BMP4受体BMPR1A在BCs中表达丰富。bmp4处理的正常BCs获得类似copd的“疲劳”表型,其特征是分化为正常粘液纤毛上皮的能力下降,同时产生鳞状上皮化生。这些作用是由BMPR1A/Smad信号介导的,抑制BMPR1A可恢复气道BCs的干/祖细胞电位,为吸烟诱导的肺疾病的治疗干预提供了一个可能的靶点。
方法
对非吸烟者、无症状吸烟者和慢性阻塞性肺疾病吸烟者进行支气管镜检查,获得人气道上皮和bc在体外公元前的主要文化。在体外采用原代BC和气液界面(ALI)培养,研究BMP4对BC分化的影响。气道上皮和基底细胞的基因表达在活的有机体内和在体外采用RNA测序/微阵列和TaqMan实时(定量)PCR (Applied Biosystems, Foster City, CA, USA)进行评估。免疫组化/免疫荧光染色检测气道上皮形态和蛋白定位。Western blot检测BMP4下游信号的磷酸化。
详情请参阅补充材料.
结果
BMP4在无症状和COPD吸烟者气道上皮中上调
为了确定吸烟是否与气道上皮中BMP信号的异常相关,我们通过RNA测序对非吸烟者、无症状吸烟者和慢性阻塞性肺疾病吸烟者大气道上皮和bc中BMP和BMP拮抗剂的基因表达进行了量化。的表达BMP5那BMP6.和BMP拮抗剂木钉那CHRD和CHRDL2在呼吸道上皮和Airway BCS(Airway BC)中非常低(每百万次数映射的每千碱基映射读数<0.2)。BMP2和BMP拮抗剂置那FSTL3和TWSG1在Airway BCS中高度表达,与完整的气道上皮中的表达相比,表达无症状吸烟者和COPD吸烟者(补充图S1a和b,及补充表如果).BMP7.在非吸烟者中表达,在无症状吸烟者和COPD吸烟者中轻度增加(补充图S1a和补充表年代我)。BMP4非吸烟者的表达相对较低,但在无症状吸烟者和COPD吸烟者的气道上皮中表达显著上调。无症状吸烟者和COPD吸烟者之间没有显著差异(图1A那补充图S2a和补充表si)。BMP4TaqMan定量PCR进一步证实了无症状吸烟者和COPD吸烟者气道上皮的上调(图1B.). 虽然两组之间没有显著性差异BMP4来自非助手,无症状吸烟者和COPD吸烟者的气道BCS的表达,无症状吸烟者和COPD吸烟者的亚组有更高BMP4表达比任何一个非闻人(补充图S2a).将气道上皮和气道BCS与无症状吸烟者进行比较,BMP4在总呼吸道上皮中高度表达(补充图S2a),建议上调BMP4主要表达于分化的气道上皮细胞。这些数据与在体外TaqMan数据BMP4在ALI模型中的BC差异期间表达增加(补充图开通).
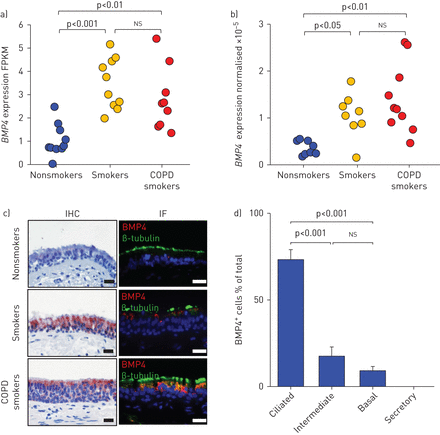
无症状吸烟者和慢性阻塞性肺病(COPD)吸烟者气道上皮中骨形态发生蛋白4 (BMP4)的上调FPKM:每千碱基的片段,每百万reads;包含IHC:免疫组织化学;如果:免疫荧光。a) RNA测序评估BMP4非吸烟者(n=10)、无症状吸烟者(n=10)和慢性阻塞性肺疾病吸烟者(n=9)的人气道上皮中表达。b) TaqMan定量PCR归一化BMP4非吸烟者(n=8)、无症状吸烟者(n=8)和慢性阻塞性肺疾病吸烟者(n=10)人气道上皮的基因表达。c) BMP4蛋白在人气道上皮中的表达:BMP4(红色)和纤毛细胞标志物β-微管蛋白(绿色)在非吸烟者、无症状吸烟者和COPD吸烟者气道上皮中的IHC染色和IF共定位。比例尺:20 μm。细胞核以4 ',6-二氨基-2-苯基吲哚(蓝色)染色。d) BMP4的分布(占气道上皮细胞总数的百分比)+无症状吸烟者(n=6)和COPD吸烟者(n=6)的纤毛细胞、中间细胞、基底细胞和分泌细胞的IHC染色(基于对12个不同样本共444个细胞的评估)。没有分泌细胞表达BMP4。ns:无情。
使用一个独特的微阵列数据集,从多个时间点(0、3、6和12个月)的人小气道上皮,我们观察到BMP4与非助手相比,在COPD吸烟者的所有时间点上调(补充图S3).当COPD吸烟者在第0个月初次支气管镜检查后戒烟时,他们的BMP4小气道上皮的表达在第3个月显著降低,在第6个月和第12个月接近非吸烟者的正常水平。然而,当COPD吸烟者停止吸烟并在第3个月后重新开始吸烟时,他们的BMP4小气道上皮中的表达再次增加(补充图S3).总之,除了大气道上皮RNA测序数据外,微阵列数据还确认BMP4在COPD吸烟者中,人小气道上皮的表达也上调,吸烟是一种“触发”BMP4气道上皮表达。
为了确定人气气道上皮,免疫组织化学和免疫荧光染色中BMP4蛋白的表达和定位是对人气道上皮活组织检查进行的。BMP4蛋白在非莫克者的正常气道上皮中几乎检测到,但在β-微管蛋白中显着增加+无症状吸烟者和COPD吸烟者正常气道上皮纤毛细胞(图1C.和补充图S4).在异常的呼吸道上皮上具有BC增生,粘液细胞增生和来自无症状吸烟者和COPD吸烟者的鳞状细胞,BMP4蛋白也在纤毛细胞中上调(图3A和补充图S4).除了在纤毛细胞中的表达外,BMP4还在BCS和中间细胞的子集中上调,来自无症状吸烟者和COPD吸烟者,但在分泌细胞中没有表达(图1D和补充图S4),其与Airway BCS中的RNA测序数据一致。BMP4的蜂窝分布+结果表明,BMP4主要诱导于纤毛细胞,少数中间细胞和BCs (图1D).而在上皮细胞下的间充质中未检测到BMP4蛋白(图1C.3,补充图S4).
BMP4抑制正常BC的增殖和分化
BCS是人类气道中的茎/祖细胞,并且能够自我更新和分化成正常纤毛和分泌细胞。为了确定BMP4对BC自我更新和增殖的影响,我们将BMP4应用于培养的正常NONMoker BCS,并确定BMP4显着降低了BC数和抑制BC增殖(补充图S5).
为了研究BMP4上调对正常BC分化的影响,我们使用ALI培养来评估人气道BC分化。结果显示,BMP4对正常BC细胞分化为粘液纤毛上皮具有广泛的抑制作用。与对照组相比,bmp4处理的BCs生成的气道上皮细胞纤毛细胞相关基因(包括动力蛋白)的表达显著降低dnai1.转录因子,FOXJ1,以及转录因子MCIDAS和RFX2.控制早期纤毛发生(图2A和补充图S6a).与基因表达数据一致,DNai1蛋白的免疫荧光染色表明BMP4降低了DNai1的比例+ALI培养中BCs衍生的纤毛细胞(图2B.,及补充图S6b和c).此外,BMP4显著抑制来自健康非吸烟者BCs的纤毛细胞的纤毛跳动(补充视频S1A和D.).
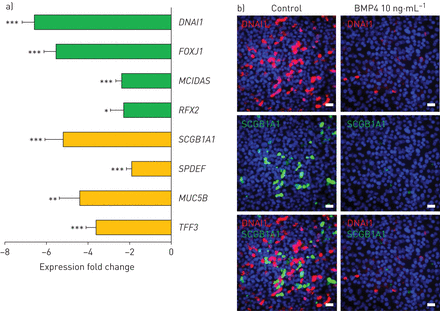
骨形态发生蛋白4 (BMP4)抑制正常气道基底干/祖细胞(BC)分化。阿里:气液界面。为了模拟在无症状吸烟者和慢性阻塞性肺疾病吸烟者气道上皮中观察到的BMP4上调的影响,BMP4 (10 ng·mL .-1),检测气道上皮分化相关基因和蛋白的表达水平。a)褶皱变化的TaqMan评估(日志)2, BMP4与调控)纤毛细胞分化相关基因mRNA表达(FOXJ1那dnai1.那MCIDAS和RFX2.;绿色条)和分泌细胞分化相关基因(SCGB1A1那SPDEF那muc5b.和TFF3;在BMP4治疗14天后,ALI培养的气道上皮细胞出现了明显的变化与未经处理的控制。n = 3或4。*: p < 0.05;* *: p < 0.01;* * *: p < 0.001。b) BMP4 (10 ng·mL) ALI培养28天后,气道上皮纤毛细胞标记物DNAI1(红色)和分泌细胞标记物SCGB1A1(绿色)免疫荧光顶部染色-1)从基石侧刺激与未经处理的控制。细胞核以4 ',6-二氨基-2-苯基吲哚(蓝色)染色。秤栏:20μm。
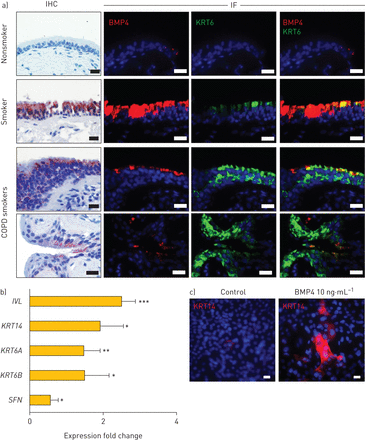
骨形态发生蛋白4 (BMP4)诱导向鳞状细胞分化。包含IHC:免疫组织化学;如果:免疫荧光;COPD:慢性阻塞性肺疾病;阿里:气液界面。a)从左到右:代表BMP4 IHC染色(阳性细胞红色)、BMP4 IF染色(红色)、鳞状细胞标志物KRT6 IF染色(绿色),BMP4(红色)和KRT6(绿色)IF染色重叠。这些染色在形态正常的非吸烟者、无症状吸烟者和形态异常的COPD吸烟者的人气道上皮上进行。细胞核以4 ',6-二氨基-2-苯基吲哚(蓝色)染色。比例尺:20 μm。每行IHC和IF染色活检图像均来自同一样本。 b) TaqMan assessment of fold change (log2,标准化以控制)在鳞状细胞相关基因的表达中(词汇附带习得那KRT14那KRT6A那KRT6B和SFN.)通过BMP4的Ali培养后14天后的气道上皮(10 ng·ml-1)从基石侧刺激与未经处理的控制。n = 3或4。*: p < 0.05;* *: p < 0.01;* * *: p < 0.001。c)在BMP4 (10 ng·mL) ALI培养14天后,气道上皮上的鳞状细胞标记物KRT14(红色)IF顶部染色-1)从基石侧刺激与未经处理的控制。细胞核以4 ',6-二氨基-2-苯基吲哚(蓝色)染色。秤栏:20μm。
同样,BMP4对分泌细胞的分化有抑制作用。分泌细胞相关基因SCGB1A1那SPDEF那muc5b.和TFF3BMP4刺激可显著下调其表达(图2A和补充图S6a).在Ali培养中的各个时间点处具有不同水平BMP4的BCS的刺激表明,BMP4的纤维和分泌细胞分化的抑制作用以浓度依赖的方式在ALI培养物中的分化期间持续(补充图S6a).BMP4刺激也抑制SCGB1A1蛋白(图2B.). TaqMan分析还显示纤毛细胞早期分化标记物的表达(MCIDAS那dnah5.和IFT172)和分泌细胞(SPDEF和TFF3)被压制(补充图S6d)通过BMP4刺激培养BCS。这些数据表明BMP4开始在早期阶段调制BCS中的纤毛和分泌细胞分化计划。
BMP4促进鳞状细胞分化
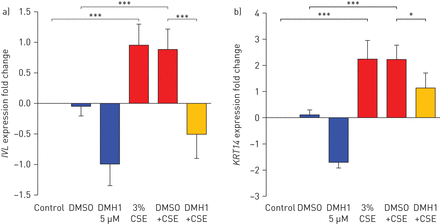
如前所述,无症状吸烟者和COPD吸烟者BMP4上调与气道上皮形态异常有关,包括鳞状上皮化生(图3A和补充图S4). 为了进一步证实这一观察结果,在非吸烟者、无症状吸烟者和COPD吸烟者的气道上皮中评估BMP4与中间/鳞状细胞标记物KRT6的免疫荧光联合染色。在正常形态的非吸烟者样本中,BMP4和KRT6的表达水平非常低。然而,在无症状吸烟者和COPD吸烟者的样本中,具有正常和鳞状化生形态,BMP4和KRT6的表达水平显著增加,BMP4的一小部分表达水平降低+细胞表达KRT6 (图3A). 基于BMP4上调似乎与鳞状化生相关的染色数据,我们假设BMP4将正常的BC分化转变为异常鳞状细胞。为了评估这一假设,我们在ALI分化培养和BC培养模型中用BMP4刺激人气道BCs。TaqMan数据显示BMP4可诱导一系列鳞状细胞标记物的上调,包括词汇附带习得那KRT14那KRT6A和KRT6B,在两个模型中(图3B.,及补充图S7a和e).BMP4诱导上调的SFN.在ALI培养中,但在BC培养中不存在(图3B.和补充图S7e).通过鳞状细胞标记物对来自BCS衍生或不含BMP4刺激的BCS的气道上皮的免疫荧光染色来加强Taqman数据。在衍生自BMP4处理的BCS的气道上皮中,对于鳞状细胞标记物KRT14和IVL,更多细胞为阳性,而在对照组中,IVL的百分比+和KRT14+细胞显着降低(图3C.和补充图S7B-D).BMP4不仅抑制纤毛细胞和分泌细胞的分化,而且以浓度依赖的方式诱导鳞状细胞分化(补充图S7a).
BMP4对完全分化的气道上皮的影响
此外,基底外侧用BMP4刺激完全分化的气道上皮也抑制纤毛细胞的表达(FOXJ1和MCIDAS)分泌细胞(SCGB1A1那SPDEF那muc5b.和TFF3)标记物,诱导鳞状细胞标记物(词汇附带习得那KRT14和KRT6A) (补充图S8).而根尖应用BMP4对纤毛细胞的表达无影响(FOXJ1)、分泌细胞(SCGB1A1那muc5b.和TFF3)及鳞状细胞(词汇附带习得和KRT14)标记,柔和地抑制了纤毛细胞标志物的表达dnai1.(补充图S9).
在气道BCs中富集的BMP I受体介导bmp4诱导的上皮重塑
BMP4通过两个受体家族的信号:BMP受体(BMPR1A,BMPR1B和BMPR2)和Activin受体(ACVR1,ACVR2A和ACVR2B)[23].使用RNA测序数据,我们检查了BMP4受体在人类气道上皮和BC样品中的表达。数据证明,BMPR1A表达略微下降,BMPR1B表达在来自无症状吸烟者和COPD吸烟者的气道上皮中增加,但不在气道BCS中。表达水平BMPR1B那Acvr2a.和ACVR2B.与BCs表达量相比,气道上皮表达量较高(补充图就是S1c和补充表年代II)。相比之下,BMPR1A那BMPR2和ACVR1BCS的表达水平高于完整的气道上皮,表明BMP4可以通过富含BCS中富集的这些受体调节BC功能。在非吸烟者,无症状吸烟者和COPD吸烟者中观察到BCS中BCP4受体富集的相同模式(图4A那补充图就是S1c和补充表年代II).免疫荧光染色进一步证实BMPR1A蛋白主要表达于KRT5的一个亚群中+BCS(图4B.).


骨形态发生蛋白(BMP)受体介导的BMP4诱导气道上皮重塑。FPKM:每百万映射读取的转录本每千碱基片段数;BC:基底干/祖细胞;二甲基亚砜;空气-液体界面。a) BMP4受体的RNA测序评估(BMPR1A那BMPR2和ACVR1)在人类气道上皮(n = 29)和气道BCS(n = 42)。显示有不同表型的个体BMP4受体的详细表达数据补充图就是S1c和补充表年代二,。b) BMPR1A(红色)和BC标记物KRT5(绿色)在正常人气道上皮中的代表性免疫荧光共定位。比例尺:20 μm。细胞核用4′,6-二氨基-2-苯基吲哚(蓝色)染色。c) TaqMan褶皱变化分析(对数2与气道BC分化相关的多种基因的表达(词汇附带习得和KRT14:鳞状细胞;FOXJ1和dnai1.:纤毛细胞;SCGB1A1和TFF.3:分泌细胞)。数据来源于ALI培养(第14天)中的气道上皮细胞和BMP4(10天) ng·mL-1)从基石侧刺激与在没有或存在BMP I型受体抑制剂DMH1 (5 μM)的情况下进行未经处理的控制。DMSO为阴性对照。n = 3。d) ALI培养14天后,气道上皮上有代表性的鳞状细胞标记物KRT14(红色)免疫荧光顶部染色。e) ALI培养28天后气道上皮纤毛细胞标记物DNAI1(红色)和分泌细胞标记物SCGB1A1(绿色)的代表性免疫荧光顶染色。细胞核以4 ',6-二氨基-2-苯基吲哚(蓝色)染色。天平条:20µm。f)鳞状细胞标记物表达的TaqMan评估词汇附带习得在BCS中的BCS(10ng·ml-1)刺激与对照组48例 h存在BMPR1A、BMPR2或ACVR1的小干扰RNA沉默。将数据标准化为未经处理的对照组(log2).n = 3或4。* *: p < 0.01;* * *: p < 0.001。
为了评估BMP受体是否介导BMP4诱导的气道上皮重塑,将BMP I型受体的选择性抑制剂DMH1应用于ALI培养,同时用BMP4刺激BCs。数据显示,DMH1逆转BMP4诱导的鳞状细胞标志物上调(词汇附带习得和KRT14),纤毛的下调(FOXJ1和dnai1.)分泌细胞(SCGB1A1和TFF3)标记(图4C.). 用鳞状细胞标记物KRT14、纤毛细胞标记物DNAI1和分泌细胞标记物SCGB1A1对气道上皮进行免疫荧光染色,证实DMH1可阻断BMP4诱导的气道上皮重塑(图4D以及(e)。此外,DMH1还能逆转BMP4抑制的纤毛细胞搏动(补充视频S1).
为了进一步评估介导BMP4诱导的BC异常分化的特异性受体,我们将BMPR1A、BMPR2和ACVR1小干扰rna (sirna)应用于BMP4处理的培养BC与控制。BMPR2 siRNA对培养的bc无影响,但BMPR1A siRNA显著降低bmp4诱导的鳞状细胞标志物上调词汇附带习得(图4f.).虽然不显著,ACVR1 siRNA倾向于抑制bmp4诱导的上调词汇附带习得.ALI分化培养中的其他证据证实,BMPR1A的沉默可以反转BMP4诱导的鳞状细胞鳞状(补充图S10A)抑制纤毛细胞分化(补充图S10B.). 通过TaqMan分析培养的BCs和ALI培养的气道上皮中的受体表达,验证了所有siRNA的有效性(补充图S11).
Smad信号介导bmp4诱导的鳞状上皮化生
为了评估BMP4下游Smad信号是否被人气道BCs上的BMP4激活,在ALI培养的BCs上进行磷酸化(p)-Smad1/5/8的Western blot分析。BMP4激活Smad1/5/8磷酸化 h、 激活持续,但在5和24时信号较弱 h(图5a).为了评估Smad信号是否介导bmp4诱导的鳞状上皮化生,在培养的bc中,siRNA沉默了Smad4,它将p-Smad1/5/8易位到细胞核(补充图S12). TaqMan分析显示bmp4诱导的鳞状细胞标志物表达(词汇附带习得和KRT14)减少(图5bc)提示Smad信号通路介导bmp4诱导人气道鳞状上皮化生。
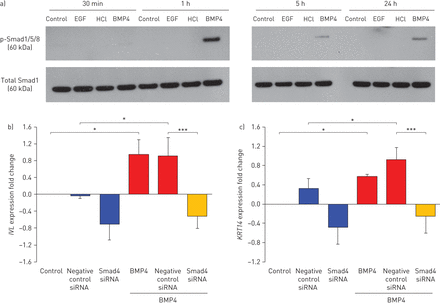
Smad信号介导的骨形态发生蛋白4(BMP4)诱导鳞状细胞分化。p-smad:磷酸化的smad;EGF:表皮生长因子;siRNA:小干扰RNA;BC:基底茎/祖细胞。a)Western印迹分析显示空气液体界面培养中的气道BCS的P-Smad1 / 5/8和总Smad1蛋白表达(第0天),有或没有BMP4(10ng·ml-1)刺激30 min、1、5和24 h。BMP4溶剂HCl和EGF (10 ng·mL-1;EGF不激活BMP4下游Smad信号[23)作为阴性对照。b, c)鳞状细胞标记物表达的TaqMan评估词汇附带习得(及c)KRT14在BCS中的BCS(10ng·ml-1)刺激与通过siRNA沉默Smad4,对48小时进行未处理的控制。使用阴性对照siRNA作为阴性对照,并将数据标准化为未处理的控制(日志2).n = 4。*: p < 0.05;* * *: p < 0.001。
BMP4信号传导的抑制反转香烟烟雾提取物和EGF诱导的异常表型
已知香烟烟雾提取物(CSE)可改变BC的分化,抑制粘液纤毛上皮的生成,并诱导鳞状细胞分化(图6和补充图S13) [12].为了评估BMP4信号是否参与CSE诱导的气道上皮重塑,我们将BMP I型受体抑制剂DMH1应用于CSE治疗的ALI培养中BC分化培养。基因表达数据显示,DMH1显著逆转了cse诱导的鳞状细胞标记物上调词汇附带习得(图6a) 和KRT14(图6b),纤毛细胞标记物下调(FOXJ1和dnai1.) (补充图S13A)和分泌细胞标记物(SCGB1A1和TFF3) (补充图S13B.).
DMH1抑制卷烟烟雾提取物(CSE)诱导的鳞状细胞分化。DMSO:二甲基磺砜;BC:基底茎/祖细胞。a,b)塔克曼对折叠变化的评估(日志2在鳞状细胞标记物的基因表达中词汇附带习得及(二)KRT14在空气-液体界面培养14天后,BCs来源的气道上皮细胞中。在CSE治疗组中,从基底外侧给予3%的CSE刺激与在没有或存在骨形态发生蛋白4 I型受体抑制剂DMH1的情况下进行未经处理的对照(5 μM)。DMSO为阴性对照。n = 4。*: p < 0.05;* * *: p < 0.001。
与CSE一样,我们之前发现EGF信号在BC分化到吸烟相关表型的重编程中发挥作用[5.那18].在这里,我们发现DMH1的BMP4信号传导的抑制可以恢复BC分化过程中的EGF诱导的异常表型,包括纤毛的下调(FOXJ1和dnai1.)分泌细胞(SCGB1A1)标记物,以及鳞状细胞标记物的上调(词汇附带习得和KRT14) (补充图S14a).然而,BMP4对Amphiregulin的表达没有影响(arc.;EGFR配体)(补充图S14B.),其上调与BC和粘液细胞增生有关[18].
讨论
慢性阻塞性肺病是一种与吸烟有关的慢性肺病,其特征是长期气流减少,并伴有慢性咳嗽、痰液增多和呼吸短促[24].COPD的早期发病机制与气道上皮的显著结构改变有关,包括BC和中间细胞增生、纤毛细胞数量减少、纤毛长度缩短、黏液过多、杯状细胞增生和鳞状上皮化生[5.-13].本研究鉴定了一种新的机制,该机制根据观察到的观察,调节无症状吸烟者和COPD吸烟者中的气道上皮重塑,即BMP4的表达在无症状吸烟者和COPD吸烟者的差异化气道上调。上调的BMP4与人类气道中的BC,茎/祖细胞,抑制正常的粘液分化并诱导鳞状细胞,IE。与COPD发病机制直接相关的过程(补充图S17)。
气道上皮的BMP4表达
BMP4是TGF-β超家族的一种配体,在许多组织中都有表达,在胚胎发生、胚胎发育和成年器官内环境稳定中发挥着重要作用[23].在发育中的胚胎小鼠肺中,BMP4在上皮末梢表达[25], BMP4在肺发育过程中内胚层的表达动态决定了肺芽的形态发生[20.和上皮近端-远端模式[21].在成年小鼠气道中,BMP4在间充质成纤维细胞样细胞中高表达,在部分腔上皮细胞中稳定弱表达。在损伤过程中,BMP4在间充质中表达减少,在上皮细胞中消失[26].此外,据报道,BMP4在小鼠肺内皮细胞中表达,受萘损伤抑制并通过博来霉素损伤诱导[27].
关于人类气道上皮中BMP4表达的信息有限。与我们的数据一致,在原代培养的人支气管上皮细胞中检测到BMP4 mRNA,并且在ALI培养中BMP4的表达增加[28,提示BMP4可能参与粘液纤毛分化。在本研究中,我们利用支气管镜下涂刷上皮细胞的RNA测序和对非吸烟者、无症状吸烟者和COPD吸烟者的人气道上皮活检的免疫染色,我们发现BMP4在正常气道上皮中表达非常低。相比之下,在无症状吸烟者和慢性阻塞性肺疾病吸烟者中,BMP4表达显著上调,主要在纤毛细胞和中间细胞以及BCs亚群中。与小鼠气道中BMP4的表达不同,无症状健康吸烟者和COPD吸烟者在人气道的间充质细胞和上皮分泌细胞中未检测到BMP4的表达。重要的是,BMP4+细胞不仅在吸烟者的正常气道上皮中观察到,但在无症状吸烟者和COPD吸烟者中的异常气道上皮均显着增加,该吸烟者也具有丰富的KRT6表达。BMP4和KRT6之间的表达相关性与鳞状区分相关[5.那18那29[表明BMP4与改造的气道上皮的产生相关。与BMP4的上调,其他BMPS(BMP2,BMP5和BMP6)的表达,BMP拮抗剂(NOG,FST,FSTL3,CHRD,CHRDL2和TWIG2)和BMP4受体(BMPR2,ACVR1和ACVR2A)没有变化从无症状吸烟者和Copd吸烟者获得的气道上皮。增加BMP7和BMPR1B表达水平,分别在无症状吸烟者和COPD吸烟者中降低BMPR1A表达水平,但变化较小。总之,这些数据表明BMP4是BMP途径中的主要成分,诱导无症状吸烟者和COPD吸烟者中的异常气道上皮。然而,吸烟如何增强BMP4表达的机制是未知的。据报道,人类气道上皮细胞中的慢性卷烟烟雾暴露唤起刺猬信号[30.]刺猬信号诱导BMP4的表达[31].如果是这样的话,吸烟者BMP4的升高可能是上皮细胞中Hedgehog信号的激活的结果。BCs是能够分化为粘液纤毛上皮的干/祖细胞,COPD吸烟者的BCs与非吸烟者的BCs有很大的不同[32那33]. 这些观察结果提出了另一个假设,IE。分化的气道上皮中增强的BMP4是由于在COPD吸烟者中改变了BCS的分化。
气道上皮中过度的BMP4诱导吸烟相关表型
在小鼠中,有条件敲除前前肠中的BMP4会导致气管丧失[34].在小鼠肺的形态发生过程中,内胚层的BMP4与远端间充质成纤维细胞生长因子10协同调控分支形态发生[20.].BMP4还控制肺部发展期间的内胚层近端图案化[21].在休息的成年小鼠气道上皮中,BMP4抑制BC增殖,同时在损伤后,BMP4信号传导被抑制,允许气道上皮增殖和修复[26].
在人类中,已显示BMP4激活气道上皮细胞中的EMT响应[22那35].BMP4对人类多能干细胞分化对肺细胞来说也是至关重要的[36那37].然而,BMP4对人类bc的影响尚不清楚。BCs是人类气道上皮中的干/祖细胞,COPD吸烟者的BCs不能生成正常的气道上皮[33,提示人类气道BCs在吸烟相关肺部疾病的发病机制中起核心作用。基于1)吸烟降低了气道上皮的连接屏障完整性,部分由EGF-EGFR信号通路介导[5.那17那182)我们观察到BMP4在吸烟者气道上皮中大量表达,我们假设上调的BMP4通过受损的气道上皮屏障连接,并与BC相互作用,将正常BC的自我更新和分化转向与吸烟相关的异常气道上皮。从我们的数据来看,BCs暴露于BMP4后,增殖率下降,无法分化为正常的粘液纤毛上皮,并被重新编程生成鳞状细胞。有趣的是,调控杯状细胞和球茎细胞分化的转录因子SPDEF的表达[38那39]也被BMP4抑制。这些数据与COPD吸烟者俱乐部细胞的减少一致[40],而与吸烟者杯状细胞增生的预期表型相反[7.那10,提示在人类气道上皮中调控吸烟相关表型的复杂机制。
人气道上皮细胞分化的BMP信号通路重编程
BMP4通过规范依赖依赖性和其他非Canonical信号通路的信号[23].在规范信号通路中,BMP4与受体结合,包括I型和II受体,以引发转导级联。通过BMP4磷酸化细胞内SMAD1 / 5/8激活受体[23]. 在Smad4的帮助下,磷酸化的Smad1/5/8易位到细胞核以调节基因表达。BMP4也能激活非常规途径,如丝裂原活化蛋白激酶(MAPK)、磷酸肌醇3激酶和p38[41-43].BMPR1A是BMP I型受体之一,对小鼠肺发育至关重要[44]. BMPR1A的缺失降低了远端胚胎肺的上皮细胞增殖,并导致小鼠肺的凋亡和异常形态发生[44].我们发现BMPR1A是介导bmp4诱导的吸烟相关异常表型的主要受体,其下游的Smad信号也介导了鳞状细胞分化。因为BMPR1A仅在bc的一个子集中表达在活的有机体内我们认为,BMP4诱导的吸烟相关表型(粘膜纤毛上皮减少和鳞状上皮化生增多)将位于气道上皮的“局部”区域。BMP4介导的气道上皮“局部改变”可能是吸烟相关疾病(包括COPD)的早期发病机制。
我们之前报道,CSE和EGF/双向调节- egfr信号改变了BC向吸烟相关病变的分化程序[5.那12那18],类似于BMP4诱导的表型。有趣的是,我们的数据显示阻断BMP受体逆转CSE / EGF诱导的吸烟相关病变,表明CSE / EGF和BMP4可能在BCS中共享一些常见的信号通路。MAPK信令可能是候选者,因为它是用于BMP4的EGF和非CANONICAL下游信令的下游信令路径[45].然而,BMP4没有改变Amphiregulin的表达,表明BMP4信号传导与EGF / Amphegulin信号传导不完全重叠。
总之,我们的研究发现了一种新的与吸烟和COPD相关的异常气道上皮重编程相关的bmp4依赖机制。调节BMP4或人气道BCs下游受体和信号级联可能是一种潜在的治疗方法,以治愈或预防吸烟诱导的气道疾病发病机制。
补充材料
补充材料
请注意:补充材料不是由编辑部编辑的,而是由作者提供的。
补充材料。erj - 02553 - 2017 - _supplement
补充视频S1。BMP4及其受体抑制对气道上皮纤毛搏动的影响在体外.ALI(第28天)的气道上皮来自正常的非吸烟者BC。BC暴露于BMP4 (10 ng·mL)-1)从基石侧刺激与在没有或存在BMP4 I型受体抑制剂DMH1(5μm)的情况下未经处理的控制。DMSO为阴性对照。A.控制。erj - 02553 - 2017 - _video_s1a
补充视频S1。B. DMSO。erj - 02553 - 2017 - _video_s1b
补充视频S1。C. dmh1 (5 μm)。erj - 02553 - 2017 - _video_s1c
补充视频S1。D. BMP4(10 ng·ml-1).erj - 02553 - 2017 - _video_s1d
补充视频S1。大肠BMP4 + DMSO溶液。erj - 02553 - 2017 - _video_s1e
补充视频S1。f . BMP4 + DMH1。erj - 02553 - 2017 - _video_s1f
确认
我们感谢R. Shaykhiev和I. Chao(遗传医学,威尔康奈尔医学院,纽约,纽约,美国)寻求实验设计和技术援助,以及N. Mohamed(遗传学医学部,威尔康奈尔医学院)对于编辑帮助。该研究中的生物样品是从总共100个受试者获得的;这些受试者中的两个也注册了螺旋形肌科的支气管镜检查。作者感谢螺旋参与者和参与的医生,调查人员和员工进行这项研究。有关研究的更多信息以及如何访问螺旋数据www.spiromics.org.我们想承认以下当前和前前调查人员的螺旋网站和阅读中心:尼尔E. Alexis,Wayne H. Anderson,Igor Barjaktarevic,R. Graham Barr,Eugene R. Bleecker,Richard C. Boucher,Russell P.Bowler,Elizabeth E.Caretta,Stephanie A. Christenson,Alejandro P.Comellas,Christopher B. Cooper,David J. Couper,Gerard J. Criner,Ronald G. Crystal,Jeffrey L. Curtis,Craire M. Doerschuk,Mark T.Dransfield,Christine M.Freeman,Meilan K. Han,Nadia N. Hansel,Annette T. Hastie,Eric A. Hoffman,Richert J. Kaner,Richard E. Kanner,Eric C. Kleerup,Jerry A. Krishnan,Lisa M.Lavange,斯蒂芬C. Lazarus,Fernando J. Martinez,Deborah A. Meyers,Wendy C. Moore,John D. Newell Jr,Laura Paulin,Stephen Peters,Cheryl Pirozzi,伊丽莎白C. Oelsner,Wanda K. O'Neal,VictorE. Ortega,Robert Paine III,Nirupama Putcha,Sanjeev Raman,Stephen I. Rennard,Donald P.Tashkin,J. Michael Wells,Robert A. Wise和Prescott G. Woodruff。来自全国心脏,肺和血液研究所的龙部门的项目官员是丽莎邮政和托马斯克罗克斯顿。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
利益冲突:W-L。左宗棠没有什么可透露的。
利益冲突:J. Yang没有什么可透露的。
利益冲突:Y. Strulovici-Barel无需披露。
利益冲突:J. Salit没有什么可透露的。
利益冲突:M. Rostami无需披露。
利益冲突:J.G.梅泽无所事事。
利益冲突:欧贝妮没有什么可透露的。
利益冲突:R.J.Kaner无需披露任何信息。
利益冲突:R.G.克里斯托没什么可透露的。
支持声明:这些研究得到HL107882、HL107882- s、HL1189541、HL094284和UL1 TR000457的部分支持。SPIROMICS支持由美国国立卫生研究院/ NHLBI合同(HHSN268200900013C、HHSN268200900014C HHSN268200900015C, HHSN268200900016C, HHSN268200900017C, HHSN268200900018C, HHSN268200900019C和HHSN268200900020C),并通过基础辅以贡献从阿斯利康COPD基金会,美国国立卫生研究院/ MedImmune公司,拜耳,Bellerophon Therapeutics、Boehringer Ingelheim Pharmaceuticals Inc.、Chiesi Farmaceutici SpA、Forest Research Institute Inc.、GlaxoSmithKline、Grifols Therapeutics Inc.、Ikaria Inc.、Nycomed GmbH、Takeda Pharmaceutical Co.、Novartis Pharmaceuticals Corp.、ProterixBio、Regeneron Pharmaceuticals Inc.、Sanofi和Sunovion。本文的资金信息已存入Crossref资助者注册表.
- 收到2017年12月8日。
- 公认2018年11月22日。
- 版权所有©2019