摘要
肺泡上皮-毛细血管屏障破坏是急性呼吸窘迫综合征(ARDS)的标志。ARDS中线粒体功能障碍对肺泡-毛细血管屏障损害的作用尚不清楚。间充质间质细胞源性细胞外囊泡(msc - ev)被认为是一种无细胞治疗ARDS的方法。线粒体转移对MSCs和msc - ev的治疗效果非常重要。在这里,我们研究了ARDS中线粒体功能障碍对肺泡上皮和内皮屏障损伤的贡献,以及msc - ev通过线粒体转移调节肺泡-毛细血管屏障完整性的能力。
用内毒素或ARDS患者的血浆样品刺激原代人小气道上皮细胞和肺微血管内皮细胞以及人精密肺切片(PCLSs),并用MSC-EVs处理,评估屏障特性和线粒体功能。脂多糖(LPS)-用MSC-EVs处理受伤小鼠,评估肺损伤程度和肺组织线粒体呼吸。
炎症刺激导致渗透性增加,并伴有原代细胞和pcls中明显的线粒体功能障碍。来自正常间充质干细胞的细胞外囊泡可以恢复屏障的完整性和正常水平的氧化磷酸化,而不含线粒体的细胞外囊泡制剂则无效。体内,线粒体的存在对于细胞外囊泡减少肺损伤和恢复肺组织线粒体呼吸的能力至关重要。
在ARDS环境中,msc - ev至少部分地通过恢复线粒体功能来改善肺泡-毛细血管屏障特性通过线粒体转移。
摘要
本研究表明线粒体功能障碍是ARDS发病的重要机制,线粒体转移对MSC细胞外小泡恢复肺泡-毛细血管屏障完整性的能力至关重要。https://bit.ly/2JuqoCY
介绍
急性呼吸窘迫综合征(ARDS)是一种危及生命的疾病,其特征是肺部广泛的不受控制的炎症。肺泡上皮-内皮屏障的损伤是ARDS病理生理学的一个关键方面,与水肿和弥漫性肺泡损伤的发展有关[1,2].
ARDS患者没有特定的药物治疗,这主要是由于不同亚群患者潜在病理生理机制的异质性[3.,4].最近,在四个随机临床试验中回顾性地确定了两种生物表型[5- - - - - -7]和一项观察性研究[8].这些表型具有不同的临床特征、生物标志物特征、临床结果,更重要的是,它们对干预(呼气末正压、液体管理策略、低剂量大环内酯治疗和辛伐他汀治疗)的反应不同。虽然这一领域仍在等待前瞻性研究证实这些发现,但在开发新的治疗方法时,考虑ARDS的表现型及其可能的反应将是重要的。
线粒体功能障碍及其在慢性阻塞性肺疾病(COPD)、哮喘、肺动脉高压或特发性肺纤维化等肺部疾病病理生理学中的潜在机制作用越来越受到重视[9- - - - - -11]临床观察数据表明,线粒体功能障碍与脓毒症危重患者的较高死亡率相关[12]多器官功能障碍综合征的幸存者在保留ATP和生物发生标记物的情况下线粒体功能更好[13]然而,迄今为止,线粒体功能障碍在ARDS发病机制中的作用尚未得到充分研究。
间充质基质细胞(MSCs)作为ARDS的一种潜在治疗方法正在积极研究中。越来越多的证据表明,MSCs主要通过分泌组发挥作用,分泌组的关键成分是细胞外小泡(EVs)[14,15].msc - ev被认为是ARDS的无细胞治疗[16,17].包括我们自己的研究在内的一些出版物此前曾报道msc - ev含有线粒体[18- - - - - -21].自从S皮et al。[22],证明从MSC转移的线粒体可恢复线粒体缺失的A549ρ°细胞的有氧呼吸,将MSC衍生的线粒体转移到肺上皮细胞可减少肺组织的炎症和损伤在活的有机体内急性肺损伤模型[18]和哮喘[23].我们已经证明,细胞外囊泡介导的线粒体转移对原代人巨噬细胞间充质干细胞调控至关重要[20]此外,我们最近发现,细胞外囊泡介导的线粒体转移是MSC促进人类远端肺上皮细胞修复能力所必需的[21].
在本研究中,我们探讨了线粒体功能障碍在ARDS肺泡上皮和内皮屏障损伤中的作用,以及MSC-EVs通过线粒体转移调节肺泡毛细血管屏障功能的能力。我们假设MSC-EVs的有益作用将取决于其缓解mi的能力软骨功能障碍和细胞外小泡在低和高炎症ARDS表型的微环境中具有不同的作用。这些研究的一些结果以前以摘要的形式报道[24].
方法
详细方法如所述补充方法.
细胞培养
人骨髓间充质基质细胞(MSCs)来自美国型培养收集(ATCC PCS-500-012)。这些细胞符合国际细胞治疗学会关于MSCs定义的所有标准[25].原代人肺微血管内皮细胞(HPMECs)和人小气道上皮细胞(HSAECs)来自PromoCell(海德堡,德国),并按照制造商说明书培养。
线粒体正常和功能失调的MSC产生细胞外囊泡
根据Z胡et al。[26]并根据国际细胞外囊泡学会指南进行了描述[27].为了获得线粒体功能不全的MSCs,用1µg·mL处理MSCs−1罗丹明- 6g (Sigma-Aldrich), 48h [20在培养液中加入50 ug·mL−1尿苷和2.5 mM丙酮酸钠(Sigma-Aldrich)支持糖酵解,然后用PBS洗涤,在无血清培养基中孵育48小时。从条件培养基(rhov - ev)中分离细胞外囊泡,处理方法与从正常间充质干细胞中分离的细胞外囊泡相同。
体内lps诱导肺损伤模型
根据1986年《英国动物(科学程序)法》,所有动物实验均由贝尔法斯特皇后大学动物福利伦理审查机构批准。使用C57BL/6雄性小鼠(8-12周龄;英国布莱克索恩Envigo RMS UK Ltd.,Blackthorn),用二甲苯嗪/氯胺酮麻醉小鼠,气管内注入LPS(2 mg/kg体重) 伤后h给予PBS、细胞外小泡或Rho-EVs通过尾静脉。伤后24小时,对小鼠实施安乐死,取支气管肺泡灌洗液(BALF)或肺进行分析或制备精确切肺切片(mPCLSs)。
ARDS患者的人精确肺切片和血浆样本
来自器官捐赠者的人肺(该器官不适合移植,且近亲同意用于研究)用于培养肺切片体外美国国家伦理审查服务局(National Review Ethics Service)对在英国获得的NHS血液和肺移植(REC 14/LO/0250)给予了伦理批准。人类PCLSs由美国霍奇金淋巴瘤等.[28].研究中使用的血浆样本来自HARP-2研究招募的患者[29].这些样本之前根据血浆炎症生物标志物的浓度分为两种表型[7].只有干预前获得的基线样本用于实验。10份具有各表型代表性的血浆样本在使用前用1%的完全培养基稀释至最终浓度为10%,健康志愿者的血浆作为对照。北爱尔兰研究伦理委员会办公室批准使用病人样本进行研究。
统计分析
使用Prism 6软件(GraphPad software, La Jolla, CA, USA)进行统计分析。至少进行3个重复的实验,将3个技术重复的平均值作为每个供体的单个数据点,并将这些数据点汇集在一起进行统计分析。合并数据以均数和标准差表示。对于参数化数据,采用学生检验或单因素方差分析事后使用Bonferroni选择的比较进行分析。对于非参数数据,使用Kruskal–Wallis检验事后使用Dunn选择的比较进行分析。统计显著性水平设定为p<0.05。
后果
MSC电动汽车特征描述
骨髓间充质干细胞(MSCs)血清饥饿48 h后,用超离心法分离细胞外囊泡。血清饥饿48 h后MSCs活力>90%。实验中使用的细胞外囊泡的剂量根据MSCs的最终细胞数量,生成条件培养基(10 μL / 1×106该剂量细胞外小泡的蛋白质和RNA浓度为98.32±34.6 μg和31.7±10.7 ng,分别为(n=3)。
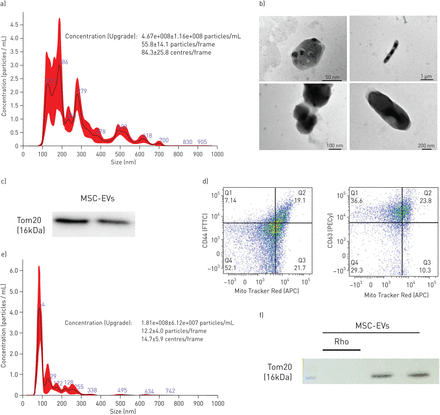
纳米颗粒追踪分析(NTA)显示了100-700的粒径范围 纳米由两种粒子组成,粒子大小为100–200 对应于外质体的nm,200-400 纳米,相当于微泡,相当大比例的较大颗粒的尺寸为500,700 nm及以上属于线粒体大小范围(图1一个)通过电子显微镜进行的精细结构分析一致显示存在外泌体、多泡体和含有线粒体的泡(图1 b).细胞外囊泡颗粒的Western blotting显示,线粒体标记物外膜转位酶20 (translocase of outer membrane 20, Tom20)蛋白(图1c).为了进一步证实细胞外囊泡制备中线粒体的存在,我们从用Mitotracker深红色FM预染色的MSCs生成的条件培养基中分离出细胞外囊泡,与anti-CD44或-CD63Ab偶联的小珠孵育,并通过流式细胞术分析,显示存在双阳性的msc来源的线粒体和msc - ev的表面标记物。定量,CD44+水户市+细胞外囊泡占总囊泡和CD63的11.3±7.9%+水户市+细胞外囊泡占细胞外囊泡总数的17.6±11.7% (图1 d).
msc来源的细胞外囊泡(msc - ev)的特征。a)用纳米颗粒跟踪分析msc - ev的特征(由五个独立测量生成的直方图)。b)具有代表性的透射电镜(TEM)图像显示:多泡体(左上,比例尺=50 nm)、外泌体(左下,比例尺=100 nm)、线粒体样结构(右上,比例尺=1µm)和线粒体样结构(右下,比例尺= 200 nm)。图像采用TEM显微镜(JEOL, JEM 1400Plus, Japan)拍摄。c)免疫印迹法检测TOM20在msc - ev和msc - ev - rho裂解物中的蛋白表达水平。所有车道的蛋白质总量都是一样的。d)结合4µm珠的msc -EV的代表性流式细胞术图显示CD44和MitoTracker深红色FM双阳性的EV群体(19.1%)和CD63和MitoTracker深红色FM双阳性的EV群体(23.8%)。e)从罗丹明- 6g预处理MSC分离的ev的纳米颗粒跟踪分析的代表性直方图(直方图由5个独立测量产生)。f)免疫印迹法检测TOM20在rhoeevs裂解物中的蛋白表达水平。所有泳道的总蛋白质含量与c泳道相同。
在之前的研究中,我们使用罗丹明- 6g诱导MSC线粒体功能的特异性不可逆抑制[19].我mportantly, this treatment does not affect MSC viability or capacity to secrete paracrine factors. Here we also tested if Rhodamine-6G treatment would affect MSC-EV particle size distribution. NTA demonstrated that the size distribution profile and concentration of Rho-EVs was comparable to the profile of extracellular vesicles isolated from control MSCs except that particles larger than 400 nm, corresponding to the size range of mitochondria, were absent (图1 e).与此一致的是,Rho-EVs的Western blot分析未检测到TOM20蛋白(图1 f).在随后的所有实验中都使用了rho - ev,以研究线粒体对整体细胞外囊泡效应的贡献。
细胞外囊泡线粒体容易被HSAECs和HPMECs内化,并恢复被LPS破坏的屏障完整性
通过Nikon Eclipse Ti-E显微镜观察肺细胞从MSC EV摄取的线粒体。EV从经Mitotracker深红FM预处理的MSC中分离,并与经Mitotracker绿预染色的HSAEC或HPMEC共培养,以观察内源性线粒体(图2a- c)。利用尼康6D Eclipse软件对多个z堆栈进行三维重建,并对图像进行反褶积。在24小时,有证据表明msc来源的线粒体被上皮细胞和内皮细胞摄取(补充视频).
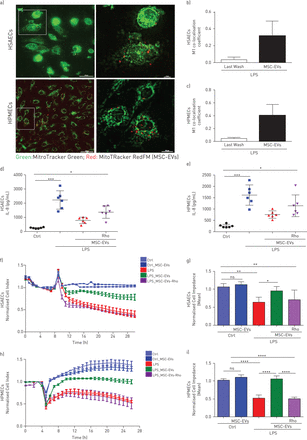
msc - ev通过功能性线粒体的转移提高人肺原代上皮和内皮细胞屏障的完整性。a)人小气道上皮细胞(HSAECs)和人肺微血管内皮细胞(HPMECs) msc - ev线粒体内化的代表性活体图像(标尺=50 nm(左图)和10 nm(右图))。b和c)在HSAECs (b)和HPMECs (c)中M1系数共定位。使用尼康6D Eclipse Ti-E倒置显微镜,Okolab触摸温度单位和CO拍摄图像2环境室(尼康仪器,日本)(40×干式超级平面荧光ELWD物镜,0.6 NA)。数据均值±sd共10幅图像。d和e)HSAECs(d)和HPMECs(e)分泌白细胞介素(IL)-8的水平。f)暴露于脂多糖(LPS)并经MSC EVs或MSC EVs Rho处理的HSAECs的代表性实时阻抗分析。数据为XCelligence RTCA测量的HSAECs的细胞阻抗。平均值±sd(n=3)。h)暴露于LPS并经MSC EVs或MSC EVs Rho处理的HPMEC的代表性实时阻抗分析。i)XCelligence RTCA测量的HPMEC的细胞阻抗。数据为平均值±sd(n=3)。ns:无显著性;*:p<0.05;***:p<0.01;***:p<0.001;***:p<0.0001。Kruskal-Wallis试验事后邓恩试验(d和e)。单因素方差分析事后Bonferroni试验(g和i)。
正如所料,在HSAEC和HPMEC中,LPS刺激导致白细胞介素(IL)-8的产生显著上调。这一效应被两种类型的细胞外小泡显著逆转(图2de),表明线粒体转移在细胞外囊泡对IL-8产生的影响中不是关键。
LPS刺激还导致上皮和内皮细胞屏障的显著破坏,这可以从细胞单层电阻抗的改变中看出(图2f我)。在两种细胞类型中,对照msc - ev能够恢复屏障的完整性,而rho - ev则没有作用。
LPS诱导HSAECs和HPMECs的线粒体功能障碍,其被细胞外小泡线粒体所缓解
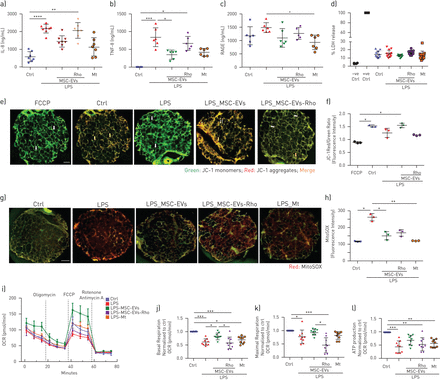
LPS诱导两种细胞的线粒体膜电位显著降低(以红色和绿色JC-1染料荧光之间的比率测量)(图3一- c)。同时线粒体活性氧(mtROS)显著上调,(图3 d-f),共同表现出lps诱导的线粒体功能障碍。
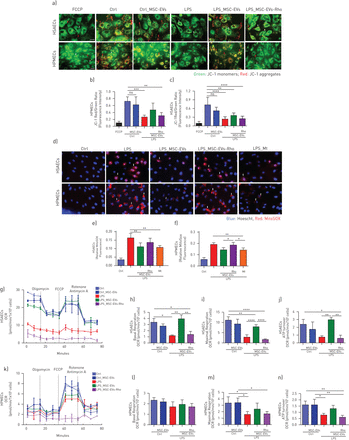
脂多糖(LPS)诱导人原代肺上皮细胞和内皮细胞的线粒体功能障碍,通过在MSC EVs中转移功能性线粒体而减轻。a)JC-1染料荧光的代表性活体图像作为人小气道上皮细胞(HSAEC)线粒体膜电位的指标和人肺微血管内皮细胞(HPMECs)暴露于LPS并用MSC-EVs或MSC-EVs-Rho处理24小时 H白色箭头指向去极化线粒体膜(JC-1单体)区域,红色箭头指向极化线粒体膜(JC-1聚集体)。FCCP被用作线粒体去极化的对照。使用尼康6D Eclipse Ti-E倒置显微镜(比例尺=100)拍摄图像 µm)。b和c)HSAECs(b)和HPMECs(c)中红/绿荧光强度比的定量。数据表示为平均值±sdd)暴露于LPS并用MSC EVs或MSC EVs Rho治疗24小时后,用MitoSOX检测到的HSAECs和HPMECs线粒体超氧化物生成的代表性实时图像 h或用米托坦波(Mt)预处理,4 h刺激前。白色箭头显示HSAECs和HPMECs中线粒体ROS的形成。使用尼康6D Eclipse Ti-E倒置显微镜(比例尺=100)拍摄图像 µm)。e和f)HSAECs(e)和HPMECs(f)中MitoSOX的定量荧光强度。数据表示为平均值±sd10幅图像。g)代表性海马有丝分裂应激试验显示HSAECs中的耗氧率(OCR)。h-j)呼吸参数的计算值:基础呼吸(h)、最大呼吸(i)和ATP生成(j),(n=3).k)代表性海马有丝分裂应激试验显示HPMECs中的OCR。l–n)呼吸参数的计算值:基础呼吸(l)、最大呼吸(m)和ATP生成(n),(n=3)。数据以平均值表示±sd.ns:不显著;*:p<0.05;***:p<0.01;***:p<0.001;***:p<0.0001。Kruskal-Wallis试验事后邓恩检验(c, d, f和g)。单因素方差分析事后Bonferroni检验(h-j和l-n)。
EV能够在两种细胞类型中部分恢复这些参数,这种效应取决于线粒体的存在,因为Rho EV没有任何作用(图3一- f)。
通过测量细胞耗氧率来评估线粒体呼吸,进一步证实了这些发现,LPS显著降低了两种细胞类型的基础和最大线粒体呼吸和ATP转换,这些影响被控制的细胞外囊泡部分逆转,但不包括Rho-EVs (图3 g- n)。
msc - ev逆转lps诱导的HSAECS和HPMECs线粒体质量控制机制的变化
为了评估对线粒体内稳态的影响,我们评估了上皮细胞和内皮细胞中的线粒体吞噬和线粒体生物生成水平。通过量化线粒体(线粒体追踪器红色)与自噬体(LC3-II溶酶体标记,绿色)的共定位来评估线粒体吞噬使用共焦显微镜。LPS刺激诱导两种细胞中的有丝分裂吞噬水平显著上调,MSC EVs恢复到正常水平(图4一- c)。
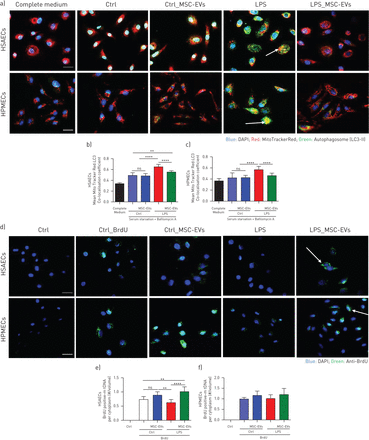
炎症环境扰乱人原发性肺上皮和内皮细胞的线粒体稳态,msc - ev可缓解这一情况。a)不同实验条件下人类小气道上皮细胞(HSAECs)和人类肺微血管内皮细胞(HPMECs)的代表性共聚焦显微镜显示细胞核(DAPI)、线粒体(红色)和LC3-II(绿色)。箭头表示共定位,表示线粒体并入自噬体。采用徕卡SP8共聚焦显微镜,40×油浸物镜(比例尺=50µm)。b和c)在HSAECs (b)和HPMECs (c)中,通过线粒体特异性红色荧光与绿色自噬体标记物LC3-II共定位评估线粒体自噬。数据为平均值±sd十帧图像。d)具有代表性的共聚焦显微镜显示HSAECs和HPMECs细胞中线粒体的生物发生。箭头指向brdu阳性mtDNA的细胞质积累。采用徕卡SP8共聚焦显微镜,40×油浸物镜(比例尺=50µm)。e和f) HSAECs (e)和HPMECs (f)中brdu阳性mtDNA /细胞质体积的定量比值。数据为平均值±sd十帧图像。ns:不显著;* *: p < 0.01;* * * *: p < 0.0001。克鲁斯卡尔-沃利斯测试事后邓恩测验。
利用BrdU掺入法测定mtDNA复制水平来评估线粒体生物发生[30].与线粒体自噬相反,LPS显著抑制了HSAECS中的线粒体生物发生水平,msc - ev处理导致mtDNA复制恢复正常水平(图4 d以及(e)。在HPMEC中,虽然生物发生水平的变化遵循相同的趋势,但影响没有达到统计学意义(图4 d和f)。
msc - ev下调lps诱导的炎症反应并减轻人pcls线粒体功能障碍
接下来,我们在生理相关的人肺组织模型中研究了细胞外囊泡对lps诱导的线粒体功能障碍的影响。人精确切肺切片(pcls)暴露于LPS和细胞外囊泡处理24 h。共聚焦显微镜观察到线粒体转移到pcls (补充图S1).LPS刺激导致PCLS条件培养液中IL-8和肿瘤坏死因子(TNF)-α分泌水平显著上调,对照组细胞外囊泡可显著缓解这一水平,但Rho-EVs (图5aLPS还诱导晚期糖基化终产物受体(RAGE)水平显著上调,提示肺泡上皮损伤[30].添加对照组而不添加rho - ev可使RAGE水平恢复至基线水平(图5c).重要的是,LPS刺激并没有引起细胞死亡(通过LDH释放测量),这表明观察到的细胞因子分泌的变化与坏死细胞的被动泄漏无关(图5d).加入一种特异性mtROS抑制剂MitoTempo,可导致TNF-α、IL-8和RAGE分泌的下调,这是控制细胞外囊泡的作用,表明抑制mtROS可能是细胞外囊泡线粒体转移的抗炎作用的部分原因(图5a- d)。
MSC-EVs通过线粒体转移抑制人肺组织炎症反应并恢复线粒体功能体外人精确切肺切片(PCLSs)。a)暴露于LPS 24小时后PCLSs上清中白细胞介素(IL)-8的分泌水平(n=6 - 8,3个供体)。b)暴露于LPS 24小时后PCLSs上清中肿瘤坏死因子(TNF)-α分泌水平(n=6 - 8,3个供体)。c)暴露于LPS 24小时后PCLSs上清中晚期糖基化终产物受体(RAGE)分泌水平(n=6 - 8,3个供体)。d)通过乳酸脱氢酶(LDH)释放量测定pcls活力(n=8 - 10,3个献血者)。e) JC-1荧光在pcls中的代表性活体图像作为线粒体膜电位的指标。FCCP作为全线粒体膜去极化的阳性对照。白色箭头指向肺组织中线粒体膜电位低的区域(JC-1单体的聚集),橙色箭头指向正常极化的区域(JC-1聚集体的聚集)。使用尼康6D Eclipse Ti-E倒置显微镜(比例尺= 1mm)拍摄。f)用ImageJ软件定量分析PCLSs中红色与绿色JC-1荧光比值。 Data represented as mean±sd10帧图像中。g)在PCLSs中用MitoSOX检测到的线粒体超氧化物生成的代表性图像。这些图像是使用尼康6D Eclipse Ti-E倒置显微镜(比例尺=1)拍摄的 mm).h)通过ImageJ软件分析定量荧光强度。数据表示为平均值±sdi)代表性海马有丝分裂应激试验,显示PCLSs中的耗氧率(OCR)。j–l)计算值标准化,以控制PCLSs的呼吸参数:基础呼吸(j)、最大呼吸(k)和ATP生成(l)。(n=3个独立实验,3个供体)。数据表示为平均值±sd.ns:不显著;*:p<0.05;***:p<0.01;***:p<0.001;***:p<0.0001。Kruskal-Wallis试验事后邓恩测验。
LPS处理PCLSs 24小时后,线粒体膜电位显著去极化,mtROS上调。这两个终点均可通过对照组细胞外囊泡恢复,但不包括rhov - evs (图5e- h)。一致地,PCLS耗氧率分析显示lps诱导的基础和最大线粒体呼吸和ATP转换的抑制。添加对照组而不添加rho - ev能够恢复线粒体呼吸(图5i–l).用MitoTempo治疗对PCLSs线粒体呼吸的恢复没有显著影响,这表明单独抑制mtROS不足以缓解LPS诱导的肺组织水平线粒体功能障碍。
当ARDS患者血浆样本刺激HSAECS和HPMECs时,MSC-EVs调节屏障特性和炎症反应;低炎症的ARDS环境对细胞外囊泡治疗更敏感
为了更密切地模拟人类ARDS环境,并研究不同ARDS表型的细胞外囊泡作用,我们将HSAECs和HPMECs在10%以前分为低或高炎症表型的ARDS患者血浆样本中培养24小时[7].
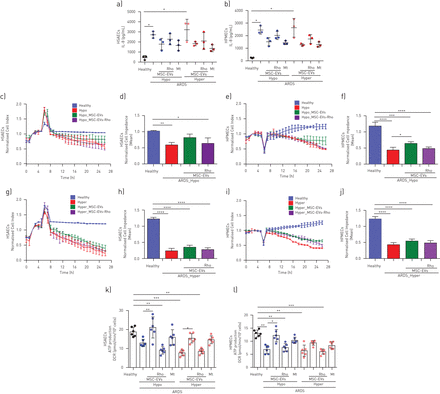
暴露于这两种类型的血浆样品引起上皮细胞和内皮细胞中IL-8分泌的相应增加。添加对照组和Rho EV可相对减少ARDS血浆刺激的增加(图6b).添加MitoTempo可导致两种细胞类型和两种ARDS表型中IL-8的分泌受到强烈抑制。
msc - ev调节炎症反应,部分恢复上皮和内皮屏障特性通过ARDS环境中的线粒体转移在体外a、b)24小时时人小气道上皮细胞(HSAECs)(a)和人肺微血管内皮细胞(HPMECs)(b)分泌白细胞介素(IL)-8的水平 两种类型的急性呼吸窘迫综合征(ARDS)血浆中的h(n=3)。c) 暴露于低炎症ARDS血浆的HSAEC的代表性实时阻抗分析。d) HSAECs中XCelligence RTCA测量的电池阻抗分析(n=3)。e) 暴露于低炎症ARDS血浆的HPMEC的代表性实时阻抗。f) HPMECs中XCelligence RTCA测量的电池阻抗分析(n=3)。g) 暴露于高炎症ARDS血浆的HSAEC的代表性实时阻抗。h) HSAECs中XCelligence RTCA测量的电池阻抗分析(n=3)。i) 暴露于高炎症ARDS血浆样本的HPMEC的代表性实时阻抗分析。j) HPMECs中XCelligence RTCA测量的电池阻抗分析(n=3)。k和l)。两种ARDS微环境中HSAECs(k)和HPMECs(l)线粒体ATP生成的计算值(n=3)。数据表示为平均值±sd*:p<0.05;***:p<0.01;***:p<0.001;***:p<0.0001。Kruskal-Wallis试验事后邓恩测验。
屏障功能评估表明,暴露于每种类型的ARDS血浆可导致HSAECs和HPMECs屏障完整性的类似破坏(图6 c- j)。只有在低炎症血浆的情况下,细胞外囊泡才能部分恢复,Rho-EVs没有作用(图6 c- f)。
暴露于两种ARDS血浆显著损害HSAECs和HPMECs的线粒体ATP转换(图6 k和(l)。在两种细胞类型中,MSC EVs在存在低炎症血浆时能够显著减弱线粒体呼吸缺陷,而在高炎症血浆中,细胞外小泡效应是部分或不存在的。Rho EVs对线粒体呼吸没有任何影响。使用MitoTempo治疗无法显著提高线粒体ATP周转率(图6 k和l)。
Angiopoietin-2
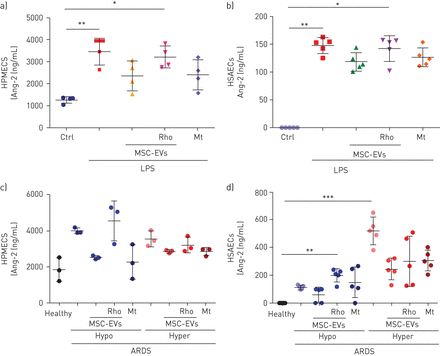
Angiopoietin-2 (Ang-2)是公认的肺和全身血管损伤的介质和生物标志物[31- - - - - -33].血浆Ang-2浓度对ARDS的发展具有重要的预测价值,可有力预测ARDS成人和儿童的不良临床结局[34,35].重要的是,6小时时血浆Ang-2浓度在统计学上显著降低 START研究(ARDS中MSC的随机2a期安全性试验)报告MSC输注后h[36].因此,在我们的模型中,我们对细胞外囊泡对内皮细胞和上皮细胞Ang-2分泌水平的影响感兴趣。LPS刺激导致HPMECs和SAECs的Ang-2分泌显著上调(值得注意的是,SAECs的Ang-2分泌水平几乎是HPMECs的10倍),这可以通过控制细胞外囊泡和MitoTempo部分恢复,但不包括rhoo - evs (图7ab)一致地,ARDS血浆刺激也引起两种细胞类型的Ang-2分泌增加。在HPMECs中,对照组的细胞外囊泡(但不包括rhov - ev)在低炎症血浆存在时能够部分降低其水平,而在高炎症血浆存在时没有检测到影响(图7c).在SAECs中,对照组的细胞外囊泡(而不是rhoo - ev)能够在低炎症血浆存在的情况下部分恢复Ang-2水平,而对照组和rhoo - ev的加入可在高炎症血浆存在的情况下相对降低Ang-2浓度(图7d).
MSC EVs下调人原代肺上皮细胞和内皮细胞的血管内皮素(Ang)-2分泌水平。a) 24小时时人肺微血管内皮细胞(HPMEC)上清液中Ang-2分泌水平 暴露于LPS(n=4)并用PBS、MSC-EVs、MSC-EVs-Rho或Mitotempo(Mt)处理后h。b) 24小时时人小气道上皮细胞(HSAECs)上清液中Ang-2分泌水平 暴露于LPS(n=5)并用PBS、MSC-EVs、MSC-EVs-Rho或Mitotempo(Mt)处理后h。c) 24小时HPMECs上清液中Ang-2分泌水平 h在两种类型的急性呼吸窘迫综合征(ARDS)血浆(n=3)中,并用PBS、MSC-EVs、MSC-EVs-Rho或米托坦波(Mt)治疗。d) 24小时时HSAECs上清液中Ang-2分泌水平 h在两种类型的ARDS血浆(n=5)中,并用PBS、MSC-EVs、MSC-EVs-Rho或Mitotempo(Mt)治疗。数据表示为平均值±sd.*: p < 0.05;* *: p < 0.01;* * *: p < 0.001。克鲁斯卡尔-沃利斯测试事后邓恩测验。
MSC-EVs减轻LPS肺损伤小鼠肺组织线粒体呼吸
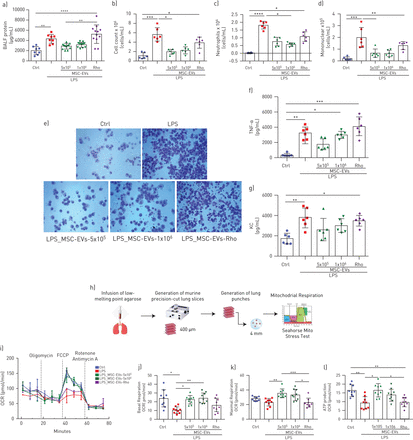
鉴于上述结果,我们假设细胞外囊泡介导的线粒体转移可以改善线粒体功能障碍在活的有机体内肺损伤模型。比较两种不同细胞外囊泡剂量的效果:5×10产生的细胞外囊泡5和1×106msc。对照组两种剂量的细胞外囊泡均可降低lps刺激下BALF总蛋白、总细胞数和差异细胞数的增加,(图8a- d)。rho - ev的管理(生成于1×106MSCs)没有影响。在LPS损伤组中,BALF的细胞自旋制剂显示肺泡腔大量炎性细胞募集,主要由中性粒细胞组成,通过给予细胞外小泡而不是Rho-EV而减少(图8e).
MSC-EVs减轻LPS诱导的肺损伤并恢复小鼠肺组织线粒体呼吸在活的有机体内. a) 支气管肺泡灌洗液(BALF)样本中的总蛋白质浓度(每组8-10只小鼠)。b–d)BALF样本中的总细胞计数(b)、绝对中性粒细胞计数(c)和绝对单核细胞计数(d)(每组n=6只小鼠)。e) BALF cytospin制剂的代表性图像显示炎症细胞招募到空气空间,使用徕卡表观荧光DM5500显微镜(原始放大倍数,x20)拍摄。f) BALF肿瘤坏死因子α(TNF-α)水平。g) 角质形成细胞衍生的趋化因子(KC,白细胞介素-8的小鼠类似物)的BALF水平。h) 生成小鼠精确切割肺切片(MPCLS)的示意图。i) 代表性海马有丝分裂应激试验分析显示MPCLS中的耗氧率(OCR)。j–l)MPCLS的基础呼吸(j)、最大呼吸(k)和ATP生成(l)的计算值。数据表示为平均值±sd*:p<0.05;***:p<0.01;***:p<0.001;***:p<0.0001。Kruskal-Wallis试验事后邓恩测验。
细胞外囊泡而非Rho-EV治疗显示出代表性炎性细胞因子(TNF-α和角质形成细胞衍生的趋化因子)的BALF水平降低的趋势,但效果未达到统计学意义(图8f和g)。
为了评估线粒体功能,我们使用PCLSs测量了该模型小鼠肺组织中的线粒体呼吸(图8h)LPS诱导的损伤导致基础和最大线粒体呼吸以及线粒体ATP转换显著下调。全身给药两种剂量的对照细胞外囊泡,但不给Rho-EVs,可恢复线粒体呼吸和ATP生成(图8i–l)。
讨论
这项研究的主要发现如下。1) msc - ev含有线粒体,容易被受体细胞内化并插入内源性线粒体网络(图1和2).2)脂多糖诱导炎症反应,增加上皮和内皮屏障通透性,并伴有明显的线粒体功能障碍。msc - ev中线粒体的转移不仅对线粒体功能的缓解至关重要,而且对两种细胞类型的屏障完整性的恢复也至关重要,表明线粒体在维持肺泡-毛细血管屏障功能中发挥重要作用(图2和3.).3)在两种细胞类型中,msc - ev均能恢复正常水平的线粒体自噬和生物发生,而这两种细胞均受到LPS (图4).4) MSC-EVs线粒体转移可在肺组织水平减轻LPS抑制的线粒体功能障碍,恢复LPS抑制的线粒体呼吸(图5).5)ARDS血浆刺激可显著损害上皮细胞和内皮细胞的屏障完整性和线粒体功能,但MSC-EV的治疗效果仅在存在低炎症表型患者血浆的情况下才能观察到(图6和7).6)MSC EVs对大鼠的治疗作用在活的有机体内lps诱导的肺损伤模型依赖于线粒体的存在,EV线粒体转移可改善肺组织的线粒体呼吸在活的有机体内(图8).
MSC细胞外小泡曾经被质疑其存在的真实性,现在作为全细胞治疗的有效替代品进入临床领域[16,37,38].我大满贯et al。[18]是第一个报道msc - ev可以作为载体转移宿主细胞的功能性线粒体,恢复炎症微环境损害的生物能。随后,Phinneyet al。[19,表明MSCs由于未完成的自噬,活跃地向细胞外囊泡中分泌线粒体。我们之前报道过,线粒体转移对巨噬细胞间充质干细胞调节非常重要,导致巨噬细胞代谢重编程向抗炎表型方向发展,也促进人小气道上皮细胞的伤口愈合能力[20,21,39]值得注意的是,最近的出版物报道单核细胞也能够在细胞外小泡中分泌线粒体,并且线粒体应激有助于其分泌体的炎症特性[40].在这里,我们通过一系列技术提供msc - ev中线粒体的特征(图1).我们证明存在大于400的囊泡 nm不负责凋亡小体,具有线粒体的超微结构特征,存在MSC线粒体和MSC-EV表面标记物CD44和CD63双阳性的小泡,以及细胞外小泡中线粒体外膜蛋白的高水平表达(图1a-d)重要的是,我们证明,经罗丹明-6G预处理后,线粒体出现功能障碍的MSC[20]也分泌细胞外小泡,其浓度和大小分布与正常MSC分泌的细胞外小泡相似,但没有400以上的小泡除外 纳米大小,与线粒体相对应(图1 e).
越来越多的证据表明,线粒体功能的改变在多种形式的危重病的发生中起着重要作用[13,41,42]然而,关于线粒体功能障碍对ARDS肺泡-毛细血管屏障破坏的作用的数据是有限的大满贯et al。[18]是第一个认为MSC治疗肺损伤的作用是通过恢复线粒体生物能和肺泡上皮细胞ATP产生介导的。同一小组最近发表的一篇论文确定了线粒体功能障碍和微血管通透性亢进之间的机制联系在活的有机体内[43].在这里,我们证明LPS刺激会显著损害人类小气道上皮和微血管内皮细胞的屏障完整性,并伴有严重的线粒体功能障碍和线粒体生物发生和线粒体自噬障碍(图3和4).外源线粒体的捐赠导致两种细胞类型的正常线粒体呼吸恢复到正常水平,并且对于细胞外小泡对上皮和内皮屏障功能恢复的治疗效果至关重要。
与这些发现一致,我们观察到LPS刺激会损害人PCLSs中的线粒体膜电位,增加mtROS的产生并抑制线粒体呼吸,并且MSC EVs的线粒体转移对于缓解线粒体功能障碍和恢复该模型中的线粒体呼吸至关重要(图5).
mtROS的过度生产被认为是线粒体功能障碍发展的关键因素,导致线粒体膜完整性的破坏,ΔΨ的耗散,并进一步损害细胞[44- - - - - -46].研究以抗氧化剂为基础的治疗方法对包括危重症在内的多种疾病的临床疗效[47- - - - - -49]有趣的是,用线粒体ROS抑制剂MitoTempo治疗足以逆转炎症反应,但不能恢复线粒体呼吸(图5和6),提示msc - ev效应不能完全用抑制mtROS的产生来解释。我们可以假设,通过细胞外囊泡线粒体转移观察到的线粒体生物发生上调可能对减轻脂多糖诱导的线粒体功能障碍很重要。
在包括HARP-2在内的四项大型临床试验中,回顾性地确定了ARDS的两种生物学亚型(低炎症型和高炎症型)[7]有趣的是,随后的一项对210例脓毒症相关ARDS患者的观察队列进行了全血基因表达微阵列分析的研究发现,三分之一的基因在“反应性”或“高度炎症”的表型和患者之间存在差异表达该组的特征是线粒体功能障碍的基因表达[50]我们发现ARDS血浆刺激上皮细胞和内皮细胞可诱导线粒体呼吸抑制,而与表型无关(图6).然而,msc - ev仅能在低炎症血浆中部分恢复线粒体功能和屏障完整性,线粒体的存在是这种作用的核心(图6)这表明,具有低炎症表型的患者可能对MSC-EVs治疗更为敏感。在高炎症微环境中,存在内皮细胞和上皮细胞损伤的阈值,超过该阈值,生理生物能功能的恢复受到阻碍。
Ang-2已被确定为ARDS中内皮损伤的关键介质和生物标志物[31- - - - - -35是START研究中MSC给药后水平显著降低的单一生物标志物[36].我t is important to highlight that in the present study control but not Rho-EVs demonstrated strong trend towards reduction of Ang-2 secretion levels by both HPMECS and SAECS in the presence of LPS and ARDS plasma, indicating relevance of extracellular vesicle mitochondrial transfer for alleviation of the severity of endothelial injury (图7).
证实MSC-EVs线粒体转移在肺损伤中的重要性在活的有机体内,内毒素损伤小鼠给予正常或罗丹明- 6g处理的间充质干细胞的细胞外囊泡。正常的细胞外囊泡,而非rhoe - evs,能在24 h后显著减轻肺损伤程度(图8).这些数据与之前发表的几篇报告一致,这些报告证明了MSC EVs在临床上的治疗效果在活的有机体内急性呼吸窘迫综合征模型[26,51- - - - - -55].此外,使用mpcls测量该模型中肺组织的耗氧量,显示内毒素灌注显著抑制小鼠肺中的线粒体呼吸和ATP产生,细胞外囊泡线粒体转移能够将线粒体呼吸恢复到正常水平(图8).
本研究有局限性。我们使用ARDS血浆按体积稀释至10%;当细胞暴露于ARDS微环境的所有成分时,这有效地降低了刺激的浓度。我们承认BALF是更适合刺激上皮细胞的环境,不幸的是,两种表型的BALF样本均不可用。内毒素致肺损伤模型较轻,不反映人ARDS的复杂性;的主要目的在活的有机体内实验旨在为msc - ev能够缓解线粒体功能障碍提供原理证明在活的有机体内. 此外,我们没有研究细胞外小泡中的线粒体在肺损伤中起保护作用的分子机制,特别是负责减轻内皮屏障功能障碍的分子机制,这是正在进行的工作的主题。我们没有使用成纤维细胞衍生的细胞外小泡作为细胞特异性对照在活的有机体内然而,先前的研究表明,成纤维细胞衍生的细胞外小泡对LPS和LPS没有治疗作用大肠杆菌-小鼠肺损伤模型[55,56]我们在本研究中的主要重点是研究MSC EV介导的线粒体转移的机制作用,因此我们使用含有类似囊泡但缺乏线粒体的Rho EV,我们相信这将构成更好的控制。
综上所述,我们首次证明ARDS环境导致人类肺组织线粒体功能障碍,与肺泡-毛细血管屏障功能受损有关。MSC-EVs对屏障完整性恢复的治疗作用是通过线粒体转移介导的。
补充材料
补充材料
请注意:补充材料不是由编辑部编辑的,而是由作者提供的。
补充图S1erj - 02978 - 2020。Figure_S1
补充视频S1ERJ-02978-2020.视频
补充视频S2ERJ-02978-2020.Video_S2
可共享的PDF
确认
我们感谢Ileana Micu在成像工作方面的技术支持,感谢John Conlon在临床样本处理方面的技术支持,感谢Ke Xu和David Butler提供的一般技术支持。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
利益冲突:J.Dutra Silva无需披露任何信息。
利益冲突:苏元没有什么可透露的。
利益冲突:C.S.Calfee在研究期间报告了NIH的补助金;罗氏/基因泰克和拜耳咨询的补助金和个人费用,Quark Pharmaceuticals和Prometic咨询委员会工作的个人费用,Gen1e Life Sciences和Vasomune咨询的个人费用,在提交的工作之外。
利益冲突:K.L.Delucchi无需披露任何信息。
利益冲突:D. Weiss没有什么可透露的。
利益冲突:D.F.McAuley报告了葛兰素史克、勃林格·英格尔海姆和拜耳咨询公司在提交工作之外的个人费用;他的机构已获得英国NIHR、威康信托基金和其他机构的资助;已向其机构颁发了ARDS治疗专利;并且是强化治疗的研究总监关怀协会和NIHR EME项目总监。
利益冲突:C.O'Kane报告了Wellcome Trust、MRC和NI HSC研发部门在提交的工作之外提供的资助,并且她的配偶收到了葛兰素史克、勃林格·英格海姆和拜耳的咨询费。
利益冲突:A.D.Krasnodembskaya在研究期间报告了英国医学研究委员会的资助。
支持声明:这项工作得到了英国医学研究委员会研究奖(MRC MR/R025096/1和MR/S009426/1–致AK)的支持。本文的资助信息已存放在Crossref资助者注册表.
- 收到2020年8月3日。
- 接受2020年12月2日。
- 版权所有©ERS 2021。
本版本根据知识共享署名许可证4.0的条款发布。