摘要
通过未知机制,无论巨大的巨噬细胞群体差异有助于器官纤维化。
我们应用了谱系追踪、单细胞RNA测序和单分子荧光原位与空间受限的石棉肺纤维化模型杂交。
我们证实,在纤维化生态位中存在组织驻留的肺泡巨噬细胞、组织驻留的支气管周围和血管周围间质巨噬细胞以及单核细胞来源的肺泡巨噬细胞。去除单核细胞来源的肺泡巨噬细胞而不去除驻留组织的肺泡巨噬细胞可改善石棉肺纤维化。单核细胞来源的肺泡巨噬细胞特异性定位于成纤维细胞附近的纤维化区域,在那里它们表达已知的驱动成纤维细胞增殖的分子,包括血小板来源的生长因子亚单位a。我们发现巨噬细胞集落刺激因子受体(M-CSFR)信号是一种新的可药物靶点,控制这些致病单核细胞来源的肺泡巨噬细胞的自我维持和持久性。药物阻断M-CSFR信号导致单核细胞来源的肺泡巨噬细胞的消失,并改善纤维化。
我们的研究结果表明,在纤维化过程中抑制M-CSFR信号破坏了一个重要的纤维化生态位,包括在石棉诱导的纤维化过程中单核细胞来源的肺泡巨噬细胞和成纤维细胞。
摘要
单核细胞来源的肺泡巨噬细胞协调纤维化生态位的发展,与纤维化的因果关系和维持通过M-CSF / M-CSFR信令http://bit.ly/2nDjS20
介绍
肺纤维化是一种复杂的过程,其临床表征是在空间限制纤维化区域的数量和尺寸的逐步增加[1].事实上,这些病变在胸部ct上的三维分布结合纤维化区域的影像学特征对肺纤维化的诊断和分类至关重要。单细胞RNA测序为检查这些纤维化区域内细胞群之间的相互作用提供了机会,但组织分离过程阻碍了理解细胞之间的空间关系[2].我们推断,结合遗传谱系追踪,单细胞RNA测序和单分子荧光原位杂交可以结合遗传学或药理学干预,以识别可能促进或维持肺中多细胞纤维化小生境的保守细胞内信号事件。为了验证这一假设,我们使用了一个石棉肺纤维化模型。石棉可在停止接触数年后诱发肺纤维化[3.],并且历史上和持续接触石棉纤维仍然是导致肺纤维化的一个重要职业原因。吸入后,石棉纤维滞留在啮齿动物的小气道中,造成空间受限的肺纤维化区域[4- - - - - -6].
最近,研究人员在肺中发现了几个不同的巨噬细胞群体。组织中的肺泡巨噬细胞起源于胎儿单核细胞,在出生后不久就分布在肺泡生态位,具有自我更新的能力,并且在小鼠模型中,在动物的生命周期中持续存在于肺中,没有明显的骨髓细胞输入[7- - - - - -10].已显示肺组织 - 常规间质巨噬细胞包括血管外和血浆巨噬细胞,其表现出明显的解剖本地化和功能[11- - - - - -14].作为肺泡巨噬细胞耗竭和/或损伤的反应,单核细胞被招募到肺中,在那里微环境中存在的因素驱使它们分化为肺泡巨噬细胞[15,16].肺泡巨噬细胞在石棉所致的损伤中起关键作用ostert等.[17据报道,试图吞噬石棉纤维的肺泡巨噬细胞中的钾电流导致NLRP3炎症的活化,这对于石棉介导的肺纤维化的发展至关重要[18].石棉引起的纤维化是否需要一个或多个巨噬细胞群,目前尚不清楚。
在这里,我们使用遗传谱系追踪系统显示,组织驻留肺泡巨噬细胞和组织驻留支气管周围和血管周围间质巨噬细胞存在于纤维化生态位中,而单核细胞来源的肺泡巨噬细胞并非来自组织驻留间质肺巨噬细胞。单核细胞来源的肺泡巨噬细胞特异性缺失可减轻纤维化程度。单分子荧光原位杂交显示单核细胞来源的肺泡巨噬细胞,表达与纤维化因果相关的纤维化前基因,存在于包括受伤的上皮细胞和组织成纤维细胞在内的致病性多细胞龛中。然后,我们使用单细胞转录组学分析了用石棉或博莱霉素治疗的小鼠和肺纤维化患者的肺,以寻找维持单核细胞来源的肺泡巨噬细胞的细胞间相互作用。这一分析表明巨噬细胞集落刺激因子(M-CSF)/M-CSF受体(M-CSFR)信号是控制单核细胞来源的肺泡巨噬细胞的关键因素之一。此外,它提供了意想不到的证据,单核细胞来源的肺泡巨噬细胞中M-CSF的表达可能以自分泌的方式参与这些细胞的维持。M-CSF/M-CSFR信号通路的中断可导致纤维化生态位内单核细胞来源的肺泡巨噬细胞选择性丢失,从而改善肺纤维化。这些发现表明,来自多个实验室的单细胞RNA测序数据可以结合和验证,以识别多细胞纤维化微域内的保守细胞间相互作用,可能用于肺纤维化的治疗。
材料和方法
老鼠
所有小鼠程序均由西北大学(芝加哥,IL,美国)动物护理和使用委员会批准。包括野生型小鼠在内的所有菌株都是在西北大学比较医学中心的一个屏障和专门的无病原体设施中培育和饲养的。所有实验均使用10-12周龄的小鼠。C57BL / 6 j,CX3CR1ER-Cre老鼠(19]及ZsGreen [20.]小鼠从Jackson实验室(Farmington, CT, USA)获得。液氧Casp8.fl / fl,CD11cCreCasp8.fl / fl和CD11cCreCasp8.fl / flRipk3−−/以前曾描述过老鼠[9].
石棉肺纤维化及给药
8-10周龄小鼠气管内灌注对照颗粒(TiO2;100µg in 50µL PBS)或青石棉石棉纤维(100µg in 50µL PBS)诱导肺纤维化,如前所述[21].在谱系追踪研究中,麻醉小鼠灌胃三苯氧胺(10 mg三苯氧胺,100µL;Sigma,圣路易斯,MO,美国)溶解在无菌玉米油(Sigma)中。抗csf1 (M-CSF)抗体(0.5 mg,克隆BE0204;BioXCell, West Lebanon, NH, USA)每5天腹腔注射一次,PLX3397 (40 mg·kg−1;MedKoo Biosciences, Morrisville, NC, USA)如前所述每天口服[22,23].在指定的时间点采集肺,进行流式细胞术、单细胞RNA测序、组织病理学、免疫组化和免疫荧光。
组织制备和流式细胞术
如前所述进行了用于流式细胞术分析和细胞分选的组织制备[9),与修改。简单地,将小鼠安乐死,并通过右心室灌注10ml汉克斯平衡盐溶液(HBSS)。取肺,灌注2mg·mL−1胶原酶D(罗氏,印第安纳波利斯,美国)和0.2 mg·mL−1DNase I (Roche)与Ca一起溶解在HBSS中2+和毫克2+,使用带30g针头的注射器。用剪刀切碎肺,组织被转移到C-Tubes(Miltenyi Biotech,Auburn,Ca,USA)中,并使用M_Lung_01程序在Gentlemacs Distociator(Miltenyi Biotech)中加工,然后在37°C下温育30分钟激动,后跟M_Lung_02程序。将得到的单细胞悬浮液过滤通过40μm尼龙电池滤网,以获得单细胞悬浮液。将细胞与抗小鼠CD45微珠(Miltenyi Biotech)温育和CD45孵育+根据制造商的协议,使用MultiMACS Cell24分离器(Miltenyi Biotech)收集细胞。进行自动细胞计数(Cellometer K2;吖啶橙/碘化丙啶试剂。用固定活力染料eFluor 506 (eBioscience, San Diego, CA, USA)对细胞进行染色,用FcBlock (BD Biosciences, San Jose, CA, USA)孵育,然后用以下荧光标记抗体混合物(列为抗原(克隆,荧光;主要组织相容性复合体II (2G9, BUV395;BD Biosciences), Ly6C (HK1.4, eFluor450;eBioscience), CD45 (30-F11,异硫氰酸荧光素;eBioscience), CD64 (X54-5/7.1,藻红蛋白(PE);BioLegend, San Diego, CA, USA), Siglec F (E50-2440, PECF594;BD Biosciences), CD11c (HL3, PECy7; BD Biosciences), CD24 (M1/69, allophycocyanin; eBioscience), CD11b (M1/70, ACPCy7; BioLegend), Ly6G (1A8, Alexa 700; BD Biosciences) and NK1.1 (PK136, Alexa 700; BD Biosciences). Single-colour controls were prepared using BD CompBeads (BD Biosciences) and Arc beads (Invitrogen, Carlsbad, CA, USA). Flow cytometry was performed at the Northwestern University Robert H. Lurie Comprehensive Cancer Center Flow Cytometry Core Facility (Chicago, IL, USA). Data were acquired on a custom BD FACSymphony instrument using BD FACSDiva software (BD Biosciences). Compensation and analysis were performed using FlowJo software (TreeStar;www.flowjo.com).使用顺序门控策略确定每个细胞群(补充图S1a).使用Cellometer K2图像流式细胞仪,将活/单链门的细胞百分比乘以活细胞数量,得到细胞计数。
单细胞RNA序列
单细胞悬浮液制备如前所述,稍加修饰。小鼠被施以过量戊巴比妥钠安乐死。打开胸腔,经右心室灌注10 mL HBSS。肺被移除,使用30 g针,注射了1毫升dispase(美国纽约康宁,康宁)DNase我之前(σ)在室温下孵化与温和搅拌45分钟,其次是嘲讽使用钳成小碎片(1 - 2毫米)和孵化消化缓冲15分钟。得到的悬浮液通过70µm细胞过滤器(Falcon;用含5%胎牛血清的DMEM(康宁)洗涤,离心成球,用BD Pharm Lyse (BD Biosciences)裂解红细胞。获得的单细胞悬液保存在DMEM/FBS中,并通过40µm细胞过滤器(Falcon)两次。细胞计数用Cellometer K2,核酸结合染料吖啶橙计算有核细胞总数,碘化丙啶计数死亡细胞;细胞存活率超过85%。所有操作均采用宽孔尖端(Axygen; Corning). Single-cell 3′ RNA sequencing libraries were prepared using Chromium Single Cell v2 Reagent Kit and Controller (10X Genomics, Pleasanton, CA, USA). Libraries were assessed for quality (TapeStation 4200; Agilent, Santa Clara, CA, USA) and then sequenced on an HiSeq 4000 instrument (Illumina, San Diego, CA, USA). Initial data processing was performed using the Cell Ranger version 2.0 pipeline (10X Genomics); reads were mapped to the mm10 version of the mouse genome. Analysis was performed using the Seurat R toolkit version 2.3.4 [24的数据集即等.[25]和3.0.2版本[26]与sctransform标准化[27获取石棉数据集。使用来自FANTOM5项目的配体和受体列表来分析细胞间假定的相互作用[28].使用velocyto管道分析单个细胞的RNA速度[29].所有用于分析的代码都可以在https://github.com/NUPulmonary/JoshiWatanabe2019.
数据可用性
来自TIO的单细胞RNA测序数据2基因表达集(GSE127803)已保存-和石棉暴露小鼠。我们还使用了来自GSE82158的流式肺泡巨噬细胞的大量RNA测序数据[9]来自GSE122960的肺纤维化患者的单细胞RNA测序数据[2]和暴露于GSE104154产品博莱霉素的小鼠[25].互动情节从数字4,4摄氏度和7一个可供探索的地点是www.nupulmonary.org/resources.
荧光原位核糖核酸杂交
多路复用荧光原位使用RNAscope (Advanced Cell Diagnostics, Newark, CA, USA)进行杂交。小鼠肺充气至15 cmH2用4%多聚甲醛(EMS, Hatfield, PA, USA)固定24小时。石蜡包埋肺,5µm组织切片置于Superfrost Plus玻片上(Thermo Fisher Scientific, Waltham, MA, USA)。载玻片在60°C下烘烤1小时,在二甲苯中脱芳,在100%乙醇中脱水。切片用H2O2(Advanced Cell Diagnostics)在室温下加热10分钟,然后在1×目标检索试剂缓冲液(Advanced Cell Diagnostics)中加热至轻微煮沸(98-102°C) 15分钟。在HybEZ烤箱(Advanced Cell Diagnostics)中,在40°C条件下将蛋白酶加(Advanced Cell Diagnostics)应用于切片30分钟。根据Advanced Cell Diagnostics Multiplex fluorescent Reagent Kit version 2和4-Plex Ancillary Kit version 2的说明,在需要的时候,与目标探针、前置放大器、放大器、荧光标签和洗涤缓冲液杂交(Advanced Cell Diagnostics)。平行切片用Advanced Cell Diagnostics阳性和阴性对照探针孵育。切片覆盖延长钻石抗褪色Mountant (Invitrogen)。使用的探针是:鼠标MRC1.、鼠标Pdgfa、鼠标Pdgfra和鼠标Csf1(所有高级细胞诊断)。蛋白石荧光团(蛋白石520、蛋白石620和蛋白石690;Perkin Elmer, Shelton, CT, USA)在Multiplex TSA缓冲液(Advanced Cell Diagnostics)中1:1500稀释。验证共本地化MRC1.,要么Pdgfa或Csf1使用尼康A1R共聚焦显微镜(东京,日本),使用×20和×40物镜拍摄图像,然后在斐济(https://imagej.net/fiji.).量化的MRC1.和Pdgfa共染色,在尼康Ti2宽视野显微镜下,用×20物镜和0.45 NA捕获小鼠全肺组织图像。使用尼康NIS-Elements软件5.20.0版本,使用General Analysis模块进行定量。采用滚动球背景减法对图像进行预处理,并采用阈值分割法进行分割。4 ',6-二氨基-2-苯基吲哚(DAPI;英杰公司)和MRC1., DAPI和Pdgfa和dapi,MRC1.和Pdgfa归一化为细胞总数。
组织病理学、免疫组化和免疫荧光
在组织病理学和免疫组化方面,将用于流式细胞术和单细胞RNA测序区域相邻区域的小鼠肺组织在4%多聚甲醛中固定24 h,脱水后石蜡包埋;制备4 μ m厚切片。苏木素/伊红染色和Masson三色染色分析纤维化评分。免疫组化在西北大学小鼠组织学和表型实验室核心设施(芝加哥,IL,美国)进行。
免疫荧光:小鼠肺组织在4%多聚甲醛中固定6 h,转移到20%蔗糖中孵育过夜。将组织包埋在Tissue- tek OCT化合物(Sakura, Torrance, CA, USA)中,在液氮中快速冷冻,然后在冷冻器上以14µm厚度切割。切片用pe标记的抗原癌基因酪氨酸蛋白激酶MER (MERTK) (BioLegend)、Alexa Fluor 647标记的抗siglec F (BD Biosciences)、兔抗抗性样分子-α (RELMα) (Abcam, Cambridge, MA, USA)和山羊抗表面活性剂蛋白C (SPC) (Santa Cruz Biotechnology, Dallas, TX, USA)风干并染色。未偶联的一抗采用合适的二抗,包括驴抗兔Alexa Fluor 647 (Invitrogen公司)和驴抗山羊Alexa Flour 568 (Invitrogen公司)。核染色采用DAPI,切片采用延长金刚石抗褪色支架。在美国西北大学尼康细胞成像设备(Chicago, IL, USA)的尼康A1R共聚焦显微镜或尼康Ti2宽视场显微镜上获取图像,并使用尼康元素软件进行处理。
统计分析
每个分析的统计测试和工具都用结果明确地描述或在图图例中详细说明。
结果
单核细胞来源的肺泡巨噬细胞的募集将石棉反应与非纤维性颗粒(TiO2)
我们量化了小鼠肺中单核细胞和巨噬细胞的数量通过流式细胞术14天后腹腔内施用石棉,可重复诱导肺纤维化,或标准对照粒子TiO2,不诱导纤维化(均为100µg) (图1一个;看到补充图S1a控制策略)。我们发现单核细胞和肺泡巨噬细胞(CD64+Siglec F+)在服用石棉或TiO的小鼠中也同样增加2与幼稚小鼠相比(补充图印地)。而肺泡巨噬细胞的增加主要是由于Siglec F的扩张高人口TiO2-处理的动物,肺泡巨噬细胞增加的动物给予石棉可归因于两个扩张的Siglec F高肺泡巨噬细胞和Siglec F的出现低肺泡巨噬细胞(约占肺泡巨噬细胞总数的15%)(图1 b和c,补充图印地).
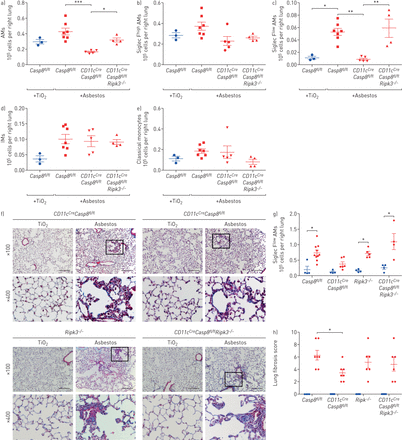
接触石棉或TiO2其特点是单核细胞来源的肺泡巨噬细胞(Mo-AMs)聚集到肺。即时通讯:间质巨噬细胞;SSC:侧散射;FSC:向前散射;GFP:绿色荧光蛋白;MFI:中值荧光强度。a)小鼠给予青石棉或TiO2(气管内100µg), 14天后用流式细胞术定量单核细胞和巨噬细胞的数量(见补充图S1a和b用于门控策略和其他髓样细胞群的量化)。b)在AMs上标记的典型等高线图(CD64)+Siglec F+)从石棉或TiO2对待动物。c) Siglec F的定量低和Siglec F高我是天真的TiO2-或根据(b)中的门控门控接触石棉的动物。CX3CR1ER-Cre×ZsGreen小鼠分别给予三苯氧胺和GFP百分比+采用流式细胞术检测经典单核细胞,免疫球蛋白m和免疫球蛋白m。有代表性的直方图显示了GFP的表达。f) (g)和(h)的实验设计示意图:谱系追踪系统,用于跟踪气管内注射石棉或TiO后AMs的个体发生2.CX3CR1ER-Cre×ZsGreen小鼠分别用石棉或TiO处理2他莫昔芬分别在第7天和第8天服用两次。GFP的数量+7天后进行AMs分析。g)有代表性的等高线图和h) GFP的量化+石棉或TiO后的Mo-ams2曝光。i)暴露于石棉14天后Mo-AMs中Siglec F和CD11b表达的代表性直方图和MFI。所有数据均以平均值±表示扫描电镜.N =每组4-5只小鼠。单因素方差分析与Tukey-Kramer检验进行多重比较。*:p < 0.05;* *:p < 0.01;* * *: p < 0.001;* * * *: p < 0.0001。来自两个独立实验的代表性数据。
我们使用遗传谱系追踪系统来确定Siglec F低肺泡巨噬细胞在石棉处理的动物中扩增,但在TiO中缺失2-处理的动物来源于单核细胞的募集或组织驻留肺泡巨噬细胞的扩张。循环Ly6C高古典单核细胞表达高水平CX3CR1,而组织栖居的肺泡巨噬细胞则不能[11,19].因此,我们走过CX3CR1ER-Cre小鼠与ZsGreen报告小鼠在石棉介导的肺纤维化过程中追踪单核细胞来源的细胞命运(图1 d).在该系统中,给药7天后,86.8%的循环单核细胞出现绿色荧光蛋白(GFP)。+(图1 e)但是因为它们是短暂的,他们在Tamoxifen脉冲后消失了[19].然而,如果GFP标记的单核细胞产生长寿命的巨噬细胞,如单核细胞来源的肺泡巨噬细胞,即使内源性表达后,也会永久标记GFPCX3CR1已经停止了。正如预期的那样,长期的组织 - 常规肺泡巨噬细胞,这不表达CX3CR1,未在本系统中标记(图1 e).相比之下,86.7%的组织驻留的支气管周和血管周间质巨噬细胞也表达CX3CR1,成为“绿色荧光蛋白”+他莫西芬脉冲后(图1 e).
为了评估单核细胞来源的巨噬细胞对肺泡巨噬细胞池扩张的贡献,报告小鼠接受他莫昔芬治疗通过给予石棉或TiO后7和8天口服2在第14天用流式细胞仪分析(图1 f).石棉的施用导致绿色荧光蛋白的大量涌入+肺泡巨噬细胞为Siglec F低和CD11b高(图1 g我)。总的来说,单核细胞来源的肺泡巨噬细胞(CD64+Siglec F低)绿色荧光蛋白+石棉暴露小鼠服用他莫昔芬1周后(图1 h与此相反,在TiO治疗的小鼠中2,只有1.4%的肺泡巨噬细胞是GFP+,与幼稚小鼠相当(图1 h和我)。
单核细胞来源的肺泡巨噬细胞和非组织驻留的间质巨噬细胞参与了纤维化生态位的巨噬细胞池
在我们的谱系追踪系统中,我们利用单核细胞来源的肺泡巨噬细胞上的GFP标签,来确定这些细胞对石棉反应的募集是否在空间上限制在纤维附近的区域。肺纤维化局限于石棉纤维沉积的支气管肺泡管连接处,但远端肺无纤维化(图2一个).免疫荧光显微镜显示为绿色荧光蛋白+在这些纤维化区域中特别发现了细胞和GFP+和绿色荧光蛋白- - - - - -细胞似乎吞噬石棉纤维(图2 bc).这些细胞位于肺泡间隙并表达MERTK和Siglec F,证实它们是单核细胞来源的肺泡巨噬细胞(补充图S2).
单核细胞来源的肺泡巨噬细胞(Mo-AMs)的募集在空间上仅限于石棉纤维附近的区域。6-diamidino-2-phenylindole DAPI: 4;GFP:绿色荧光蛋白;即时通讯:间质巨噬细胞;FSC:向前散射。a)气管内注射石棉纤维会在石棉纤维所在的支气管肺泡导管连接处附近引起纤维化。左面板:中等气道的低功率图像(梅森氏三色)。天平条:100µm。右图:高功率图像(分别是Mason的三色和苏木精/伊红)。纤维化区域出现在气道附近,可观察到石棉纤维(箭头,右下角)。 In contrast, alveolar structures in the distal lung parenchyma are relatively preserved. b) Top panels: representative lung histology fromCX3CR1ER-Cre×ZsGreen小鼠在第14和15天给予它莫西芬(10 mg通过口服牧草)和石棉暴露后21天收获。天平条:100µm。底部行面板对应于盒子中概述的区域。左侧面板:单核细胞衍生的细胞是GFP+;DAPI染色。中间面板:相位对比度图像;石棉纤维用箭头表示。右面板:合并。底板:石棉纤维被绿色荧光蛋白包围+细胞(短箭头)和GFP−具有巨噬细胞形态的细胞(箭头)。c) GFP定量+石棉和TiO中Mo-AMs在支气管周围的分布2治疗的老鼠。双向方差分析与Tukey多重比较检验。* * * *: p < 0.0001。d) GFP实验设计原理图及动力学+三苯氧胺脉冲后的单核细胞、组织驻留细胞和组织驻留细胞CX3CR1ER-Cre×ZsGreen老鼠。绿色荧光蛋白的比例+流式细胞术检测细胞。e)显示GFP的代表性荧光图像+三苯氧胺脉冲后21天组织驻留IMs。f)在AMs上显示GFP表达的代表性等高线图CX3CR1ER-Cre×Zsgreen小鼠21天后他莫昔芬和石棉滴注后14天。绿色荧光蛋白的比例+采用流式细胞术检测经典单核细胞,免疫球蛋白m和免疫球蛋白m。所有数据均以平均值±表示扫描电镜.N = 3-5只小鼠每组或时间点。
组织驻留间质巨噬细胞(CD64+Siglec F−)最近被报道有助于肿瘤相关巨噬细胞的种群[12].为了排除这些驻留组织的支气管周围或血管周围间质巨噬细胞在响应石棉诱导的上皮损伤时迁移到肺泡间隙并分化为肺泡巨噬细胞的可能性,我们进行了治疗CX3CR1ER-Cre×Zsgreen报告小鼠用他莫昔芬标记组织植物间质巨噬细胞(图2 d).在他莫昔芬治疗21天后,几乎所有标记GFP的单核细胞从循环中消失,而82%的组织间质巨噬细胞仍保留GFP+(图2 de)。这些小鼠气管内注射石棉,14天后用流式细胞仪分析肺(图2 d).绿色荧光蛋白的百分比+石棉暴露小鼠的肺泡巨噬细胞与未暴露小鼠没有区别,这表明单核细胞,而不是驻留组织的间质巨噬细胞,驱动了石棉介导的损伤和纤维化部位的肺泡巨噬细胞的扩张(图2 f).
单核细胞来源的肺泡巨噬细胞基因缺失可减弱石棉肺纤维化
之前,我们已经证明,单核细胞来源的肺泡巨噬细胞中caspase-8的缺失会导致它们的死亡通过分化过程中的坏死[9].因此,我们采用巨噬细胞特异性缺失Casp8.是否通过缺失来预防坏死Ripk3确定单核细胞来源的肺泡巨噬细胞在石棉肺纤维化的发展中是否必要。控制老鼠(Casp8.fl/fl)和肺泡巨噬细胞中缺乏caspase-8的小鼠(CD11cCreCasp8.fl/fl)或石棉或TiO2气管内的。单核细胞来源的肺泡巨噬细胞(CD64+Siglec F低)明显减少CD11cCreCasp8.fl/fl和....相比Casp8.fl/fl在服用石棉后28天进行管制(图3一- d)。其他细胞群在CD11cCreCasp8.fl/fl小鼠与之相比Casp8.fl/fl对照组除嗜酸性粒细胞外,嗜酸性粒细胞减少CD11cCreCasp8.fl/fl小鼠与之相比Casp8.fl/fl控制(图3 e和补充图S3a).CD11cCreCasp8.fl/fl小鼠表现出较少的石棉诱导纤维化Casp8.fl/fl控制(图3 f- h)。来证实对肝纤维化的保护CD11cCreCasp8.fl/fl小鼠的单核细胞来源的肺泡巨噬细胞坏死损失,我们进行了相同的实验CD11cCreCasp8.fl/flRipk3−/−老鼠和Ripk3−/−老鼠。虽然全球丧失Ripk3没有影响单核细胞衍生的肺泡巨噬细胞的招募或纤维化的严重程度,失去了Ripk3在CD11cCreCasp8.fl/flRipk3−/−小鼠恢复单核细胞来源的肺泡巨噬细胞和挽救石棉诱导的纤维化(图3一- h)。为了确定组织内肺泡巨噬细胞是否也参与了石棉诱导的纤维化的发展,我们在给小鼠气管内石棉或TiO前24小时用气管内脂质体clodronate处理小鼠,以耗尽组织内肺泡巨噬细胞2.28天后,肺切片定量评分和Picrosirius红沉淀法测定肺可溶性胶原蛋白的结果表明,纤维化的发展并不需要组织内的肺泡巨噬细胞(补充图S3b).这些数据表明,单核细胞来源的肺泡巨噬细胞在石棉的反应中形成一个空间受限的纤维化生态位是必要的。
单核细胞来源的肺泡巨噬细胞(AMs)的缺失可减弱石棉肺纤维化。即时通讯:间质巨噬细胞。Casp8.fl/fl,CD11cCreCasp8.fl/fl,CD11cCreCasp8.fl/flRipk3−/−和Ripk3−/−小鼠给予青石棉或TiO2(气管内100µg) 28天后取肺。a-e)用流式细胞仪分析肺,量化单核细胞和巨噬细胞的数量。f)具有代表性的组织学图像(Mason三色)。天平条:100µm。g)定量测定肺匀浆中可溶性胶原蛋白。h)肺纤维化评分:对每只小鼠单个纵向切片进行盲法评分。蓝色的圆圈:TiO2治疗;红色符号:石棉行政。所有数据均以平均值±表示扫描电镜.n =每组3-7只小鼠。单因素方差分析与Tukey-Kramer检验进行多重比较。*:p < 0.05;* *:p < 0.01;***:P <0.001。
单细胞RNA测序区分对纤维性石棉纤维和控制颗粒的反应
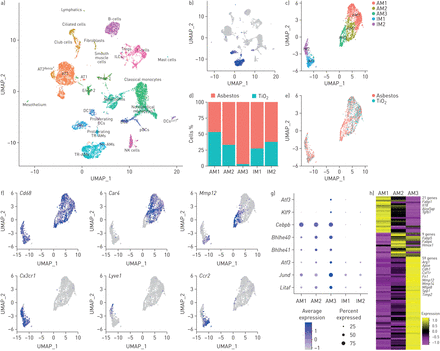
我们推断单细胞RNA测序结合空间技术,例如原位RNA杂交,可以用来了解细胞间的相互作用,通过单核细胞来源的肺泡巨噬细胞在石棉暴露的肺纤维化龛内维持和信号。因此,我们对暴露于石棉或TiO 14天后的野生型小鼠肺部未富集的单细胞悬液进行了单细胞RNA测序2,当纤维化刚刚开始(每一种情况一只老鼠)。使用Seurat R工具箱进行聚类,并根据细胞类型特异性基因的表达对聚类进行注释(图4一和补充表S1).在排除双重和低质量的细胞后,来自两个文库的15个288个细胞用于后续分析。我们捕获并解决了小鼠肺中的所有主要细胞群,包括间质和肺泡巨噬细胞,肺泡上皮型I和II型细胞,树突细胞,成纤维细胞,间皮细胞,平滑肌细胞和内皮细胞亚组。每个聚类包括来自两种实验组的细胞(即。小鼠暴露于石棉或TiO2) (补充图S4a和b).与我们的单核细胞来源的肺泡巨噬细胞内流的谱系追踪研究一致,我们确定了一个肺泡巨噬细胞亚簇(图4 f),来自接触石棉的动物(补充图S4b).
我们根据巨噬细胞相关基因的表达鉴定巨噬细胞(Cd68,MRC1.,Lyz2,Adgre1和妳) (图4 b和补充图自己).对巨噬细胞群体的集中分析发现了肺泡巨噬细胞和组织栖居间质巨噬细胞这两个主要群体。驻留组织的间质巨噬细胞可进一步细分为支气管周围巨噬细胞和血管周围巨噬细胞,以表达Ccr2,F13a1和Lyve1, 分别 (图4 c-f和补充图自己) [11].而一些标记物在肺泡和间质巨噬细胞中均有表达(Cd68,MRC1.,Lyz2,Adgre1和妳),其他局限于肺泡巨噬细胞(Siglecf,马可和Il18) (补充图自己和补充表S2).
肺泡巨噬细胞包含三个亚簇。AM1簇由暴露于石棉或TiO的小鼠肺泡巨噬细胞组成2(图4 d与此相反,AM2和AM3集群主要由接触石棉的动物细胞组成。AM1集群中的肺泡巨噬细胞通过表达与正常稳态功能相关的基因(ear1.和Fabp1) (补充图S4d).来自簇的巨噬细胞AM2表达炎症反应的基因,细胞因子生产和基质金属蛋白酶活化(Car4,Ctsk,Chil3,S100a1和Wfdc21) (补充图S4d).与命运图谱研究一致,来自AM3簇的巨噬细胞表现出更不成熟的肺泡巨噬细胞表型,特征是低表达PPARG.,Car4,ear1.,Siglecf和马可增加的表达Itgam,Cd36和Gpnmb(补充图S4c和d),以及参与巨噬细胞发育和维持的转录因子表达增加(LITAF.,Jund,Bhlhe40,Bhlhe41.和Klf9)和展开的蛋白质反应(Atf3和Atf4) (图4 g).RNA速度分析[29表明AM3簇代表了一种转录稳定的细胞状态,而不是单核细胞到组织栖居巨噬细胞分化之间的中间状态(补充图S4E和F.).
然后,我们使用比较毒理学基因组数据库查询了与肺纤维化相关的947个基因的表达[31]发现在肺泡巨噬细胞中检测到89个基因(图4 h和补充图S4g).簇AM1和AM2包含与肺泡巨噬细胞身份和功能相关的“属”基因(相应有21和9个基因)(Fabp1,Fabp4,Fabp5和Tgfb1) [32].相比之下,聚类AM3富含促纤维化基因,包含59个参与基质重塑和细胞-细胞相互作用的基因(背景,Fn1,Mmp12,Mmp14,Spp1和Timp2) (图4 h和补充图S4g).
在最近的出版物中,X即等.[25使用单细胞RNA测序评估成纤维细胞诱导的肺纤维纤维细胞的响应。虽然作者的分析集成成纤维细胞,但它们的数据集包含大量非白选择细胞,包括肺泡巨噬细胞(补充图S4h和i,补充表S3).对巨噬细胞人口的分析证明了三个亚型的存在:AM1,AM2和AM3(补充图S4j和补充表S4).与我们在石棉中的发现相似,AM1集群主要由pbs处理的对照动物的细胞组成,而AM2和AM3集群由博莱霉素处理的动物的细胞组成(补充图S4k和l).在比较毒理学基因组数据库(Comparative Toxicogenomic Database)中与肺纤维化相关的947个基因中,我们发现了80个来自博莱霉素数据集(补充图S4m).富集的簇AM3用于表达纤维化相关基因(53个基因),其中许多许多与来自我们的ASBestos数据集的AM3簇基因重叠(Gpnmb,Fn1,Mmp12,Mmp14,Spp1和Timp2) (补充图S4g和m).
我们以前报道过,与正常供肺活检相比,肺纤维化患者的肺外植体中出现了一个新的肺泡巨噬细胞亚群[2].20的基因,包括SPP1.,MMP14.,TREM2和GPNMB重叠在表征来自肺纤维化患者的人体纤维化肺泡巨噬细胞群之间的基因之间,从AM3簇中观察到的AM3诱导和博莱霉素诱导的肺纤维化(补充图S4n和补充表S5).因此,我们的分析表明,在不同的肺纤维化模型(石棉和博莱霉素)和肺纤维化患者中出现了同源群体。
单细胞RNA测序识别配体-受体相互作用出现在肺纤维化
我们的数据表明单核细胞来源的肺泡巨噬细胞在肺纤维化的发展过程中。为了了解它们通过信号促进肺纤维化的分子基础,我们分析了可能的配体-受体相互作用,这些相互作用在石棉肺处理的单细胞数据中被识别,但在TiO中没有2治疗肺。我们的初步分析确定了超过50,000种可能的交互作用(补充图S4o-q;详情请参阅数据可用性和在线代码)[28].为了缩小这一列表,我们关注了位于纤维化区域附近的细胞类型(巨噬细胞、成纤维细胞和肺泡II型细胞)之间的相互作用,并特别关注了仅在石棉诱导的肺纤维化期间出现的两种细胞类型:单核细胞来源的肺泡巨噬细胞和Retnla.+肺泡II型细胞(补充图S4r和补充表S6).然后,我们继续验证了一些已确定的相互作用,特别关注1)可以促进单核细胞来源的肺泡巨噬细胞被受伤的肺泡上皮细胞招募的因素,2)促进单核细胞来源的肺泡巨噬细胞在纤维化区域的持久性的因子;3)单核细胞来源的肺泡巨噬细胞产生的因子可以驱动成纤维细胞增殖。
M-CSF/M-CSFR信号通路对于单核细胞来源的肺泡巨噬细胞在纤维化龛内的维持是必要的
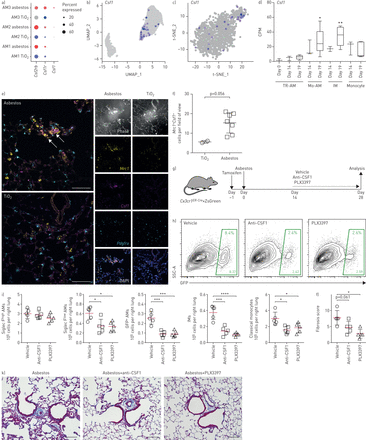
组织常见的肺泡巨噬细胞依赖于粒细胞 - 巨噬细胞菌落刺激因子(GM-CSF;Csf2),由肺泡上皮细胞产生,以维持其体内平衡[33].相比之下,来自m - csf缺陷小鼠和M-CSFR药物阻断的数据(Csf1r)提示M-CSF (Csf1)信号传导可用于肺泡巨噬细胞的稳态维持[34- - - - - -36].我们发现Csf1r在石棉和博莱霉素处理的小鼠中,AM3簇表达上调(图5一个,补充图S4g和m).我们问过哪个细胞表达Csf1和Il34(M-CSFR的配体),特别是是否有新的Csf1/Il34- 在纤维化期间产生的细胞出现。在Tio.2以及接触石棉的动物,Il34表达于肺泡II型细胞和球杆细胞,而Csf1表达于成纤维细胞、间皮和内皮细胞(补充图S5a和b).有趣的是,AM3集群中约有10%的巨噬细胞表达Csf1在石棉和博莱霉素诱导的肺纤维化(图5一个- c和补充表S6).表达式Csf1来自博莱霉素诱导纤维化小鼠的巨噬细胞(来自我们之前发表的数据集[9))(图5 d).在人类中,表达CSF1在正常供体和肺纤维化患者的肺泡巨噬细胞中检测到(补充图S5c),表达CSF1R在肺纤维化患者中增加,特别是在含有促纤维化肺泡巨噬细胞(补充图S5d和e).然后我们用原位核糖核酸杂交。Double-positiveMRC1.+Csf1+肺泡巨噬细胞在纤维化区域的邻近Pdgfra+石棉暴露后28天(图5 e和f,补充图S5f).
单细胞RNA测序显示在石棉诱导的肺纤维化期间的促纤维状单核细胞衍生的肺泡巨噬细胞(MO-AMS)。UMAP:一致流形近似和投影;Treg:调节性T细胞;AT1:肺泡上皮型I细胞;AT2:肺泡上皮II型细胞;内科:内皮细胞;DC:树突细胞;即时通讯:间质巨噬细胞;PDC:血浆谱DC;TR-AM:组织居民。 a) UMAP plot demonstrating 26 cell clusters from 15 452 cells identified by single-cell RNA sequencing 14 days after asbestos or TiO2暴露(每一种情况一只老鼠)。b)巨噬细胞使用典型谱系限制性标记物进行鉴定,例如MRC1.,如UMAP图所示。c)表达的细胞簇MRC1.是主要数据集的子集,并重新聚类,揭示了两个亚簇的组织驻留肺IMs (IM1和IM2)和三个亚簇的AMs (AM1, AM2和AM3)。d)条形图和e)显示石棉-和TiO细胞中巨噬细胞亚簇组成的特征图2接触动物。f)显示聚类特异性基因表达的特征图:Cd68作为一种泛巨噬细胞标志物,Car4作为成熟TR-AMs (AM1和AM2)的标记Mmp12作为Mo-AMs (AM3)的标记物。组织驻留IMs的特点是表达CX3CR1,并且可以进一步细分为血管内(Lyve1)泛刺激(Ccr2IMs。g)点图显示Mo-AMs (AM3)中差异表达的转录因子的表达。h)比较毒理学基因组数据库中AMs和肺纤维化相关基因之间93个基因重叠的热图(截至2019年2月的947个基因)。选定的基因特征群集显示;看到补充图S4e获取完整的基因列表。交互式地图可在www.nupulmonary.org/resources.
自分泌巨噬细胞集落刺激因子(M-CSF)信号对于维持纤维化壁龛内的单核细胞来源的肺泡巨噬细胞(Mo-AMs)是必需的。UMAP:一致流形近似和投影;t-SNE: t分布随机邻域嵌入;TR-AM: tissue-resident点;即时通讯:间质巨噬细胞;SSC:侧散射;绿色荧光蛋白。a)表示表示的点图CSF2RB.,Csf1r和Csf1在TIO后的AMS亚运会中2和石棉暴露。b, c)表示的特征图Csf1亚群AM3在b)石棉和c)博莱霉素暴露后。d)盒须图表示为Csf1在博莱霉素诱导的肺纤维化过程中,血流分类AMs(数据来自Misharin等.[9])。箱线图中心线是中位数,箱限是上四分位数和下四分位数,须是最小值和最大值。多重比较的单因素方差分析与Bonferroni校正。e)原位RNA杂交证实Csf1石棉肺纤维化的AMs。在TiO后28天进行分析2或石棉暴露。巨噬细胞被鉴定为MRC1.+细胞和成纤维细胞被鉴定为Pdgfra+细胞。箭头表示MRC1.+Csf1+自动对盘及成交系统.天平条:50µm。f)数量MRC1.+Csf1+石棉暴露后AMs增加。数据来自每个条件下的一个鼠标。平均值±sd.Mann-Whitney测试。g)实验设计原理图。CX3CR1ER-Cre×ZsGreen小鼠接受他莫西芬脉冲通过给药前1天灌胃青石棉(气管内100µg)。从第14天开始,小鼠腹腔注射抗csf1抗体(0.5 mg,每5天)或PLX3397 (40 mg·kg)−1口服,每天),并于第28天收获。第28天用流式细胞术检测单核细胞和巨噬细胞数量,并用组织学分析纤维化程度。h) CD64标记的代表性流式细胞术图+Siglec F+AMs。i)接触石棉动物的TR-AMs、Mo-AMs、IMs和经典单核细胞数量。j)石棉暴露后28天纤维化评分。k)具有代表性的组织学表现。梅森的三色的。天平条100µm。数据以平均值±表示扫描电镜.N =每组5只。单因素方差分析与Tukey-Kramer检验进行多重比较。*:p < 0.05;* *:p < 0.01;* * *: p < 0.001;* * * *: p < 0.0001。
这些数据表明,单核细胞来源的肺泡巨噬细胞能够产生自分泌信号,以维持其持久性。我们用CX3CR1ER-Cre×zsgreen报告鼠鼠标前面描述。在诱导肺纤维化之前的1天通过气管内给药石棉,我们用他莫昔芬脉冲处理这些小鼠,暂时标记循环单核细胞和来自这些单核细胞的单核细胞来源的肺泡巨噬细胞(图5克).肉纤维化诱导后14天在肺部(图1 g然后,我们用中和性抗csf1抗体或PLX3397(一种M-CSFR激酶信号通路的小分子抑制剂)处理小鼠,然后分析肺巨噬细胞数量和肺纤维化程度14 (图5克).M-CSFR信号通路的药物阻断降低了单核细胞来源的肺泡巨噬细胞的数量,并降低了肺纤维化的严重程度,而驻留组织的肺泡巨噬细胞的数量没有受到影响,而循环单核细胞的水平仅中度降低(图5 h- k)。
单核细胞来源的肺泡巨噬细胞在上皮损伤和空间受限的前纤维细胞龛内常驻成纤维细胞的激活之间提供了联系
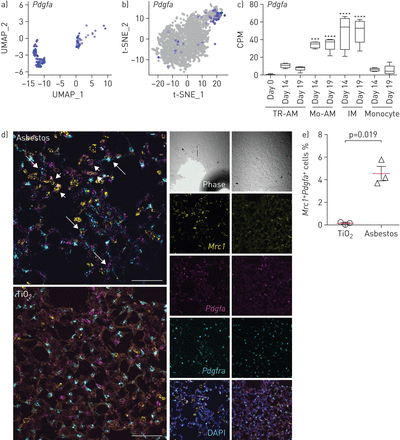
接下来,我们询问了石棉和博莱霉素[25肺泡巨噬细胞单细胞RNA测序数据集的表达配体在成纤维细胞上有伴侣受体,并可能参与其增殖。使用配体-受体对的数据库[28,我们发现,在石棉和博莱霉素处理的小鼠中,AM3簇的巨噬细胞表达了几个可以促进成纤维细胞增殖的分子,包括Pdgfa(图6和b,补充表S6).我们确认增加了表达Pdgfa在单核细胞来源的肺泡巨噬细胞中,通过查询来自博莱霉素模型的流分类巨噬细胞的大块RNA测序数据(图6 c) [9].此外,我们通过表演验证了我们的研究结果原位核糖核酸杂交的MRC1.,Pdgfa和Pdgfra石棉暴露后,检测呈双阳性MRC1.+Pdgfa+肺泡巨噬细胞在纤维化区域的邻近Pdgfra+成纤维细胞(图6 d和e,补充图S6).
单核细胞来源的肺泡巨噬细胞(Mo-AMs)表达Pdgfa这是成纤维细胞增殖所必需的。UMAP:一致流形近似和投影;t-SNE: t分布随机邻域嵌入;TR-AM: tissue-resident点;即时通讯:间质巨噬细胞。a, b) UMAP和t-SNE图显示的表达Pdgfa在a)石棉和b)博莱霉素暴露后的AMs中。表示的条形图Pdgfa在博莱霉素诱导的肺纤维化过程中,血流分选AMs的变化。数据从米isharin等.[9].箱线图中心线是中位数,箱限是上四分位数和下四分位数,须是最小值和最大值。多重比较的单因素方差分析与Bonferroni校正。* * *: p < 0.001;* * * *: p < 0.0001。d)原位RNA杂交证实Pdgfa在肺纤维化期间的AMS。在TiO后28天进行分析2或石棉暴露。巨噬细胞被鉴定为MRC1.+细胞和成纤维细胞被鉴定为Pdgfra+细胞.短箭头表示MRC1.+Pdgfa+巨噬细胞和长箭头表示Pdgfra+成纤维细胞相邻MRC1.+Pdgfa+巨噬细胞。天平条:50µm。e)百分比MRC1.+Pdgfa+石棉暴露后AMs增加。数据来自每个条件的三只小鼠。平均值±sd.Mann-Whitney测试。
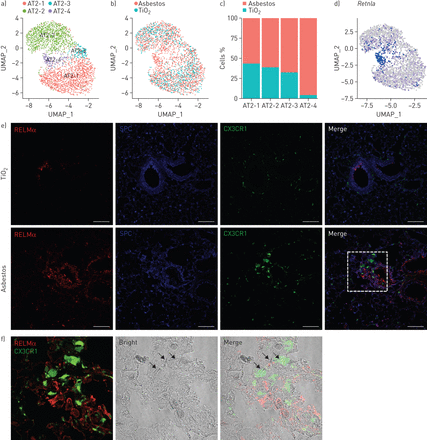
最后,为了探索单核细胞来源的肺泡巨噬细胞是否代表了石棉诱导的上皮损伤和成纤维细胞激活之间的联系,我们对肺泡上皮II型细胞进行了重点分析,这在我们的数据集中得到了很好的体现。分析确定了四个子集群。AT2-1和AT2-2亚群代表典型的II型肺泡细胞(图7- c和补充图S7).亚簇AT2-3包含石棉-和TiO细胞2,其特征是表现为Krt8,Krt18,Ndnf和Lgals3与最近描述的KRT8相匹配+远端肺部的上皮细胞(补充图S7) [37].最后,AT2-4群集由石棉暴露后发现的细胞组成,表达与肺纤维化相关的几个基因,包括Retnla.(RELMα),Il33和Chia1.(补充图S7d和补充表S7).Retnla.主要在上皮细胞中表达,被认为是单核细胞和单核细胞源性细胞的趋化剂。此外,Retnla.-有报道称缺陷小鼠对实验性肺纤维化有保护作用[38].看看是否Retnla.- 治疗上皮细胞被限制为纤维化的区域,治疗CX3CR1ER-Cre×ZsGreen小鼠在给予石棉或TiO后14、15天给予三苯氧胺2在第21天使用共聚焦免疫荧光显微镜对肺部进行分析。RELMα和SPC双染色证实,表达RELMα的肺泡II型细胞局限于纤维化区域,其中也包含GFP+单核细胞来源的肺泡巨噬细胞(图7 e和f)。因此,我们的数据表明单核细胞衍生的肺泡巨噬细胞链接空间限制上皮损伤和成纤维细胞增殖。
抵抗素样分子-α (RELMα)的表达局限于纤维化区域的上皮细胞。UMAP:一致流形近似和投影;SPC:表面活性蛋白c。a) UMAP图显示II型肺泡细胞亚簇。b) UMAP图和c)显示肺泡II型细胞亚群组成的条形图。d)表达增加的特征图Retnla.在石棉暴露后14天的肺泡II型细胞。e)CX3CR1ER-Cre×ZsGreen小鼠气管内注射石棉,并在暴露后14和15天给予他莫昔芬;第21天取肺进行分析。荧光图像显示TiO肺组织中RELMα(红色)、SPC(蓝色)和cx3cr1 -绿色荧光蛋白(绿色)的表达2- 在第21天暴露后21天或石棉治疗的动物。在石棉模型中的纤维化区中的气道上皮细胞和肺泡II型细胞中检测到Relmα,但在TIO之后没有在肺泡II型细胞中2曝光。天平条:100µm。f) (e)框放大:relm α阳性上皮细胞(红色)和单核细胞来源的肺泡巨噬细胞(绿色)与石棉纤维共定位。实验设计与(e)相同。
讨论
我们对来自肺纤维化患者肺组织和两个小鼠肺纤维化模型的单细胞RNA测序数据进行了综合分析,以确定纤维化生态位内细胞内通信的推定机制。从这个分析,我们预测单核细胞来源的肺泡巨噬细胞驱动纤维化,并有自我维持的能力通过自分泌csf / M-CSFR信号。我们使用遗传谱系追踪系统和单分子原位RNA杂交证明了这一点Csf1- - -Pdgfa -表达单核细胞来源的肺泡巨噬细胞,Retnla.-表达上皮细胞Pdgfra-表达的成纤维细胞定位于肺内石棉纤维附近的纤维化壁龛。然后我们使用遗传和药理学策略进行因果联系Csf1-表达单核细胞来源的肺泡巨噬细胞纤维化。这些发现证明了一种联合方法的力量,该方法使用人类和小鼠的单细胞RNA测序、空间转录组学、遗传谱系追踪和小鼠模型中的因果干预来解开纤维化所需的复杂细胞间相互作用。
单细胞RNA测序通过揭示疾病期间出现的细胞群的异质性,正在改变我们对生物学的理解。我们的研究表明,单细胞RNA测序可以用于将不同动物疾病模型中不同实验室产生的数据与来自患病患者的同源数据相结合,以确定疾病发病机制中的共同机制[2,25].通过使用标志着募集巨噬细胞的Ontogeny的遗传谱系追踪系统,我们能够在小区RNA测序数据预测到从小鼠肺中的石棉纤维周围的纤维化区域预测的细胞间信号。在其他模型的纤维化模型中产生的单细胞RNA测序数据集是一种有望的方法,可以在纤维化病发生中产生假设,这些发病机会可以用因果遗传或药理学干预测试[39].
我们的研究结果表明,在肺纤维化过程中出现了空间受限的多细胞前纤维化小生境。在这些小生境中,受损的上皮细胞促使单核细胞来源的肺泡巨噬细胞募集,从而为成纤维细胞增殖提供信号。肺外驻留组织的巨噬细胞依赖于包括生态位的其他细胞产生的生长因子[40],特别是通过成纤维细胞产生的M-CSF [41].相比之下,肺中的组织驻留肺泡巨噬细胞不需要M-CSF,但需要GM-CSF来维持自身,后者通常由肺泡II型细胞产生[8,33].我们发现单核细胞衍生的肺纤维化和(可能是单核细胞衍生的)肺纤维化患者的肺纤维化肺泡巨噬细胞的单核细胞衍生的肺泡巨噬细胞,表达了增加的表达Csf1r/CSF1R.类似的upregulationCSF1R在最近对特发性肺纤维化患者的肺进行的独立单细胞转录组分析中,可以发现纤维化相关巨噬细胞的表达,表明我们的研究结果具有高重现性[42].检测Csf1/CSF1这些肺泡巨噬细胞的表达表明它们可以维持其在纤维化生态位的数量通过M-CSF的自分泌,因此独立于来自其他驻留肺细胞的信号而生存,这是最近在一个包含巨噬细胞和成纤维细胞的纤维化的优雅计算模型中假设的[41,43].我们通过展示两种抑制CSF1信号的药理学策略来证实这一假设,减少了生态位中单核细胞来源的肺泡巨噬细胞的数量,并降低了石棉诱导纤维化的严重程度。自分泌M-CSF信号可能提供了一种机制,通过这种机制巨噬细胞在纤维母细胞灶的“前进前沿”维持,在此位置,来自肺泡上皮和间充质的正常信号缺乏[44].在这个生态位中,纤维化前巨噬细胞分泌成纤维细胞增殖所必需的因子,包括血小板来源的生长因子亚单位A (PDGFA),该因子在肺纤维化患者的肺泡巨噬细胞中也升高[45,46].我们和另一组辐射诱导肺纤维化研究的结果支持M-CSF/M-CSFR抑制治疗某些形式的肺纤维化的治疗考虑[47].值得注意的是,在博莱霉素诱导的肺纤维化过程中,单核细胞来源的肺泡巨噬细胞也表达M-CSF和M-CSFR,但博莱霉素诱导的纤维化会自行消退。结合我们的谱系追踪系统和来自解决博莱霉素诱导的纤维化和持久性石棉诱导的纤维化的单细胞RNA测序数据,可能会提示单核细胞来源的肺泡巨噬细胞如何随着纤维化的解决而改变。
利用之前验证过的基因作为标记物,我们从单细胞RNA测序数据分析了之前描述的正常小鼠肺中三个转录和解剖学上不同的巨噬细胞群体:肺泡巨噬细胞、支气管周围间质巨噬细胞和血管周围间质巨噬细胞[11,13].我们使用一种遗传谱系追踪系统来区分组织驻留间质巨噬细胞、组织驻留肺泡巨噬细胞和单核细胞来源的肺泡巨噬细胞,我们基于我们小组的工作预测了在石棉诱导的纤维化中会出现的这些巨噬细胞,并已被其他人证实[9,48,49].所有三种种群都存在于纤维化的利基中,但只有单核细胞衍生的肺泡巨噬细胞在纤维化区域唯一地发现。谱系追踪研究表明,这些单核细胞衍生的肺泡巨噬细胞不会由间质巨噬细胞产生。组织植物间质巨噬细胞未扩大,在纤维化期间被激活或分化为肺泡巨噬细胞,单核细胞衍生但不是组织静脉肺泡巨噬细胞改善纤维化严重程度。我们将石棉诱导纤维化的单细胞RNA测序数据与最近公开的单细胞RNA测序数据集相结合,来自Bleomycin诱导的纤维化[25]以证明在两种模型中都存在同源巨噬细胞群体。此外,我们还发现在纤维化的后期,单核细胞来源的肺泡巨噬细胞在纤维化过程中是一个转录同质的群体。相比之下,博莱霉素诱导的肺纤维化早期多个时间点的高分辨率分析显示单核细胞来源的巨噬细胞异质性[37].这些影响可能是与单核细胞到巨噬细胞分化相关的细胞自主变化和与单核细胞来源的肺泡巨噬细胞到损伤区域的空间定位相关的环境驱动的转录程序的组合,正如我们在这里报道的,正如我们在博莱霉素诱导的纤维化中发现的,使用一个独特的谱系追踪系统[10].
我们之前已经证明巨噬细胞特异性的缺失Casp8.导致单核细胞在分化为肺泡巨噬细胞时死亡通过当严重的纤维化被抢救出来时,证明是坏死Casp8.和Ripk3同时删除[9].我们利用该系统从遗传学角度论证了单核细胞来源的肺泡巨噬细胞在石棉肺纤维化发展中的因果作用。相比之下,在石棉暴露前通过气管内注射氯膦酸脂质体来清除组织中的肺泡巨噬细胞对纤维化的严重程度没有影响。这些发现提示在解释纤维化过程中基因“肺泡巨噬细胞特异性缺失”的结果时要谨慎。单核细胞到肺泡巨噬细胞的分化涉及到70%的细胞转录组的重塑,并需要多种转录途径。因此,单核细胞向肺泡巨噬细胞分化所必需的任何基因的缺失都可能减少或消除单核细胞来源的肺泡巨噬细胞,并改善纤维化。这些作用可能与成熟肺泡巨噬细胞中所描述的基因功能无关[15].例如单核细胞/肺泡巨噬细胞缺失Tgfb1[50],Torc1[51],PPARG.[52],Casp8.[9]或Cflar[48会阻止单核细胞向巨噬细胞分化,这可能部分解释了它们对纤维化或气道炎症的有益作用。
我们的研究有局限性。首先,虽然我们使用一种有效的谱系追踪系统来排除组织内支气管周围或血管周围间质巨噬细胞作为促纤维化肺泡巨噬细胞的重要来源的可能性,正如最近所描述的,它们可能调节单核细胞的招募或分化,以响应前纤维化刺激[14].其次,虽然我们的单细胞RNA测序分析能够捕获和解析在小鼠肺中识别的许多典型细胞类型,但一些细胞类型,包括肺泡I型细胞、成纤维细胞和平滑肌细胞/肌成纤维细胞,在我们的数据集中代表性不足。因此,我们无法解决这些人群在肺纤维化期间的异质性。其他技术,如富集特定群体的兴趣或单核RNA测序,可能解决这些局限性[25,53,54].
总之,我们发现在肺纤维化中,单核细胞来源的肺泡巨噬细胞的募集仅限于空间受限的纤维化壁龛。通过单细胞RNA测序,可以检测受损的上皮细胞、单核细胞来源的巨噬细胞和成纤维细胞表达的基因,然后用于指导空间分析(例如原位(RNA杂交)重建多细胞生态位对纤维化的发展和维持是必要的。在单核细胞来源的肺泡巨噬细胞分化过程中,通过坏死的基因诱导单核细胞来源的肺泡巨噬细胞的缺失,改善了肺纤维化,使其与疾病发病机制有因果联系。单细胞RNA测序表明,单核细胞来源的肺泡巨噬细胞通过M-CSF/M-CSFR信号来维持自身,给药M-CSF抗体或用小分子抑制剂阻断M-CSFR会导致已经确定的单核细胞来源的肺泡巨噬细胞数量的损失。而其他群体,如活化的成纤维细胞,可作为M-CSF的来源,以维持单核细胞来源的肺泡巨噬细胞群体,单细胞RNA测序和荧光原位RNA杂交数据表明单核细胞来源的肺泡巨噬细胞表达Csf1,提出了一种有趣的可能性,即这些细胞能够维持它们的数量通过一个自分泌的M-CSF/M-CSFR环路。如果这是真的,这一发现可能具有高度重要性,表明致病性单核细胞来源的肺泡巨噬细胞可以维持其种群,并驱动成纤维细胞增殖,即使在没有活性上皮损伤的情况下[43].总的来说,我们的结果支持结合谱系追踪,计算整合来自小鼠和人类纤维化的单细胞RNA测序数据集原位RNA杂交成像作为鉴定可以针对肺纤维化患者治疗不同疾病内型的途径的有力方法。
补充材料
可分享的PDF.
确认
这项工作得到了国防部卫生事务助理部长办公室的支持,通过授予G.R.S. Budinger和A.V. Misharin W81XWH-15-1-0215的同行评议医学研究项目。意见、解释、结论和建议是作者的意见,不一定得到国防部的认可。Illumina HiSeq 4000的下一代测序由NUSeq核心设施完成,该设施由西北大学遗传医学中心、Feinberg医学院和大学研究办公室共享和核心设施支持。美国西北大学流式细胞术中心、先进显微镜中心和病理学核心设施由NCI癌症中心支持基金P30 CA060553授予Robert H. Lurie综合癌症中心。多光子显微镜采用NIH 1S10OD010398-01支持的尼康A1R多光子显微镜。这项研究支持在一定程度上通过基因组学提供的计算资源和员工贡献计算集群(基因节点任务),这是共同支持的Feinberg医学院遗传医学中心和Feinberg的生物化学和分子遗传学部门,教务长办公室,研究办公室和西北信息技术。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
作者贡献:N. Joshi:设计了这项研究,进行了实验,分析了结果,进行了生物信息学分析,撰写了手稿。S.渡边:设计研究,进行实验,分析结果,撰写手稿。R. Verma:进行生物信息学分析,撰写手稿。R.P. Jablonski, C-I Chen, P. Cheresh:进行实验,分析结果。P.A. Reyfman, N.S. Markov:进行生物信息学分析。A.C. McQuattie-Pimentel, Z. Lu, L. Sichizya, R. Piseaux-Aillon, A.S. Flozak:进行了实验,分析了结果。D. Kirchenbuechler:对RNAscope实验进行分析。C.J. Gottardi:分析结果,撰写手稿。C.M. Cuda, H. Perlman:开发并提供转基因动物,提供试剂和资源。M. Jain:提供试剂和资源,撰写手稿。 D.W. Kamp: designed and supervised the study, provided reagents and resources, wrote the manuscript. G.R.S. Budinger and A.V. Misharin: designed and supervised the study, performed analysis, wrote the manuscript, provided funding for the project. All authors discussed the results and commented on the manuscript.
利益冲突:渡边(S. Watanabe)没什么可披露的。
利益冲突:R. Verma没有什么可披露的。
利益冲突:R.P.雅布隆斯基没什么可透露的。
利益冲突:陈C-I没有什么可透露的。
利益冲突:P. Cheresh没有什么可披露的。
利益冲突:N.S. Markov没什么可透露的。
利益冲突:P.A. Reyfman没有什么可披露的。
利益冲突:A.C.Mcquattie-Pimentel无需披露。
利益冲突:L. Sichizya没有什么可披露的。
利益冲突:Z. Lu没有什么可披露的。
利益冲突:R. Piseaux-Aillon没什么可透露的。
利益冲突:D. Kirchenbuechler没有什么可透露的。
利益冲突:A.S.Flozak没有什么可披露的。
利益冲突:C.J. Gottardi没有什么可透露的。
利益冲突:库达没有什么可透露的。
利益冲突:H. Perlman无需披露。
利益冲突:M. Jain没有什么可透露的。
利益冲突:D.W.kamp没有什么可以披露的。
利益冲突:G.R.S.巴丁格没什么可披露的。
利益冲突:A.V.Misharin没有什么可披露的。
支持声明:S. Watanabe是由MSD生命科学基金会、日本公共利益公司基金会、美国西北大学David W. Cugell和Christina Enroth-Cugell奖学金项目支持的。P.A. Reyfman由西北大学肺科学培训项目5T32HL076139-13和1F32HL136111-01A1支持。H. Perlman项目由NIH资助AR064546, HL134375, AG049665和UH2AR067687;美国-以色列两国科学基金会(2013247),风湿病研究基金会(Agmt 05/06/14), Mabel Greene Myers医学教授,并慷慨捐赠给风湿病精准医学基金。C.J. Gottardi得到了NIH HL143800基金的支持。M. Jain是由退伍军人管理局BX000201资助的。D.W.坎普获得退伍军人事务优异奖2IO1BX000786-05A2。该项目由美国国家卫生研究院ES013995、HL071643和AG049665、退伍军人管理局BX000201和国防部PR141319资助。A.V. Misharin得到了NIH HL135124、AG049665和AI135964以及美国国防部PR141319的资助。本文的资金信息已存入Crossref资助者注册表.
利益冲突:乔希没有什么可透露的。
- 收到了2019年4月1日。
- 接受2019年9月26日。
- 版权©2020人队
本文是在知识共享署名非商业许可4188滚球软件.0的条款下开放获取和发布的。