抽象
营养和代谢已经在慢性阻塞性肺疾病(COPD),广泛的科学研究,但影响的饮食习惯,营养状况和营养干预的临床意识的话题可能对COPD发病,进展和成果是有限的。一个多学科工作组是由欧洲呼吸学会创造,提供证据,并在COPD营养评估和治疗目前的做法说明的总结,并为188bet官网地址未来的研究方向。进行工作组成员集中在相关主题的文学评论,由方法论建议。它是公认的营养状况,并在特定的非正常身体组成,是COPD结果的一个重要的独立因素。该工作组确认COPD的不同表型的代谢作为营养风险评估的基础是在临床试验设计和耐心辅导有用。当一个锻炼计划,结合营养干预可能是有效的营养不良患者,可能最多。营养干预的成本效益提供证据需要支持报销,从而增加获得营养干预。总体而言,有证据表明,一个均衡的饮食是所有COPD患者,不仅因为其潜在的肺的好处,也为新陈代谢和心血管疾病的危险及其证明的好处是有益的。
抽象
代谢和营养:在COPD的管理模式发生变化http://ow.ly/As0xh
介绍
营养已经在慢性阻塞性肺疾病(COPD)广泛的科研课题。本文将分析的影响,饮食习惯,营养状况和营养干预可能对发病,进展和慢性阻塞性肺病的结果。本文旨在提高认识关于COPD饮食和营养,并提供资源,这将有助于临床医生和学者提供高品质的营养评估和照顾到个人与慢性阻塞性肺病。
讨论的主题包括了解COPD的代谢改变和相关治疗目标,改善饮食习惯,营养干预的结果和成本效益,包括对未来转化、流行病学和临床研究的建议。主题选择基于科学重要性和临床相关性,以确保文章会引起欧洲呼吸学会(ERS)成员的兴趣。188bet官网地址
方法
ERS成立了一个多学科工作组,由12名成员组成,他们代表了广泛的呼吸系统临床医生、基础科学家、专门从事膳食干预实践挑战的营养护理人员、流行病学家和卫生经济学家。几位代表也是欧洲临床营养与代谢协会(ESPEN)的成员,以确保ERS声明与最新的ESPEN COPD营养指南之间的最佳一致性。按照ERS标准程序处理利益冲突。该文件是由一个以证据为基础的方法和工作组成员的临床专业知识相结合而成的。然而,没有对证据进行正式的分级,因此,本文件不包含临床实践的建议。本声明所采用的程序已得到工作队全体成员的同意。一项声明并不是对文献的系统审查,而是在开始对该文件进行工作之前就确定和纳入这一声明的文献的方法达成一致。证据的层次已经达成一致,因此,来自系统审查和精心设计的随机对照试验的数据在评估过程中被优先考虑。工作队成员审查了与授权主题领域有关的科学证据。2006年至2013年出版的出版物被选中进行进一步审查。 Systematic reviews and randomised controlled trials from Medline/PubMed, EMBASE, the Cochrane Central Register of Controlled Trials, CINAHL and the Cochrane Collaboration were collected. In addition, the references of the selected papers were scrutinised for further relevant evidence. Each topic was presented by the assigned author at the initial meeting in Lausanne, Switzerland (June 2012), and drafts were presented and discussed during meetings in Maastricht, the Netherlands (December 2012), and Barcelona, Spain (September 2013). The final document was drawn together by the chairs of the Task Force. The draft manuscripts were reviewed by all Task Force members to ensure appropriateness and relevance, and the final document was accepted by all Task Force members.
范围
COPD是一种重要的全球性健康问题。该疾病的特征在于持续的气流阻塞从炎症导致与气道重塑,并且可以包括肺气肿的发展。另外,全身性疾病表现与急性发作影响的疾病负担和死亡风险[1]. 扩展了经典的“粉红河豚”和“蓝色气泡”的描述,最近的无偏统计方法[2,3.]支持体重和身体成分区分肺表型的概念,是独立于肺功能损害的预后预测因子。将身体成分纳入营养评估是理解系统性COPD病理生理学和营养潜能的重要一步。虽然最初被认为是疾病过程不可避免和最终发展的一个指标,但现在有令人信服的证据表明,意外的体重减轻并不是降低晚期COPD代谢率的一种适应性机制。4而是生存的独立决定因素,主张在病人护理中保持体重。肌肉损失和肌肉氧化代谢减少在身体机能受损中的重要作用已被证实,这为营养补充作为运动训练的辅助手段提供了新的证据,不仅局限于晚期疾病,而且在早期疾病阶段也是如此。此外,骨质疏松、内脏肥胖和饮食质量差在COPD风险和进展中的关键作用已经出现,这使得饮食意识和干预成为疾病管理的重要组成部分,从预防到慢性呼吸衰竭。
营养评估
为了制定和评估有效的预防和干预策略,需要将患者群体分层为特定的代谢表型。虽然体重和身体组成变量代表了一个连续的光谱,但在过去的十年中,明确的定义和预测治疗结果和反应的表型参考价值已经得到了发展,如表格1。这些不同的情况反映了(epi)基因、生活方式和疾病触发因素对肌肉、骨骼和脂肪组织的影响之间复杂的相互作用。众多的声明文献都将个体代谢表型作为干预目标[6,7]。鉴于慢性阻塞性肺病病程中不同代谢表型的共存,本工作组成员基于对体重(变化)和身体组成(图1)。这种营养风险分层隔膜将有助于临床试验设计和个性化的营养管理。在这方面,世界卫生组织根据最新人口研究的最低标准化死亡率,采用经修订的身体质量指数分类[8,9]。作为一个经验,非自愿减肥的规则>在过去6个月5%被认为是临床上显著,考虑自然变化考虑在内。最近重量损失可以通过病人回忆来评估,尽管在由护理人员或自我监测有规律的间隔标准化重量测量经常掺入和更多的信息。体重变化和BMI分类不采取身体组成的变化,包括脂肪量和分布,瘦肉质量和分布,和骨矿物质密度(BMD)考虑在内。低和正常脂肪量之间进行区分(FFM)(FFM =瘦肉质量+ BMD),待评估身体组成的需求。体成分及研究和临床实践的替代指标的适当的测量都在表2。在正常体重不足COPD患者,年龄和性别调整后的无脂肪质量指数(FFMI)(FFMI = FFM /高度2)<第10百分位是基于低FFMI的物理性能和生存行之有效不利影响定义为异常低。在大多数高加索COPD患者处于危险之中,这个对应的年龄范围为FFMI <17公斤·米−2男性和<15千克。米−2作为临床有用的慢性阻塞性肺疾病(COPD)正常到体重不足患者的代用指标[10个]。骨骼肌减少症的特征是骨骼肌指数(SMI)低(SMI =瘦的阑尾肿块(通过双能x线骨密度仪(DEXA)评估)/身高2)即等于或低于同一民族20-30岁健康人的平均值减去两个标准差[11个]。骨骼肌减少症在越来越多的老年和超重患者中增加了骨骼肌无力的风险。风险分层图与常规营养风险评分(如营养不良普及筛查工具)之间的重要区别[德意志北方银行]或微型营养评估[13个,后者主要关注的是营养不良,而没有考虑到不正常的身体组成。
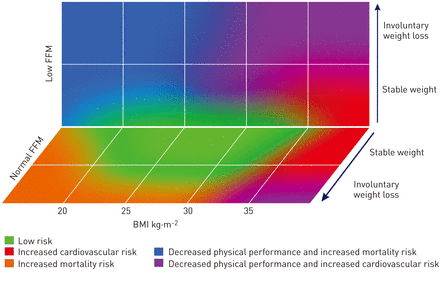
营养风险分层图。FFM:无脂质量;BMI:身体质量指数。
慢性阻塞性肺病的代谢表型和营养风险分析
最近,大量的人口研究表明,年龄标准化的死亡率在体重指数为22.5-24.9 kg·m的参与者中是最低的−2和的20-25公斤·米−2在仅限于那些分析谁从不吸烟[8,9]。在患有中度至重度的气流阻塞,一个BMI <25千克。米−2始终与相对于超重和肥胖,甚至患者[增加死亡风险14个-16个]。在慢性阻塞性肺病中,BMI增加的这种预后优势,也被称为“肥胖悖论”,可能与脂肪组织对肺力学的直接影响有关(如。肥胖COPD患者静态容积的相对减少[17岁])。但是,它也可能是其他的,未知的疾病特征赋予既降低死亡风险,并保留脂肪量和/或FFM附带现象。此外,尚不清楚是否是过度的脂肪或保藏FFM有助于在COPD的生存优势,如低FFMI(<第10百分位),独立BMI和脂肪量的,是死亡率的强预测[18岁]。减持与疾病严重程度增加COPD的患病率[18岁]并且显然与肺气肿的存在相关联19个]。在正常到超重的患者中,低的FFMI意味着相应的高脂肪质量指数。此外,脂肪团可能会从皮下脂肪组织重新分布到内脏脂肪组织,这与轻度至中度慢性阻塞性肺病增加心血管风险有关[20个]。COPD患者体重或低FFM更容易BMD的损失比超重患者[21岁]。DEXA是最适合联合筛查骨质疏松症,FFM和脂肪量。虽然腹部内脏和皮下脂肪量之间的区别需要更多先进的影像技术(如。计算机断层扫描和磁共振成像),临床上有用的估计可以通过DEXA导出。
体成分异常的病理生理学及营养干预的靶点
了解慢性阻塞性肺病中肌肉损失和肥胖的病理生理学和交叉对话对于开发针对特定代谢表型的针对性营养干预至关重要。对这一病理生理学的全面综述超出了本文的范围。因此,我们对营养状况的改变和营养干预进行了简要的总结。要了解慢性阻塞性肺病患者骨骼肌消耗的更详细情况,读者可参阅最近更新的美国胸科学会/ERS关于慢性阻塞性肺病患者下肢肌肉功能障碍的声明[22个]。
脂肪损失
当能量消耗超过能量供应时,体重和脂肪量就会减少。吃本身是一种会对血红蛋白饱和度产生不利影响并增加严重COPD患者呼吸困难的活动[23个]。老化也是一个因素减少饮食摄入量在COPD由于症状(如。味觉丧失、牙列不清、吞咽困难、咀嚼和吞咽能力差、食欲不振或厌恶食物)、社会问题(如。生活或单独食用,或贫困)和不能自我喂食[24个]。厌食症是,但是,在没有稳定的临床疾病的干扰能量平衡的主要触发,如一般,食欲正常饮食摄入增加报告在体重患者[25个,26个]。此外,虽然以半饥饿的正常响应是降低的代谢率和按压全身蛋白质周转,重失去COPD患者可能显示升高的静息能量消耗和增加的全身蛋白质周转[27个]。此外,除了由于肺力学异常而增加通气成本外,肌肉收缩的ATP成本也更高[28个]可能有助于降低下肢运动的机械效率[29个]和某些慢性阻塞性肺病患者每日能量需求的增加[三十]。支持这一观点的是,肺减容手术后体重增加与肺功能改善和呼吸做功减少有关[31]。总的来说,这表明可能有助于减肥,如果能源需求不能得到充分满足,并提供补充热量,以维持或增加脂肪量令人信服的理由高代谢状态。关于COPD碳水化合物补充剂的不利影响,由于增加二氧化碳的产生早期的关注,从碳水化合物氧化负荷通风造成,还没有被证实在最近的研究中,但高营养后只观察到32]。这是在实践中,不可能以口服营养的情况发生,尤其是在患者的食欲不振,并可以很容易地以及分布在天小餐部分是可以避免的。
肌肉损失
肌肉质量是由肌肉蛋白合成和蛋白分解的净平衡决定的。有证据表明恶病质性COPD患者的肌肉蛋白降解率增加,其特点是BMI低和FFMI低[33]. 对蛋白质降解的效应途径的分析显示泛素26S蛋白酶体系统的组成成分一致升高[34]和增强的自噬[35]。相反地,远端蛋白质合成信令线索(胰岛素样生长因子I和磷酸化Akt的表达水平)主要是未改变的[34]。需要更多的研究来排除蛋白质合成信号通路的任何损伤(即它对分解代谢触发的反应),但假设不是这样[36],刺激蛋白质合成更接近于使用营养干预来平衡蛋白质分解的增加可能有助于在恶病质患者蛋白质周转增加的情况下维持肌肉质量。以提供足够的氨基酸支持蛋白质合成信号为目标的营养干预可引起对蛋白质分解线索增加的补偿反应,显然假定能量平衡为正36。蛋白质合成的刺激取决于血液中氨基酸的有效性。与年龄匹配的对照组相比,低FFM的COPD患者血浆支链氨基酸(BCAAs)水平较低[37]。这是众所周知的,支链氨基酸,亮氨酸尤其,能够刺激肌肉蛋白合成。饮食的营养物质的提取,特别是氨基酸,经肠道,对他们的可用性外周组织,因此,在全身氨基酸需求具有决定性的影响。降低与一种蛋白粉的增强的合成代谢反应相关的内脏提取[38]在sarcopenic COPD患者,这可能与损害肠道功能找到[39]。与支链氨基酸大豆蛋白的补充有利于肌肉舱的改变脏器间的代谢,甚至进一步COPD [40]。在慢性呼吸衰竭或恶病质易感的肺气肿表型中,高质量蛋白的合成代谢潜能是否较低,还需要进一步的研究,因为后者在急性运动后也表现出一种全体蛋白代谢的减弱[41]。氧化应激水平的增加已经在COPD患者的骨骼肌一贯报道。信号传导途径对氧化应激敏感的和涉及肌肉质量调节的,肌肉活检分析提示FOXO(叉头框O),MAPK(促分裂原活化蛋白激酶)和NF-κB(核因子,κ轻链活化剂的活化B细胞)。MAPK和NF-κB信号也由炎症引发,增加炎症细胞浸润,促炎症细胞因子的表达确实已经在一些研究报告。因此,这些分解代谢途径(或上游触发器如氧化应激和炎症)可以是用于营养调制合适的靶[34]。
骨密度损失
骨质疏松症是骨骼疾病,其特征为低骨质量和微结构退化骨脆性的净增加,因此,易于骨折[42]。髋部骨折是直接关系到跌倒,导致住院和死亡率过高。椎体骨折更经常发生静默和被认为从日常活动如弯曲或解除所引起的。COPD患者,脊椎和胸廓骨折可能导致增加的后凸,降低胸廓移动性和肺功能的进一步减少。慢性阻塞性肺病和骨质疏松症往往不谋而合。取决于所用的诊断方法,人口设置和疾病的严重程度[率数据变化从5%至60%43]. 造成这种联系的一个原因是存在一些常见的危险因素,如老化、吸烟、体重不足、肌肉减少和身体或功能受限。此外,全身炎症、全身皮质类固醇的使用和维生素D缺乏症的高发率,这些在COPD更严重的阶段经常被观察到,明确地导致了骨骼和肌肉质量的进一步丧失[43,45]. 观察研究也表明肺气肿代表一种与肌肉骨骼损伤相关的特殊表型,但其潜在机制尚不清楚[46-48]。骨组织在整个寿命不断延长。在达到25至30岁的峰值骨量后,骨形成结余回吸收与0.5-1%的年度亏损。在细胞水平上,重塑和骨重建由成骨细胞之间的相互作用,从而产生骨样蛋白基质细胞,其随后mineralises,和破骨细胞,其吸收从它的商店骨和释放钙回来。这种相互作用通过紧紧NF-κB和两种细胞类型的表面上表达的其配体(NF-κB(RANK)/ RANK配体(RANKL)系统的受体激活剂)调节。维生素d起着钙和骨稳态,但其他因素,包括几个促炎细胞因子的调节中起关键作用,也作用于这个途径。低25-羟基d(25-OHD)水平刺激甲状旁腺激素,它通过RANK / RANKL系统的激活,激活破骨细胞为骨重吸收,钙释放和血钙水平的后续稳定化[的49]. 包括COPD患者在内的不同人群中,25-OHD水平低与骨密度之间存在显著相关性[45,50]。低25-OHD水平也与肌肉无力和下跌的风险增加相关,摄入足够的维生素D和钙,除了生活方式的修改(增加体力活动,花更多的时间在外面,戒烟和有限的使用酒精),仍然组成骨质疏松症的预防和治疗策略的基础(51]。
肥胖
在晚期疾病患者中,呼吸衰竭是最常见的死亡原因,而骨骼肌减少症和恶病质是重要的危险因素。相比之下,在轻度至中度疾病患者中,死亡的主要原因是缺血性心血管疾病,其中肥胖是重要的生活方式诱发的危险因素[52]。有越来越多的证据表明,在COPD患者的相对或绝对脂肪丰富的脂肪组织是一个显著贡献者全身炎症负荷[53]。与皮下脂肪相比,腹部内脏脂肪与心血管疾病的风险关系更大,而皮下脂肪可能与较高的炎症能力有关。在轻度至中度、非肥胖的COPD患者中,与对照组相比,脂肪再分配显示为更多的腹部内脏脂肪,尽管总脂肪量相当[20个]。目前还不清楚这种再分配在多大程度上反映了不健康的生活方式,或者是疾病导致的,以及这两者是否有协同作用[54]。与正常体重患者相比,肥胖COPD患者在休息时呼吸困难增加,健康状况较差,而静止性肺恶性充气则减少,无论疾病的严重程度如何[17岁]。肥胖和慢性阻塞性肺病对运动耐受性的联合影响似乎取决于运动的类型(负重)与非负重),其被执行。而峰循环容量在肥胖COPD患者与保存非肥胖患者相比,呼吸困难的评分在肥胖患者循环过程是始终较低时,6分钟步行距离(6MWD)降低和疲劳程度在肥胖患者的增加55]. 没有研究系统地研究减肥干预对COPD患者肥胖、功能和全身炎症的影响。虽然在其他危险人群中,在短时间的减肥后保持体重是一个主要的挑战,但是即使适度的减肥也可以通过改善体脂分布来降低心血管疾病的风险[56]。饮食干预和有氧运动相结合可能最好地实现这一目标,因为有氧运动训练可提高胰岛素敏感性,诱导骨骼肌线粒体生物生成,并可减少内脏脂肪量[54]。然而,这种方法的可行性和有效性可能受到通气限制运动强度的限制。另一种或作为附属物,加入生物活性营养素(如。多酚,多不饱和脂肪酸(PUFAs)和维生素B3.)已经有人提出促进肌肉线粒体代谢和限制异位脂肪堆积[57,但这需要在未来对慢性阻塞性肺病进行充分的临床试验。
急性发作
在需要住院治疗的严重急性加重期,由于包括营养不良在内的不同分解代谢刺激的汇合,可能会诱发或加速肌肉和骨组织的体重下降和消瘦[58,体力活动不足[59],缺氧,炎症[60]及全身糖皮质激素[61]. 此外,这可能是由于呼吸困难或其他治疗,如无创通气,在提供足够营养方面的实际困难而影响能量摄入的时候。此外,对肌肉再生和蛋白质合成信号线索的反应受损可能会延迟恢复,增加再入院的风险[62]. 在呼吸系统恶化的急性期,食欲不振和饮食摄入减少常常伴随着食欲调节激素瘦素和促炎症细胞因子的全身水平升高[58,60]。除了营养风险筛查和初级保健的早期干预外,住院治疗还可被视为进行详细营养评估和实施长期营养管理的另一个机会,因为这是一段“营养风险”升高的时期,其本身可能需要强化营养治疗[63]。如此密集的制度对临床结果和底层机制的影响仍有待明确确立。
饮食管理和营养补充
由于营养和每一种食物,营养素或微量元素引起的多种代谢作用无处不在的性质,随机在这方面的脸特定障碍的临床试验。就其性质而言,有些障碍是难以解决的,如具有安慰剂或适当致盲的食物。由于营养物的多种代谢的影响,选择一个主要结果和样本大小的确定是特别困难的。单食品营养研究也是复杂的,因为它利用了作用广泛的相互作用的过程中网络上的生物活性化合物的大量。
慢性阻塞性肺病的减肥治疗
正处于负能量平衡和减肥中的患者需要增加能量摄入,因为在COPD中额外减少能量消耗是非常不可取的。适当的能量和蛋白质丰富的饮食可以通过一天中分散的几小份来实现[64]。在能源和富含蛋白质的饮食往往具有比在健康个体的建议脂肪含量较高(总能量的45%)。由于脂肪的比例高,考虑需要给予的脂肪质量,特别是在用于烹饪的脂肪的选择,以饱和脂肪的比例最小化。一般建议在目前的指导方针,蛋白质应提供的总能量摄入的20%。设防产品可用于增加不同的膳食能量和蛋白质含量[65]。营养师能够量身能源和富含蛋白质的饮食考虑到每个对象的饮食习惯,生活习惯,症状,好恶。在低能量摄入,可能很难满足对维生素,矿物质和微量元素的需求。口服营养补充剂(如粉,布丁或液体)可以用来补充饮食营养的时候要求无法通过正常的食物和饮料满意。
虽然营养支持,以维持或增加体重丢失和体重COPD患者能源供应和肌肉蛋白质合成的理由是令人信服的,随机临床试验研究的临床疗效一般都很小,并初步荟萃分析显示只有很小的影响估计。该Cochrane评价用Ferreiraet al。(66]最近更新,现在包括了≥2周营养支持的17个试验(632名参与者)(图2和3.)。所有结果合并治疗后值,主要结果合并基线评分(变化评分)的变化。修订后的检讨亦包括建议的评级、评估、发展及评估[89]确定证据质量的方法(即纳入研究,结果不一致,证据的间接性,数据和可能的发表偏倚的不精确性)的偏倚风险。这增加了证据的机身给人的营养补充和具体COPD亚群的影响整体效果更清晰的画面。中等质量的证据(由于偏置的混合风险)表明,补充营养促进体重增加COPD患者中,尤其是营养不良。后干预和改变分数:这是使用两个合并估算证明。只有改变得分为增益的总人口(包括营养和营养不良)的重量显著,但营养不良患者表现显著体重增加,无论使用何种方法的。有在人体测量(FFM,中臂肌围和三头肌皮肤皱褶)显著改善(图3),6MWD,通过St George呼吸问卷对营养不良的慢性阻塞性肺病患者的呼吸肌力(最大吸气和呼气压力)和总体健康相关生活质量进行测量。重度COPD患者6MWD的升高达到最小的临床重要差异[90,91的证据支持其他成果] .The质量低,这主要是因为数据的偏差和不精确性的多种风险(由于小的数字)。这意味着,未来的研究很可能对我们的效果估计信心的影响,很可能会改变的估计。此外,多中心III期临床试验似乎是有道理的。
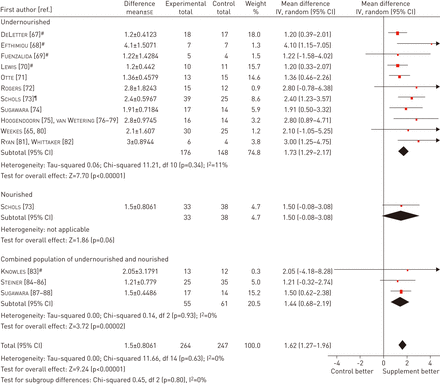
以体重(公斤)变化为结果的营养补充与安慰剂或常规饮食之间的比较森林图。自由度。#:估算标准误差;¶:耗尽。复制及修改自[67得到出版者的许可。
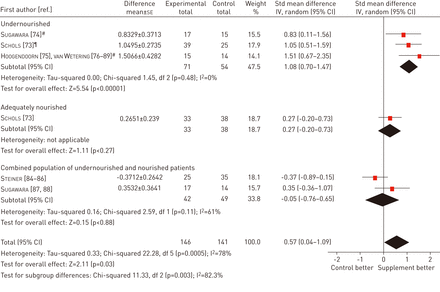
营养补充和安慰剂或不含脂肪质量(FFM)改变平时的饮食之间的比较森林图(kg)作为结果。DF:自由度;标准:标准化的平均差异。#:FFM指数(公斤·米−2);¶: FFM测量为生物电阻。复制及修改自[66得到出版者的许可。
Collins和同事(92,93]也发布了使用不同的方法最近的一项荟萃分析。他们并没有包括所有的试卷相同,但他们的研究结果与Cochrane评价线大致相同。它们还包括了总能量摄入显著阳性结果,并把手和股四头肌力量。
最近的系统评价和结果荟萃分析表明,现在营养补充应该营养不良COPD患者的管理加以考虑。包含在更新的荟萃分析五出的17个试验[66],特别是有FFM作为结果的试验中,曾营养补充与运动相结合。这是可能的,补充的好处将如果配合运动,但根据目前的文献,营养和运动的影响,无法明确区分开来,这是未来的一个研究课题最大化。
营养作为机能辅助
营养对提高运动成绩和训练的重要性在体育运动领域早已得到承认。有证据显示,确保摄取足够的碳水化合物和蛋白质(视乎运动纪律而定),有助优化运动表现[94]和证据表明,一些特定的营养素(如。肌酸、PUFAs和硝酸盐)可增强体能[95-98]。增强体能是慢性阻塞性肺病的一个关键治疗目标,因此,假设营养干预可能提高这一人群的体能表现或增强运动训练的结果是有理论依据的,这种干预已被证明对慢性阻塞性肺病有临床和生理益处。有氧运动训练对慢性阻塞性肺病的疗效是确定的,但其益处的大小是否可与类似的老年健康受试者相比仍不确定。此外,慢性阻塞性肺病患者下肢肌肉的特征是I型肌肉纤维比例减少,与肌肉氧化代谢标志物和细胞能量状态的营养传感调节器水平降低相关(如。过氧化物酶体增殖物激活受体(PPAR)γ共激活因子1、PPARs、AMP激活激酶和席鲁汀类药物99]. 这些观察结果支持了用营养疗法加强运动训练的基本原理,正如工作组成员最近所审查的那样,研究营养疗法对慢性阻塞性肺病患者运动表现或训练的影响的试验数量有限[96]。这些涉及到各种措施,包括碳水化合物和脂肪丰富的补充[85],必需氨基酸[100],乳清蛋白(富含支链氨基酸)[88],肌酸[101-103]和多不饱和脂肪酸(PPAR的天然配体)104个]. 文献的特点是干预的性质、登记的人群和研究的运动结果具有相当大的异质性。许多研究动力不足,大多数是单中心调查。早期的大量营养素研究(包括富含脂肪的补充剂)并没有显示干预组的性能优势,但随后的研究使用富含碳水化合物的补充剂和多不饱和脂肪酸(PUFAs)表明,在选定的患者中,结果或运动训练可能得到加强[85,104个]。小试的调查表明乳清蛋白和肉碱的潜在利益,但必须为要绘制更宽的结论,统计力量不足。三个试验测试肌酸在COPD运动训练中的效果没有一致的积极作用,通过后续的系统回顾和荟萃分析证实[105个]。在一组整体未浪费的COPD患者中,阻力训练后补充蛋白质和碳水化合物并没有增加功能或分子运动反应[106个]。营养支持是否可以增加运动训练和肺康复的绩效成果的问题在很大程度上仍然没有答案。
成本效益问题
营养咨询和口服营养补充剂与其他治疗方法竞争,争取公共卫生预算的一部分;因此,必须评估它们的成本效益。对于慢性阻塞性肺病的这些干预措施的经济影响几乎没有数据。然而,大量研究报告了营养状况与医疗保健使用之间的关系,重点关注因COPD加重或其预测因素而住院的患者。研究表明,慢性阻塞性肺病患者营养不良可能与住院时间较长有关[107个,108个],重新提交的可能性更高[62,109个]及医疗服务使用率的增加[110个与正常营养的病人相比。慢性阻塞性肺病的三个随机对照试验调查了营养补充对医疗保健使用和/或成本的影响[65,76,111个]. 两项研究没有发现住院人数的差异。然而,在这些研究中,小于等于6个月的随访时间可能太短,无法发现对医疗保健利用率的影响。唯一全面的经济评估,即24个月的基于社区的COPD管理项目试验的预先指定的亚组分析,比较了低肌肉质量COPD患者的营养康复和常规护理,发现医院成本显著降低[76]。每名患者的平均总COPD和非COPD有关的费用2年后为12€为830干预组和€14 025对常规治疗组,从而导致€1195(95%CI -7905-5759)的净节省。与常规治疗组相比,干预组的住院费用€-4724(95%CI -7704- -1734)一个显著下降。由于这些净节省成本的,没有成本效益比计算。还有营养咨询和补充,以支持决策有关COPD这些干预的报销更具成本效益的研究显然需要。有几种可能性。一个是设计随机临床试验,其中加入了营养干预常规护理的额外成本和收益进行了研究传统的方法。由于常规治疗是最有可能已经包含营养咨询多式联运肺康复计划或疾病管理方案,全新设计的试验应重点考核营养咨询的口服补充剂或长期的增值。鉴于目前缺乏任何成本效益的数据,这些试验可以招收从不同的目标基团,包括终末期COPD患者兼有肌肉损失和体重减轻(恶病质)的患者以及重稳定COPD的患者的肌肉萎缩(少肌症)。此外,我们还需要对风险因素的权重变化,BMI与FFMI变化,COPD恶化和住院的风险之间的关联纵向更好的数据。 Such data could come from observational studies. They could be used in cost-effectiveness modelling studies to simulate potential long-term effects of changes in weight, BMI and FFM on health status, healthcare utilisation and costs. The latter is necessary because the costs of nutritional intervention in sarcopenic COPD patients are likely to precede the benefits by far.
膳食质量和营养缺乏
维生素d缺乏和摄入不足的用抗氧化能力维生素(维生素A,C和E)已经报道了在COPD。维生素d具有重要作用在骨骼和钙平衡,但可能会出现超出骨骼健康的影响,抗炎,抗感染和抗肿瘤的行动,以及神经肌肉的改善,都被归咎于维生素d [112个]。维生素d状态由25-OHD,活性激素的前体的血清水平的测量评估。在一般人群,维生素d状态是所有原因的死亡率,上呼吸道呼吸道感染和肺功能的独立预测因子。对于慢性阻塞性肺病,相互矛盾的证据25-OHD水平是否与肺功能下降,感染加重和肌肉功能[关联存在113个-116个]。维生素D的状况是由皮肤的合成能力、日照时间(紫外线照射)、相关途径关键酶的遗传变异和食物中的补充摄入决定的。在慢性阻塞性肺病中,由于吸烟导致的皮肤老化、减少户外活动和低质量的饮食摄入,维生素D缺乏经常发生。根据国际公认的标准,维生素D缺乏(25-OHD水平<20 ng·mL)−1)在慢性阻塞性肺病中高度流行,并随疾病严重程度的增加而增加。关于维生素D缺乏症也可能导致慢性阻塞性肺病发病机制的假设存在很大争议,但最近的前瞻性流行病学证据表明,维生素D缺乏症与慢性阻塞性肺病发病率增加和慢性阻塞性肺病患者肺功能更快下降有关[117个]。在更先进的COPD,并且以营养耗尽的状态下的发病率较高表明筛选维生素d缺乏可能是在这些人群中的值。这可能会限制终身补充维生素d缺乏的患者,在人的骨骼和预防跌倒的有利影响,特别是如果与钙的摄入量相结合,已被证明。除了紫外辐射曝光的最小量的每日摄入量随着年龄而变化,但800 IU的与1g钙的剂量被认为是很大程度上足够。高剂量补充的电势,以获得比其他calcaemic效应,包括肺功能下降和COPD恶化,需要进一步探讨[118个]。
新鲜水果和蔬菜摄入不足可能会导致缺乏抗氧化能力的维生素。相反,长期补充维生素E已被证明可降低慢性阻塞性肺病的风险[119个]但是没有证据表明在COPD人群中补充维生素对临床结果有积极影响。众所周知,吸烟和肺部炎症会导致严重的氧化应激,因此抗氧化能力的降低可能会对COPD的病程产生负面影响。大规模的、以人群为基础的流行病学研究表明,谨慎的饮食与更好的肺功能、更少的肺功能下降和降低患COPD的风险有关[120个-122个]. 更具体地说,摄入更多的膳食纤维与降低慢性阻塞性肺病风险、改善肺功能和减轻呼吸症状有着一致的联系[123个]。三项研究报告腌肉,频繁或高消费和发展COPD [风险增加之间的关联120个,124个,125个]。最近的一项研究已扩展此协会包括疾病的演变,揭示了高治愈肉类消费量是与再入院的风险更高医院与COPD [126个]。最后,尽管在临床实践中很少评估,铁缺乏症常发生在慢性阻塞性肺病,这可能由几个因素,包括全身炎症反应,吸收不良铁从肠道,肾功能衰竭引起的(如伴慢性肾脏疾病或糖尿病的后果),和药物,如血管紧张素转换酶抑制剂和皮质类固醇[127个]. 总的来说,这些证据表明,均衡饮食,摄入足够的新鲜水果和蔬菜,不仅对COPD患者的肺部有潜在的益处,而且对代谢和心血管风险也有明显的益处。
营养作为综合疾病管理的一部分
到目前为止,营养干预已被研究作为单一治疗或作为运动训练的辅助手段在衰竭的COPD患者中,通常是在肺康复的背景下进行的。通过额外的干预措施,包括戒烟、长期氧疗和/或无创通气纠正低氧血症和/或高碳酸血症、使用长效支气管扩张剂减少静态和动态高充气或减少肺容积或雄激素,可以提高营养补充的效果纠正性腺机能减退或促进肌肉合成代谢。两项研究表明,由营养补充剂、雄激素和运动训练组成的多模式康复计划在改善晚期COPD营养不良患者的临床疗效甚至生存率方面具有潜力[73,128个]。缺乏长期的多模式干预研究,以证明这些模式是否确实能够显著改变体重减轻和肌肉消耗的自然史,并降低发病率和死亡率。在急性加重期预防或纠正体重减轻的尝试很少,事实上,到目前为止,只有一项安慰剂对照随机临床试验证明了营养补充在住院COPD患者中维持能量平衡和增加蛋白质摄入的可行性和有效性[58]。肠内营养支持对COPD患者谁不口服营养补充回应附加值尚未得到系统的研究。
粉红色河豚和蓝色熏鱼再访
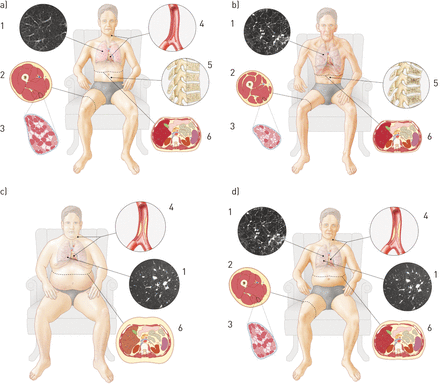
1968年,F伊利等。(4已经将身体习惯纳入两种对比类型的终末期COPD患者的临床表现中,即肺气肿型(粉红色粉扑)和支气管型(蓝色气泡)。作为这一分类的延伸,考虑到肺损伤和共病,三种代谢表型出现在图4该示出的(EPI)遗传学,生活方式和对肌肉,骨和脂肪组织,以及相关的功能和心血管疾病的危险性肺源性触发器的影响,如本文中讨论。图4也预示了一个集成的,往往多干预办法的需要。代谢表型是基于当前的科学证据,但很可能会在不久的将来被细化。在网上补充材料,这些代谢表型三种情况都以帮助临床诊断和实践。
异常代谢表型和慢性阻塞性肺疾病相关的营养风险。一个)健康(参考)其中:1)肺组织的正常高分辨率计算机断层;2)磁共振成像(MRI)用四头肌(红色)和脂肪组织(黄色)的图形表示;3)正常股四头肌横截面积和纤维型分布(红:I型;粉色:IIA型;白色:式IIX);4)健康动脉血管中;5)正常骨组织;和6)腹部MRI图像显示内脏和皮下脂肪组织(黄色)的图形表示。b)中恶病质经常与1)肺气肿和过度充气,与2)骨骼肌质量的损失与3相结合)肌纤维萎缩,和一个型I至II转变导致降低骨骼肌功能,5)骨质疏松症和6)消耗的脂肪量。c)中肥胖往往与1)慢性支气管炎,6)增加的皮下和内脏脂肪组织,和4)动脉僵硬度和增加的心血管疾病的危险。 d) Sarcopenia and hidden obesity is not clearly linked to a specific pulmonary phenotype, but is characterised by 2) loss of skeletal muscle mass combined with 3) muscle fibre atrophy and a type I to II shift leading to decreased muscle function, preservation of fat mass but redistribution of adipose tissue towards increased 6) visceral adipose tissue, 4) arterial stiffness and increased cardiovascular risk.
结论和指导今后的研究
1)营养状况是COPD的成果的一个重要决定因素。
2) 营养风险可以通过纵向测量体重和身体成分来评估。
3)慢性阻塞性肺病维生素D营养缺乏患病率高,可纳入营养风险筛查。
4)与COPD患者的不同代谢表型相关的营养风险特征可能是患者咨询有用。
5) 营养干预可能对营养不良患者有效(基于Cochrane综述[66]),如果有一个锻炼计划相结合可能是最有效的。
6)需要提供营养干预的成本效益证据,以支持对营养干预的报销,从而增加对营养干预的获取。
7)总的来说,有证据表明,均衡的饮食,摄入足够的新鲜水果和蔬菜对COPD患者是有益的,不仅对肺有潜在的益处,而且对代谢和心血管风险也有已证实的益处。
路线由工作队确定未来的研究中被提出表3。
脚注
这篇文章有补充资料www.qdcxjkg.com
利益冲突:可以在本文的在线版本中找到披露www.qdcxjkg.com
- 收到2014年4月15日。
- 公认2014年6月29日。
- ©2014人队