抽象的
特发性肺纤维化(IPF)仍然是一个真正特发性的纤维化疾病,具有适度的遗传偏移和候选人触发,但没有整体解释非家庭病例的疾病。术语协议有助于自千年以来的主要临床和翻译进展。术语“IPF”目前捕获的实体可能会在未来十年内完全重新分类,无论是通过“分裂”(进入IPF子群)或选择性地响应单个疾病修改代理)或通过其他IPF的“Lumping”渐进式纤维化肺病的形式(具有共同的致病机制和IPF样疾病行为)。在这种观点中,我们总结了临床和致病性理由,重点关注未来的临床和翻译研究中的“渐进式纤维化表型”。通过这意味着,我们可以希望解决非IPF患者的不可原性渐进性纤维化疾病的需求,目前通过IPF中缺乏获得性的药剂缺乏获得的药剂。在这方面,在渐进纤维化的非IPF患者中进行抗纤维化疗法的持续试验可能是高度影响力的。如果有重大的概念变动但没有引人注目的理由,可能需要保证IPF命名的未来修订,重命名IPF的益处可能会因由此产生的混乱而超过。
抽象的
IPF仍然是一种真正的特发性纤维化肺疾病,尽管它不是特发性的。迫切需要在临床研究和治疗试验中探索IPF与其他形式进行性肺纤维化的“结块”http://///wly/dtys30jpqr5.
介绍
艾萨克·阿西莫夫爵士曾经说过:“打牌的人一开始就会安排他的手以达到最大的感觉。”科学家们对他们收集的事实也做了同样的事情。”这一基本事实支配了特发性肺纤维化(IPF)定义的历史变化。正如千年前的定义,“IPF”标签包括一组不同的特发性间质性肺炎(IIPs),现在被视为独立的实体。2002年修订国际工业ip重新分类的理由[1]奠定了累积的经验,确定其他IIPs平均而言,从现在被称为IPF的实体的完全不同的结果[2]. 用实用主义哲学运动创始人威廉·詹姆斯的话说,“每一种对事物进行分类的方法都只是为了某一特定目的而对其进行处理的一种方法。”一种疾病的新命名法以临床实用性为依据:特发性非特异性间质性肺炎(NSIP)是根据自然史和治疗过程中的主要差异从IPF中分离出来的。虽然我们对IPF的概念在最近几十年发生了巨大的变化,2011年的诊断标准[3.]目前正在修订中,指规数的定义和分类很可能仍是一个“移动目标”。
正如下面详细讨论的,IPF的未来定义和分类可能是由“分割者”(他们更喜欢根据观察到的细节绘制差别)或“lumpers”(他们在诊断细微差别之上搜索大图)驱动的。分裂和集中之间的紧张关系应该被视为健康辩论的来源。在IPF中,我们可以简单地概括这一困境。在我们目前的治疗方法下,在不同的患者亚组中会发现不同的结果吗?或者,在IPF患者和具有IPF样行为的非IPF患者合并后,对临床进行性纤维化表型的识别是否会更加有效?要论证这两种方法的重要性,需要假定我们还不具备的知识水平。事实上,拆分和合并可以说是合理的互补策略。最近在脓毒症和急性呼吸窘迫综合征的试验设计中提倡“更聪明的集块和更聪明的分割”[4].唯一的确定性是IPF的未来形状不确定。
正是在这种情况下,我们对最近关于改变命名法的建议持怀疑态度,建议将“IPF”一词替换为“上皮细胞驱动的肺纤维化”、“原发性肺纤维化”或“进行性年龄依赖性肺纤维化”[5]. 就其本身而言,这些非常不同的替代术语抓住了IPF发病机制的神秘性和特发性。作者认为“特发性”这个词现在已经过时了。他们基于这样一种看法,即“对IPF发展过程中涉及的遗传、环境、细胞和分子机制有着广泛的理解”。他们强调了目前流行的IPF致病假说,即纤维化主要由上皮细胞功能障碍引起。他们还质疑“纤维化”一词,因为纤维化只是IPF的一个组成部分,基质积聚是由功能失调的上皮细胞引起的。他们认为,“纤维化”一词的使用忽略了导致肺重塑的其他致病过程。基于这些考虑,作者认为IPF标签可能会限制治疗进展并抑制精确医学的实施。
尽管Wolterset al。[5]可能会挑起富有成效的辩论,我们相信此刻的命名变化为时过早,可能会产生不良后果。作为特发性疾病的指定并不意味着没有潜在的原因(或原因),但仅表明疾病的关键触发器目前未知或不完全理解。近年来,近年来的潜在机制很多,但在其他地方争论,个别患者(除家庭形式除外)的IPF的发展仍然是未解释的[6].在这方面,IPF的遗传倾向的鉴定,包括一个单核苷酸多态性(rs35705950)存在于38%的IPF患者,但9%的普通人群[7,其致病解释能力仅为5%。事实上,如果认为所有的慢性疾病过程都是由遗传偏好和环境因素共同作用的结果,那么揭示适度的IPF与muc5B阳性之间的关联本身并不能解开IPF之谜。
上皮细胞功能障碍是IPF发病途径的关键这一观点在2001年的一篇关键综述文章中首次得到广泛传播[8].Wolterset al。[5]认为IPF现在可以被视为基本上是上皮病。然而,IPF中识别的病理学机制包括上皮细胞功能障碍,宿主防毒,T细胞耗尽,成纤维细胞活化,氧化应激,血管重塑,替代巨噬细胞活化和衰老/老化[9这些途径之间的相互作用可能是关键的。例如,与端粒稳态相关的基因中非常罕见的突变之间的关系(如塔特,TERC.,PARN或RTEL1)或表面活性剂稳态(如sftpc.,SFTPA1和SFTPA2),肺纤维化的发展是相当强大的,并支持衰老和肺纤维化发展中的肺泡上皮异常之间的病理联系[10,11].此外,负责疾病启动的机制可能与进展的机制不同。例如,尽管大多数癌症的上皮细胞来源,但癌症进展均可依赖于肿瘤微环境,包括基质和免疫细胞。IPF进展可以由异常细胞表型驱动,包括外观重编程的间充质细胞[12],与诸如上皮细胞损伤或再生受损的引发事件不同。实际上,对免疫机制的支持[13,14]和基质机制[15- - - - - -18]有助于纤维化进展。此外,在大多数其他纤维类肺病中,上皮异常可能是致命的重要性,包括过敏肺炎,结缔组织病情相关的间质性肺病(CTD-ILD)和结节病,破坏了“上皮驱动的肺纤维化”的争论作为一个IPF的替代术语。
我们还质疑术语“纤维化”一词是IPF中的不恰当描述符。它是IPF中致命的纤维化。IPF中的纤维化疾病平均比其他间质性肺病更广泛,更渐进,如纤维化过敏性肺炎与特发性肺炎纤维化非特异性间质性肺炎,一种至少部分由免疫失调引起的纤维化疾病。我们认为,在IPF中,致病的争论并没有胜过纤维化的临床重要性。
认为IPF标签是我们进一步理解的障碍的想法似乎是违反直觉的。“动脉粥样硬化”一词并没有阻碍人们对其复杂的多细胞发病机制的理解,这种机制远远超出了“硬化症”的范畴。同样,“囊性纤维化”的名称也没有阻碍研究计划,尽管纤维化或囊肿形成没有一个主要的致病作用。可以认为,指定指规数为“尚未解释”或“自我延续”(IE。特发性),而不是由最近的进展充分解释(IE。非特发性的)本身就是对必要的进一步研究的刺激。我们订阅了使用术语“特发病性”的观点适当的用Wolterset al。[5],“患者(或照顾者)对其疾病的理解和对其行为和管理的期望。”
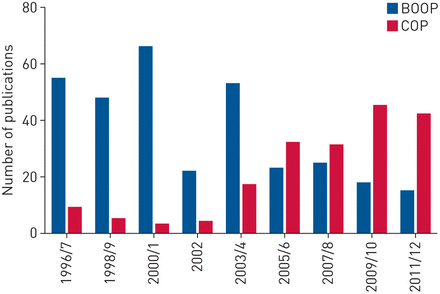
即使在理想的时候,疾病命名的激进变化也是一种主要的承诺,必须不可避免地导致短期混乱。通常承认,“支气管炎梗死组织肺炎(BOOP)”(BOOP)至“密码组织肺炎”(COP)的变化[1]是必要的,因为术语“BOOP”创造的混乱,含有“支气管炎梗阻”,但指定从灭错的支气管炎的根本不同的疾病。然而在未来十年中,“BOOP”几乎与医学文献中的“警察”一样普遍存在(图1)。
在2002年特发性间质性肺炎分类发表前后,“闭塞性细支气管炎组织性肺炎”(BOOP)和“隐源性组织性肺炎”(COP)的出现频率。
IIPS并非所有特发性,并不总是夸张和很少的肺炎,但该术语被保留,因为自2002年自2002年自2002年以来,这一临床效用具有广泛的理解和临床效用,其意义基于2002年的IIP标准1].“IIP”一词内在的不准确性并不妨碍对这些疾病的改进和更深入的理解。2013年IIP分类更新的主流观点[19就是在命名法上做无谓的改变不会有什么实际价值。
IPF也是如此。所示表格1在美国,历史上有很多术语被用来描述特发性肺纤维化,这本身就是一个混淆的主要来源。2002年统一术语[1为后来的重大进展铺平了道路。现在国际上普遍认识到" IPF "一词所表示的疾病的临床性质和行为。如果发现IPF患者的一个亚组在使用基于生物标志物信号选择的特定药物后,结果出现了重大改善,那么该患者亚组的分类改变可能确实是有必要的,正如NSIP作为可分离疾病出现时所发生的那样。在这种情况下,目前拟议的从指规数改为备选名称之后,将需要进一步更改名称。我们相信,这是一条通往混乱的道路。
最重要的是,最近的进展,包括《Wolterset al。[5的观点,并没有让我们对IPF的发病机制有一个最终的认识。IPF拼图还没有解决,在不久的将来可能也可能不会解决。我们反对更名提议的根本理由是,在应该优先考虑IPF可能的拆分以实施精准医疗,并同时将IPF与其他形式的进行性纤维化合并的时候,这是一个错误的倡议。
分裂IPF和精密药
精准医疗在很大程度上依赖于可靠和可重复的生物标志物的发现。在这种特殊情况下,生物标志物可以被广泛定义为通过组合组学方法(例如基因组学、转录组学、代谢组学、蛋白质组学和微生物组)[20.,21]、循环血浆中特定蛋白质和/或它们的修饰[22- - - - - -26],以及基于肺组织的取样/分析[26].与关键机制通路相关的生物标记物可能识别对靶向治疗有选择性反应的IPF亚组的希望仍未实现。目前唯一提供“概念证明”的IPF数据来自一个小队列的回顾性研究,其中抗氧化治疗的好和坏结果与TOLLIP基因变异有关[20.].这不是为了否认精密医学作为IPF治疗目标的重要性,这是几种影响力的观点发展的想法[27- - - - - -30.].然而,必须发出警告。精准医疗在概念上是优雅的,但科学史上充斥着优雅的想法,比如希腊的四种体液理论,最终被证明是不可持续的。
恶性疾病中有效的靶向治疗的先例主要涉及指向肿瘤启动子途径的干预,该途径被特异性基因突变异常激活。在非恶性肺病中成功的个性化疗法,也许与IPF更相关,包括患有G551D突变的囊性纤维化的个体中的Ivacafaceor [31,以及美泊珠单抗和苯拉珠单抗治疗嗜酸性哮喘[32,33].有关lebrikizumab在由2型辅助T细胞(Th2) - 驱动的炎症定义的哮喘亚组中的潜在作用存在矛盾的数据[34,35].这些观察只能被视为令人鼓舞。然而,在接近术语中,类似的方法是否在IPF中同样有效仍然不确定。
纤维化是一种复杂的,但高度保守的组织修复反应,对损伤变得不适应或表现为组织再生能力的失败[9].当在组织学上占主导地位时,它被视为主导疾病模式,如在IPF中。然而,纤维化可以使大多数ILD和哮喘和慢性阻塞性肺病复杂化,并且可以识别一般疾病内型。挑战是将子型与纵向临床行为联系起来。缺乏物质型 - 表型亚组的鉴定可以解释IPF中许多临床试验的失败。直到在IPF中识别并验证此类内型表型子核酸,IPF的子类化(“分裂”)不能用于有用的临床目的。
结节性IPF与其他纤维化疾病:进展性纤维化表型
针对IPF的分裂所做的大量努力并没有反映在确定IPF和其他进行性纤维化间质性肺病共同机制的倡议中。具体来说,IPF和其他进行性纤维化ILDs之间可能有相似之处,这些相似之处与下游生物通路上起始沉淀物的汇聚有关,基于这些最终共同通路对这些疾病进行分组或集总可能具有临床应用价值。随着时间的推移,对IPF的定义越来越狭窄,小心地将其与其他形式的ILD区分开来,并将其与分成个体障碍的对照组进行比较[36或合并[37].这种严格的表型没有没有缺点。例如,一些介入性IPF试验中的屏幕故障率超过50%,其中大多数被排除的患者未能满足严格的诊断标准[38].明确诊断IPF所需的狭窄定义的胸部影像学模式与更广泛定义的模式相关的进展率没有区别[39].未经分类的IIP的实体是主要管理不确定性的源泉,对于未能满足诊断IPF或其他IIP的诊断,为未能达到严格的分类标准的患者提供诊断家庭19].
IPF中的疾病进展比其他ILD更常见,尽管具有高度可变率,但这种临床行为是该疾病的定义特征。由于IPF是最常见的纤维化ILD,推荐中心的IPF研究比较容易,并且具有合理清晰的诊断标准。相比之下,通过纤维化复杂的其他个体ILD对疾病进展的评估需要选择动力患者亚组,需要多元协作并要求疾病和进展的强大定义。也许是不可避免的,研究进步肺纤维化机制将重点关注IPF。
疾病进展的IPF模型有明确诊断的优势,但不能满足目前对非IPF纤维化肺病患者的临床需要。对个体间质性肺病进行安全诊断的主要作用是告知临床医生和患者预期的未经治疗的自然史以及治疗的病程。诊断IPF就是诊断一种不可避免的进展性纤维化疾病。然而,在其他ILDs中,病程的变异性要大得多。例如,在过敏性肺炎中,有一些患者亚组的疾病是完全可逆的(无论是自限性的还是需要治疗的),纤维化但内在稳定的(“燃尽”疾病),纤维化和进行性的但可以通过传统治疗稳定下来,以及不可逆转的进行性的。这些纵向疾病行为模式也适用于结缔组织疾病相关的ILD、结节病和其他形式的ILD(包括不可分类的疾病),并在2003年首次提出的ILD疾病行为分类中得到了捕获[40],并由美国胸科学会/欧洲呼吸学会专家组正式推荐用于不可分类的ILD [188bet官网地址19].在这个角度上,我们关注的是非ipf纤维化疾病的患者亚组,尽管治疗仍表现出疾病进展。这一患者亚群在各个ILDs中的合并,以下称为“进行性纤维化表型”,充分得到了临床数据的证明,并得到了翻译观察的支持(表2)。
临床数据
纤维化性ILD的纵向行为可以有效地细分为疾病行为分类中指定的五种模式中的三种[19].
肺纤维化可能本质上是不进行性的(IIP疾病行为分类的第3类),如“烧坏”结节病或去除触发器后的残余损伤(例如药物诱导的肺病,一些过敏肺炎病例)。
在另一个大的患者亚组中,进行性疾病通过免疫调节得以稳定,至少在短期内(疾病行为分类的第4类)。口服环磷酰胺安慰剂对照试验观察到的“平均”结果[41]并比较口服环磷酰胺和霉酚酸酯治疗系统性硬化症的疗效[42]是生理稳定性。也有非受控数据记录了霉酚酸酯治疗结缔组织病相关ILD的疾病稳定性[43]和慢性过敏肺炎[44,45].
非ipf疾病的进行性纤维化表型的特征是,无论在单个ILDs(疾病行为分类的第5类)中是否认为适当的治疗,均以进展为特征,包括具有ipf样疾病行为和死亡率的亚组(图2)和一组纤维化进展更隐蔽。
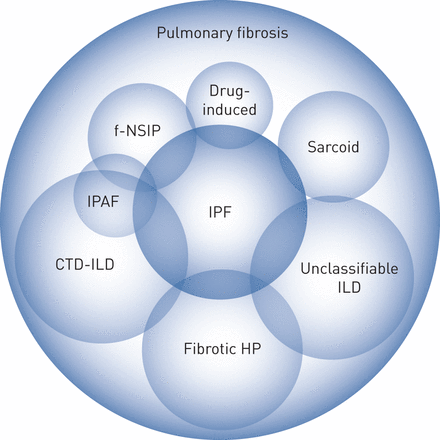
特发性肺纤维化(IPF)和其他疾病之间纵向疾病行为的重叠。圆圈的大小反映了间质性肺病(ILD)中心所遇到的个别疾病的大致流行率。IPAF:具有自身免疫特征的间质性肺炎;CTD:结缔组织病;f-NSIP:纤维化性非特异性间质性肺炎;惠普:过敏性肺炎。
类似于IPF的结果在活检或胸部成像(高分辨率计算机断层扫描;HRCT)。在两个最大的慢性超敏性肺炎组织学系列中,通常间质性肺炎(UIP)组织学模式的患者预后最差[46,47],其存活率与IPF相似[46],确认先前的观察[48- - - - - -50].HRCT上的大囊性蜂巢状,提示了可能的UIP模式,是慢性超敏性肺炎死亡率的独立决定因素[51].在类风湿肺中,UIP的组织学模式是恶性预后决定因素,其存在类似于某些系列的IPF [52- - - - - -54],但在其他方面则没有[55,56].在一个系列中,HRCT上的UIP模式与IPF对照队列中相同[57一般来说,一般来说,一直指示了差的结果[58- - - - - -61].在一项研究声明中定义的具有自身免疫特征的间质性肺炎(IPAF)实体中[62]活检或HRCT上的UIP模式具有与IPF相同的结果[63].
然而,渐进式纤维化表型不仅限于手术活组织检查或HRCT的UIP模式的患者。在类风湿肺中,经典的UIP HRCT模式在不到50%的UIP组织学模式的患者中发生[64].在其余病例中,HRCT模式包括可能的UIP(也与NSIP兼容)和“与UIP不一致”,定义见2011年美国胸科协会/欧洲呼吸学会/日本呼吸学会/拉丁美洲胸科协会指南[188bet官网地址3.].在非IPF ILDs中,生存率介于IPF和其他非IPF ILDs之间[65- - - - - -67].手术活检时特发性NSIP的亚组患者,以疾病进展超过6至12个月为特征,其死亡率与IPF相似[68,69].有许多关于药物诱导的肺部疾病演变为致命的进行性纤维化表型的轶事报道,尽管起作用的药物已经停用[70].虽然Sarcotizoss倾向于进展,但仍然比其他纤维化ILD更加危及,但在胸部射线照相上与IV阶段疾病相关的10年8%的存活率低于一般人群的预期,死亡率大部分均衡对肺病[71].
在识别不良长期结果时,在NSIP,超敏肺炎,类风湿性肺,全身乳化菌相关的ILD和无分配ILD的研究中阐述了短期疾病行为的力量,其中死亡率主要与短暂相关- 疾病进展,由肺功能趋势定义[59,68,69,72,73]或在HRCT上进行疾病的连续进展[65].在这些研究中,在考虑了其他基线信息后,疾病进展是死亡率的独立决定因素。
我们认为提出进展性纤维化表型的确切定义还为时过早。我们非常希望在第一次展示时应用准确的标准,但需要对疾病行为进行前瞻性验证。根据目前的知识,从这个角度总结,表明可能UIP的HRCT特征、组织学发现和新出现的分子数据可能最终提供基线定义,以及与观察到的疾病进展相关的附加标准。目前,进展性纤维化表型只能通过观察到的疾病进展来确定,尽管治疗被认为是适合于个别ILDs的。
致病考虑因素
从病理生理学的角度来看,当上皮细胞或内皮细胞屏障完整性不可挽回的丧失时,纤维化几乎普遍发生[74,75],见于许多非IPF ILD,尤其是CTD-ILD和慢性过敏性肺炎。因此,尽管细胞损伤的病因可能不同,无论是CTD-ILD中的自身免疫机制、过敏性肺炎中的吸入性有机粉尘颗粒,还是IPF中的未知损伤,纤维化反应的开始可能与持续性损伤和受损的上皮细胞和/或内皮细胞修复有关。类似地,尽管疾病的发病机制可能与进展机制不同,但很可能是一系列保守的病理生物学机制,包括生长因子激活和成纤维细胞的表观遗传重编程,构成了各种ILD疾病进展率的基础,尽管有不同的潜在病因和最初不同的生物学途径。导致IPF纤维化进展的相同病理生物学机制也可能导致非IPF纤维化疾病(如CTD-ILD和慢性过敏性肺炎)的进展性疾病表型。因此,从发病学的角度来看,将这些不同的纤维化疾病“包埋”起来并确定其类型可能更有用−表型亚组更精确地分配预后和启动靶向治疗。
虽然存在探索IPF和其他纤维化障碍的疾病进展之间的联系的平移研究的相对缺乏,但是存在普遍的机制可能存在的数据。最近证明了IPF和类风湿性关节炎相关ILD中的共同遗传易感性,表明常见的致病事件涉及这些疾病[76].端粒长度,预测IPF中的死亡率增加[77,在慢性超敏性肺炎中具有类似的预后意义[78].此外,肺泡上皮细胞损伤或功能障碍的血清生物标志物与系统性硬化相关性ILD (SSc-ILD)和IPF中随后的肺功能下降相关[79].患有SSC-ILD和IPF疾病进展的常见病症机制可包括肺泡干细胞耗尽/细胞衰老,线粒体功能障碍,患有损伤的自噬,表观遗传修饰和免疫失调[80- - - - - -83].
SSc-ILD和IPF亚组患者的疾病进展可能独立于疾病发生的风险,如IPF风险MUC5B基因变异与SSc-ILD或结节病缺乏相关性所示[84].有趣的是,MUC5B中相同的单核苷酸多态性增加了发生IPF的风险,也与生存率的提高显著相关[85].此外,Tollip单核苷酸多态性与开发IPF的风险降低有关,但预后差86].尽管这些看似矛盾的发现的原因尚不清楚,但它们进一步强调了区分疾病风险和疾病进展的重要性。
渐进式纤维化表型:含义和未来的策略
从这个角度来看,我们强调了将IPF与其他形式的进行性纤维化肺疾病合并的潜在价值,作为对最近提出的将IPF分离的建议的对照,最终目标是实现精准治疗或个性化治疗。纤维化是包括但不限于IPF在内的一组进行性肺部疾病的典型特征。许多患者的纤维化进展,以及这种进展导致生活质量损害、功能状态下降和早期死亡,这是无可置疑的。很可能是多种机制导致了疾病的开始,而那些导致其进展的机制仍不确定。我们认为,通过转译和介入研究,确定IPF和其他纤维化性ILDs常见的器官纤维化发展和进展的机制,提供了一条更有说服力的前进道路。经过20多年的经验与大型多中心IPF试验,我们断言,一个严格的方法,要求新发现的疾病修饰治疗的功效必须证明了控制数据在每个ILD,是不现实的,效率低下,可能剥夺non-IPF IPF患者类似的临床过程。与肿瘤学中的一揽子试验设计类似,在药物研究中对具有进行性纤维化表型的非ipf患者进行分组,如正在进行的nintedanib和吡非尼酮在进行性纤维化(合并非ipf疾病)患者中的试验[87,88],提供更科学的理性方法。
分裂和集总最好被看作是互补的方法。诊断生物标记物,被认为是特异性的IPF或其亚群体,应该理想地检查,以对抗疾病进展的其他纤维化的ILDs。同样,在IPF中显示有预后价值的生物标记物,从而定义IPF亚组,也应该在伴有纤维化肺疾病的非IPF患者中进行研究。在这方面,结节和分裂最好被视为纤维化性ILD发病思维的阴阳。
结论
总而言之,我们认为应保留“指规数”一词,但认识到这是一个不断发展的领域。随着对不同的疾病亚群和可能也存在于其他纤维化性ILDs的关键病理生物学途径的新认识的产生,目前对IPF的理解肯定会增加。目前关于更改名称的争论从根本上说是没有说服力的,目前主要关注的是更改名称的不良后果。千年后达成的术语协议是对指规数的理解和管理方面的主要进步之一,总结如下表3[1,3.,7,8,19,38,89- - - - - -105].我们认为,更重要的举措是扩大我们的定义,探索进展性纤维化表型,同时保留IPF作为与其他进展性纤维化ILD形式的比较指标。
脚注
指规数协商一致工作组:K.M.安东尼奥由于,j . Behr P.B. Bitterman, C.D.酷,Costabel,电视科尔比,诉Cottin, b,伽马安基丁酸几何级数唐尼,j . Gauldie Groshong,时任a德J.C.霍洛维茨y Inoue, J.A.斯基,A.H.资金流,D.A. Lynch F.J.马丁内斯,J.L.迈尔斯A.G.尼克尔森诺斯,诉Poletti C.J.瑞尔森,J.H. Ryu, d . Valeyre c . Vancheri静电的白色。
利益冲突:A.U. Wells报告了Intermune/Roche、Boehringer Ingelheim和Bayer的咨询和讲座个人费用,以及吉利德的咨询个人费用。
利益冲突:K.K. Brown报道,NHLBI的多项肺纤维化拨款,阿斯利康、百健保、Fibrogen、Galecto、吉利德、MedImmune、诺华、Aeolus、ProMetic、Patara、Third Pole、aTyr、Galapagos和Boehringer Ingelheim的个人费用,已向罗氏/Genentech提交拨款,并仅与Global Blood Therapeutics和Genoa进行了CDA对话。提交的工作之外。
利益冲突:K.R. Flaherty报告了勃林格殷格翰(Boehringer Ingelheim)和罗氏/基因泰克(Roche/Genentech)的拨款和个人费用,Afferent的拨款,Veracyte、Fibrogen、Immuneworks、Aeolus、Pharmakea、赛诺菲-健酶(Sanofi-genzyme)和Celgene的个人费用。
利益冲突:M. Kolb报告了来自罗氏、勃林格殷格翰、葛兰素史克和普罗默的拨款和个人费用,来自吉利德和热那亚的个人费用,以及来自Actelion、Respivert、Alkermes和Pharmaxis的拨款。
- 已收到2018年4月11日。
- 接受5月1日2018年。
- 版权所有©ers 2018