文摘
细胞衰老永久逮捕各种细胞类型的复制和有助于与年龄有关的疾病。特别是,细胞衰老可提高慢性肺疾病包括慢性阻塞性肺病和特发性肺纤维化。然而,细胞衰老的病理生理学中所起的作用急性炎性疾病,特别是病毒感染,不太清楚。有证据表明,细胞衰老阻止病毒复制通过增加抗病毒细胞因子,但其他证据表明,衰老可能通过下调抗病毒信号增强病毒复制。此外,细胞衰老导致炎症介质的分泌,这可能会促进宿主防御或加剧在病毒感染免疫病理。在这个角度看篇文章中,我们总结如何衰老导致生理和疾病、慢性肺疾病衰老的作用,衰老如何影响急性呼吸道病毒感染。最后,我们开发一个潜在的框架如何衰老可能贡献,正面和负面,病毒性呼吸道感染的病理生理学,包括冠状病毒导致的严重急性呼吸系统综合症SARS-CoV-2。
文摘
与肺纤维化疾病衰老的同事。新兴疗法减少衰老可能治疗慢性肺部疾病,但衰老期间急性呼吸道病毒感染的影响还不清楚,需要未来的调查。https://bit.ly/2SAPpx6
细胞衰老:定义和进化起源
细胞衰老了永久的复制的逮捕在正常增殖的细胞。最初发现的在体外人类成纤维细胞的Hayflick和同事(1,2),细胞衰老的概念引起了争论。起初,一些研究者认为衰老是一个持怀疑态度在体外人工制品。但随着积累在活的有机体内证据,包括在年龄在人类皮肤细胞衰老的存在3),科学家接受衰老是一个真正的生物现象。衰老目前所知为各种老年性疾病,包括2型糖尿病、肥胖、动脉粥样硬化、慢性阻塞性肺病、肺纤维化等(4- - - - - -6]。与衰老,我们的细胞不断分裂,缩短端粒和积累突变和DNA损伤,所有这一切最终增加肿瘤形成的可能性(7,8]。
在典型的生理条件下,oncogene-induced衰老可能会阻碍某些癌症的发展包括淋巴瘤(9)和前列腺癌(10和改善病人的化疗反应11]。此外,衰老细胞可能上调吞噬受体,因此增加吞噬作用和免疫监视减少癌症发展。此外,衰老细胞分泌细胞外基质蛋白和生长因子,导致一些恢复过程包括伤口愈合(12]。同样,衰老细胞被证实能够减少肝脏(13,14和胰腺纤维化和促进伤口愈合15]。此外,成纤维细胞衰老由matricellular蛋白CCN1限制纤维化在皮肤的伤口16]。衰老细胞可能导致组织生长在胚胎发育阶段(17,18]。总之,衰老可能进化的急性应激应对器官发展,减轻对受损细胞的急性影响返回组织内稳态,并最终减少癌症的发展(19]。
改善公共卫生在20世纪和后续扩展人类的寿命,衰老已成为一些慢性与年龄有关的疾病的因素。的确,我们现在认识到衰老作为老化的关键特征之一,当衰老发生随着年龄的自然(20.]。虽然衰老的一个重要标志,衰老是不够的对所有衰老表型(20.),衰老可以发生在年轻的主机由于急性压力(见下一节)。然而,在急性炎症条件下衰老的重要性,特别是呼吸道病毒感染,不太欣赏。在这里,我们首先简要回顾一下如何衰老导致慢性炎症,尤其是在肺部疾病的背景下,新兴疗法治疗衰老。然后,我们讨论衰老作用在急性呼吸道病毒感染和影响这样的角色在感染严重急性呼吸系统综合症冠状病毒2 (SARS-CoV-2)。
什么导致衰老和由此产生的senescence-associated分泌表型?
衰老可能出现重复的细胞分裂和细胞的压力。复制衰老来自多次细胞分裂,这自然发生当我们的年龄。压力诱导衰老来自细胞压力增加等活性氧(ROS),这与DNA损伤(21,22]。化疗药物,这些可以从辐照结果慢性暴露于污染物(香烟),暴露于病原体和某些形式的加速老化症状,如早衰症(23- - - - - -26]。因此,细胞年轻和老主机都可以表现出衰老。如前所述,衰老是老化的关键生物特征之一,有助于老化通过炎症,疲惫和受损组织干细胞更新(20.]。
重要的是,干细胞可以随着我们的长大而变得衰老。具体来说,旧的人类间充质干细胞分离(> 70岁)表现出衰老包括扩散和检查参与组成分泌腺慢性炎症,减少损害造血干细胞和祖细胞(公司)复制和增加公司单核细胞化学引诱物蛋白1和白介素8 (IL)表达(27]。因此,衰老间充质干细胞不能用于干细胞疗法由于无法增殖和减少表达pro-angiogenic因素(28]。此外,神经祖细胞衰老导致多发性硬化的发展(29日]。具体来说,衰老神经祖细胞抑制少突细胞分化和导致脱髓鞘通过生产的高机动组框(HMGB) 1,抑制少突细胞祖细胞增殖和诱导炎性转录组变化少突细胞祖细胞(29日]。因此,干细胞衰老影响伤口愈合,促进炎症的发展,限制使用干细胞治疗应用。
除了直接作用于干细胞,有两个潜在通路的衰老可能导致疾病。首先,衰老细胞停止增殖,从而防止组织损伤后修复。第二,随着衰老细胞积累,他们生产,不清楚原因,低水平的炎症介质,这种现象被称为“inflammaging”,尤其是老年人明显(30.- - - - - -33]。衰老细胞导致慢性炎症通过senescence-associated分泌表型(SASP)、集体的促炎症趋化因子和细胞因子释放的衰老细胞(34]。SASP由许多炎性分子,包括肿瘤坏死因子(TNF) -αIL-1α/β,il - 6,引发,CC-chemokine配体(CCL) 2和其他人(35- - - - - -38]。SASP似乎是一把双刃剑。一方面,长期接触的SASP炎症介质可能导致破坏免疫细胞对于招聘活动,导致慢性炎性疾病,甚至纤维化(5,39]。另一方面,在短期内,SASP促进伤口愈合需要应对急性细胞损伤(12,13,40]。
重要的是,的具体特征SASP可能依赖于细胞类型和衰老的机理归纳41]。例如,SASP与成纤维细胞包含SASP因素明显多于SASP与肾上皮细胞(41]。一些SASP通路之间共享成纤维细胞和上皮细胞,而一些途径是不同的细胞类型。具体来说,衰老上皮细胞移植途径与蛋白质翻译和退化;衰老成纤维细胞移植途径与细胞凋亡有关,ROS生成和细胞外基质重组;衰老成纤维细胞和上皮细胞移植途径与囊泡运输、代谢和解毒41]。注意,在这个研究中,衰老是诱导在体外在人类细胞系。不过,调查人员发现几个分泌蛋白质的在体外模型也发现老年受试者中等离子体的,这表明这个研究的发现可能是可译的在活的有机体内。在体外衰老与无菌炎症介质的积累有关,像HMGB1核蛋白质可以激活炎症(41]。此外,SASP介质如TNF-α可以诱导衰老,这可能进一步提高SASP前馈回路(42]。因此,衰老的机制之一,导致慢性炎症可能通过无菌炎症介质的释放,也称为分子模式有关。此外,SASP是暂时的动态和动态变化根据细胞类型(43]。总的来说,衰老引发不同的细胞项目,导致蛋白质的分泌,促进慢性炎症。显然,解剖的生理衰老的病理生理方面的发展需要有效的针对衰老缓解与年龄有关的症状的治疗疾病。
Senescence-targeted疗法
最近,有专注于减轻使用senescence-targeted治疗细胞衰老的负面影响。这样的治疗分为两个主要类别:SASP抑制和清除衰老细胞。SASP抑制包括下调SASP的各种组件,或抑制炎症通路SASP因素参与,与改善的目标SASP的有害的影响因素。这种策略在各种环境中成功。例如,Janus激酶抑制减轻炎症,局部脂肪组织和全身,减少脆弱在老年小鼠44]。证据表明SASP可能与年龄相关疾病的发病机理来自报道,药理工具来抑制NF-κB信号改善与年龄相关的疾病。抑制哺乳动物雷帕霉素靶的雷帕霉素有选择地减少NF-κB信号(主要炎症信号中心)衰老细胞通过抑制IL-1α活动,减少与年龄有关的认知能力下降,改善老年人的免疫功能,增加小鼠的寿命(45- - - - - -49]。常用的抗2型糖尿病药物二甲双胍,还能抑制NF-κB,导致改善小鼠的寿命,并降低全因死亡率和与年龄相关的疾病在人类50- - - - - -53]。然而,抑制SASP导致脱靶的副作用包括嗜中性、肾毒性和t细胞表型的变化由于无数相互联系的通路参与炎症信号(54]。具体来说,抑制NF-κB通路,通过基因缺失或小分子抑制,可以抑制t细胞、b细胞和淋巴祖细胞发展(54,55];诱导细胞凋亡胸腺细胞,b细胞和巨噬细胞56,57];影响淋巴细胞的生长和细胞因子的生产58];和潜在的增加对各种感染(59]。所有这些策略目标衰老可能激活的炎症通路,但不要专门针对衰老细胞。
清除衰老细胞包括直接针对衰老细胞诱导细胞凋亡。第一个治疗旨在直接杀死衰老细胞(称为“senolytics”)有针对性的bcl - 2蛋白家族,一个抗凋亡途径参与肿瘤形成。然而,研究最广泛的治疗策略是一种酪氨酸激酶抑制剂的联合治疗涉及管理达沙替尼(D)和类黄酮素槲皮素(Q)。”D + Q”组合减少衰老细胞的负担和提高健寿和老年小鼠的寿命,降低血管硬化,改善血管舒缩功能,改善肺功能在小鼠肺纤维化模型60- - - - - -64年]。的确,初步临床试验证据表明,D + Q治疗减少衰老细胞的负担,可以改善患者的身体功能肺纤维化(65年,66年]。然而,我们还不完全了解的潜在脱靶效应senolytic代理如D + Q,以及他们的作用机制在人类,这就需要说明之前可用于治疗老年性疾病。
在肺癌细胞衰老
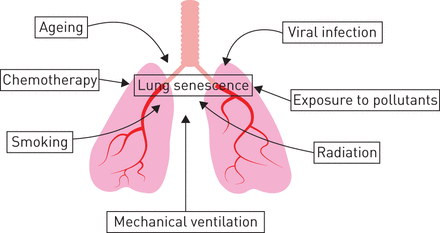
除了复制衰老引起的老化,一些其他因素导致肺部压力诱导衰老的发展,包括放射治疗、吸烟、机械通风和长期使用补充氧气(图1)[24,67年- - - - - -70年),支持其他进程除了自然老化导致衰老。越来越多的衰老细胞浓度增加与SASP因素。这是支持的发现,细胞因子il - 6和il - 10和中性白细胞计数升高在支气管肺泡灌洗液的捐助者(注:“老”是指定的年龄> 65年综述),肺(可能出现衰老的71年]。这与年龄相关的表型与年龄相关的肺部疾病,如慢性阻塞性肺病。此外,COPD患者表现出浓度的增加衰老II型肺泡上皮细胞(72年,73年)和肺成纤维细胞(74年),以及高浓度的炎性细胞因子包括IL-1β,il - 6,引发,il - 10和CCL-2 [75年- - - - - -78年]。虽然很难证明因果关系,慢性炎症引起的肺衰老细胞可能导致慢性阻塞性肺病和/或加剧的发展。相似的炎性细胞因子水平升高和衰老细胞与其他慢性肺部疾病如哮喘(79年,80年]。此外,旺盛的愈合反应由SASP因素,加上无法有效地修复组织由于停止增殖,并可能损伤干细胞功能,促进纤维化,可能导致特发性肺纤维化(81年- - - - - -84年]。因此,肺衰老细胞可能导致许多慢性肺部疾病的严重程度。
肺衰老的原因。许多因素导致肺细胞内衰老的感应。除了自然衰老,衰老的其他来源的包括慢性接触污染物和香烟烟雾、化疗、电离辐射、呼吸道病毒感染和呼吸机的使用。这些来源可能不同程度的诱导衰老,衰老,目前尚不清楚是否来自不同来源和不同细胞有助于病理相似或不同。
肺细胞衰老的潜在贡献在急性呼吸道条件尚不清楚。在急性肺损伤的小鼠模型,衰老肺泡巨噬细胞表现出增强的激活和促炎细胞因子的分泌,导致增强疾病严重程度(85年]。同样,老老鼠,它可能表现出增强的肺衰老,表现出增强肺通透性和增加活性氧的水平,以应对脂多糖的挑战,与缺乏Nox4 (ROS-generating线粒体蛋白质)ubiquination [86年]。此外,老年创伤患者更容易患上急性呼吸窘迫综合征(ARDS)及以上ARDS患者表现出更高的死亡率(87年]。然而,在所有这些研究衰老的病理作用没有测试。此外,最近的一项研究发现,肺细胞衰老预防机械通气引起的肺损伤,防止细胞凋亡(68年]。显然,在急性肺细胞衰老的影响条件要求未来的调查。
细胞衰老和呼吸道病毒感染
冠状病毒病2019年(COVID-19)大流行继续声称每天成千上万人的生命,老年人居多。有鉴于此,细胞衰老如何影响急性呼吸道病毒感染的宿主反应是特别相关的。老年人的经验增加易受呼吸道病毒如流感、呼吸道合胞体病毒(RSV),非典和现在SARS-CoV-2 (88年- - - - - -92年]。COVID-19,结果从SARS-CoV-2感染的疾病,老年人∼20倍比年轻人更有可能死(93年]。这种效应部分归因于缺陷与衰老相关的免疫系统,称为“免疫衰老”,这是不同于经典的细胞衰老之前定义和他处94年- - - - - -96年]。简单地说,免疫衰老有多效性的影响免疫系统包括1)造血干细胞的增殖能力下降;2)先天免疫失调;3)与胸腺退化的幼稚t细胞数量减少;4)积累记忆T - b细胞;,5)和T - b细胞功能下降(94年,97年- - - - - -99年]。具体地说,两个CD4+和CD8+从年龄主机t细胞(如。啮齿动物,人类)表现出降低表面costimulatory差别增殖能力与对这些受体,CD27和CD28伴随着缩短端粒长度。总的来说,这些改变在老化导致能力受损的免疫系统对抗病毒感染和导致减少疫苗效率(90年]。除了自然老化、慢性病毒感染(如。艾滋病毒、巨细胞病毒感染)诱导t细胞功能下降的表型(即。减少增殖和细胞因子分泌)与免疫衰老(相同的特征One hundred.,101年]。虽然衰老免疫系统的损害宿主防御急性呼吸道病毒感染(90年),细胞衰老的作用,肺细胞在急性呼吸道病毒感染的病理生理学是不清楚。很明显,老年人是很容易被病毒感染由于无数老化施加于免疫系统的影响。但这是由细胞衰老,正如前面定义的,还有待阐明。事实上,目前尚不清楚细胞衰老,由于自然老化或由于age-independent压力源,促进或阻止急性呼吸道病毒感染。我们所知,只有少数研究细胞衰老和急性呼吸道病毒感染的作用,有一些显示对比的结果。
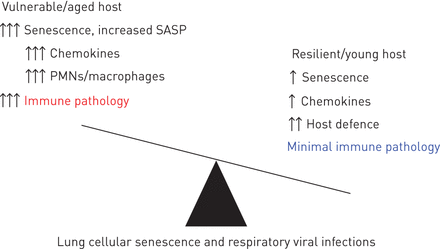
有研究认为细胞衰老增强抗病毒免疫(102年生物),这是合理的,SASP因素,包括趋化因子(如。CxCL1/2吸收先天免疫细胞,如中性粒细胞),可能会增加宿主防御病毒感染(103年]。具体地说,一项研究表明,细胞衰老抑制疱疹stomatis病毒(一种RNA病毒)复制主要与replication-induced衰老小鼠成纤维细胞和肿瘤细胞衰老与化疗所致[102年),可能由于SASP因素,包括释放的I型干扰素(IFN),重要的抗病毒细胞因子(104年]。此外,老鼠诱导肺内表现出衰老通过博来霉素接触疱疹stomatis病毒感染有抵抗力在活的有机体内比老鼠没有暴露于博来霉素。这是兼容在体外研究发现,I型干扰素,除了其他SASP组件如il - 6和引发,引起细胞衰老(105年,106年),而反之亦然。此外,细胞融合fusogenic麻疹病毒诱导细胞衰老引起的,包括SASP因素的释放,在成纤维细胞在体外(107年),虽然在活的有机体内这个结果的影响还不清楚。总的来说,这些研究表明,衰老是由病毒诱导强烈的可能是一个身体的一部分的抗病毒免疫反应108年,109年]。这种防御机制可能已经进化到允许病毒感染细胞分泌SASP因素限制病毒复制在邻近的细胞,最终整个肺病毒传播。此外,SASP因素可能通过促进免疫细胞增强宿主防御招聘到肺。但如果这些SASP因素产生生气勃勃地,免疫病理可能接踵而来(图2)。最后,一些病毒,包括人类乳头状瘤病毒和乙型肝炎、进化机械专门来克服细胞衰老(110年,111年),这表明衰老在抗病毒防御中发挥作用在某些情况下。
假说:衰老可能扮演不同的角色在急性呼吸道病毒感染取决于主机韧性。在年轻的主人,病毒感染引起的衰老可能发挥积极作用通过招募中性粒细胞(中性粒细胞)和其他免疫细胞通过senescence-associated分泌表型(SASP),导致病毒性间隙和组织修复。然而,在年龄或脆弱的主机,病毒感染引起的衰老,除了衰老已经存在,也会使平衡朝着病理学。这病理学的特点是一个旺盛的免疫反应,包括高水平的SASP细胞因子和趋化因子,导致夸大招募中性粒细胞和其他免疫细胞,导致肺组织损伤。
然而,有证据表明,衰老导致呼吸道病毒感染的病理生理学。RSV引起DNA损伤导致衰老的单核细胞和肺上皮细胞在年轻的老鼠25],它增强了气道组织改造(展出的纤毛细胞和分泌细胞的增加(112年),可能导致永久性的组织损伤和纤维化。而且,衰老细胞可能促进病毒复制。例如,流感病毒复制衰老人类支气管上皮细胞内更有效地比non-senescent细胞(113年]。也发现了类似的结果水痘带状疱疹病毒,疱疹病毒,更有效地复制在人类衰老真皮成纤维细胞比nonsenescent细胞(113年]。一个潜在的解释这一现象可能是这些病毒引起的衰老会使抗病毒I型干扰素项目,包括关键信号蛋白,如。刺痛和干扰素监管因素3、感染在体外水痘病毒(113年]。可能导致减少差别这对这些抗病毒干扰素的分泌,促进病毒复制。然而,尚不清楚这是否发生在活的有机体内。本研究之间的差异和对比前面所讨论的,从而发现衰老减少水泡stomatis病毒的复制102年),可能是由于使用的不同的病毒(即。水泡性口炎与流感、水痘),不同的细胞类型(MCF7, A549细胞株和初级水泡性口炎小鼠胚胎成纤维细胞的研究与主要人类支气管上皮细胞原代人真皮成纤维细胞和流感/水痘研究),和不同方法诱导衰老(复制衰老和博来霉素水泡性口炎的研究与只复制衰老流感/水痘研究)。显然,未来的研究需要确定衰老是有害的或有益的病理相关的呼吸道病毒。
呼吸道病毒感染的细胞衰老:朋友还是敌人?
细胞衰老的总体影响急性呼吸道病毒可能取决于主机弹性因素(图2)。例如,SASP可能增强宿主防御通过增加免疫细胞的招募。这可能是有益的在弹性年轻主机不过度生产SASP因素。事实上,最初的中性粒细胞招募肺是流感感染的宿主防御的关键(103年]。但在脆弱主机岁SASP因素可能产生异常高水平促进免疫病理学。特别是CXCL-1, CXCL-2 IL-17增加老年小鼠的肺病毒感染之前,和伴随中性粒细胞招募到肺过度提高死亡率在急性流感感染(103年]。在这项研究中,发现衰老肺泡上皮细胞产生更多的中性粒细胞化学引诱物,从而增加中性粒细胞趋化性。同样,恒河猴表达更高水平的CCL-2岁il - 6和应对流感引发肺部感染,建议一个夸张的先天免疫反应(114年]。基于这些研究,抑制SASP或减少肺衰老细胞可能是有益的年龄主机感染了急性呼吸道病毒感染。然而,正式调查之前需要确定清除衰老细胞感染是充分的,或如果在感染治疗是必需的。重要的是,脆弱的主机,包括老年人和并发症如糖尿病患者,更容易受到SARS-CoV-2,新兴研究表明是由于细胞激素风暴和过度肺内中性粒细胞效应函数(90年]。
我们仍然不知道是否衰老细胞在肺最终增加或减少病毒复制。呼吸道病毒可能“劫持”衰老机制在感染细胞内表达下调干扰素通路促进病毒包装,最终提高细胞内的病毒复制。如果发生这种情况,目前还不清楚在活的有机体内如果是这样,潜在的机制。相比之下,一个病毒感染细胞内激活衰老机械可能损坏反应机制,导致抗病毒细胞因子的分泌限制病毒复制,未来还需要调查的问题。另外,衰老可能只是病毒感染的副作用;在感染后,各种炎性细胞因子调节,导致衰老的感应感染细胞。
结论
最终,衰老对呼吸道病毒感染的影响公司的结论之前,还需要进一步调查。衰老的影响病毒的复制和死亡率在流感等呼吸道病毒感染,RSV,非典和SARS-CoV-2应该综合研究确定senescence-targeted疗法,如senolytics,可能是有效的,不信,减少急性呼吸道病毒感染的年龄相关性死亡。此外,目前尚不清楚是否衰老与自然老化的结果影响呼吸道病毒感染与压力诱导衰老;因此,这样的模型之间的直接比较衰老是十分必要的。例如,做小鼠bleomycin-induced肺衰老表现出相似的表型和死亡率应对老年小鼠感染流感,RSV或其他呼吸道病毒感染吗?
此外,senescence-targeted疗法的有效性(或缺乏),和senolytics,具体地说,尚未评估在呼吸道病毒感染。虽然senolytics显示一些治疗效果在慢性疾病如肺纤维化的临床前模型,它是未知的如果这些效应转化为更多的急性病,如果是这样,如何优化治疗方案。例如,它可能是预防senolytic治疗是有效地减少总肺衰老细胞浓度,从而提高疾病的结果,在感染后治疗可能不是那么有效,特别是如果清除衰老细胞损害伤口愈合,减少炎症的决议。检查这些问题将阐明衰老如何影响我们呼吸道病毒的宿主防御,这将继续不成比例地影响老年人在可预见的未来,特别是在当前COVID-19大流行。因此,前进,重大研究成果集中在细胞衰老和呼吸道病毒感染之间的相互作用显然是必要的。
可共享的PDF
脚注
作者的贡献:所有作者参与的设计审查。j•凯利写了初稿,然后编辑湄Goldstein和R.L.泽曼。所有作者同意最后的手稿。
利益冲突:j•凯利没有披露。
利益冲突:R.L.泽曼没有披露。
利益冲突:湄戈尔茨坦没有披露。
支持支持声明:j•凯利格兰特T32HL007622国立卫生研究院培训。湄Goldstein支持NIH奖:R01AG028082 R01HL127687, R01AI13834, K07AG050096 T32AG062403。R.L.泽曼支持NIH奖:R01HL147920 R01HL131608 R01AG028082。资金信息,本文已沉积的Crossref资助者注册表。
- 收到了2020年7月9日。
- 接受2020年9月30日。
- 版权©2020人队
这个版本分布在创作共用署名非商业性许可证的条款4.0。