摘要
背景积累的数据表明,较高的利福平剂量更有效,并缩短结核病治疗时间。本研究评估了增加剂量利福平的安全性、耐受性、药代动力学以及7天和14天早期杀菌活性(EBA)。在这里,我们报告了PanACEA HIGHRIF1的最终队列结果,这是一项针对未接受治疗的涂片阳性成人结核病患者的剂量递增研究。
方法在连续队列中,患者接受40或50 mg·kg−1利福平单药治疗每日1次(第1-7天),8 - 14天补充标准剂量异烟肼、吡嗪酰胺和乙胺丁醇。
结果在40毫克·公斤−1队列(n=15), 13例患者在单药治疗期间共发生36例不良事件,导致1例治疗中断。在50毫克·公斤−1队列(n=17),所有患者在单药治疗期间发生不良事件,共93例;11名患者退出或停止了研究用药。不良事件多为轻度/中度和耐受性,与安全性无关,即。胃肠疾病、瘙痒、高胆红素血症和黄疸。在0 ~ 12 h的血药浓度-时间曲线下,利福平的几何平均面积(AUC)有超过比例的增加0-24 h)为50 mg·kg−1与40 mg·kg相比−1;571 (320 - 995)与387(量程201-847)mg·L−1·h,而峰值暴露呈比例增加。50 mg·kg后蛋白游离暴露−1(11%(范围8-17%))与低剂量利福平相当。利福平暴露与胆红素浓度相关(第3天的Spearman ρ值=0.670,p<0.001)。EBA随剂量增加而显著增加,在50 mg·kg时达到最高−1: 14天EBA−0.427 (95% CI−0.500 -−0.355)log10CFU·毫升−1·天−1.
结论虽然与增加杀菌效果有关,50 mg·kg−1剂量耐受不良。利福平40 mg·kg−1耐受性良好,因此被选为IIc期缩短治疗试验的评估对象。
摘要
虽然杀菌活性随着剂量的增加而继续增加,但我们首次发现了50 mg·kg剂量利福平的剂量限制不耐受性−1;40毫克·公斤−1似乎是结核病缩短治疗试验中评估的最佳耐受剂量https://bit.ly/37dUIuB
介绍
1971年,美国食品和药物管理局批准了关键的结核病(TB)药物利福平,剂量为10 mg·kg−1.推荐剂量的选择是基于它以最低成本有效并受到对副作用的恐惧的限制[1].一项评估最大耐受剂量(MTD)的剂量发现研究尚未进行。
在体外小鼠模型显示,更大剂量的利福平与更强的杀菌和杀菌活性有关,这表明有可能缩短肺结核的治疗时间[2- - - - - -4].终结结核病战略为到2025年治疗覆盖率设定了高达≥90%的目标,这将增加诊断为结核病的患者人数,并将利福平作为其结核病治疗方案的一部分接受治疗的人数,强调了优化这一关键药物剂量的紧迫性[5].总的来说,利福平预计将继续在结核病治疗中发挥基础性作用。
PanACEA HIGHRIF1对非洲肺结核患者的研究表明,剂量可达35 mg·kg−1服用两周后,与10 mg·kg相比,平均暴露量增加了9倍−1[6,并且安全,耐受性良好。药代动力学/药效学模型表明,利福平暴露增加可能与早期杀菌活性(EBA)增加有关[7,8].在一项涉及365名患者的更大规模的研究中,高剂量利福平(35 mg·kg)−1)联合异烟肼、吡嗪酰胺、乙胺丁醇,经较长时间使用3个月,可缩短肺结核患者痰培养转化时间[9].
鉴于这些发现,迫切需要评估利福平增加剂量的安全性、耐受性、药代动力学和EBA,以确定最佳剂量。为了完成这项任务,我们扩展了HIGHRIF1研究(ClinicalTrials.gov:NCT01392911),包括40和50 mg·kg的受试者−1利福平。
方法
研究设计和参与者
我们进行了一项开放标签、II期、多剂量范围的研究,以评估40和50 mg·kg的安全性、耐受性、药代动力学以及7天和14天早期EBA−1利福平。研究纳入了新诊断、以前未经治疗、药物敏感和痰涂片阳性肺结核且无医学禁忌症的成人(年龄18-65岁)。患者在南非开普敦的两个研究地点之一住院治疗。我们招募了15名连续队列受试者,他们接受利福平单药治疗7天,并补充标准剂量的异烟肼(5 mg·kg)−1)、吡嗪酰胺(25-30 mg·kg−1)和乙胺丁醇(15-20 mg·kg−1)在第8-14天。然后患者继续使用标准剂量的所有药物进行结核病治疗。研究药物为体重束带(补充图E1),并在早上与一份简单的早餐和一杯水一起服用。在完成每个队列后,试验指导委员会(TSC)进行了安全性审查,以评估是否可能增加剂量或是否评估MTD。MTD被定义为低于产生不可接受但可逆毒性的剂量水平,并被认为是患者耐受的上限。该研究方案由适用的伦理审查委员会和南非卫生产品监管局批准,并根据国际和南非良好临床实践指南进行。有关先前HIGHRIF1队列的资格标准和结果的详细资料已在其他地方发表[6].
安全性和耐受性
每天进行症状评估和身体检查,包括生命体征。在基线和第1、3、6、10、14和21天进行了血液学、肾功能和肝功能测试、葡萄糖、尿酸和尿液分析以及心电图。不良事件根据美国国家卫生研究院不良事件通用术语标准4.0版本进行分级,并由现场调查者评估为与研究治疗无关,可能或肯定相关[6].严重不良事件被定义为研究者认为导致死亡、危及生命、需要住院(延长)、导致持续或严重残疾/丧失能力或在医学上具有重要意义的任何不利医疗事件。TSC的会议,讨论研究的延续或终止将如果两个受试者经历三年级相关不良事件评估可能或肯定政府高剂量的利福平,还是经历4或5级不良事件评估肯定与利福平,会在一组中发生。
药物动力学
在给药前和利福平摄入后0.5、1、1.5、2、3、4、6、8、12和24 h采血,并在第7天和第14天采用标准化膳食,以获得完整的药代动力学资料。每个队列后测定利福平总(蛋白结合+蛋白非结合)和蛋白非结合血浆浓度。血浆样本为40 mg·kg−1使用与前一队列相同的验证过的超高效液相色谱紫外检测方法分析剂量组[6].50毫克·公斤−1使用广泛验证的液相色谱-质谱(LC-MS/MS)多药分析方法分析抗结核药物的总浓度。利福平定量的准确度为94.24 ~ 102.06%;误差范围为0.9% ~ 4.89%。发生利福平蛋白非结合检测通过如前所述的超滤[10].如前所述,使用Phoenix WinNonlin 6.4版本(Certara, Princeton, NJ, USA)进行非室性药代动力学分析[11].50 mg·kg中未结合的部分−1以0 ~ 12 h血浆浓度-时间曲线下的未结合面积(AUC)计算0-24 h)的总AUC0-24 h这一组的所有受试者。生物分析和药代动力学分析的完整描述在补充材料.
抗细菌的活动
在基线、每日至第7天、第9天和第14天收集过夜(16小时)的痰标本。采用BACTEC MGIT 960 (BD, Franklin Lakes, NJ, USA)分枝杆菌生长指示管系统,样品在选择性的Middlebrook 7H10S琼脂板和液体培养基上进行培养。在入组前、研究治疗开始后第19天和12周采集痰液斑点标本,准备金胺o染色直接镜检和快速耐药检测通过Xpert MTB/RIF (Cepheid, Sunnyvale, CA, USA)分析。如前所述,所有微生物检测均在Stellenbosch大学(南非开普敦)医学和健康科学系医学生物化学系进行[12].
统计分析
这是一项描述性研究,没有推理统计或假设检验[6].
每组15例患者的计划样本量与该类型的其他试验保持一致,并估计每组有3例患者中途退出。MGIT上的时间正态分布(TTP)是正偏态的,对数变换后的TTP更接近对称正态分布。以来访日作为离散随机效应的混合效应模型被用来估计平均对数10CFU和日志10TTP在每个治疗组每次来访时描述数据。正如我们之前的研究[6,我们发现,在治疗时间较短的情况下,阴性培养的数量出乎意料地高。为了包括这些被审查的观察,Tobit回归[13]用来估计14天的EBA,使用检测审查下限来计算阴性培养物10CFU为1,TTP上限为42天。对每个患者采用单独的模型进行拟合,参数估计由治疗组使用一个随机效应模型,该模型考虑了患者内部和患者之间的变异性。我们担心第5天未培养的患者的数据夸大了CFU随时间的下降或TTP增加的估计。考虑到这些早期停药,排除了这些患者的数据,以解释在50 mg·kg的随访中损失的原因−1在另一项分析中。敏感性分析包括按照计划对全部数据进行分析,并采用一阶段混合效应模型,允许审查负面文化,以评估结果的稳健性。
安全人群包括所有服用至少一剂试验药物的参与者。暴露与肝脏实验室评估之间的关联采用Spearman秩相关法。此外,评估了单药治疗期间的剂量-暴露-耐受性关系事后通过一个有序的分类模型,估计在服用利福平剂量和暴露的情况下出现无、一、二、三或更多不良反应的概率。在这些分析中,血浆总暴露量(AUC)0-24 h)作为研究中利福平暴露的测量指标。所有与耐受性相关的不良事件的系统器官分类都被纳入分析(见补充表E2详情)。
使用Stata版本15.1 (StataCorp, College Station, TX, USA)和NONMEM版本7.4 (Icon Development Solutions, Ellicott City, MD, USA)进行分析。
结果
病人
以40 mg·kg为组,15例结核菌培养阳性肺结核患者−1其中14例患者完成了研究。一名患者因肝酶升高而停药。在50 mg·kg剂量组共纳入17例患者−1队列。该队列的招募暂时暂停,以进行TSC对中期数据的审查。9例(53%)患者早期退出了50 mg·kg−1组:单药治疗7例,联合治疗2例。另一名患者从第11天开始停止治疗,但完成了研究访问(不包括药代动力学评估),等待中期TSC审查结果,另一名患者从第10天到第12天中断了3天的剂量。病人的特征显示在表1.
安全性和耐受性
15名患者开始服用40 mg·kg−1利福平,13例(87%)报告了单药治疗期间的不良事件(总共36例)。所有17例患者在50 mg·kg−1队列报告了单药治疗期间的不良事件(总共93个事件)。看到表2概述40和50 mg·kg单药和联合治疗期间的不良事件及其严重程度−1组及以前的剂量组[6].40和50 mg·kg组的不良事件−1队列大多是轻度/中度,即。在两个队列中,单药治疗期间所有不良事件的97%为1/2级。此外,不良事件与耐受性无关,与安全性无关,即。胃肠疾病、瘙痒、高胆红素血症和黄疸。在这两个队列中均未发生4级或5级不良事件。
最常见的不良事件发生在40和50 mg·kg−1队列包括胃肠道疾病(1-2级)、高胆红素血症(1-3级)、瘙痒症(1-2级)和黄疸(50 mg·kg)−1只有利福平,1-2级),所有预期来自利福平。总的来说,50 mg·kg−1队列包含更多胃肠道疾病病例(12例(71%)与7例(47%)患者在单药治疗期间)、高胆红素血症(10例(59%)与4例(27%)和黄疸9例(53%)与零病人)。在利福平开始使用后的第3-4天左右,胆红素升高(1-3级)达到高峰(补充图E6).看到补充表E2和E3在单药治疗和联合治疗中,两组每个系统器官分类的不良事件发生率的概述。
在40毫克公斤−1联合治疗后,4例患者出现3级不良事件。在四名患者中,有一名患者被定义为与高剂量利福平(高尿酸血症)无关,而在四名患者中,有三名患者被定义为可能相关(n=1名高尿酸血症,n=2名肝酶升高)。对这些不良事件的TSC评估认为,这些3级不良事件要么不是大剂量利福平的典型(n=2高尿酸血症),要么被认为与大剂量利福平无关或仅可能相关(转氨酶增加仅在联合治疗后出现)。尽管如此,转氨酶升高被归类为“严重不良事件”,一名患者被撤药,尽管没有立即危及生命的风险。所有3级不良事件均已解决。
而50 mg·kg组未发生严重不良事件−1队列中,有9人提前撤离。其中4人因不良事件被研究者从研究中撤出(如。2级胆红素升高),5名患者因为社会/个人原因而撤销了同意书,研究者和TSC假设这与经历的不耐受有关。此外,1例患者在10 - 12天期间因不耐受而停止研究治疗。
基于50mg·kg的不良反应发生率高和多次停药−1TSC评估50 mg·kg−1剂量不耐受,为40 mg·kg−1剂量被视为MTD。TSC认为40 mg·kg的安全性−1利福平是可接受的,大多数是轻/中度和可逆的,因此40 mg·kg−1被认为是MTD。此外,安全性与35 mg·kg相当−1,在一项随机对照试验中也发现,连续服用12周的这种剂量是安全有效的[9].
药物动力学
几何平均AUC0-24 h及血药浓度峰值(C马克斯)利福平在第7天和第14天的值显示在表3.添加25%的利福平剂量,从40 mg·kg增加到50 mg·kg−1,即几何平均AUC0-24 h增加了~ 50%,这反映了先前观察到的类似剂量的照射量超过剂量比例的增加(补充图E2) [6].与此相反,利福平的峰值暴露与剂量成正比。值得注意的是,AUC的个体间差异很大0-24 h和C马克斯被观察到,两组之间的暴露量重叠相当大(表3和补充图E2).蛋白非结合利福平暴露,或游离部分,与其他(较低)剂量的利福平相当[14].有关利福平的药代动力学谱和其他研究药物的药代动力学参数,请参见补充图E3和补充表E1,分别。
抗细菌的活动
1例患者从50毫克·公斤−1组在基线和整个治疗过程中培养均为阴性,因此从所有分析中删除。图1总结了7天和14天期间痰中活菌载量的变化,表现为CFU的下降和TTP的增加。7天EBA显示,第一周细菌载量的下降是由于利福平的单独作用,并在第二周继续下降。在一个事后分析,6例患者在50 mg·kg−1第5天后没有培养的组被排除在外,因为他们只贡献了第4天的数据,因此很难估计14天期间的变化(补充图E4).这是一个事后在统计分析计划中没有预期的分析,但是保守的,导致较小的估计斜率比我们计划的初步分析。总的来说,在固体和液体介质上测量的杀菌活性都在10-50 mg·kg以上增加−1在所有分析中,最高剂量队列中出现了最高的14天活动。采用单阶段混合效应模型进行的敏感性分析显示,当所有阴性培养物按各自培养方法的检测下限估算时,当第一个阴性培养物按检测下限估算时,当忽略阴性培养物时,结果是一致的。支持我们研究结果的稳健性。随时间变化,CFU和TTP的细菌负荷与基线的差异见补充图E5.
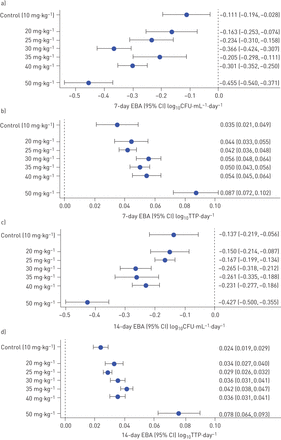
a, b) 7-和c, d)利福平14天早期杀菌活性(EBA) (95% CI),基于a, c) CFU和b, d)阳性时间(TTP)。除20和50 mg·kg组各1名患者的数据外,所有患者的数据均纳入−1在基线和整个过程中都有一致的阴性培养。10和20 mg·kg的估计值略有变化−1与以前相比[6原因是数据修正(四种CFU培养物被记录为阴性,而实际上它们是缺失的)。
Exposure-safety分析
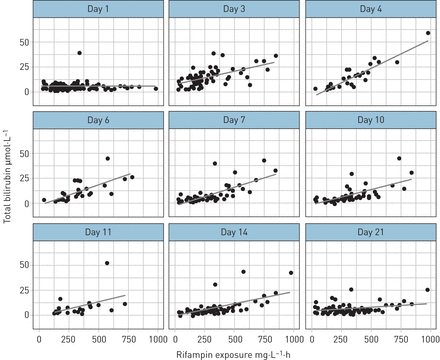
图2显示了利福平AUC之间的关系0-24 h在HIGHRIF1队列中,所有预定的安全来访的总血清胆红素(n=93)。利福平暴露与胆红素浓度相关(第3天的Spearman ρ值=0.670,p<0.001)。丙氨酸转氨酶和天冬氨酸转氨酶浓度与利福平暴露无相关性(补充图E7和E8).
每天服用利福平的总血清胆红素与利福平总暴露对照(0 - 12小时血浆浓度-时间曲线下的面积(AUC)0-24 h)在HIGHRIF1研究中所有有药代动力学结果的患者中(n=93)。这些线表示线性回归(为说明;文本中描述的统计检验)。的y-轴为70µmol·L−1为便于阅读,排除3个外围点(1例患者第3天40 mg·kg)−1组AUC0-24 h338 mg·L−1·h,胆红素111 mol·L−1;在第7天和第10天,一名患者的剂量为50 mg·kg−1组AUC0-24 h980 mg·L−1·h,胆红素100µmol·L和175µmol·L−1分别)。
关于剂量-暴露-耐受性评价,logit尺度上的线性关系适当地描述了数据(适应度罐提供在补充图E9).剂量和暴露(AUC0-24 h第7天)都是发生耐受性不良事件概率的有力预测因子(似然比检验,p<0.0001)。一个50 mg·公斤−1对于40和10 mg·kg,剂量与发生3次或3次以上耐受性相关(而非安全性相关)不良事件的风险76% (90% CI 56-88%)相关−1相应风险分别为47% (90% CI 29-64%)和2.0% (90% CI 0.1-5.4%)。与相关不确定度的关系在图3.
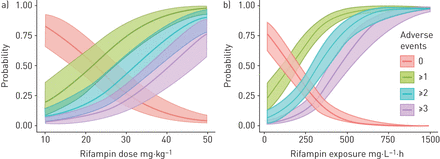
利福平单药治疗第一周与利福平相关的耐受性相关不良事件的概率a)剂量或b)暴露(0 - 12小时血浆浓度-时间曲线下面积(AUC)0-24 h)。阴影区域代表基于估计参数不确定性的90%置信区间
讨论
在引进利福平40多年后,在此期间,利福平已成为治疗结核病最重要的药物,我们现在确定了一种MTD。在我们对HIGHRIF1研究的第一份报告中,我们发现高剂量利福平可达35 mg·kg−1是安全且耐受性良好的,暴露增加的比例大于剂量,且暴露越多,EBA越高[6- - - - - -8].我们现在已经显示药物暴露持续增加,EBA在40和50 mg·kg范围扩大−1军团。40 mg·公斤−1队列与既往队列一致,不良事件仅为轻至中度。利福平50mg·kg−1然而,每日一次的耐受性较差,与40 mg·kg相比,不良事件发生频率和严重程度以及受试者停药的频率和严重程度急剧增加−1.因此,我们认为利福平的剂量为40 mg·kg−1MTD。
总的来说,所经历的不良事件是轻微或中度的,大多数与耐受性有关,即。胃肠紊乱(1-2级)、瘙痒(1-2级)和黄疸(1-2级,50 mg·kg−1仅限组,与高胆红素血症有关)。导致耐受性差和停药的是大量不良事件,而不是严重的个别不良事件−1组。
虽然胆红素轻微升高在所有组中都很常见,但在最高剂量组中观察到高胆红素血症(1-3级)的显著高发生率。胆红素的升高在利福平开始后的第3-4天达到峰值,是暴露依赖的,与其他肝酶升高无关(图2和补充数据E6-E8).值得注意的是,50毫克·公斤的胆红素水平正常化−1手臂比其他手臂慢(补充图E6).米cColl等.[15]发现在健康受试者中,使用利福平后未结合胆红素增加,我们现在认为这是因为抑制了胆红素肝细胞摄取通过有机阴离子转运蛋白(OATP)和/或UDP葡萄糖醛酸转移酶家族1成员A1 (UGTA1A1)的葡萄糖醛酸化[16].继续服用利福平后,胆红素水平下降至低于治疗前值,提示诱导净胆红素清除[15].相比之下,在50 mg·kg试验的患者亚组中,胆红素水平的升高都是共轭的(直接的)−1臂(补充图E10汽油),提示多药耐药蛋白2 (MRP2)在肝脏细胞内偶联后胆道清除率降低[17].与此一致,我们可能预计在这些高细胞内暴露时,利福平也会抑制其他肝转运蛋白[17].
利福平剂量在40和50 mg·kg之后−1很高,但基于先前的结果和建模预测范围内的预期范围[7],并且同样没有如利福喷丁的药代动力学中所报道的上限效应[18].更重要的是,除了平均暴露量外,观察到的最小AUC0-24 h和C马克斯几乎每一剂量步骤的剂量值都增加(补充图E2).这些低暴露可能导致治疗失败和复发,并为耐药性的出现创造条件[19,20.].值得注意的是,在高暴露水平下,血浆蛋白没有发生饱和,因为未结合蛋白部分(游离、活性药物)与其他报道具有可比性[14,21].
早期临床结核病研究通常只包括根据非常严格的标准选择的少数患者,他们只接受短期治疗。因此,我们的EBA发现需要在纳入标准更狭窄、患者数量足够的II期研究中得到证实。然而,尽管这项研究并不是为了检验组间的统计差异而设计的,但EBA的结果却是惊人的。EBA随剂量和暴露明显增加,迄今为止最高的EBA为50 mg·kg−1队列。在液体和固体介质中,EBA均有随剂量增加而普遍增加的趋势;建议增加40 mg·kg−1虽然我们的研究规模太小,还不能得出明确的结论,但在液体介质上比在固体介质上更不明显。纳入6例早期停用50 mg·kg的患者的分析−1Arm可能人为地夸大了14天杀菌活性的估计;排除这些患者后,我们的敏感性分析确实显示14天活性略低,尽管它仍然明显高于任何其他剂量组。我们选择保留包括所有患者的分析,因为这是一个观察性的、假设生成的研究,我们渴望在初级分析中包括所有数据。此外,我们不能排除过早退出研究的参与者也可能因为利福平暴露的增加而导致EBA增加,这可能解释了与耐受性相关的早期退出研究的原因。总的来说,我们的EBA结果与其他大剂量利福平治疗肺结核的研究结果一致[8,9,22,23]和结核病小鼠模型[4,24].在我们之前对肺结核患者的研究中,高剂量利福平35 mg·kg−112周被发现是安全的,并减少了培养转换的时间,一个中间临床终点[9].我们目前的研究进一步证明,高剂量的利福平效果更好,因此有可能改善临床结果,降低复发率,减少利福平耐药性的出现,并缩短治疗时间。
为了进一步优化利福平剂量及其给药策略,可以考虑多种方法。从规划的角度来看,最有希望的策略是开始使用较低剂量的利福平治疗,使机体在胃肠道耐受性方面适应利福平,同时促进诱导利福平和胆红素清除。在这个初始阶段之后,可以在所有患者中引入更高剂量的利福平。采用滴定法对个人最大暴露量进行个性化药物是有希望的,因为较高剂量的暴露量会增加,而较高的利福平暴露反过来与提高杀菌活性和培养转化有关[8,22].不幸的是,最大的影响尚未确定,因此没有明确的暴露目标。一种用于实时估计利福平浓度的低成本即时护理装置可支持在规划环境中实施大剂量利福平治疗[25].最后,我们小组最近报道了重量带剂量在AUC可变性方面产生了小的和非临床相关的降低0-24 h与平剂量相比[26].这支持平剂量的使用,我们计划在后续试验中实施这一方法。
目前,我们有足够的数据将大剂量利福平推向一项纳入标准更狭窄、患者人数更多、治疗时间更长和临床终点更长的研究,即。所谓的带有延长治疗后随访(STEP)的ii - ic期选择试验设计[27].在本试验中,该试验方案将在III期研究期间(目前为3或4个月)给予,并随访患者治疗失败和复发的临床结局,随访时间为12个月。生成的数据将为未来III期试验中高剂量含利福平方案的成功可能性提供有价值的信息。
目前,一项旨在通过增加利福平的剂量来缩短治疗时间的III期研究正在纳入(RIFASHORT;ClinicalTrials.gov:NCT02581527).主要终点是治疗失败和12个月后复发。根据这里提供的数据,在利福平治疗中评估的利福平剂量增加,即。1200或1800毫克利福平相当于约20-30毫克·公斤−1,可能看起来很谦虚[28,29,但仍将提供重要投入,以支持高剂量预防失败和复发的能力。
综上所述,利福平剂量为50 mg·kg−1每天一次,在结核病治疗开始时立即引入,难以耐受。与其他剂量相比,它显著改善了细菌负荷的减少。40 mg·公斤−1剂量是安全的、可耐受的,并与提高杀菌效果相关,因此在后续的IIc期试验中评估高剂量利福平缩短治疗的潜力是合适的剂量。该研究也为研究40 mg·kg的耐受性提供了机会−1在更大的人群中,持续时间更长。
我们的研究总结了一个始于20世纪60年代的历程。我们需要推进确证性临床试验,进一步为规划和指南中大剂量利福平的实施提供信息。
补充材料
可共享的PDF
确认
作者感谢Peter R. Donald(南非开普敦Stellenbosch大学儿科和儿童健康系)和Helmuth Reuter(南非开普敦Stellenbosch大学临床药理学系)。
脚注
作者贡献:所有作者的所有作者都促成了工作的概念/设计和/或参与了工作数据的收购,分析或解释;帮助起草了工作或批判性修订;批准了要发布的版本;并同意对工作的各个方面负责。
这篇文章有补充资料可从www.qdcxjkg.com
本研究注册于ClinicalTrials.gov标识号NCT01392911.
利益冲突:L.H.M. te Brake没有什么可披露的。
利益冲突:V. de Jager没有什么可披露的。
利益冲突:纳伦斯基没有什么可披露的。
利益冲突:Vanker没有什么可披露的。
利益冲突:E.M. Svensson没有什么可披露的。
利益冲突:P.P.J.菲利普斯报告了路德维希马克西米利安慕尼黑大学在进行研究期间的拨款。
利益冲突:S.H. Gillespie报告了欧洲和发展中国家临床试验伙伴关系和结核病联盟在提交工作之外的拨款。
利益冲突:N. Heinrich报告了欧洲和发展中国家临床试验伙伴关系和德国教育和研究部在研究进行期间的拨款;其他来自阿斯利康的(付费展示),在提交的作品之外。
利益冲突:M. Hoelscher没有什么可披露的。
利益冲突:R.道森没有什么可披露的。
利益冲突:a·h·迪肯没有什么可披露的。
利益冲突:R.E. Aarnoutse没有什么可披露的。
利益冲突:M.J. Boeree没有什么可透露的。
支持声明:本出版物由PanACEA出版,PanACEA是欧洲和发展中国家临床试验伙伴关系(EDCTP) 1项目(项目代码IP.2007.32011.012 (HIGHRIF))和欧盟支持的EDCTP2项目(授权编号TRIA2015-1102-PanACEA)的一部分。研究经费来源对研究设计没有影响;在数据的收集、分析和解释;或者写报告的时候。文章的发布被定义为授权协议下的可交付内容。本文的资金信息已存入Crossref资助者注册表.
- 收到了2020年4月10日。
- 接受2020年12月7日。
- 版权©2021人队。
这个版本是在知识共享署名非商业许可4.0的条款下发布的。有关商业复制权利和许可,请联系权限在}{ersnet.org