摘要
背景本研究旨在在医院排放后3个月内描述锻炼期间的心肺功能,并根据呼吸困难和重症监护单位(ICU)停留。
方法Covid-19的参与者从五个大型挪威医院出院,连续邀请到多方面,前瞻性队列研究。在排出后3个月,在排出后3个月,将156名参与者(平均年龄为56.2岁,60名女性)进行检查,并与参考人口进行比较。使用改良的医学研究委员会(MMRC)呼吸困难量表评估了呼吸困难。
结果峰值摄氧量(V”O2 峰) <80%的31% (n=49)。呼吸效率降低15% (n=24),呼吸储备<15%为16% (n=25)。预测氧脉冲<80%的患者占18% (n=28)。呼吸困难(mMRC≥1)的报告占47% (n=59)。这些参与者有着相似的V”O2 峰(p = 0.10)但较低平均值±SD.V”O2 峰·公斤−1% (mMRC 0)(76±16%)与89±18%;P =0.009),因为体重指数较高(P =0.03)。ICU -与non-ICU-treated参与者,意味着±SD.V”O2 峰%预测值分别为82±15%和90±17% (p=0.004)。ICU组和非ICU组的通气、呼吸储备和呼吸效率相似。
结论三分之一的参与者经历了V”O2 峰出院后3个月预测的COVID-19发生率小于80%。呼吸困难的参与者的特点是由于肥胖和较低的呼吸效率的运动能力。ICU治疗组和非ICU治疗组患者的通气和呼吸效率相似。
摘要
在因COVID-19住院3个月后,三分之一的参与者的摄氧量降低。最常见的运动限制是脱位。运动时的循环限制比呼吸限制更常见。https://bit.ly/3jmVDQ6
介绍
严重急性呼吸综合征冠状病毒2 (SARS-CoV-2)是COVID-19大流行的罪魁祸首[1,2].COVID-19主要影响呼吸系统,但也可能涉及其他器官[3.].最近一项6个月的随访研究发现,COVID-19最常见的持续性症状是疲劳/肌肉无力(63%)和呼吸困难(26%)[4].多项研究报告了在COVID-19后1.5-6个月住院和非住院参与者中呼吸困难的高患病率(16-89%)[5- - - - - -8].
挪威一组COVID-19住院患者最近的一份报告发现,3个月时呼吸困难与气体扩散能力降低之间没有很强的相关性[7],尽管近五分之一的人在改良医学研究委员会(mMRC)呼吸困难量表中报告呼吸困难>1 [7,9].心肺运动试验(CPET)可能区分运动能力降低和呼吸困难的病理生理机制[10.],因为它在最大努力期间整合了心血管,呼吸系统和肌肉系统的评估[11.].两项报告81名中至重度COVID-19患者住院后CPET数据的研究发现,峰值摄氧量降低(V”O2 峰)在大部分参与者中[3.,12.].其中一项研究选择性地纳入了接受机械通气治疗的参与者,而两项研究都只纳入了有限数量的参与者。据我们所知,目前还没有多中心、以人群为基础的研究报告广泛的CPET结果或比较住院COVID-19患者的不同亚组。我们假设COVID-19患者的运动能力会降低。此外,我们假设持续的心肺运动限制,特别是在自我报告呼吸困难或重症监护病房(ICU)入院的患者。因此,我们的目的是确定COVID-19出院后3-4个月与参考人群相比的运动心肺功能,并描述运动受限参与者的特征。
方法
研究设计和样本
目前的研究是COVID-19住院后患者报告结果和肺功能的亚研究,是在挪威南部6家医院进行的多中心前瞻性队列研究[7].亚研究包括了来自五家医院的参与者。年龄≥18岁且在2020年6月1日之前出院诊断为COVID-19,入院治疗>8小时的参与者被认为符合条件。排除标准包括慢性阻塞性肺疾病(COPD)、心肌梗死、心力衰竭或外周动脉疾病的事先诊断、居住在医院集水地区以外、无法提供知情同意或参与世界卫生组织(世卫组织)团结试验。有关研究设计和参与者的进一步细节已被报告[7].符合条件的参与者在医院排放后2-4周邮寄邀请。通过返回书面签署的同意书或通过安全的数字同意书(敏感数据(TSD),奥斯陆大学,挪威的服务,挪威的敏感数据(TSD)服务获得了知情同意书。在提供主要研究同意的264名参与者中,邀请236人参加当前的落户。在医院放电后3个月检查参与者。临床改善的秩序规模用于评分Covid-19感染的严重程度[13.].
挪威东南部地区伦理委员会(125384年)和每个参与中心的数据保护人员批准,并在ClinicalTrials.gov标识号NCT04535154.
肺功能测试
肺功能测试包括肺活量测定和肺的一氧化碳扩散能力(DLCOJaeger主屏幕PFT;Vyaire Medical, Höchberg,德国)。采用国际参考值[14.,15.].mMRC呼吸困难量表作为一种自评工具,测量呼吸困难对日常生活活动造成的残疾程度,量表从0到4 [9].参与者分为患有呼吸困难(MMRC 1-4)或NO呼吸困难(MMRC 0)。
心肺运动试验
CPET(JAEGER Vyntus CPX; Vyaire Medical)在跑步机上进行,连续测量分钟通风(V”E),V”O2,产生二氧化碳(V”有限公司2)、心率、心电及血氧饱和度(年代宝2)[10.,16.].基于报告的运动耐受性,针对每个参与者指定了一个增量修改的布鲁斯协议。使用Borg CR10规模评估同时,感知的劳累和呼吸困难[17.].V”O2·公斤−1,氧脉冲(V”O2/心率),V”E/V”有限公司2计算斜率和通气当量。V”O2·公斤−1将被称为运动能力。通气效率被评估V”E/V”有限公司2倾斜到通风补偿点以及由二氧化碳的Nadir通风等同物(V”E/V”有限公司2最低点).呼吸储备计算为(1-V”Epeak/最大自愿通气(MVV))×100%,使用1秒内用力呼气量(FEV)估算1)×40 for MVV [10.].通过V斜率方法评估厌氧阈值[16.].运动终止后立即从指尖抽取毛细管血样,分析乳酸、pH值和二氧化碳张力(ABL 800 Flex;辐射计医学,哥本哈根,丹麦)。所有的CPETs均在两个测试中心进行:LHL Hospital Gardermoen (Jessheim, Norway)或St Olavs University Hospital (Trondheim, Norway)。
解释CPET
研究人员使用挪威具有类似合并症(高血压和糖尿病)的参考人群的正常值来比较参与者在运动期间的心肺功能[18.].Z-scores≤1.96定义为异常减少,Z-scores >1.96定义为异常增加,分别对应参考人群的第2.5和97.5个百分位[14.,19.].为了与其他已发表的研究进行比较,一些CPET变量被报道为小于预测值的80%。
限制运动的原因被确定为所有的参与者V”O2 峰< 80%的预测。当呼吸储备<15%时考虑呼吸限制运动。当Wassermann流程图导致循环类别时,考虑了循环限制[16.[包括ECG改变与缺血或心律失常一致。我schaemia was defined as ≥1 mm horizontal or downsloping ST segment depression in at least two adjacent leads that persisted at 80 ms after the J point. Deconditioning was considered in participants withV”O2 峰<80%预测无呼吸机或循环运动限制的证据。考虑到不正常的呼吸是高的原因V 'E/V”有限公司2 最低点和V”E/V”有限公司2观察运动时潮气量和呼吸频率的变化,评价运动峰值时毛细血管二氧化碳张力和pH值。
生物化学
收集无快速的静脉血液样品以测量血红蛋白,C-反应蛋白,N-末端促胰岛Natrietic肽(Cobas 8000,E801,E601; Roche Diagnostics,Mannheim,德国和建筑师I2000SR; Abbott,Chicago,IL,USA)和高敏感性心肌肌钙蛋白T(COBAS 8000,E801,E601)。报告了住院期间和3个月后的最大值。
统计分析
描述性统计数据与标准偏差,中位数(IQR(IQR))或数量(百分比)一样呈现为平均值。使用Wilcoxon签名秩检验将Z分数与0进行比较。呼吸困难的群体比较与没有呼吸困难和ICU与对非icu患者进行连续变量线性回归分析,校正年龄和性别。由于在一些线性回归模型中残差的分布与正态分布有轻微的偏差,我们对所有模型进行了10,000次重复的自举估计p值。所有统计分析使用Stata 16.1版本(StataCorp, College Station, TX, USA)进行。我们使用双侧检验选择了5%的显著性水平。
结果
参与者特征和初始治疗
在236名被邀请参加主研究的参与者中,189人同意参与当前的亚研究,该亚研究在出院后的中位数(IQR)为104(90-139)天完成。26名参与者因共病(COPD、心肌梗死、心衰或外周动脉疾病)被排除在外,其中7人有次最大的、不确定的CPET (图1).表1总结研究的描述。年龄变化范围为18 - 88岁(表1).肥胖(体重指数(BMI) >30 kg·m−2)在46名参与者(30%)中发现。5%的患者观察到与目前住院相关的肺栓塞或深静脉血栓。参与者住院治疗的中位数(IQR)为6(3-11)天。共有31名参与者(20%)在ICU接受了中位(IQR) 9(4-14)天的治疗,20名参与者(13%)接受了插管和机械通气,中位(IQR) 9(7-15)天。在研究期间,出院3个月后,13% (n=19)的FEV结果低于正常下限(z-score≤1.64)1强制肺活量为5%(7例),强制肺活量为20%(31例)DLCO6%(n = 9)DLCO/肺泡体积。59名受试者(47%)报告mMRC 1-4显示呼吸困难(表1).
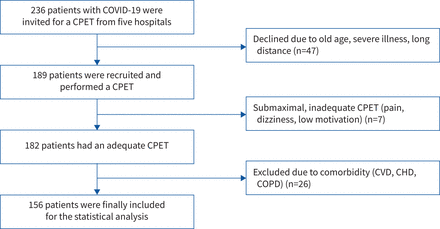
病人流程图。CPET:心肺运动试验;心血管疾病:心血管疾病;CHD:冠心病;COPD:慢性阻塞性肺疾病。
心肺功能
V”O2 峰49名参与者(31%)的预测值小于80%。V”O2 峰·公斤−173名参与者(47%)的预测值小于80%。病理性厌氧阈值,<40%预测V”O2 最大限度,在23名参与者(15%)中观察到。
25名参与者(16%)观察到呼吸受限,以呼吸储备<15%表示[16.,19.].
均值±SD.年代宝2休息时为98±1%,最大负荷时为95±4%。我们发现>的饱和度降低5%年代宝234名参与者(23%)在休息和最大负荷之间。
在28名参与者中观察到氧脉冲<80%(18%)。其中四种表现出随负荷增加而下降的氧脉冲曲线。在运动期间,12名参与者(8%)在心电图上观察到病理反应。其中,分别有7人和5人出现了缺血和心律失常(主要是多灶性室性早搏)。
在15%(n = 24)中观察到的通气效率降低,由高分度定义V”E/V”有限公司2斜坡和/或V”E/ V.”有限公司2 最低点(z分数> 1.96)。一个高V”E/V”有限公司219例(12%)出现坡度,且坡度较高V”E/V”有限公司2 最低点在16个(10%)。在那些呼吸效率降低的参与者中,4名(17%)有呼吸受限,9名(38%)有循环受限,11名(46%)有呼吸功能障碍(过度通气,应激反应)。9名因循环因素导致呼吸效率降低的患者中,7人在运动时出现心电图病理,2人在COVID-19急性期出现静脉血栓栓塞。
运动限制因素是多因素,并在49名参与者中描述V”O2 峰< 80%的预测。呼吸受限7例(14%),循环受限11例(22%),脱位31例(63%)。
表2与参考人群相比,总结了Covid-19患者中CPET变量的差异。
亚组的心肺功能
呼吸困难
报告呼吸困难的参与者显着降低V”O2 峰·公斤−1、呼吸效率、心率及收缩压(表3).低V”O2 峰·公斤−1在呼吸困难组中,与较高的BMI有关,如V”O2 峰在组之间类似(P = 0.052)。
ICU停留
ICU逗留的参与者显着降低V”O2 峰%预测(90±17%与82±15%;p = 0.004)和V”O2 峰·公斤−1预测%(86±19%)与76±15%;p=0.002)。年龄、BMI、通气、呼吸储备、氧去饱和、呼吸效率和氧脉搏无差异。
讨论
目前的研究表明V”O2 峰在医院排放后3个月内,在Covid-19患者的三分之一预测中预测<80%。每个第六位参与者都有降低的呼吸储备,通风效率,氧气脉冲或组合。解剖是锻炼限制的主要原因,其次是循环和通风锻炼限制。自我报告的呼吸困难与较低的通气效率和更低相关V”O2 峰·公斤−1因为BMI较高在ICU或普通医院病房的参与者之间,心肺运动反应的差异小于预期。
运动能力下降是男性死亡的独立预测因素[20.]和妇女[21.].我们发现V”O2 峰因此,与参考人群相比,强调了COVID-19后恢复运动能力的重要性。B埃利-等.[22.]报道Covid-19后重新获得身体能力的难度导致了康复计划的建议[22.].我们观察到,V”O2 峰·公斤−1与参考人群的差异更大V”O2 峰,反映了我们研究人口的肥胖。肥胖是严重Covid-19的公认风险因素[23.].
两项研究包括Covid-19患者V”O2 峰预测81%及73% [3.,24.,这与我们的结果相当,而另一项研究报道V”O2 峰预测机械通风的Covid-19患者的57%[12.].
限制运动的因素可能与通气、循环、脱位或外周机制有关。在目前的研究中,退行性运动是运动限制的主要原因,每五分之一的参与者都有这种情况。住院期间10天不能活动,再加上运动性呼吸困难导致的进一步不活动,可能是我们的参与者的条件退化的原因,其中心输出量减少,外周限制因素和肌肉浪费。在最近对18名COVID-19患者出院时的报告中,外周限制因素,包括贫血和外周肌肉抽氧减少,是运动限制的主要决定因素[25.].然而,我们的研究人群在住院期间或随访期间没有出现贫血。
导致运动受限的第二大常见原因是循环因素。COVID-19可能会影响多个器官,包括心脏和血管[26.].频繁循环运动受限的发现可能依赖于covid后后遗症以外的因素。即使我们排除了已知的既存心血管疾病的参与者,一些人可能仍然有未诊断的既存心血管疾病,在CPET中发现。此外,运动心电图的诊断准确率约为70% [27.我们也不能排除某些参与者真正的运动限制因素是身体条件变差。两名循环运动受限的患者在住院期间发生肺栓塞,但出院3个月后不太可能导致循环运动受限。一项对21例机械通气COVID-19患者(包括3例肺栓塞患者)的血流动力学研究发现,所有患者的肺血管阻力均正常。76%的患者存在毛细血管后肺动脉高压,但没有出现与肺栓塞相关的毛细血管前形态[28.].
呼吸受限是运动受限的第三大常见原因。我们最近报道了同一人群中25%的样本经胸部计算机断层扫描发现肺实质异常[7].然而,低呼吸储备在我们的参与者中并不常见,这表明呼吸储备可能在正常范围内,即使存在实质异常。与大流行开始时对这一人群的预期相反,几乎没有参与者降低了肺活量测定和气体扩散能力,以及在运动期间降低了呼吸储备。肺功能测试结果的不一致性和较低的运动能力支持呼吸受限发生率较低的发现,因为退行性是研究人群的主要局限性。在通过康复恢复身体功能的情况下,去适应是一个积极的发现。
七分之一的病人呼吸效率降低。有通气/灌注的证据(V'/问')在这些患者中约一半的肺或循环因子导致不匹配。对于另一半,功能失调的呼吸模式似乎有助于降低的通气效率。不幸的是,我们没有动脉血气分析以证明过度通气。然而,呼吸功能障碍呼吸模式和过度通气剂被报告为呼吸困难在轻度Covid-19幸存者的研究中的常见原因[29.].这是否与自主神经异常或其他因素有关尚不清楚。
由于共病影响运动能力,我们排除了严重共病的参与者。相比之下,我们没有排除糖尿病或高血压患者,因为cpet的参考人群也包括这些患者[18.].哮喘在研究人群中常见,但哮喘患者没有表现出透气限制,良好控制的哮喘不应干扰运动能力。
亚组的心肺功能
我们的参与者经常报告运动性呼吸困难,这与其他研究一致[4- - - - - -8].呼吸困难是一种复杂的症状,由美国胸部社会定义为多种生理,心理,社会和环境因素的净结果[30.].
当我们比较有和没有呼吸困难的参与者时,呼吸困难的参与者明显更低V”O2 峰,但在通气、呼吸储备、年代宝2和DLCO.这表明呼吸困难与肺功能以外的其他因素有关。
V”E/V”有限公司2斜率和V”E/V”有限公司2 最低点呼吸困难组较高。这些高值主要反映V'/问'不匹配,但也可能代表功能失调的呼吸。单独解散不能解释呼吸困难感知的差异,如V”O2在厌氧阈值,绝对和相对于预测V”O2 最大限度,在两组中都是相似且低的。因此,我们的研究结果表明,COVID-19后的呼吸困难是复杂的,有多种解释。
入住ICU的参与者在急性期内具有更严重的氧气问题,而且比未达到ICU的人的住院时间长三倍。在出院后3个月,ICU参与者显着降低V”O2顶峰。否则,它们具有类似的测试结果。我们预计ICU参与者有更多的通风局限性,更糟糕的氧气去饱和度,更多V'/问不匹配和较早的厌氧阈值是由于退化。据我们所知,目前还没有针对ICU治疗的COVID-19患者的CPET研究与与我们的发现进行比较。ICU参与者观察到的结果可能是由于出院后的额外护理,住院康复项目的出席率高于非ICU参与者。结果可能也反映了前3个月实质性肺组织修复的效果[31.,32.].
限制和优势
我们没有客观措施,以获得现有功能状况和锻炼能力的研究人口。我们已经将参与者与健康的参考人口进行了比较,尽管我们已经记录了预先存在的合并症。使用脉冲血液血管运动期间氧饱和度的估计应小心地观察,因为可能发生了错误。CPET生成众多变量,由于多次测试而导致错误的风险。ICU集团的有限数量可能导致2型错误。该研究的实力是其设计,具有未选择的医院人口和对参与者的广泛体检。尽管与许多其他国家相比,在ICU的患者中较少的患者,但是,合并症和肥胖的比例也与其他研究相当,我们认为我们的研究以及其他国家的结果均可展开。
结论
在Covid-19后从医院排放后3个月,V”O2峰值在三分之一的参与者中减少。最常见的锻炼限制是解散,强调康复计划的重要性。运动时的循环限制比呼吸限制更常见。自我报告的呼吸困难的参与者较低V”O2 峰·公斤−1和通气效率。有无ICU住院的患者在通气和呼吸效率方面没有差异。在COVID-19后存在持续运动受限和呼吸困难的患者中,CPET对确定病因至关重要。
可共享的PDF
脚注
本研究注册于ClinicalTrials.gov标识号NCT04535154.
利益冲突:I. Skjørten在挪威卫生理事会和挪威医学协会的资助下为医生提供教育讲座。
利益冲突:O.A.W. Ankerstjerne没什么可透露的。
利益冲突:D. Trebinjac无需披露。
利益冲突:E. Brønstad没有什么可披露的。
利益冲突:Ø。Rasch-Halvorsen没有什么可透露的。
利益冲突:G. EINVIK从Astrazeneca和Boehringer Ingelheim接受了研究赠款,以执行当前的研究。
利益冲突:T.V. Lerum没有什么可披露的。
利益冲突:K. Stavem无需披露。
利益冲突:A. Edvardsen是挪威社会的临床生理学协会的领导者(未付),并已收到来自GlaxoSmithkline和Chiesi的讲座,演讲,发言者局,稿件写作或教育活动的付款或酬金。
利益冲突:C.B. Ingul已从拜耳的讲义收到拜耳,与目前的研究无关。
支持声明:这项工作得到了Landsforeningen for Hjerte- og Lungesyke、Akershus Universitetssykehus和Nasjonalforeningen for Folkehelsen支持。
- 已收到2021年4月5日。
- 接受2021年6月21日。
- 版权所有©作者2021。
这个版本是在知识共享署名非商业许可4.0的条款下发布的。有关商业复制权利和许可,请联系权限在}{ersnet.org















