抽象
Omalizumab是一种用于治疗严重变应性哮喘(SAA)的抗ige单克隆抗体。STELLAIR研究的目的是确定治疗前血嗜酸性粒细胞计数作为对奥马单抗反应的预测措施的重要性。
这项回顾性的现实生活研究是在2015年12月至2016年9月期间在法国进行的,使用的是奥马里珠玛布治疗的SAA患者的医疗记录。对奥玛利珠单抗的反应通过三个标准进行评估:医师评估、年恶化率降低≥40%以及两者结合。根据奥玛利珠单抗启动前一年的血嗜酸性粒细胞计数计算应答率。
723名成人(年龄≥18岁)和149名未成年人(年龄6-17岁)接受SAA奥马利马珠单抗治疗的患者共872例。血嗜酸性粒细胞计数·µL≥300细胞−152.1%的成年人和73.8%的未成年人。经医师评估,67.2%的成人和77.2%的未成年人有反应,71.1%的成人和78.5%的未成年人有≥40%的恶化率降低。在成年人中,结合标准的反应率为58.4% (95% CI 53.2 -63.4%)·µL血嗜酸性粒细胞≥300细胞−1(n = 377)和58.1%(95%可信区间52.7 - -63.4%)血嗜酸性粒细胞·µL < 300细胞−1(n = 346)。
这项研究表明,患者大比例与SAA有血嗜酸性粒细胞计数≥300细胞·μL−1,并表明奥马珠单抗的有效性是在“高”和“低”子组嗜酸性粒细胞相似。
抽象
奥玛利珠单抗是治疗严重过敏性哮喘的一种选择,与血嗜酸性粒细胞计数无关http://ow.ly/7tQh30iXNTW
介绍
严重哮喘是一种异质性疾病,有多种表型,包括过敏性和嗜酸性哮喘[1,2]。约70%的气喘病患者会出现过敏反应[3.]。进入气道的过敏原通过树突状细胞呈现给t淋巴细胞,树突状细胞启动细胞介导的免疫反应,特别是2型t辅助性细胞(Th2)的成熟和迁移。Th2细胞刺激b细胞产生IgE抗体,刺激促过敏细胞因子IL -4、IL -5、IL -9、IL -13的分泌。IL-4对IgE的产生至关重要,而IL-5则参与嗜酸性粒细胞和嗜碱性粒细胞的募集,进而促进炎症的发生。
一种人源化抗ige单克隆抗体omalizumab,于2005年首次在欧洲推出,作为儿童(6岁起)和成人(SAA)的一种附加治疗手段[4,5]。在大规模的随机研究中,Omalizumab已被证明可以预防病情恶化,改善症状和生活质量,并减少全身皮质类固醇的使用[6- - - - - -8]和“现实生活”的研究[9- - - - - -15]。
针对IL-5或其在同一Th2通路中的受体的新疗法正在出现,用于治疗严重的嗜酸性哮喘(SEA) [16]。这些疗法的临床效益更加明显高患者血液中嗜酸性粒细胞计数和显示结果局限于成人海耐火材料由血液嗜酸性粒细胞计数·µL≥300细胞−1超过12个月[16]。有趣的是,大部分SAA患者也有血嗜酸性粒细胞计数·µL≥300细胞−1(17]。
STELLAIR(迈向个性化护理的下一步:评估SAA患者对XoLAIR治疗的应答者)研究的目的是确定治疗前血嗜酸性粒细胞计数作为对奥马单抗应答的预测措施的重要性。
方法
研究设计和参与者
这项多中心、非介入性、回顾性、观察性研究于2015年12月21日至2016年9月30日在法国进行,使用的数据来自使用奥玛利珠单抗治疗的SAA患者的医疗记录。以医院为基础的肺科医师和有治疗严重哮喘经验的儿科肺科医师被要求提供符合STELLAIR纳入标准的所有连续患者的数据。医生可包括符合纳入标准的连续病人,每位医生最多可包括30名病人。STELLAIR是一项回顾性非介入性研究,不需要注册ClinicalTrials.gov。这项现实生活中的研究得到了法国生物医学研究中负责数据保护的机构委员会的批准(法国研究机构信息特性委员会和国家信息自由委员会)。
纳入标准为所有患者:≥6岁;曾因SAA控制不良而接受奥玛利珠单抗治疗的患者;在奥玛利珠单抗开始治疗前12个月内进行了血嗜酸性粒细胞测量;在开始使用奥马单抗之前的12个月内记录的恶化次数;世卫组织在4-6个月的治疗和记录的恶化次数后,对奥玛利珠单抗的反应进行了有记录的医师评估。根据伦理委员会的要求,拒绝收集医疗数据用于研究目的的患者被排除在外。
调查人员以电子病例报告形式输入患者数据,并提取四个时间点的数据:T-12与奥马单抗启动前12个月相对应,T0与奥玛珠单抗开始治疗的时间相对应,T4 - 6在治疗4-6个月时进行第一次疗效评估(根据奥玛瑞珠单抗对产品特性总结的要求)和T12corresponding to effectiveness assessment at 12 months following treatment initiation (12-month effectiveness evaluation for renewal of prescription, if available). The study being retrospective, T4 - 6和T12(如果有的话)是在2015年12月开始研究之前。
结果
主要结果是在T4 - 6相比之下,T-12使用三个标准。
1)医生根据全球治疗效果评估(GETE)量表进行整体评估。GETE是一个五分制的量表,其中1=优秀(完全控制哮喘),2=良好(明显改善),3=中等(可辨,但改善有限),4=差(无明显变化),5=恶化。症状控制等级为“极好”/“良好”或“中等”/“较差”/“恶化”,使患者分别被定义为“有反应者”或“无反应者”。
2)年恶化率降低,“应答者”定义为年恶化率降低≥40%。哮喘恶化被定义为哮喘的显著恶化,需要口服皮质类固醇(OCSs)的短时间爆发,或者对于接受OCS治疗的患者,需要增加OCS剂量方案。根据暴露于奥马单抗治疗的时间调整恶化的数量,计算每年的恶化率;所有患者的治疗时间为4-6个月,706例患者为12个月(81%)。
3) GETE评估与年加重率(“合并反应”)降低≥40%相结合。
反应是根据分析·µL血嗜酸性粒细胞计数(细胞−1)在奥玛利珠单抗开始前一年测量(开始前的最后一次测量)。
统计分析
使用SAS版本9.4进行统计分析(SAS Institute, Cary, NC, USA)。定性变量的描述性分析以每个类别的患者人数和百分比表示。定量变量表示为正态分布变量的均值和标准差,或者表示为中位数和四分位数范围(IQR)。95%的置信区间分别为三个结果终点。在指定的地方,报告每个变量缺失值的数量。所有统计测试是双边和α的风险被设定为5%。
结果
邀请的510名医生中,102名被接受,最终开放了80个场所;其中,78名(62名肺科医师和16名儿科肺科医师)积极招募了总共879名符合资格标准的患者。这些患者中有872人(其中723人(83%)是成年人(年龄≥18岁),149人(17%)是未成年人(年龄6-17岁)。图1)。7例年龄均≥18岁的患者因T时病历不完整而被排除在分析之外4 - 6(n=5)或因为没有其他哮喘控制器治疗的文献(n=2)。
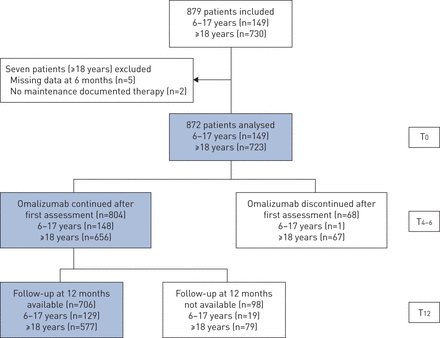
研究流程图。T0:奥马单抗治疗起始;T4 - 6:治疗4-6个月后首次疗效评估;T12:治疗开始后12个月的有效性评估。
大部分患者(n=804(92.2%))在T期第一次疗效评估后仍在使用奥马单抗治疗4 - 681% (n=706)在T12,即。奥玛利珠单抗启动后12个月。
病人的特征在表1。对于成年人和未成年人,omalizumab被规定为一个附加治疗改善患者的哮喘控制多个记录严重哮喘发作,尽管每天大剂量吸入激素(ICS),加上一个长效β2-激动剂(LABA),有或没有OCS治疗。在T0,超过三分之一的成年患者(n=243(34.4%))接受了OCS维持治疗(平均每日剂量20.4 mg·天)−1)。
本研究纳入的所有患者的SAA均不受控制,这反映在过去12个月的哮喘事件数量上(恶化:均数±)sd5.2±3.9(未成年人),4.3±3.1(成人);经常意外住院:未成年人79例(53%),成人295例(40.8%)。在奥玛利珠单抗之前的12个月,未成年人和成年人的血嗜酸性粒细胞计数的恶化和住院情况显示在表中表2。
在未成年人中,严重过敏人群的特征是总IgE水平非常高(中位IgE水平为850 IU·mL)−1)。成人血清总IgE中位值为285 IU·mL−1。
中位血嗜酸性粒细胞计数T-12未成年人的自杀率是成年人的两倍多(619与3.08 cells·µL−1)(表3)。血液中嗜酸性粒细胞计数在T分布-12范围从0·µL≥1000细胞−1未成年人的平均比例高于成年人。377只成年SAA患者(52.1%)有血嗜酸性粒细胞·µL≥300细胞−1。
Omalizumab的有效性首次在T4 - 6接受治疗的肺科医生或儿科医生在经过154天的平均治疗后使用GETE量表:77.2%的未成年人(n=115)和67.2%的成人(n=486)被报告为应答者(即。优(完全控制)或良好(显着改善哮喘)),以奥马珠单抗(图2)。
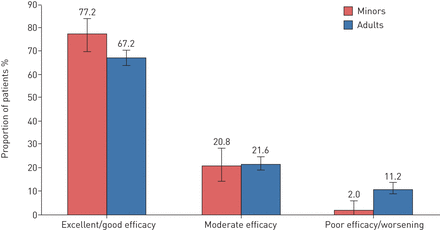
治疗效果评价的全球评估在T4 - 6(4-6个月治疗后首次有效性评估的时间):未成年人(6-17岁;n=149)和成人(年龄≥18岁;n = 723)。误差条表示95%置信区间。
在治疗期间,T0和T4 - 6,34.9%的未成年人(n=52)和43%的成年人(n=311)至少有一次病情加重。至少有一次恶化的患者中,未成年患者的平均恶化数为1.9次,成年人为1.8次。均值±sd年加重率在未成年患者中下降60.2±88.8%,在成人中下降48.5±93.5%。根据年加重率降低(降低≥40%),大部分患者为应答者:未成年人78.5% (95% CI 71.1-84.8%),成人71.1% (95% CI 67.6-74.4%)。
到奥马珠单抗治疗(GETE和恶化率减少的组合)的组合响应于未成年人与成年人的67.8%(95%CI 59.7-75.2%)和58.2%(95%CI 54.5-61.8%)分别达到。
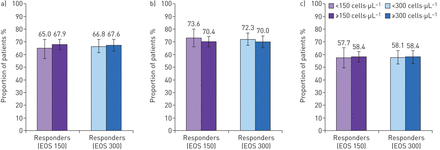
723名成年人中,377年血嗜酸性粒细胞·µL≥300细胞−1和346年血嗜酸性粒细胞·µL < 300细胞−1。在成人中,GETE响应,减少≥40%的恶化反应和结合反应率omalizumab治疗相似不论血液嗜酸性粒细胞计数,使用·µL截止300年或150年的细胞−1(图3)。此外,结合响应相似的比例“低”·µL嗜酸性粒细胞(< 300细胞−1)和“高”·µL嗜酸性粒细胞(≥300细胞−1)在整个成年人口(图4)。
成人(≥18岁)在T4 - 6(时间4 - 6个月的治疗后的第一个有效性评估)根据血液嗜酸性粒细胞计数在150个细胞·µL截止−1(“EOS 150”: < 150·µL细胞−1n = 163;≥150个细胞·µL−1,n = 560)和300·µL细胞−1(“EOS 300”: < 300·µL细胞−1n = 346;≥300个细胞·µL−1中,n = 377)。GETE:治疗效果的全局决策。一)依据医师的整体评价(GETE)应答者。b)中反应者基于在年度恶化率≥40一%的降低。c)中合并的应答者(GETE的组合和恶化率减小)。误差条表示95%置信区间。
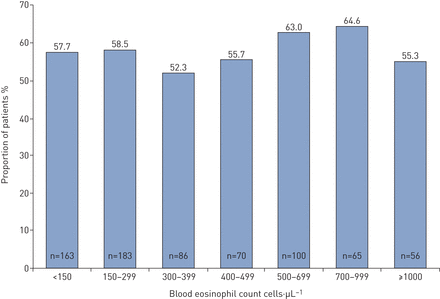
根据全人群中嗜酸性粒细胞计数的分布,成人(≥18岁)对奥玛利珠单抗治疗的联合应答者。
比例减少哮喘发作患者血液中嗜酸性粒细胞·µL < 300或≥300细胞−1和IgE < 75或≥75 IU·µL−1示于图5,并表明奥玛利珠单抗在所有这些患者亚组中都是有效的。
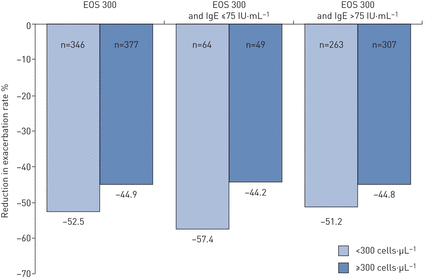
根据血液嗜酸性粒细胞计数减少哮喘恶化率(截止300年·µL细胞−1(“EOS 300”))和血清IgE(截止75 IU·µL−1)严重变应性哮喘成人(≥18岁)。
在未成年人(n = 149), 110年血嗜酸性粒细胞·µL≥300细胞−1和39·µL血嗜酸性粒细胞< 300细胞−1。急救员omalizumab也分析了使用·µL截止600细胞−1。该截止是在T的中位数血嗜酸性粒细胞计数-12in this subgroup and allowed a better distribution of the population: 80 patients had blood eosinophils ≥600 cells·µL−1和69年患者血液嗜酸性粒细胞·µL < 600细胞−1。联合应对omalizumab治疗为70.9% (95% CI 61.5 - -79.2%)与血液嗜酸性粒细胞≥300个细胞·µL未成年人−1(n = 110)和59%(95%可信区间42.1 - -74.4%)与血液中嗜酸性粒细胞·µL < 300细胞−1(N = 39)。With a cut-off of 600 cells·µL−1,结合响应达到72.5% (95% CI 61.4 -81.9%)≥600个细胞·µL−1(n = 80)和62.3%(95%可信区间49.8 - -73.7%)·µL < 600细胞−1(n = 69)。
总而言之,成人和未成年人的应答率是相似的,不管是否研究了嗜酸性粒细胞切断,也不管应答的所有定义(表4)。
在T12日,data for treatment effectiveness (including number of exacerbations, hospitalisations and modification in OCS therapy) were available for 706 of the study participants, with 577 adults and 129 minors completing 373 and 403 days of omalizumab therapy, respectively. The results were adjusted on a mean duration of 12 months. 50% of minors (46 out of 92) and 61.9% (179 out of 289) of adults experienced at least one exacerbation during the 12 months of treatment (mean±sd分别为1.1±1.6和1.4±2)。与治疗前12个月相比,未成年患者的恶化率降低了70.4±50%,成人降低了58.6±67.8%。15.5%的未成年人(20 / 129)和10.9%的成年人(63 / 577)在12个月的治疗期间至少住院一次(平均值±)sd分别为0.2±0.6和0.2±0.6)。年住院率在未成年人和成年人中平均相同(平均值±)sd0.2±0.6)。与12个月的治疗前期相比,未成年人的住院率平均下降了73.2%,成年人下降了72.6%。
共有243名成年人接受了OCS治疗(平均每日剂量20.4 mg·d−1)在T0。195名患者(80.2%)与OCS,作为在T维持治疗0在T12。在T12日,96名患者(49.2%)完全停止了OCS治疗。在那些仍在接受OCS治疗的患者中,大多数(62.1%)已经将他们的中位数(IQR)每日剂量降低了10 (5-15)mg·天−1,这表示OCS每日剂量的中位数(IQR)减少了50%(40-70%)。Omalizumab有效性(GETE口服治疗的急性加重和修改数量)在成人与OCS维持治疗观察患者血液中嗜酸性粒细胞·µL < 300和≥300细胞−1(数据没有显示)。
血嗜酸性粒细胞计数资料12对212名患者(173名成人和39名未成年人)有效。根据GETE量表,反应良好的成年患者(n=35)血嗜酸性粒细胞计数中位数下降45.5%,而反应良好(n=88)和无反应者(n=48)中位数分别下降20.1%和0%。在未成年患者中也观察到类似的结果,优秀(n=11)和良好(n=17)应答者分别减少了55.7%和53.3%,而无应答(n=10)应答者减少了11.4%。这些结果表明,当SAA患者对奥马单抗产生应答时,血嗜酸性粒细胞计数下降。变化与反应状态(ANOVA)无统计学相关性。
6 - 12岁年龄组68例(男性50例(74%))(均数±)sd开始使用奥马单抗时,年龄8.6±1.7岁)。中位数·µL血嗜酸性粒细胞计数是776细胞−1and was ≥300 cells·µL−1在74%的案例中。Omalizumab在T4 - 6经治疗的肺科医师或儿科医师使用GETE量表,优良率为80.9% (95% CI 69.5-89.4%)。这是73.7% (95% CI 48.8 -90.9%)血液嗜酸性粒细胞·µL < 300细胞−1和83.7%(95%可信区间70.3 - -92.7%)·µL血嗜酸性粒细胞≥300细胞−1。均值±sd年哮喘恶化率从奥马单抗治疗前的5.7±3.3下降到T时的1.4±3.34 - 6。联合应对omalizumab治疗达到75% (95% CI 63.0 - -84.7%)的情况下,68.4%(43.5 - -87.4%)血液嗜酸性粒细胞·µL < 300细胞−1和77.6%(63.4 -88.2%)·µL血嗜酸性粒细胞≥300细胞−1。
64例为现吸烟者,180例为戒烟者(均数±)sd18.0±13.4久)。目前和戒烟者的戒烟效果有下降的趋势与不吸烟者。奥玛利珠单抗联合治疗的有效率为48.4% (95% CI 36.2-60.7%), 55.6% (95% CI 48.3-62.81%), 61.2% (95% CI 56.7-65.8%)。当血液嗜酸性粒细胞计数·µL < 300细胞−1目前吸烟者的综合反应率为42.5% (95% CI 27.2-57.8%),已戒烟者的综合反应率为56.8% (95% CI 46.5-67.2%),不吸烟者的综合反应率为62.0% (95% CI 55.3-68.7%)。
讨论
This report suggests that omalizumab response in patients with SAA does not vary with blood eosinophil count: omalizumab appears to be as effective in patients with “high” eosinophils (≥300 cells·µL−1),在那些“低”·µL嗜酸性粒细胞(< 300细胞−1)。这些结果仍与所有其他研究的嗜酸粒细胞的截断和响应的所有定义相似。
这些现实生活中的发现证实了那些已经发表在omalizumab上的额外研究事后分析显示相似的恶化率在48周omalizumab治疗时期·µL低(< 260细胞−1在基线)和高(≥260个细胞·µL−1基线时)嗜酸细胞亚群分别为0.65和0.70 [18]。然而,奥玛利珠单抗(与(安慰剂组)较低与基线时的高嗜酸性粒细胞计数[18];这种差异的一种可能解释可能是安慰剂治疗的高嗜酸性粒细胞组的高恶化率[18]。同样,在一个事后分析创新的研究,奥马单抗产生了一个更大的降低恶化率的患者较高与低基线嗜酸性粒细胞计数[19]和最近的事后对两项临床研究的分析也表明,奥玛利珠单抗对病情加重率降低的幅度更大与低嗜酸性粒细胞计数[20.]。在后者的研究中,只有3%的病人已经住院了前一年的恶化,表明患者中度到重度哮喘,而恶化率减少45% omalizumab嗜酸性粒细胞计数低基线显示患者临床疗效甚至较低的嗜酸性粒细胞(20.]。这些差异的可能解释事后分析和我们的研究包括STELLAIR是一个现实生活中学习,而不是随机,对照临床试验,STELLAIR不是事后分析表明,这里的病人有更严重的哮喘。不管这些,从STELLAIR研究和其他研究中可以清楚地看出事后到目前为止发表的分析是,奥马单抗可以有效降低SAA患者的恶化率,虽然一些研究显示,高基线嗜酸性粒细胞计数患者的反应更强烈,但这并不排除奥马单抗治疗的有效性。
STELLAIR的研究提供了关于SAA患者在启动哮喘第5步治疗全球计划(附加噻托吡肟、抗ige或抗il -5治疗)之前的嗜酸性粒细胞计数分布的新数据。研究显示不同意味着血液嗜酸性粒细胞计数为成人(451·µL细胞−1)和未成年人(685·µL细胞−1)在开始使用奥马单抗之前的12个月。未成年人的73.8%,52.1%的成年人·µL血嗜酸性粒细胞≥300细胞−1。这样的成年人可能有资格获得抗IL-5的治疗。由于一些患者经治疗OCSS这个数字可能被低估。在一个事后创新临床试验分析[19),59%(245例)的12 - 75岁患者血液嗜酸性粒细胞·µL≥300细胞−1在基线。在a中也发现了类似的结果事后额外试验的分析,52%的患者有一个平均基线·µL血液嗜酸性粒细胞数≥260细胞−1(18]。SAA患者的比例和血液嗜酸性粒细胞·µL≥300细胞−1接近这三个研究,评估重症哮喘患者符合生物治疗。一个cut-off of 400 cells·µL−1也在一些出版物中使用过,这些出版物关注的是哮喘患者的嗜酸性粒细胞计数,不论其严重程度如何[21,22];these studies showed a prevalence rate of 18–26% of patients with blood eosinophils ≥400 cells·µL−1。英国最近的一大群130 000哮喘病人发现血液嗜酸性粒细胞·µL > 400细胞−116%的患者(和26%的重症患者)(根据英国胸科协定治疗步骤,步骤4和步骤5)[23]。在我们的研究中,40%的成年人·µL血嗜酸性粒细胞≥400细胞−1在基线。综上所述,这些发现表明SAA和SEA患者之间有相当多的重叠,都对应于2型(Th2-high)哮喘。
本研究的主要局限性在于其回顾性设计。然而,患者特征和奥马单抗的有效性与以往临床研究的结果相似[6- - - - - -8]和在现实生活中设置[9- - - - - -15],包括成人及未成年人。STELLAIR的研究证实了成人中严重哮喘患者与未成年人之间的差异:成人中女性患者较多(60.9%),而未成年患者中男性患者较多(63.1%)。通过要求所有参与调查者包括符合严格选择标准的连续病人,也减少了选择偏差。电子病例报告表在一定程度上解决了偏倚问题。电子病例报告表的设计目的是通过适当的控制,将遗漏的数据降至最低,特别是对于带有强制字段的端点。数据检查和回顾证实患者有效地符合奥马单抗的条件,只有极少数患者(n=7)被排除在分析之外。此外,为了确保结果的稳健性,对omalizumab的响应被定义为三组完全收敛的标准。最后,STELLAIR研究是在法国进行的最大的真实世界的奥玛利珠单抗研究,包括10%的奥玛利珠单抗治疗的SAA患者的>。综上所述,很可能这些结果可以推广到符合奥玛利珠单抗条件的SAA患者,并由法国的肺科医生和儿科医生以及其他类似机构进行管理。
尽管针对每种表型存在或正在开发各种具有不同作用机制的生物疗法,但确定最佳治疗方案是一项具有挑战性的任务[24]。考虑到SAA和SEA有相当多的重叠,医生必须决定哪种治疗策略对出现SAA和SEA的患者更有效。STELLAIR的研究结果表明,与特异性针对嗜酸粒细胞激活途径的抗体相反,奥马单抗治疗对符合条件的SAA患者有效,而与治疗前的血嗜酸粒细胞计数无关。这些发现值得进一步研究,通过前瞻性研究评估针对重叠人群的严重持续性过敏性哮喘患者和高血嗜酸性粒细胞计数的生物制剂的临床有效性。
补充材料
确认
我们感谢所有研究中心的工作人员参与这项研究,感谢Matrix Consultants(法国)提供编辑服务,感谢Ian Wright(英国)和Celine Thonnelier(法国)为我们复印提交的手稿的最终版本。
STELLAIR的调查人员:M. Agossou (Fort de France), C. Appere de Vecchi (Argenteuil), E. Barbare (Meaux), M. Barbry (Taden), C. Belleguic-Lebreton (Rennes), D. Benhamou (Bois-Guillaume Bihorel), A. Bentaleb (Amiens), A. Blanc (Aix en Provence), P. Bonniaud (Dijon), M. Bourgoin (Paris), J. Brouard (Caen), P-M。Broussier (Bois-Guillaume Bihorel), d . Caimmi(蒙彼利埃),大肠Catherinot (Suresnes), r .凯龙星(蒙彼利埃),m . Claussner-Paulignan (Forbach), p . Combe-Cayla (Villefranche de Rouergue), p .横(布雷斯特),g . Dauriat(巴黎),b . Delaisi(布洛涅-比扬古),g . Devouassoux(里昂),t·迪迪(Metz-Tessy), a迪迪埃(图卢兹),美国多米尼克(鲁昂),p .杜蒙(Chauny) s杜利(兰斯),d . Dusser(巴黎),m . Fayon(波尔多),m . Gainet-Brun(比),g·加西亚-比塞特尔(Le),L. Guilleminault(圣皮埃尔留尼旺岛),N. Hesse(雷恩岛),S. Jeandeau(圣费雷岛),V. Jubin(勒布朗岛),J. Just(巴黎),N. Just(鲁拜岛),P-E。Kelkel (Chambery)的。Kerjan(马鲁),a·拉贝风(法国克莱蒙费朗),h . Laize (Sceaux), y Laoudi (Aulnay-sous-Bois), m . Larrousse(土伦),y勒冈(圣格雷戈勒),o . Leleu(阿布维尔),g . Letanche (Venissieux), g . Lorillon(巴黎),g . Mangiapan(完成),大肠马朗戈尼(圣死孚日),美国Marchand-Adam(旅游),p·马丁(Metz-Vantoux), c·毛雷尔(孟费?),f . Menivale (Colombiers), b . Mouget (Vandoeuvre les南希),d·穆勒(梅斯),m . Nasr(公报),l .阮(波尔多),j]。奥斯特(科尔),h . Pegliasco(马赛),b·菲利普(Pontoise),即销(La Tronche), c .第一道(La Tronche), a普鲁斯特(尼姆),a .普(塔布),c·拉(斯特拉斯堡),a Rakoto(沙龙餐厅苏尔Saone), c . Rochefort-Morel(雷恩),c . Rolland-Debord(巴黎),p . Romand (Contamine苏尔Arve), p . Roux(比),c .解决(Le克里姆林宫Bicetre), d . Siret(圣Nazaire), c .身材(巴黎),l . Tetu(图卢兹)-ⅰ。Tiotiu (Vandoeuvre les Nancy)、C. Tummino (Marseille)、J. Valcke (Vanves)、S. Verdier (Perpignan)、P. Vigneron (Lorient)、J. Virally (Aulnay-sous-Bois)、S. Wanin (Paris)都在法国。
脚注
作者贡献:M. Humbert, M. Molimard, L. Mala和V. Le Gros对数据获取、数据分析和解释做出了贡献。M. Humbert和M. Molimard对研究概念、设计、分析和解释作出了贡献。C. Taille和J.只是对分析和解释有贡献。所有作者都参与了手稿的准备和审查,并批准了最终版本的提交。
支持声明:诺华制药。该研究的资助人对研究设计、数据解释和报告的撰写作出了贡献。通信作者可以完全访问所有数据,并有提交发表的最终责任。本文的资助信息已存入Crossref资助者注册表。
利益冲突:M. Humbert与包括阿斯利康(AstraZeneca)、葛兰素史克(GSK)、诺华(Novartis)、罗氏(Roche)、赛诺菲(Sanofi/Regeneron)和梯瓦(Teva)在内的制药公司有关系。除了在涉及这些公司的试验中担任调查人员外,与这些公司的关系还包括咨询服务和科学顾问委员会的成员资格。C.在进行研究期间,泰勒从Kappa Sante收取个人费用;从阿斯利康公司、勃林格公司、诺华公司和ALK公司收取个人费用并担任研究调查员;从Chiesi公司和Teva公司收取个人费用;从葛兰素史克公司收取研究补助金和个人费用并担任研究调查员;L. Mala是诺华制药公司SAS的一名员工。V. Le Gros是诺华制药公司SAS的一名员工。J.刚刚从ALK和Stallergenes获得了个人费用,并从诺华公司获得了资助和个人费用。M. Molimard从诺华制药(Novartis Pharma)、葛兰素史克(GSK)和勃林格殷格翰(Boehringer Ingelheim)获得个人费用(用于咨询协议和参与科学顾问委员会),并在研究期间受雇于波尔多大学(University of Bordeaux);并获得了诺华制药公司提供的无条件教育资助。
- 收到了2017年12月5日。
- 接受2018年3月12日。
- 版权©2018人队
这篇ERJ开放文章是开放获取的,并根据知识共享署名188滚球软件非商业许可4.0条款发布。