文摘
医生需要护理路径中选择一个生物2型严重哮喘(omalizumab、mepolizumab reslizumab)http://ow.ly/pygw30gB7Bv
介绍
严重哮喘患者通常受益于与哮喘专家磋商优化管理,其中可能包括潜在的起始的生物制剂治疗严重疾病方面取得了突破。
Omalizumab,单克隆抗体(mAb)对免疫球蛋白E (ige),是第一个生物开发用于治疗严重的过敏哮喘和一致的随机对照试验的结果(相关的)1)或现实生活中试验(2]证明减少严重发作在成人和儿童3]。一些nonatopic哮喘患者也可能受益于omalizumab [4]。需要进一步的调查,以更好地评估其临床疗效在此设置,并识别预测治疗反应。
嗜酸性粒细胞是重要的细胞在哮喘。Mepolizumab或reslizumab anti-interleukin-5 (anti-IL-5)马伯或benralizumab anti-IL-5受体马伯,有效减少急性加重患者的严重哮喘(嗜酸性5]。
其他生物制剂针对哮喘在发展的不同路径。Dupilumab,一个对IL-4-receptor-α阻断il - 4 / IL-13马伯,有前景的结果(6]。
不同生物制剂针对IgE和IL-5目前可用,但医生优先考虑最优有困难对于一个给定的病人。这是由于重叠在病人人群可以享受不同的生物制剂,由于不存在直接比较和荟萃分析治疗不能确凿的(7,8]。护理路径需要帮助医生分层严重哮喘患者(9)选择适当的生物。
从指导护理途径
综合保健途径(icp)结构化的多学科治疗详细计划是必不可少的病人管理步骤。他们促进翻译的指导方针为协议和随后的应用于临床实践。他们还让患者和健康和社会保健专业人员。icp不同于实践指南,他们由一个多学科小组,专注于利用和协调护理质量。icp,标准的护理在肿瘤或姑息治疗,已经提出了哮喘,慢性阻塞性肺疾病和过敏性鼻炎10和已经数字化11,12]。
护理路径在严重的哮喘
哮喘严重程度的定义,提出了控制和急性加重,世界卫生组织(世卫组织)(13]。U-BIOPRED的共识(无偏预测生物标志物的呼吸道疾病的结果)还提供了一个算法基于不足严重哮喘治疗,治疗依从性差和/或multimorbidity [14,15]。最近,美国胸科学会/欧洲呼吸学会工作组提出了发达国家的严重哮喘(建议188bet官网地址16]。
适当诊断的病人,严重哮喘是由当前临床水平的控制和风险:“不受控制的哮喘会导致频繁的严重恶化的风险(或死亡)和/或药物不良反应和/或慢性疾病(包括肺功能受损)”(13]。icp的分段方法严重哮喘提出了他在2009年(13]。患者要求生物制剂是不受控制的哮喘,尽管最佳药物治疗。
所有生物制剂批准用于哮喘的欧洲药品局(EMA)和美国食品和药物管理局(FDA)包括分层严重哮喘患者控制控制器尽管在高剂量治疗包括至少吸入激素(ICS)和严重恶化。全球倡议的哮喘(吉娜)策略,omalizumab, mepolizumab和reslizumab代表第一个(目前,只有)治疗严重哮喘(步骤5)(数据来自吉娜:ginasthma.org)。英国国家健康和保健研究所(NICE)在2013年提出了omalizumab替代指导(17),回顾了2016年,2017年和mepolizumab reslizumab (表1)。
组件生物制剂治疗途径的哮喘
改善保健途径理解机制
生物制剂的作用机制
严重哮喘的治疗方法主要是2型哮喘的表型特征的突出作用2型细胞因子il - 4、IL-5 IL-13, IgE [18]。生物制剂的作用机制需要考虑由于omalizumab表示为中度到重度过敏哮喘不管基线嗜酸性粒细胞计数,而anti-IL-5可以有效的过敏性和非过敏性哮喘嗜酸性。
生物标志物是重要的帮助指导个性化治疗严重的哮喘,但可用的代表的不完美的鉴别器选择个别病人的最佳选择(18]。呼出一氧化氮分数的角色(F伊诺)和periostin不够理解,所有可用的生物制剂是有效的在主题与高嗜酸性粒细胞计数19]。此外,与当前的知识,利用现有生物标志物没有有用的评估在短期或长期的疗效。
年龄
Omalizumab批准6岁以上的儿童教育津贴在2009年和2016年FDA (3]。其他现有的生物制剂尚未批准在12岁以下儿童年。
调整剂量
Omalizumab每2 - 4周皮下基于基线管理总IgE水平和体重。Reslizumab管理基于体重每4周静脉注射(3毫克公斤−1)。Mepolizumab管理作为一种固定剂量皮下注射每4周。
停止规则
生物制剂是昂贵的治疗有效,应该持续了好几年。因此重要的是要评估他们是否应该继续在短疗程(如。不到4个月:早期的停止规则),可以停止在较长的疗程(如。3年:末停止规则)。
早期停止规则
早期的停止规则是追究omalizumab [24]。基线特征没有准确预测与omalizumab受益。的全球评估治疗效果治疗16周后,医生是最有意义的衡量对治疗的反应。这是确认在所有相关的或现实生活中研究[25]。没有数据支持验证停止规则anti-IL-5马伯。然而,好12月提出了指导停止规则anti-IL-5马伯(表1)。
末停止规则
一些数据可以帮助临床医生决定长期使用哮喘生物制剂。效益和持久性的前瞻性研究评估反应主题继续或退出长期omalizumab治疗(26]。更多学科omalizumab组(67%)没有恶化相比安慰剂组(47.7%)。时间先恶化也不再omalizumab治疗病人,和主题继续omalizumab明显比那些更好的哮喘控制停止。无后期停止规则研究可供anti-IL-5马伯。
护理路径严重哮喘的生物
病人分层生物制剂
患者分层可用生物疗法是主要基于临床终点,过敏测试,IgE水平和血液嗜酸性粒细胞(表2)。有数据periostin等其他生物标记或不足F伊诺。最优切断的嗜酸性粒细胞的起始anti-IL-5仍受争论。最低级别的150毫米3通常是利用mepolizumab基于关键试验(27),但提出了一个更高的水平好(表1)。血嗜酸性粒细胞计数为400毫米3被认为是reslizumab的阈值初始化28]。
护理路径严重哮喘的生物制剂
基于当前的知识,我们提出生物制剂的ICP严重哮喘帮助医生辨别病人资格omalizumab或anti-IL-5马伯使用一个简单的循序渐进的工作方式(盒子1)。这不仅基于马伯的疗效和安全性,但也可用性的早期停止规则和年龄(图1)。
箱1综合保健途径帮助医生辨别的严重哮喘患者有资格获得omalizumab或anti-interleukin-5单克隆抗体(anti-IL-5 mab)
步骤1
有一些简单的情况:
为患者过敏但不是嗜酸性(水平< 300 mm3),omalizumab应该是第一选择。
不过敏的患者和有一个高血嗜酸性粒细胞计数(mepolizumab≥300毫米3,reslizumab≥400毫米3应该考虑),anti-IL-5马伯第一行(29日]。
儿童6岁和< 12岁,符合规定标准,omalizumab是唯一的选择。
的患者都是过敏和嗜酸性,符合规定标准的这些代理,没有直接的比较数据
存在,荟萃分析没有信息,这两种类型的治疗可能被视为第一线治疗。然而,当
决定,临床医生应考虑能够停止omalizumab 16周后,结合大量的
现实生活中的数据和十多年的上市后监管确认其安全性。
步骤2
对于omalizumab-treated患者,16周后,全球在omalizumab-treated评价治疗效果的评估
病人和一个开关anti-IL-5马伯提出了那些没有回应和高血嗜酸性粒细胞计数。这是可能的
之前因为mepolizumab可能有效的病人治疗omalizumab [30.]。
对于anti-IL-5 mAbs-treated病人,一个相对模糊的停止规则提供了不错的(表1在12个月)。
重要的是,没有数据检查与不同的生物制剂联合治疗对于那些部分反应。
有一个重大的未满足的治疗需求人嗜酸性粒细胞计数较低,不过敏。支气管热成型术
可以考虑在这个实2患者人群和实质性的应进行检查,评价为合规
治疗,其他哮喘multimorbidities (如。胃酸倒流,鼻窦炎),危险因素(如。吸烟、过敏原接触)或差
诊断(如。慢性阻塞性肺疾病、愿望、声带功能障碍)。
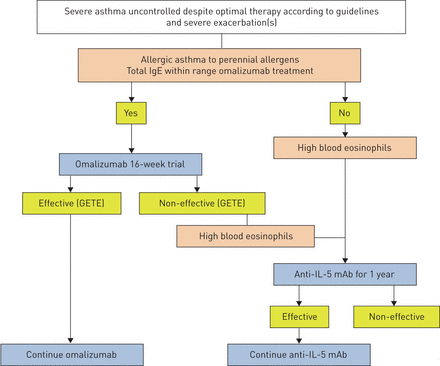
护理路径哮喘的生物制剂。搞笑:免疫球蛋白;GETE:全球评估治疗效果;IL:白介素;马伯:单克隆抗体。
结论
这手稿处理一个快速变化的领域,因此提议应该定期更新(31日]。高水平的证据比较疗效和生物制剂的有效性缺乏严重哮喘,因为没有直接相关的比较ige和anti-IL5。严重哮喘需要平台试验比较不同生物制剂,但也比较其他药物(如。长效毒蕈碱的拮抗剂、阿奇霉素、口服前列腺素D2拮抗剂(CRTH2拮抗剂))和后备治疗(如。支气管热成型术;肺康复;减肥)作为马伯的附加或更换。
披露的信息
补充材料
j . Bousqueterj - 01782 - 2017 - _bousquet
g . Brusselleerj - 01782 - 2017 - _brusselle
r . Buhlerj - 01782 - 2017 - _buhl
一部关于会先erj - 01782 - 2017 - _busse
嗜克鲁兹erj - 01782 - 2017 - _cruz
r .也有erj - 01782 - 2017 - _djukanovic
n.a Hananiaerj - 01782 - 2017 - _hanania
m·亨伯特erj - 01782 - 2017 - _humbert
答:孟战争机器erj - 01782 - 2017 - _menzies麻醉品
w . Phipatanakulerj - 01782 - 2017 - _phipatanakul
脚注
利益冲突:披露可以找到与这篇文章www.qdcxjkg.com
- 收到了2017年8月31日。
- 接受2017年10月3日。
- 版权©2017人队















