抽象
使用来自26个中心的耐多药结核病(耐异烟肼和利福平)患者的个人数据进行了治疗反应的荟萃分析。分析评估了对氟喹诺酮类和/或二线注射药物的额外耐药性对治疗结果的影响。
与治疗失败、复发和死亡相比,感染无附加耐药性菌株的耐多药结核病患者的治疗成功更高(n=4763;64%, 95% CI 57-72%)或仅对二线注射剂耐药(n=1130;与对氟喹诺酮类药物耐药的患者相比(n=426;48%, 95% CI 36-60%)或氟喹诺酮类药物加二线注射药物(广泛耐药(XDR)-TB) (n=405;40%, 95% CI 27-53%)。在广泛耐药结核患者中,如果在强化阶段使用至少6种药物,治疗成功率最高(调整或4.9,95% CI 1.4-16.6;参考少于三种药物)和四种(OR 6.1, 95% CI 1.4-26.3)。当强化期达到6.6-9.0个月,总治疗期达到20.1-25.0个月时,广泛耐药结核患者的成功几率最大。
在广泛耐药结核病患者中,与耐多药结核病推荐的药物相比,含有更多药物但持续时间相似的方案与成功率最高相关。
所有数据均来自观察性研究和中心之间变化的方法,因此,偏差可能是很大的。更优质的证据需要优化方案。
介绍
耐药性的结核病(TB)菌株中出现首次报道> 60年前引进的第一个抗生素来治疗结核病后不久[1- - - - - -3.]。从那时起,世界范围内出现了更广泛的耐药模式,近年来结核病患者的耐药水平最高[4]。在白俄罗斯和前苏联其他国家,超过初治结核病患者的四分之一,并且超过谁以前治疗,现在感染的菌株既利福平和异烟肼(耐多药耐药的一半结核分枝杆菌(耐多药结核病)[5]。2010年,全球估计有1200万结核流行病例,其中约65万例感染了耐多药结核菌株。据估计,中国和印度每年均有6万例耐多药结核病病例出现在这些国家通报的肺结核患者中[6]。从一些设置监视数据表明,平均来说,9.4%MDR-TB的菌株(95%CI 7.4-11.6%)具有与两个氟喹诺酮类和二线注射药物的附加阻力,即。广泛耐药(XDR)-TB [7]。XDR-TB,从而发生在高HIV感染率设置,所述的第一个报道爆发特征在于非常高的死亡率[8]。随后的报告已经证实,XDR-TB治疗效果通常比MDR-TB [更糟9]. 关于耐氟喹诺酮类药物和二线可注射药物对耐多药结核病患者的个体化耐药对预后的影响,目前还缺乏相关资料[10]。
耐多药结核病的治疗是困难的。当前的治疗方案与用于治疗药物敏感型结核病的方案相比,效果较差,但成本更高、毒性更大、疗程更长[11,12]。由于没有发表关于耐多药结核病患者治疗的随机试验,支持当前建议的证据质量较低,而且主要基于观察性研究[13]。这导致了相当大的争议有关最佳的治疗。有关于治疗患者的耐药性更先进的模式,比如XDR-TB甚至更少的证据。其结果是,目前世界卫生组织(WHO)对广泛耐药结核病患者的治疗建议是基于单独专家意见[11]。
我们进行了个体患者数据荟萃分析探索的患者特征,方案组合物和持续时间上的治疗结果为MDR-TB患者根据它们的感染菌株是否必须要么氟喹诺酮类或二线注射药物的附加阻力分组的效果,或两者(XDR-TB)。
方法
数据采集
收集和分析个别患者数据是为了解决由世卫组织召集的专家指南开发小组提出的具体问题,该小组旨在修订耐药结核病治疗建议[13]. 必要时,该研究得到了蒙特莱尔胸部研究所和麦吉尔大学健康中心(加拿大蒙特莱尔)道德审查委员会委员会以及参与中心当地道德审查委员会的批准。这项研究被美国疾病控制和预防中心确定为不涉及可识别人类受试者的研究,因为最初收集的匿名数据用于不同的目的。
纳入个体患者数据荟萃分析的研究是根据最近三篇耐多药结核病患者耐多药结核病治疗结果系统综述中发表的原始研究确定的[14- - - - - -16]。这些审查搜索的文摘和MEDLINE数据库,Cochrane图书馆和科学ISI Web和纳入研究1970年以后发表了报道与至少一个治疗结果的原始数据与商定的定义[一致17]适用于经细菌学证实的耐多药结核病患者。所有确定的研究都来自于对患者群体的观察性研究;没有一个是随机试验。大多数患者在专门的转诊中心接受个性化治疗。
这项荟萃分析的附加纳入标准是可以联系研究作者;他们愿意分享他们的数据;该队列包括≥25名耐多药结核病患者。匿名提供的信息包括病人的人口统计数据(年龄和性别),临床特征(网站的疾病,预处理痰涂片结果抗酸的细菌和文化,胸部x线摄影,艾滋病毒感染,使用抗逆转录病毒疗法(ART)),药敏测试(DST)结果(初始DST)使用的所有一线和二线药物,治疗因素(药物首次和连续阶段和持续时间的治疗,手术切除)和治疗结果,包括不良事件。如果患者只有肺外结核病或缺少药物治疗方案或治疗结果方面的信息,则个别患者被排除在数据集之外。我们只纳入了至少有一种氟喹诺酮和一种二线注射药物的DST结果可用的患者。大多数中心对阿米卡星或卡那霉素的敏感性进行了检测;本分析将这两种氨基糖苷的抗性归为一个变量。在本研究中,阿米卡星、卡那霉素和卷曲霉素被认为是二线注射药物,而不是链霉素。 The term macrolide refers to azithromycin, clarithromycin or roxithromycin. Later-generation fluoroquinolones refer to gatifloxacin, levofloxacin, moxifloxacin and sparfloxacin. Low-dose levofloxacin refers to a daily administration of <750 mg. The drugs belonging to group 4 and group 5 used in patients included in this study are listed in online supplementary table S1 (data from [18]).
数据分析
用于进行个体患者数据荟萃分析的方法基于Cochrane协办建立的标准[19],并在其他地方进行了更详细的描述[20]。在我们的分析中,我们考虑了药物暴露的三个因素:1)个体用药;2)可能有效的药物使用数量;3)治疗疗程。如果DST结果显示该菌株是易感的,则认为药物可能有效。如果一种药物被报告在治疗期间的任何时候都被使用过,那么病人就被认为接触过这种特定的药物。用于分析治疗期间(强化期和总期)的时间间隔规定了每个子组中相当数量的病例。
首先,我们估计使用跨中心二项随机效应荟萃分析不同耐药模式的情况下汇集的比例(PROC NLMIXED在SAS 9.2版; SAS研究所,卡里,NC,USA)。对个体患者数据荟萃分析,我们使用随机效应的多变量logistic回归(随机截距和随机斜率)与惩罚拟似然为了评估药物 - 暴露对治疗结果(使用PROC GLIMMIX在SAS)的影响[21- - - - - -23]. 对五个协变量的估计值进行了调整:年龄、性别、艾滋病毒感染、疾病程度(通过合并痰涂片阳性率和胸片上的空洞得分的复合协变量)和结核病治疗的既往史(这是一个三级变量:既往没有结核病治疗、既往使用一线药物治疗结核病和既往耐多药结核病使用二线药物治疗)。对多变量分析中使用的五个协变量进行缺失值估算。在插补时,如果超过一半的队列成员具有该变量的值,或者所有被分析的个体的平均值,我们使用来自该个体所属的同一队列的其他成员的平均值。调整后的优势比及其置信区间用于报告不同患者组的患者特征和结果之间的关联。
治疗成功定义为治愈或治疗完成[17]和用1)治疗失败,复发或死亡单个药物和药物数量的分析结果相比较;和2)失败或复发治疗持续时间的分析。谁死或拖欠的病人,因为大量的研究记录的实际,而不是治疗计划的长度,因此,持续时间是由死亡或默认缩短并没有在治疗时间分析中考虑。
结果
研究中心和患者的特征
来自31个中心耐多药结核病患者的个人数据可用于分析[24- - - - - -55(网上补充表S2)。五个中心没有关于药敏试验结果氟喹诺酮类和/或二线注射药物的信息。总体而言,与其他26个中心6724 MDR-TB病例被纳入分析。患者被放置在治疗中的各种队列1980和2009年22中心之间报道MDR-TB加到至少一个二线注射药物只(MDR-TB + INJr)电阻中的至少一个的情况下,18报告例MDR-TB加氟喹诺酮类只(MDR-TB + FQR)和17个中心有XDR-TB病例。在每个中心的队列的大小范围从一个到1786 MDR-TB病例。总体而言,4763(71%)患者具有MDR-TB,但易受到两个氟喹诺酮类和二线注射药物(仅MDR-TB),1130(17%)有MDR-TB + INJr,426(6%)具有MDR-TB + FQR和405(6%)具有XDR-TB。
6724例耐多药结核病患者的平均值为±SD39.5±13.5年岁,69%为男性,70%的人以前(一线和二线药物的10%,60%)和11%的治疗结核病是艾滋病病毒感染者(表格1). 两组患者的年龄和性别特征具有可比性。MDR-TB+FQr感染率(1.7%)和MDR-TB+INJr感染率(5.1%)均低于单纯MDR-TB患者(14%)。总共只有不到10名艾滋病毒感染者接受了抗逆转录病毒治疗。与其他耐多药结核病患者相比,XDR-TB患者在胸片上更容易出现空洞,并且使用二线药物治疗。
耐药模式
大多数中心的测试易感性单氟喹诺酮,主要是氧氟沙星,和更高代氟喹诺酮类药物很少。超过3000患者必须链霉素抗性,占所有测试的那些的61%(表2)。链霉素耐药性的流行是最高的患者耐二线注射药物中(即。广泛耐药结核或耐多药结核+注射)。对二线氨基糖苷(阿米卡星和/或卡那霉素)和卷曲霉素的耐药率分别为13%、30%的广泛耐药结核和33%的耐多药结核+注射。90%以上的广泛耐药结核患者对6种或6种以上的抗结核药物耐药。
结果
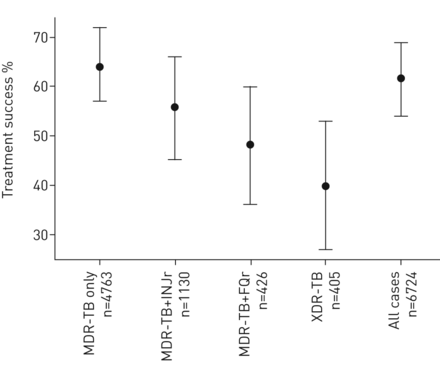
总的来说,62%的患者治疗成功,7%治疗失败或患者复发,9%死亡,17%违约(表3)。XDR-TB病例有治疗成功率最低和失败,复发和死亡的发生率最高。调整患者的临床特征和聚类的中心后,治疗的成功是显著与附加电阻所有三个MDR-TB患者组降低(表4)。治疗成功下降,因为耐药模式推进;治疗成功的最低赔率均可见XDR-TB并且是一个最低的患者的MDR-TB + FQR(图1)。对于年龄较大、疾病较严重、感染艾滋病毒或有结核病治疗史的患者,尤其是使用二线药物的患者,治疗成功的可能性也较低。
不同的耐多药结核病(MDR-TB)病人群体的治疗成功。数据显示为点估计和95%CI。MDRTB + INJr:MDRTB加耐阿米卡星/卡那霉素和/或卷曲霉素,但易被氟喹诺酮类;MDR-TB + FQR:MDR-TB加至任何氟喹诺酮抗性,但易被阿米卡星/卡那霉素和/或卷曲霉素(至少一个二线注射药物测试);XDR-TB:广泛耐药结核(MDR-TB加上电阻对任何氟喹诺酮类和任何二线注射药物(阿米卡星/卡那霉素和/或卷曲霉素))。
治疗与结果相关
特定的药物和疗法
治疗方案包括44%的患者服用乙胺丁醇,67%的患者服用吡嗪酰胺;超过85%的患者接受了注射药物(仅14%使用链霉素)。几乎90%的患者接受了氟喹诺酮,但只有5%的患者接受了新一代氟喹诺酮(在线补充表S1)。如果检测到氟喹诺酮类药物的耐药性,则较少使用(73% - 76%)与91-92%如果易感)。卷曲霉素是比阿米卡星/卡那霉素给予更频繁地给患者MDR-TB + INJr(56%与22%)和XDR-TB(40%与33%)。的患者在每个亚组几乎95%接受了至少一分4的药物,通常ethionamide药物或protionamide。环丝氨酸或特立齐酮给予更频繁时MDR-TB患者与附加电阻株(84-89%与58%),因为是P-氨基水杨酸(46 - 64%与35%。第5组药物在耐多药肺结核患者中的使用率(36-44%)也高于无耐多药肺结核患者(18%)。6%的患者进行了辅助性肺切除术;这在耐多药结核病+肺功能衰竭患者中最为常见(在线补充表S1)。
表5总结了不同耐多药结核病患者组中个体抗结核药物与治疗成功的相关性,并与失败、复发或死亡进行了比较。MDR-TB+FQr组和XDR-TB组的治疗成功与否无统计学显著相关。在耐多药结核病+注射组中,阿米卡星或卡那霉素(链霉素以上)和炔诺酮胺或普罗托纳胺与治疗成功显著相关。在仅限耐多药结核病患者组中,使用阿米卡星或卡那霉素、卷曲霉素、氧氟沙星、炔诺酮胺或普罗托纳胺和环丝氨酸均显著提高治疗成功率。相反,与接受一种第5组药物的患者相比,接受两种第5组药物的患者治疗成功的可能性更低,而接受不含氟喹诺酮或仅含一线药物的方案的患者治疗成功的可能性也更低(在线补充表S3)。MDR-TB+注射用含卷曲霉素方案治疗的患者比单用卡那霉素治疗的患者病情更严重。
讨论
我们发现,在多个中心治疗的耐多药结核病例的治疗结果逐步恶化,因为感染结核菌株的耐药模式是从无额外耐药性的MDR进展到对二线注射药物产生耐药性,再到对氟喹诺酮产生耐药性,然后对两者都产生耐药性(广泛耐药结核)。这一效应可归因于构成耐多药结核病治疗支柱的两类药物的有效性逐渐丧失。当异烟肼和利福平失去耐药性时,对治疗成功的负面影响在几年前就被证明了[56]。我们的研究结果来自于不同的患者群发表的作品,这表明在MDR-TB患者氟喹诺酮类或二线注射药物抗性较差的预后相关的补充[57,58对广泛耐药结核病患者的结果尤其不利[8- - - - - -10,35,40]。
为MDR-TB目前的治疗指南推荐使用的吡嗪酰胺与至少四个二线结核病药物一起被给予的可能是有效的在体外药敏结果及既往治疗史[13]。典型的治疗方案可以使用氟喹诺酮、二线氨基糖苷或卷曲霉素、乙硫胺或丙硫胺和环丝氨酸或特立西酮或P-氨基水杨酸。与任氟喹诺酮类或二线注射药物抗性,四个有效的药物的方案仍然是可能的,而无需使用任何的组5周的药物,其中大部分具有抗TB不确定活性。然而,到这两个类药物的抗性,难以构建含有足够数量的有效药物[容许方案11]。在创建可靠的治疗方案能力,这种差异可以解释为什么治疗效果是如此之低的XDR-TB小组。我们的荟萃分析的结果表明,XDR-TB患者的类似期限的方案,但更多的药物比方案由推荐用于MDR-TB患者无需额外的阻力更可能获得成功[20]。
在我们的研究中,我们发现大约三分之一对二线氨基糖苷类和卷曲霉素耐药的患者对这两类药物都有耐药性。这一发现可能表明这些药物类别之间存在交叉耐药,这种耐药已被描述过,但已知其不完整,因此其发生频率较低[59]。然而,它也可以由前面的曝光用的菌株轴承这个电阻图案解释这两种类型的注射药物或原发感染。中心可以凭经验使用卷曲霉素治疗例菌株二线氨基糖苷类抗没有能力来测试耐这种药物。许多患者接受多于一种类型的可注射药物的,但这些都顺序地接收,因为指示对第一注射的药物抗性DST的结果的居多,。我们的研究结果表明,卷曲霉素可能会不利于此类患者,并可能导致弊大于利,因为这个代理的已知毒性。二线药物的患者常常需要改变治疗的严重不良事件[60]。在我们的系列不良事件导致治疗的变化发生的情况下32%的整体。
另外一个重要发现是,病人的菌株对氟喹诺酮类药物,二线注射药物,或两种抗中,只有四分之一先前已与二线抗结核药物治疗。其余均与一线药物治疗或根本从未处理。这表明,许多的MDR-TB例株轴承附加阻力是由于与抗性菌株和,通过推断原发感染,即由应变采集耐药性并不一定损害其传递率〔61]。此外,广泛耐药结核菌株导致流行的倾向已得到充分认识,特别是在艾滋病毒流行率高的环境中[8]. 这一发现加强了在所有结核病控制方案中纳入全面感染控制部分的重要性。对耐药结核病患者的治疗也应及早制定适当的治疗方案,并在全球范围内扩大治疗范围,以覆盖比目前正在接受适当治疗的少数人更多的患者,特别是在高负担的环境中[6,62,63]。在2010年,已经开始治疗只有16%的估计世界范围内通知被报告的结核病患者中发生耐多药结核病例。此外,在艾滋病毒感染患者的耐多药结核病的早期ART的使用是非常重要的[13]。
这项研究是与株窝藏附加电阻的MDR-TB患者预后的最大的单个病人数据的荟萃分析。患者于多种设置(网上补充表S2),坐落在许多国家和所有世卫组织区域进行治疗,从而提高了结果的普适性。详细的数据,其被标准化,尽可能,是适用于所有情况。在治疗方案的差异往往体现在治疗医师的意见,过去的经验差异。因此,该数据集包括在所述的方法来治疗实质变化,独立的患者特征的差异。我们有机会来研究如何与治疗结果相关,这将是不可能的单中心报告。
然而,这项研究确实存在一些重要的局限性。在试图标准化变量的同时,结核病先前治疗的残余异质性、诊断方法、额外耐药性、药物质量、治疗方案、药物剂量、给药频率和胸部手术的使用使观察结果的汇集复杂化。已知乙胺丁醇、吡嗪酰胺和第4组药物的DST结果比定义广泛耐药结核的药物的DST结果更不准确和重复性。由于没有一项研究是随机对照试验,因此预期会出现严重的偏差和混淆,证据质量会被认为很低[64]。患有更严重疾病的患者,或感染了耐药性更强且有相当长的治疗历史的菌株的患者,可能更有可能接受更长时间的治疗,使用更多的药物,因为他们中的大多数人接受了个性化的治疗方案。我们发现使用任何5组药物或两组5组药物与较差的治疗结果相关,这可能反映了这种偏差,在多变量回归中无法充分调整。许多耐多药结核病和氟喹诺酮类药物耐药的患者接受了早期氟喹诺酮类药物治疗,他们几乎肯定是耐药的。对早期氟喹诺酮类药物产生耐药性的菌株可能仍然对后期药物敏感,应尽可能对这些药物进行DSTs治疗[65]. 很少使用新一代氟喹诺酮可以解释为什么在使用它们和成功的治疗结果之间没有发现显著的关联。最后,大多数数据集缺乏关于涂片或培养转换时间的信息,这被认为对指导临床医生的工作是有用的[11]。
致谢
对耐多药结核病患者个人数据进行荟萃分析的协作小组成员如下:s.d Ahuja(美国纽约长岛市),D . Ashkin(美国FL马樱丹属),m .阿根廷(多伦多,加拿大),r·巴纳吉(美国罗切斯特、锰),m·鲍尔(加拿大蒙特利尔,QC),贝拉一步(美国波士顿),a·贝内代蒂(加拿大蒙特利尔,QC), m .布尔戈斯(美国阿尔伯克基纳米),r .好像(Tradate、意大利),既有陈(美国科罗拉多州丹佛市)C.Y.蒋介石(台北,台湾),f . Cobelens h·考克斯(南非开普敦),l D 'Ambrosio (Tradate、意大利),W.C.M.德兰格(,荷兰哈伦的),k . DeRiemer(戴维斯、钙、美国),d . Enarson(法国巴黎),d . Falzon(瑞士日内瓦)K.L.弗拉纳根(Fajara、冈比亚),j .洪水(美国里士满CA), n·甘地(美国纽约布朗克斯),马丁Garcia-Garcia(库埃纳瓦卡,墨西哥).格拉尼奇(瑞士日内瓦)M.G. Hollm-Delgado(加拿大蒙特利尔,QC), T.H.霍尔兹(美国亚特兰大,佐治亚州),p .霍普韦尔医学Iseman(美国科罗拉多州丹佛市),低速齿轮Jarlsberg(美国旧金山,CA),美国Keshavjee(美国波士顿),H.R.金(韩国首尔)j•Koh(韩国首尔)J.L.兰开斯特(比勒陀利亚,南非),c·兰格(Borstel、德国)诉Leimane (Upeslejas、拉脱维亚),林祖嘉梁(中国香港),j·李(美国纽约),d .孟席斯(加拿大蒙特利尔,QC), G.B. Migliori (Tradate、意大利),C.D.米特尼克(美国波士顿),m .成田机场(美国西雅图,华盛顿州),大肠内桑森,r . Odendaal p baillie gifford(英国伦敦),m . Pai(加拿大蒙特利尔,QC), d . Palmero(布宜诺斯艾利斯,阿根廷),”栏目公园(马山市、韩国),g . Pasvol(伦敦,英国),J.M.佩纳(马德里,西班牙),c . Perez-Guzman(墨西哥的阿瓜斯卡连特斯),a·庞塞德利昂(墨西哥城,墨西哥),M.I.D. Quelapio(马卡迪、菲律宾),高韧性Quy,诉Riekstina (Upeslejas、拉脱维亚),j .罗伯特(法国巴黎),美国罗伊斯(美国旧金山,CA), m·萨利姆H.S. Schaaf (Tygerberg、南非),kj Seung(美国波士顿),l·沙阿(加拿大蒙特利尔,QC), k .珊T.S.垫片(韩国首尔),轮心(美国波士顿),y Shiraishi(日本东京)J . Sifuentes-Osornio(墨西哥城,墨西哥),g . Sotgiu(萨萨里,意大利),M.J.链(美国科罗拉多州丹佛市)S.W.唱,p . Tabarsi(德黑兰,伊朗),式样Tupasi(马卡迪、菲律宾),M.H.巴尔加斯(墨西哥城,墨西哥),r . van Altena(格罗宁根、荷兰),马丁范德沃特(比勒陀利亚,南非),T.S. van der Werf(格罗宁根、荷兰),p . Viiklepp(爱沙尼亚塔林),J Westenhouse(美国里士满CA),一部关于紫杉(中国香港),J.J.严(韩国首尔)。
作者还感谢以下个人在以下方面的帮助:R.Guilatco、G.Balane和M.Galipot在菲律宾的数据收集;M.Haslah和J.McNamee在多伦多的数据收集;P.Lobue在CDC(美国)的研究协助;D.Weissman、S.Atwood、T.Buu和E.Desmond在数据管理方面的协助,M、 Kato Maeda、J.Kirsten和G.Lin;R.Choe和S.Ramoutar提供秘书和行政协助;P.Becker提供南非数据的统计和后勤帮助。
免责声明:丹尼斯·法尔宗,鲁M.格兰尼奇和伊娃内桑森是世界卫生组织(WHO)的工作人员。作者单独负责本出版物中表达的观点,他们并不一定代表的决定或WHO的政策。蒂莫西H.霍尔茨是美国疾病控制和预防中心(CDC)的一名工作人员。单是笔者负责本出版物中表达的观点,他们并不一定代表的决定或CDC的政策。
脚注
有关编辑意见,请参阅第5页。
这篇文章有提供补充材料www.qdcxjkg.com网站
利益冲突:未申报。
- 收到2012年8月27日。
- 接受2012年10月5日。
- ©2013人队