摘要
阻塞性睡眠呼吸暂停综合征(OSAS)的诊断技术要求高、成本高、耗时长。电子鼻测量挥发性有机化合物是一种创新方法,可确定不同患者群体呼出气体的不同分子模式。我们解决了以下问题:电子鼻在检测中的诊断准确性如何OSAS的诊断和检测OSAS患者标准治疗效果的能力?这些结果是否与气道炎症和细胞外重塑的不同标志物的变化有关?
我们包括40名OSAS患者和20名健康对照。使用Cyranose 320电子鼻对所有参与者的呼出气进行分析。进行咽部冲洗以采集上呼吸道腔室样本。统计分析采用线性判别分析。
我们确定了将OSAS与对照组分开的线性判别函数(p<0.0001)。受试者操作曲线下的相应面积为0.85(95%可信区间0.75–0.96;敏感性0.93,特异性0.7)。在OSAS患者的咽冲洗液中,我们观察到α水平较高1.-与对照组相比,抗胰蛋白酶和细胞外重塑标记物。
电子鼻可以高精度区分OSAS患者和对照组。
介绍
阻塞性睡眠呼吸暂停综合征(OSAS)是一种常见病[1.]与心血管疾病风险增加相关[2.,3.].目前确认阻塞性睡眠呼吸暂停综合症的黄金标准是多通道多导睡眠描记(PSG) [4.]。这在技术上要求很高,耗时,而且劳动力和成本密集,可用性有限。
已经开发了不同的筛查工具来减少需要PSG的患者数量,但其中大多数缺乏敏感性和/或特异性。Epworth嗜睡量表、颈围和综合临床评分等临床参数显示,健康对照组和OSAS患者之间存在很大的重叠[5.–7.].
感知身体位置变化作为呼吸运动替代物的技术工具[8.],声音分析[9]心电图记录的复杂计算机分析[10都以不同的成功率进行了评估。一种新型的不需要夜间测量就能准确预测OSAS的筛选工具可以改进OSAS筛选算法。
一些研究表明,OSAS与氧化应激增加有关[11]以及全身和局部炎症[12]如呼气冷凝液(EBC)和血清中促炎细胞因子和其他标记物浓度增加所示[11].血清α水平1.-抗胰蛋白酶(α1.-AT),一种在炎症控制中起主要作用的急性期反应物[13],似乎也有所提升[14]其他化合物如基质金属蛋白酶(MMPs)和基质金属蛋白酶组织抑制剂(TIMPs)也可能作为正在进行的气道重塑的介质参与疾病过程[15].
经质谱分析证实,呼出的气体含有数百种挥发性有机化合物[16],其分析可提供有关全身或局部炎症的信息。呼出气体的评估也可通过能够识别挥发性有机化合物模式的设备进行,而不是识别单一化合物[17].事实上,这种设备可以区分多种疾病通过他们的挥发性有机化合物概况[18–20]。最近一篇综述潜在医学应用的文章已在其他地方发表[21]。据我们所知,尚未对OSAS患者的VOC谱进行评估。
我们的假设是模式识别电子鼻能够区分阻塞性睡眠呼吸暂停患者和健康对照组。此外,我们假设持续气道正压(CPAP)治疗对气道炎症和VOC水平有显著影响。为了通过直接测量生化化合物来证实这些数据,我们评估了健康对照组和osa患者在CPAP治疗前后的炎症和气道重塑标志物是否存在差异。为此,我们选择了EBC的pH和电导率,以及MMP-9, TIMP-1和α1.-至少在咽冲洗液中。
方法
学科与研究设计
在接受CPAP治疗之前,从医院工作人员中招募了20名健康志愿者,从睡眠呼吸暂停门诊招募了40名OSAS患者。健康对照组的纳入标准是参与的能力和意愿。在研究开始前的最后4周内患有任何已知慢性病或任何急性病或定期服用任何药物的志愿者被排除在外。OSAS被定义为呼吸暂停/呼吸暂停指数(AHI)>5个事件·h−1.结合阻塞性睡眠呼吸暂停的临床症状,我们排除了患有任何其他慢性和/或急性上呼吸道和/或下呼吸道疾病的患者(如.哮喘和慢性阻塞性肺疾病(COPD))。通过问卷调查(患者报告)对这些疾病进行评估。在任何怀疑的情况下,进行肺功能测试。系统记录了以下共病情况:冠心病、糖尿病和动脉高血压。在研究过程中,允许并保持疾病特异性药物治疗不变。该研究由当地伦理委员会(马尔堡伦理委员会AZ 59/06修正案3;德国马尔堡)批准,并获得每位受试者的书面知情同意。
所有参与者都进行了睡眠研究,并回答了有关症状、吸烟习惯、健康状况、药物和病史的问卷。此外,还进行了以下检查:收集咽冲洗液、收集EBC、使用Cyranose 320电子鼻测量呼出气(英国沃特福德史密斯检测集团有限公司)。40名OSAS患者中的前20名在CPAP治疗3个月后再次接受检查。
多导睡眠图/ polygraphy
疑似OSAS患者接受过夜PSG检查(Embla N7000;TNI Medical AG,Bad Ems,德国).使用既定程序测量脑电图、眼电图和肌电图。此外,记录胸部和腹部呼吸偏移、呼吸音、鼻腔气流、心电图和血氧饱和度。在健康对照组中,家庭多导图(德国汉堡SOMNOcheck2 R?Weinmann)AHI<5个事件·h−1.被定义为没有OSAS。
咽冲洗液
所有参与者必须禁食至少2小时,包括不嚼口香糖或任何糖果,不吸烟。他们用水漱口,然后用25毫升水漱口。液体储存在-80°C下,用于基于ELISA的TIMP-1和MMP-9分析(美国明尼苏达州明尼阿波利斯研发系统公司),根据制造商建议的常规程序进行。α1.-如前所述,通过ELISA测定AT[22].elisa检测TIMP-1、MMP-9和α的敏感性1.-AT为30pg·mL−1.,30pg·mL−1.和40pg·mL−1.分别地
EBC
使用ECoScreen Turbo(VIASYS;CareFusion Germany 234 GmbH,德国Höchberg)在15分钟内通过潮气呼吸收集EBC,如前所述[23].
电子鼻
呼出气用Cyranose 320电子鼻进行评估。参与者吸入医用空气(Aer medicinalis Linde;Linde Gas Therapeutics GmbH,Unterschleiβheim,德国)并以100–200 mL·s的流速呼气10 s−1.放入一次性收集袋中,然后在60秒内对其进行评估。该医用空气也用作60秒基线的参考空气,随后从收集袋中抽取60秒样品,并通过60秒电子鼻吹扫完成。这些测量一式三份[20].
数据分析
电子鼻获得的三个数据集通过每个个体的算术平均值取平均值。对这些数据进行主成分分析。将得到的转换数据输入线性判别分析。然后将线性判别分析结果用于进一步分析,包括非参数统计显著性检验。如前所述,测定各组之间的马氏距离,并对数据进行遗漏交叉验证,以计算交叉验证值[24]此外,使用线性判别式作为判别变量,构建受试者操作特征(ROC)曲线,以确定曲线下面积(AUC)。灵敏度和特异性值由线性判别式分析“自我预测”得出[25],这意味着使用完整的数据集来计算值。为了支持这一分析,我们另外进行了分半分析,将前20名患者作为训练集,将后一半作为测试集(以及反之亦然)敏感性和特异性是在特定的临界水平上报告的,其中敏感性和特异性之和(Youden评分)最高[26].
在进行统计比较之前,通过Kolmogorov–Smirnov检验对数据进行正态分布检验。对于非正态分布的数据,使用非参数检验(配对数据的未配对和Wilcoxon配对对的Mann–Whitney U检验符号秩检验),否则使用t检验(未配对或配对)。为了确定线性判别分析与炎症参数之间的相关性,计算了Spearman秩相关系数。数据表示为平均值±sd除非另有说明,所有统计分析均使用软件GraphPad Prism 5.00(美国加利福尼亚州圣地亚哥GraphPad Inc.)和SPSS版本20(美国伊利诺伊州芝加哥市SPSS Inc.)。
后果
患者与控制
40名OSAS患者和20名健康志愿者的基线特征如图所示表1.
OSAS患者和健康对照组的线性判别分析得分在统计学上存在显著差异(p<0.0001;Mann–Whitney U检验)(图1a)两组之间的马氏距离为1.88,交叉验证值为79.5%。当使用分半分析时,80%的“后半部分”被正确预测为OSAS。相反,当预测“前半部分”时在使用第二部分作为训练集后,85%的患者被正确预测患有OSAS。ROC曲线下的相应面积为0.85(95%可信区间0.745–0.960)(图1b),表明敏感性为0.93,特异性为0.70。此外,线性判别分析与AHI显著相关(Spearman's r=0.58,p<0.001),表明存在“剂量-反应”关系。线性判别分析与其他测量指标(EBC pH、EBC电导率和咽部冲洗液中的炎症指标)之间没有显著相关性。

a) 睡眠呼吸暂停患者和健康对照组的线性判别分析在统计学上有显著差异。b)受试者工作特征曲线下的面积等于0.85,导致敏感性为0.93,特异性为0.70。OSAS:阻塞性睡眠呼吸暂停综合征;HC:健康对照组。#:p<0.0001,Mann–Whitney U检验。
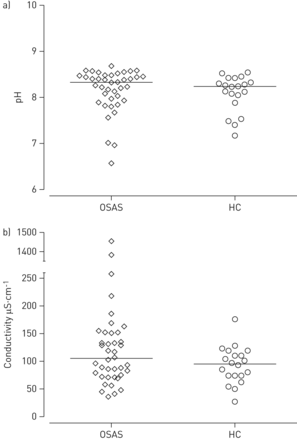
EBC pH值(OSAS中为8.16±0.47与健康对照组为8.09±0.40;p=0.27;t检验)和EBC电导率(175.5±292.9μS·cm−1.在OSAS中与93±33.36μS·cm−1.在健康对照组中,两组的p=0.17;t检验)无显著差异(图2).
a)pH值和b)电导率的呼出气冷凝液值在统计学上没有显著差异(t检验,分别为p=0.27和p=0.17)。OSAS:阻塞性睡眠呼吸暂停综合征;HC:健康对照组。
α1.-OSAS患者咽部冲洗液中的AT浓度显著高于健康对照组(60.6±52.0μg·mL)−1.与25.3±21.7μg·mL−1.;p=0.007;t检验)(图3a)相反,MMP-9的浓度差异(OSAS 5077.3±9104.5 pg·mL−1.与健康对照组1008.6±872.9 pg·mL−1.p=0.06;t检验)和TIMP-1(OSAS 7918.9±7075.7 pg·mL−1.与健康对照组6961.6±11412 pg·mL−1.; p=0.16;Mann–Whitney U检验)未达到统计学意义。然而,MMP-9/TIMP-1比值在各组之间显示出显著差异(OSAS 0.69±1.11)与健康对照组0.24±0.25;p=0.02;Mann-Whitney U检验)(图3b).与VOC分析相比,任何其他标记物(EBC pH、EBC电导率和咽洗液中任何标记物)在预测osa方面均较差(ROC曲线的AUC范围为0.59 ~ 0.71;数据未显示)。然而,咽部洗液中的炎症标志物和EBC pH/电导率结合线性判别分析将诊断准确率提高到100% (AUC of the ROC 1,95% CI 0.94-1.00)。
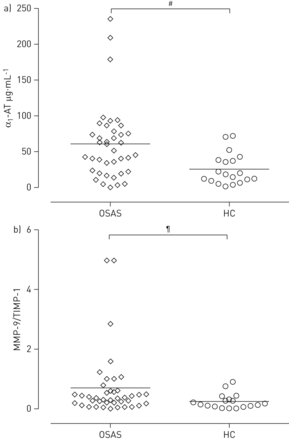
一)α1.-抗胰蛋白酶(α1.-阻塞性睡眠呼吸暂停综合征(OSAS)患者咽部冲洗液中AT)浓度和b)基质金属蛋白酶(MMP)-9/基质金属蛋白酶组织抑制剂(TIMP)-1比值明显高于健康对照组(HCs)。#:p=0.007,t检验;¶:p=0.02,Mann–Whitney U型试验。
CPAP治疗3个月前后的患者
在CPAP治疗开始之前和之后测量的前20名OSAS患者的特征列于表2.
标准CPAP治疗开始前后的线性判别分析值存在显著差异(p=0.0003;Wilcoxon检验)(图4a)两组之间的马氏距离为1.83,交叉验证值为63.1%,ROC曲线下的相应面积为0.82(95%可信区间0.6825–0.9475)(图4b),敏感性为0.80,特异性为0.65。
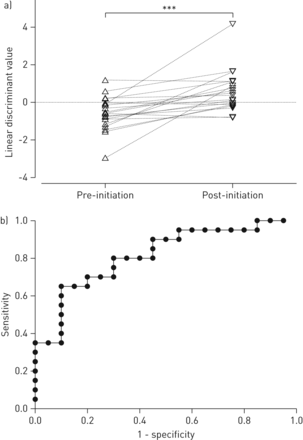
a) 连续气道正压治疗开始前(开始前)和开始后3个月(开始后)睡眠呼吸暂停患者的线性判别分析(配对)值在统计学上存在显著差异。b) 接收器工作特性曲线下的面积等于0.82,导致灵敏度为0.80,特异性为0.65。***:p<0.001,Wilcoxon符号秩检验。
两次就诊的EBC pH值相似(前-8.08±0.52)与起始后8.05±0.85;p=0.63,Wilcoxon试验)(图5a)然而,电导率不同(在-186.7±303.6μS·cm之前)−1.与起始后97.9±59.35μS·cm−1.;p<0.05,Wilcoxon检验)(图5b).
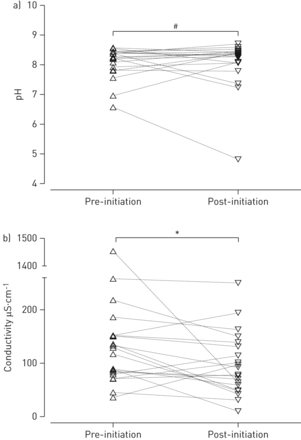
a)两次随访的呼出气体冷凝液(EBC)的pH值在统计学上没有显著差异,但b)两次随访的EBC的电导率值在统计学上有显著差异。#:p=0.63;*:p<0.05,均为Wilcoxon符号秩检验。
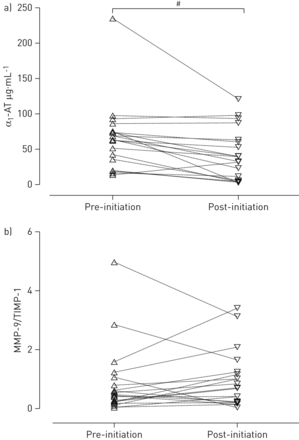
此外,α1.- at浓度在CPAP处理后显著降低(- 66.3±48.4 μg·mL)−1.与起始后42.8±36.3μg·mL−1.;p=0.017,配对t检验)(图6a)对于MMP-9(前-7785.6±10500 pg·mL−1.与起始后9185.8±11 003 pg·mL−1.p=0.421,Wilcoxon试验)和TIMP-1(前-8344.7±7201.1 pg·mL−1.与起始后13201±13151 pg·mL−1.;p=0.314,Wilcoxon检验)无显著差异。同样适用于MMP-9/TIMP-1比率(前-0.87±1.2)与起始后0.98±0.97;p=0.37,Wilcoxon试验)(图6b).
一)α1.-抗胰蛋白酶(α1.-持续气道正压治疗3个月后,咽部冲洗液中的AT)浓度显著降低。#:p=0.017,配对样本的t检验。b) 基质金属蛋白酶(MMP)-9/基质金属蛋白酶组织抑制剂(TIMP)-1比值在阻塞性睡眠呼吸暂停综合征患者治疗前(开始前)和治疗后(开始后)无显著变化(p=0.37,Wilcoxon符号秩检验)。
讨论
这项研究表明,Cyranose 320电子鼻能够区分OSAS患者和健康受试者呼出气体中VOCs的模式。线性判别法与AHI之间存在显著相关性。此外,电子鼻可以区分CPAP治疗前后的状态。这表明呼出气中的特定VOC模式与未经治疗的OSA有关。
呼出气挥发性有机物分析是获取疾病信息的一种相对新颖的方法。过去曾使用气相色谱法和质谱法[16].更简单的模式识别电子鼻允许快速识别“气味指纹”方面的挥发性有机化合物混合物[27],但不是单个分子组分的鉴定[17].
各种复杂的电子鼻已经在各种呼吸道疾病中进行了测试。原则上,耳、鼻和喉感染的诊断[28]还是肺炎[29]这是可能的。此外,肺癌患者[30],哮喘[31],慢性阻塞性肺病[18]或α1.-不足[20]与健康对照组或患有其他呼吸系统疾病的个体相比,可以被识别。在我们的研究中,我们旨在验证以下假设,即OSAS可以通过其VOC谱被识别,并且在CPAP治疗后该谱会发生变化。据我们所知,这是首次对OSAS患者的气味进行检测的研究与健康受试者比较。
我们的结果可能很有趣,因为几乎所有OSA筛查工具都需要夜间测量。尽管可用的设备易于操作,但一些记录质量较差,从而限制了其诊断价值。此外,一些患者在“连接到电子设备”时不愿意睡觉.相反,使用有限通道的夜间测谎不需要昂贵的医务人员,只需要两名患者到诊所就诊。因此,从其他来源进行诊断,如. “一口气”就可以了。
有人可能希望可以用单一物质来预测不同患者群体呼出呼吸曲线的差异。虽然气相色谱法和/或质谱法可以实现这一点,但由于成本巨大且耗时的数据分析,这些方法在临床环境中是不可行的在不知道疾病特异性物质的情况下,e(在计算水平上)模式是一种具有临床指导的现场方法的有希望的新尝试。
可以说,AUC为0.85不足以作为诊断工具。但是,诊断测试用于特定的临床情况。电子鼻在两种情况下可能有用。首先,为了排除低流行人群中的疾病,如.在全科医生办公室,OSAS的患病率是∼2–4% [1.]。阴性结果的阴性预测值为99.6%(95%可信区间为90.3–100%),因此具有高度的确定性。其次,该设备可以作为一种辅助决策工具,用于进行夜间PSG。在OSAS患病率较高的人群中(肥胖、打鼾的受试者高达35%),阳性结果的阳性预测值为62.4%(95%可信区间43.3–79.1%),并将为隔夜PSG铺平道路。相反,阴性结果的阴性预测值为94.5%(95%可信区间为78.9–99.6%),因此引起对OSAS以外诊断的注意。此外,AUC的值为0.85在日常临床实践中使用的其他诊断试验范围内,例如用于诊断心肌梗死的肌钙蛋白(AUC为0.87[32]).
为了揭示OSAS患者是否会有特定的化学或物理化学改变,我们还分析了EBC,重点关注易于获取的标记物,如pH值和电导率,我们最近发现这些标记物是稳健且可重复的,不受呼吸操作的影响[24].EBC pH值在8范围内,这与之前的报告相当[33–35].然而,我们没有发现这些措施的重大差异,这可能对该疾病来说太不具体了。
相反,α1.咽洗液中作为炎症标志物的-AT值在osaas患者中升高,仅在CPAP治疗3个月后降低。这可能反映了对间歇性缺氧和/或循环纯粹力量的反应,缓解了CPAP。炎症和/或氧化应激的局部和全身标志物也显示了类似的结果[36,37]我们使用MMP-9、TIMP-1及其比值作为进一步的标记物;该比率显示OSAS患者的水平升高。据我们所知,这是首次在OSAS局部隔室检测MMP-9/TIMP-1比率。在系统水平上,OSAS中MMP-9浓度和活性的增加已经被描述,CPAP治疗可以减少这些改变[38]这使我们相信MMP-9/TIMP-1比率的增加是慢性间歇性缺氧和用力后上气道重塑的一个指标。
这项研究有很多局限性。两组的年龄和体重指数(BMI)不匹配,这两个因素都是呼气分析中的潜在混杂因素。为了研究年龄和BMI是否是改变的VOC混合物的混杂因素,我们进行了以AHI为因变量的逻辑回归分析。电子鼻衍生的线性判别分析是最佳且唯一显著的预测因素AHI(OR 3.03,95%CI 1.41–6.51)与BMI(OR 1.17,95%CI 0.99–1.37)和年龄(OR 1.05,95%CI 0.98–1.12)相比,这也反映在AHI和线性判别分析之间的显著相关性(Spearman's r=0.58,p<0.001)中。此外,之前的VOC曲线的显著变化与CPAP治疗后表明,组间VOC谱的差异主要是由于OSAS的存在。与之前的出版物相比,这是一个主要优势,之前的出版物仅对VOC谱进行了一次评估,且未证明与其他生物标记物存在显著相关性。
由于OSAS患者共病情况的高患病率,可以认为VOC混合物的改变主要是由于共病和/或相关药物所致。然而,看看线性判别分析图(图1a)将冠心病(n=3)、糖尿病(n=5)和动脉高血压(n=27)患者作为标记,共病患者的分布没有趋势(见在线补充资料)。
由于缺少评估特定标志物绝对值的标准化程序,咽部清洗中炎症标志物的数据受到限制犯错等.[39]描述了吸烟者的防御素测量和咽部冲洗液已用于检测潜在的呼吸道病原体[40].尽管如此,α的数据1.-AT强化了α的假设1.-在未经治疗的OSAS中AT表达上调,咽冲洗有助于进一步研究这一点。
此外,假CPAP和随访数据将加强我们的研究,并增加关于呼吸印随时间变化的可重复性的数据。然而,这项概念验证研究的重点是诊断方法,目的是证明呼气分析对OSAS的诊断潜力的一般可能性。我们使用有限的呼气前/后比较来表明标准治疗改变了呼吸纹,并强调了观察到的OSAS呼气剖面差异的假设与健康对照组主要是由于存在/不存在梗阻性发作。
最重要的是,结果必须在一个单独的队列中进行验证,可能是在一个独立的中心,符合诊断准确性研究报告标准(STARD)诊断试验验证声明[41].
结论:Cyranose 320电子鼻能够较准确地识别OSAS患者和对照组的呼出气体。
致谢
Silke Mronga和Angelique Holland(马尔堡大学,Gießen和马尔堡大学医院,马尔堡,德国马尔堡)在2010年和2011年取代了第一和高级作者的临床职责。否则这项工作就不可能完成。
脚注
有关编辑评论,请参见第1页.
有关本文的新闻稿,请访问www.www.qdcxjkg.com/site/misc/presspack.xhtml这篇文章有补充资料可从www.www.qdcxjkg.com
支持声明:本研究由德国研究基金会(DFG)、SFB/Tr22A19和BeLund伦琴基金会(56-036)授予。
利益冲突:披露内容可与本文的在线版本一起在www.www.qdcxjkg.com
- 收到2012年6月10日。
- 认可的2012年10月4日。
- ©2013人队