摘要
肺泡2型(AT2)细胞是异质细胞,该谱系中的特化AT2亚群表现出干细胞特性。然而,在肺再生过程中被激活的AT2谱系中静止的未成熟细胞的存在是未知的。
SftpcCreERT2 / +; tdTomato液氧/液氧使用小鼠标记AT2细胞,标记亚群通过流式细胞术、定量PCR、利用测序(ATAC-seq)测定转座酶可及染色质、基因阵列、肺切除术和精确切肺切片培养进行分析。分析了来自人类肺部的单细胞rna测序(scRNA-seq)数据。
在小鼠中,我们检测到两个不同的AT2亚群,tdTomato水平较低(Tom低)和高td番茄水平(汤姆高).汤姆低细胞表达较低水平的AT2分化标志物Fgfr2b而且Etv5,而汤姆高,因为善意的成熟的AT2细胞,显示出较高水平的Sftpc,Sftpb,Sftpa1,Fgfr2b而且Etv5表达式。ATAC-seq分析显示汤姆低和汤姆高细胞构成两种不同的细胞群,具有特异性的沉默Sftpc,Rosa26和细胞周期基因位点低人口。在肺切除术后,汤姆的号码低但汤姆不是高细胞增加,Tom低细胞表达上调Fgfr2b,Etv5,Sftpc,Ccnd1而且Ccnd2与Sham相比。汤姆低细胞过表达程序性细胞死亡1配体1 (PD-L1),这是一种免疫抑制膜受体配体,通过流式细胞术来区分这两个亚群。在人类肺部,最近的scRNA-seq AT2数据集的数据挖掘证明了一个存在PD-L1Pos人口。因此,我们在小鼠中发现了一种新的AT2静止不成熟祖细胞群,它们在肺切除术后扩增,我们为这种细胞在人类中存在提供了证据。
摘要
一种新的AT2祖细胞群体已被鉴定为PD-L1富集。这种通常处于静止状态的AT2细胞亚群在肺泡损伤时变得高度增殖并分化为成熟的AT2。https://bit.ly/31G0IIW
简介
肺泡2型(Alveolar type 2, AT2)祖细胞在肺损伤后表现出自我更新能力,维持AT2细胞池并分化为AT1细胞[1- - - - - -5].然而,静止和未成熟的AT2祖细胞是否存在于小鼠和人类肺部,以及是否可以使用表面标记物分离这些细胞仍有争议。
在啮齿动物中,AT2细胞是异质的。基于e -钙粘蛋白(E-CAD)、AXIN2、整合素α6β4和表面活性剂蛋白C (SFTPC)/分泌珠蛋白家族1A成员1 (SCGB1A1)等多种标记,该谱系中具有不同干细胞特性的不同亚群已被鉴定[6- - - - - -9].AT2细胞可平均分为E-CADPos和E-CAD负的细胞。E-CAD负的细胞对高氧损伤的抵抗力更强,增殖能力更强,端粒酶活性水平更高,而E-CADPos细胞对损伤更敏感[6].在成年小鼠肺中,AXIN2Pos成熟AT2 (SFTPC)细胞占1%高)细胞,并分布于整个肺[8].这是AXIN2的比值Pos细胞是稳定的。在活的有机体内AXIN2的谱系追踪Pos(SFTPC高)细胞显示它们能够形成2 - 5个细胞的克隆,并扩增分化为表达podoplanin (PDPN)的AT1细胞。此外,与AXIN2相比,这些细胞在肺泡球中显示出增强的自我更新能力负的AT2细胞,表明这些AXIN2Pos细胞代表成熟AT2细胞亚群,具有增强的干细胞能力[8].在一项类似的独立研究中,AXIN2Pos属于成熟AT2细胞群的细胞被鉴定。这些细胞被称为肺泡上皮祖细胞(AEP),约占成年成熟AT2细胞的20%,富含WNT靶基因和发育基因,如Fgfr2,Nkx2.1,Id2下,Etv4,Etv5而且Foxa1。与总AT2细胞相比,这些细胞在肺泡球中也表现出更高的自我更新能力[9].
AT2细胞异质性不仅限于成人肺。在肺发育的肺泡发生阶段,AXIN2Pos与总AT2细胞相比,AT2细胞增殖增强[10].SFTPC的子集负的,层粘连蛋白受体整合素α6β4Pos位于支气管肺泡管连接处(BADJ)和肺泡内的细胞可再生AT2 SFTPCPos严重肺损伤后肺泡内的细胞[7].最后,肺泡标记物SFTPC和俱乐部细胞标记物SCGB1A1阳性的支气管肺泡干细胞位于BADJ,并在损伤时扩增,产生肺泡上皮细胞或俱乐部细胞[11- - - - - -13].在白喉毒素损伤的情况下,AT2细胞的异质性同样表现出来,具有谱系标记的AT2细胞亚群对白喉毒素毒性表现出相对更强的抗性,能够在损伤后重新填充AT2细胞池。然而,这些幸存细胞的身份尚不清楚。3.].
在本研究中,我们发现了一种新的AT2静止和未成熟祖细胞群,其特征为低Sftpc表面标记程序性细胞死亡1配体1(PD-L1)(也称为CD274)的水平和高表达,这是一种在癌症干细胞中表达并介导抗肿瘤抑制反应的免疫检查点蛋白[14- - - - - -16].我们部署了一系列在活的有机体内在小鼠中标记AT2细胞的不同亚群,检查它们的表观遗传和转录组特征,并测试它们各自的反应在活的有机体内在肺切除术后的肺再生过程中在体外使用精密切肺切片(PCLS)培养。我们还验证了PD-L1抗体对上皮亚群进行差异排序的使用,并对最近发表的AT2单细胞rna测序(scRNA-seq)实验进行了数据挖掘。我们的工作为深入描述这种新型静止和不成熟的AT2干细胞群开辟了道路。
材料与方法
动物实验
所有动物研究均按照德国吉森自治区动物伦理委员会批准的规程进行(许可编号:G7/2017-No . 1)。844-GP和G11/2019-No。931 - gp)。
全肺切除术
看到补充材料.
肺游离和荧光激活细胞分选
从成人肺中提取单细胞悬液,用抗epcam (apc - cy7偶联的,Biolegend, 1:50)、CD49F (apc偶联的,Biolegend, 1:50)、抗pdpn (fitc偶联的,Biolegend, 1:20)和抗pd - l1(未偶联的,赛默飞雪公司,1:100)抗体在冰中染色20分钟,然后清洗。然后用山羊抗兔二抗Alexa fluor 488 (Invitrogen, 1:500)对细胞在黑暗中冰上染色20分钟。接下来,根据制造商的说明,用SYTOX (Invitrogen)(一种活细胞/死细胞染色剂)对细胞进行清洗和染色。流式细胞仪数据采集和细胞分选使用FACSAria III细胞分选仪(BD Biosciences)进行。数据分析使用FlowJo软件版本X (FlowJo, LLC)。
看到补充材料为小鼠肺游离。
RNA提取和实时定量PCR
看到补充材料.
免疫荧光染色
看到补充材料.
Alveolosphere化验
看到补充材料.
微阵列
看到补充材料.
ATAC-seq
看到补充材料.
人类AT2细胞scRNA-seq数据集的挖掘
为了进行分析,我们使用存储在的突触ID (syn21041850)数据集https://www.synapse.org/ !年代ynapse:syn21041850/wiki/600865由T出版ravagliniet al。[17].Seurat对象更新到Seurat v3 [18]和AT2细胞采用子集函数提取。使用Seurat中的SCTransform包装器从原始计数开始重新分析数据集。然后使用ALRA包的低秩近似来执行数据imputation [19].
量化和统计分析
为了定量免疫荧光,每个样品在10个独立的63×场中计数细胞。使用GraphPad Prism 6 (GraphPad Prism Software)进行统计分析和图形组装。显著性由未配对双尾t检验确定。数据以均数±表示扫描电镜.p<0.05为显著。每组生物样品的数量(n)在相应的图例中表示。
结果
两种不同AT2亚群的鉴定Sftpc而且Fgfr2b水平
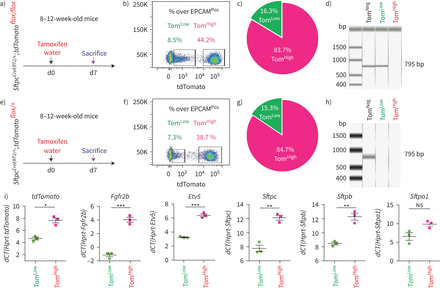
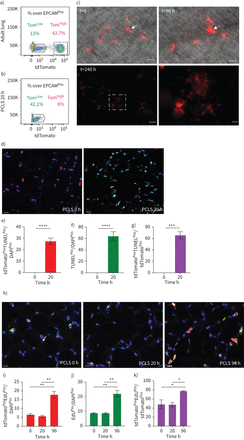
SftpcCreERT2 / +; tdTomato液氧/液氧小鼠被用来标记成年肺中的AT2细胞。在我们的实验方法中,他莫西芬在水中放置1周。tdTomato的两个不同亚群Pos(汤姆Pos)细胞,我们称之为tdTomato低(汤姆低)和tdTomato高(汤姆高),经流式细胞术分析(图1一个- c)。值得注意的是,一个类似的观察,这是没有后续的,之前报道使用SftpcCre-ERF .生成的鼠标行酒店et al。[20.].平均来说,汤姆低占EPCAM总细胞数的9.93±1.73%Pos细胞(n=4)和汤姆高占总EPCAM的42.75±1.22%Pos细胞(n = 4)。从汤姆身上Pos均数为17.58±2.52% (n=4)低Tom占81.93±2.3% (n=4)高.我们还确定了重组的程度LoxP-STOP-LoxP-tdTomato磁带在孤立的汤姆低和汤姆高细胞。我们的结果表明在Tom中观察到完全的重组高而Tom则出现不完全重组低,由存在795 bp的终止密码子带(图1 d).这一结果表明,汤姆的污染低池被非at2细胞或缺乏访问Cre到LoxP-STOP-LoxP-tdTomato盒式磁带Rosa26汤姆位点低细胞。基于番茄强度的两个亚群的存在也可以通过LoxP-STOP-LoxP-tdTomato卡带的一个或两个拷贝的不适当重组来解释tdTomato液氧/液氧老鼠。为了测试这些不同的可能性,我们进行了类似的实验SftpcCreERT2 / +; tdTomato液氧/ +老鼠,只展示一个拷贝的LoxP-STOP-LoxP-tdTomato盒(图1 e- h)。同样,我们也发现了汤姆的两个亚群Pos重要的是,细胞的完全重组LoxP-STOP-LoxP-tdTomato盒式磁带低,表明Tom中没有被非at2细胞污染低池。这一结论得到了我们对内皮细胞、造血细胞、巨噬细胞和成纤维细胞标记物的定量PCR数据的支持(补充图S1).总的来说,我们的数据支持存在两个AT2细胞亚群SftpcCreERT2 / +; tdTomato液氧/液氧肺,根据不同的水平番茄表达式。这是由于的微分表达式番茄本身从Rosa26汤姆的启动子高与汤姆低细胞。此外,在SftpcCreERT2 / +; tdTomato液氧/液氧肺,这也与不完全重组有关LoxP-STOP-LoxP卡带,其中也位于Rosa26轨迹。
鉴定at2谱系标记细胞的两个亚群,命名为tdTomato低(汤姆低)和tdTomato高(汤姆高).a)他莫西芬治疗的时间表SftpcCreERT2 / +; tdTomato液氧/液氧老鼠(n = 4)。医生:一天。b) EPCAM代表性流式细胞术Pos汤姆的群体选择与鉴定低(8.5%)和汤姆高(44.2%)基于tdTomato水平的种群。c) Tom的百分比低(16.3%)和Tom高(83.7%)Pos细胞。d)荧光激活细胞分选(FACS)分离的Tom基因组DNA PCR低和汤姆高细胞SftpcCreERT2 / +; tdTomato液氧/液氧小鼠为停止密码子。e)他莫西芬治疗的时间表SftpcCreERT2 / +; tdTomato液氧/ +f) Tom的代表性流式细胞术分析低(7.3%)和Tom高(38.7%)。g)饼状图显示了Tom的百分比低(15.3%)和汤姆高(84.7%)占总tdTomatoPos细胞。h)对分离的Tom基因组DNA进行PCR分析低和汤姆高细胞SftpcCreERT2 / +; tdTomato液氧/ +老鼠。i)基于facs分类的Tom的定量PCR分析低和汤姆高细胞的表达番茄,Fgfr2b,Etv5,Sftpc,Sftpb而且Sftpa1.dCT:增量周期阈值。数据以均数±表示扫描电镜.*: p < 0.05;* *: p < 0.01;* * *: p < 0.001。
我们还证实上皮细胞在该小鼠系中被特异性标记,且标记主要针对AT2 SFTPCPos细胞(补充图S2).通过BADJ定位发现的少量BACS细胞被标记(占总数的0.1%)Pos细胞,数据未显示),与文献一致[7].AT2细胞的标记效率为77±5.40% (n=4) (补充图S2b).在这条老鼠线,4.5%的汤姆Pos在暴露于正常水的小鼠中标记/总细胞,表明渗漏。这一比例增加到汤姆的20.5%Pos/暴露于他莫西芬水1周的小鼠细胞总数(补充图S3),表明标签有很强的诱导作用。我们还在8周龄时将小鼠暴露在他莫西芬水中1周,然后进行6个月和9个月的追踪期。我们的数据表明汤姆低和汤姆高在这两个时间点检测到亚种群,并且是稳定的种群(补充图S4).
接下来,对荧光激活细胞分选(FACS)分离的Tom进行qPCR低和汤姆高细胞。我们的结果表明Fgfr2b及其相关的下游目标Etv5,以及分化标记Sftpc, Sftpb而且年代ftpa1,在汤姆体内显著富集高与汤姆低细胞(图1我).因此,我们得出结论,汤姆高代表了善意的成熟的AT2细胞,我们假设谱系相关的汤姆低细胞代表未成熟的AT2细胞。
ATAC-seq分析显示汤姆低cells和Tom高细胞是不同的细胞群
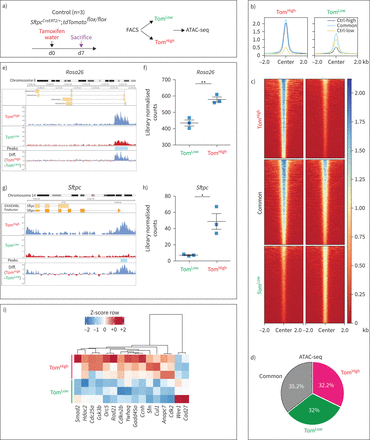
为了对表观基因组景观进行全基因组分析,对Tom进行了利用测序(ATAC-seq)进行转座酶可及染色质分析低和汤姆高亚种群(图2一个).汤姆有共同的和不同的峰低和汤姆高细胞(图2 b- d)。
基于荧光激活细胞分选(FACS)的番茄转座酶可达染色质测序(ATAC-seq)分析低(汤姆低)和tdTomato高(汤姆高)的人口。a)他莫西芬治疗的时间表SftpcCreERT2 / +; tdTomato液氧/液氧老鼠(n = 3)。ATAC-seq在基于facs的Tom分类上进行低和汤姆高亚种。医生:一天。b, c) Tom的覆盖热图低和汤姆高,显示了Tom的差异开放染色质峰的全基因组区域低与汤姆高.汤姆低与Tom相比,染色质较少开放,转录活性也较低高.Ctrl-low显示Tom中与开放染色质区域相关的峰低.Ctrl-high显示Tom中与开放染色质区域相关的峰高.Common表示在两个Tom中检测到峰值低和汤姆高亚种。d)基于截断点的ATAC-seq峰分析显示,Tom基因中3605位点上调高(错误发现率(FDR)<0.05, log2(FC)>0.585, base mean>20), Tom上调3512低(罗斯福< 0.05,日志2(FC)>0.585,基本平均值>20)和3878非管制(基本平均值>20,FDR>0.5, log2(FC)介于- 0.15和0.15之间),这意味着32%和32.2%的基因组在汤姆身上是不同的可访问性低和汤姆高,分别。e)的平均读覆盖率的ATAC-seq直方图Rosa26该位点在Tom的启动子和染色质上显示明显的ATAC-seq峰低和汤姆相比高在这个地方。汤姆的代表性山峰低和汤姆高是三个独立样本的平均值。f)峰值的量化Rosa26轨迹。g) ATAC-seq剖面在Sftpc该位点在Tom的启动子和染色质上显示明显的ATAC-seq峰低和汤姆相比高.汤姆的代表性山峰低和汤姆高是三个独立样本的平均值。h)的峰区量化Sftpc轨迹。ATAC-seq数据已被归一化用于测序深度,并选择y轴上的刻度用于最佳的峰可视化。i) Tom中差异调控的顶级细胞周期相关基因ATAC-seq数据的ATAC-Heat-pVAI Z-score, Pearson,平均热图低和汤姆高.FDR:多重试验Benjamini-Hochberg校正结果的显著性(n=3)。
利用Reactome数据库对ATAC-seq数据进行进一步分析表明,与代谢、胆固醇代谢、表面活性剂代谢和甘油三酯生物合成相关的基因位点的染色质在Tom中更为开放高细胞。这些数据与已知的成熟AT2细胞在表面活性剂生产中的作用相一致。相比之下,汤姆低细胞表现出更容易获得与适应性和先天免疫系统相关的基因,以及参与细胞外基质(ECM)组织、ECM蛋白多糖和ECM降解的基因。这些结果表明了汤姆的一个新的和重要的功能低细胞与免疫系统相互作用,也可能通过ECM降解显示迁移能力(补充图S5a).
我们的ATAC-seq数据也支持所观察到的番茄(由Rosa26启动子),Sftpc在mRNA水平上的表达低与汤姆高.在Rosa26而且Sftpc在Tom的基因座中,检测到与开放染色质结构相对应的峰值水平要高得多高而不是汤姆低,经量化后,证实该差异有统计学意义(图2 e- h)。有趣的是,ATAC-seq数据的分析也表明Tom低与Tom相比,细胞周期基因表达减少高细胞(图2我).这种细胞周期基因的减少被我们对Tom之间的基因阵列数据的分析所证实低和汤姆高(补充图S5b).总的来说,我们的数据表明,在稳态条件下,汤姆低细胞符合静止种群的特征。
at₂汤姆低和汤姆高显示不同的菌落形成能力
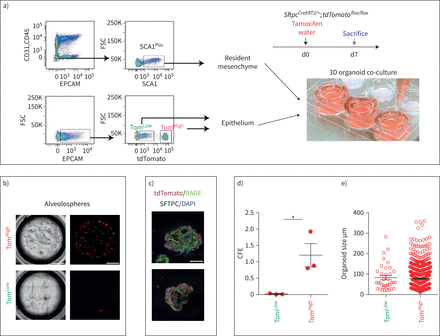
比较Tom的自我更新能力低和汤姆高,流式细胞术分类细胞与CD31共培养负的CD45负的EPCAM负的SCA1Pos常驻肺间充质细胞根据先前发表的方案(图3一).汤姆高表现得像善意的AT2细胞,形成具有预期菌落形成效率的肺泡球(图3 b, d, e) [3.,9,21],而汤姆低显示出非常弱的有机形成能力,这与他们提出的静止状态是一致的。两个群体在培养14天后都转分化为晚期糖基化终产物受体(RAGE)阳性的AT1细胞(图3 c).
tdTomato不同的菌落形成能力低(汤姆低)和tdTomato高(汤姆高)细胞。a)有代表性的流式细胞术显示CD31的门控策略负的CD45负的EPCAM负的群体和进一步选择SCA1Pos来自C57BL/6肺的常驻间充质细胞(上图),以及Tom的选择低和汤姆高来自EPCAMPos人口从SftpcCreERT2 / +; tdTomato液氧/液氧(较低的情节)。间充质细胞与Tom共培养低和汤姆高分别(n = 3)。医生:一天。b) Tom的代表性肺泡低和汤姆高(n = 3)。比例尺:100 μm。c)培养14天后,肺泡球的代表性SFTPC和RAGE免疫荧光染色。比例尺:50 μm。d)定量化菌落形成效率(CFE), e)肺泡球大小高和汤姆低(n = 3)。数据以均数±表示扫描电镜.*: p < 0.05。
汤姆的扩展低肺切除术后的人群
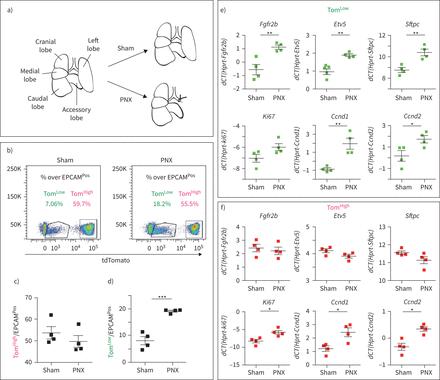
关于这两个AT2细胞亚群的一个关键问题是,它们是否在肺再生的背景下有不同的参与。因此,我们使用小鼠肺切除术(PNX)模型来触发肺再生,这一过程与AT2细胞的增殖密切相关[22,23].SftpcCreERT2 / +; tdTomato液氧/液氧小鼠(n=4)用他莫西芬水处理1周,以标记AT2谱系。然后将小鼠置于正常水中2周,以确保有足够的时间清除他莫西芬。然后进行单侧左肺全肺切除术,以诱导剩余右叶代偿性生长过程。对照组小鼠(Sham)经历了同样的过程,但没有切除左叶(图4一).术后第7天处死动物,对右叶进行FACS处理。因为副瓣已被证明对PNX的反应最大[24,我们的结果可能低估了Tom的反应低在PNX环境下的细胞。汤姆的丰裕度的量化低和汤姆高细胞总数比上EPCAMPosSham小鼠和PNX小鼠的细胞变化表明高细胞数/ EPCAM总数Pos细胞在两种条件下保持不变,而Tom的比例低细胞在PNX环境下显著增加与虚假的(图4 b- d)。这表明它是汤姆低细胞,而不是之前认为的汤姆高这些细胞有助于肺再生的过程。这两个AT2群体经FACS分离,qPCR进一步分析。在PNX上,的表达式Fgfr2b,Etv5,Sftpc,细胞周期蛋白D1(Ccnd1),细胞周期蛋白D2(Ccnd2)在汤姆体内显著上调低.也有增加的趋势Ki67表达式(图4 e).这些结果与FGFR2b信号通路在Tom中的激活和增殖一致低肺再生背景下的细胞。相比之下,汤姆高细胞间无差异Fgfr2b,Etv5或SftpcPNX和Sham条件之间的差异(图4 f).令人惊讶的是,我们注意到Ki67,Ccnd1而且Ccnd2(图4 f)而是因为汤姆的号码高PNX细胞没有增加与假小鼠,这些结果的意义尚不清楚。我们还使用单剂量腹腔注射5-乙基-2-脱氧尿苷(EdU) (0.1 mg·g)对增殖细胞进行了标记−1小鼠)在PNX后第6天。我们分析了第7天(1天追逐期,n=2只小鼠)和第14天(8天追逐期,n=3只小鼠)的肺。at₂PD-L1Pos(相当于汤姆低)和at2pd - l1负的(相当于汤姆高)经FACS分离。我们对这些分离的细胞进行细胞旋合,并对EdU进行免疫荧光。而很容易观察到大量的AT2 PD-L1负的细胞,即AT2 PD-L1的数量Pos载玻片上的细胞含量非常低,因此很难分析这些细胞中EdU的掺入。我们的结果表明,2.3±0.8% (n=2只独立小鼠,每只小鼠计数300个细胞)的AT2 PD-L1负的是EdUPos第7天。然而,在第14天,EdU为12.2±0.4%Pos(n=3只小鼠,每只小鼠300个细胞)。经过8天的追踪期后,这两个时间点之间标记细胞数量的增加表明EdUPosAT2 PD-L1中的细胞负的来自于AT2 PD-L1Pos单元格(数据未显示)。
tdTomato扩展低(汤姆低)但不是tdTomato高(汤姆高肺切除术(PNX)后。a) PNX和Sham模型示意图。b) Tom的代表性流式细胞术分析低和汤姆高PNX和Sham后7天的人群,c) Tom定量高e)汤姆低EPCAM百分比PosSham组和PNX组的总体差异(n=4)。f)基于荧光激活细胞分选(FACS)分选Tom的定量PCR (qPCR)分析低用于表达的人口Fgfr2b,Etv5,Sftpc, Ki67, Ccnd1而且Ccnd2.g)基于facs分类的Tom qPCR分析高用于表达的人口Fgfr2b,Etv5,Sftpc, Ki67, Ccnd1而且Ccnd2.数据以均数±表示扫描电镜.dCT:增量周期阈值。*: p < 0.05;* *: p < 0.01;* * *: p < 0.001。
失去汤姆高细胞导致Tom的扩张低细胞
我们利用PCLS跟踪Tom的命运Pos细胞随时间变化在体外.我们的流式细胞术结果表明,这种方法导致Tom的急剧损失高细胞(图5一个b).因此,我们利用这个系统来监控Tom的命运低在失去Tom之后高.在培养96小时后,我们观察到细胞簇的形成和tdTomato强度的显著增加(图5 c),暗示了汤姆的差异低细胞趋于成熟(汤姆高) AT2细胞。此外,我们还观察到Tom星团的存在Pos细胞在240小时后(图5 c).我们还使用视频荧光显微镜来跟踪单个Tom低细胞(n=6)在PCLS超过45小时。我们的结果表明,tdTomato信号在这些细胞中的强度随着时间的推移而逐渐增加,从而证实了从Tom的转变低汤姆高状态(数据未显示)。最后,我们分析了这些PCLS随时间的凋亡和增殖。我们的结果表明tdTomato有非常显著的增加PosTUNELPos总tdTomatoPos细胞(图5 d-k),这与没有检测到Tom是一致的高在该时间点(图5 b).此外,增殖分析表明tdTomato的数量有稳健的增长PosEdUPos总tdTomatoPos20h至96h之间的PCLS (图5 h-k),支持我们之前在PNX上下文中得出的结论,即Tom低损伤后细胞正在增殖。
tdTomato的命运特征低(汤姆低)细胞在精确切肺切片(PCLS)。a, b) Tom的代表性流式细胞术分析低和tdTomato高(汤姆高),然后在新生成的PCLS中处理肺的PCLS (a)和培养20小时后的PCLS (b)。c) Tom的可视化低在t=0, t=96 h和t=240 h时,PCLS的效果显著。箭头表示细胞簇的形成。比例尺:250 μm(低倍)和50 μm(高倍)。d)在PCLS上用代表性末端脱氧核苷酸转移酶dUTP缺口末端标记(TUNEL)免疫荧光染色(比例尺:50 μm)和e) tdTomato定量分析细胞凋亡PosTUNELPosf) TUNELPosg) tdTomatoPosTUNELPostdTomato中的细胞Pos细胞(n = 4)。数据以均数±表示扫描电镜.h)在PCLS上用具有代表性的EdU免疫荧光染色(比例尺:50 μm)分析增殖情况,并定量i) tdTomatoPosEdUPos总的单元格,j) EdUPosk) tdTomatoPosEdUPostdTomato中的细胞Pos细胞(n = 4)。数据以均数±表示扫描电镜.*: p < 0.05;* *: p < 0.01;* * *: p < 0.001;* * * *: p < 0.0001。
PD-L1是Tom中富集的特异性表面标记物低
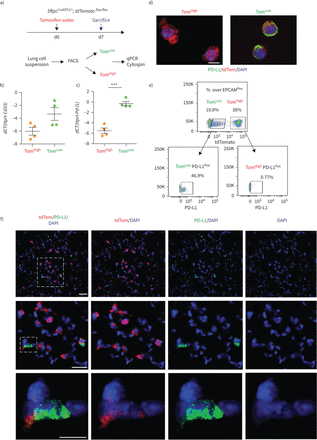
识别Tom和Tom之间的差异表达标记低和汤姆高,我们对分离出的Tom进行了基因阵列低和汤姆高细胞(图6,补充图S5b).在汤姆身上100个最高差异表达基因中低与汤姆高细胞,三种细胞表面标记,Cd33的,Cd300lf而且Cd274(亦称Pd-l1),被认为在汤姆身上得到了丰富低和汤姆相比高.qPCR分析证实Cd33的而且Pd-l1在汤姆低和汤姆相比高(图6 b).PD-L1是一种有趣的标记物,因为它是一种免疫抑制受体配体,在腺癌中表达高度增加[14,25].这个标记的使用也是相关的,因为我们的ATAC-seq分析显示Tom低细胞富含属于免疫系统的基因(补充图S5a).利用PD-L1作为Tom富集的表面标记物低PD-L1免疫荧光染色和流式细胞术进一步验证细胞。为此,细胞旋上的PD-L1免疫荧光染色证实Tom的质膜蛋白水平较高低而不是汤姆高细胞(图6 c).此外,流式细胞术分析Tom低和汤姆高单独的种群显示46.9%的汤姆低细胞为PD-L1Pos而Tom只有0.77%高细胞为PD-L1Pos(图6 d).此外,PD-L1免疫荧光染色肺切片定位tdTomatoPosPD-L1Pos肺泡内的细胞(图6 e).总之,这些结果表明PD-L1抗体可能有助于区别分离Tom的等价物低与汤姆高在野生型肺中。
PD-L1是tdTomato中富集的特异性表面标记物低(汤姆低)细胞。a)通过定量PCR (qPCR)验证基因阵列数据。医生:一天。b, c)的表达水平的量化Cd33的(b)和Pd-l1(c)在汤姆低相比tdTomato高(汤姆高).数据以均数±表示扫描电镜.dCT:增量周期阈值。* * *: p < 0.001。d) Tom具有代表性的PD-L1免疫荧光染色低和汤姆高cytospin细胞。比例尺:50 μm。e) PD-L1的代表性流式细胞术分析Pos汤姆人口低和汤姆高.f)肺切片代表性PD-L1免疫荧光染色。比例尺:10 μm。
AT2 PD-L1的鉴定PosSFTPC低在野生型小鼠的肺部
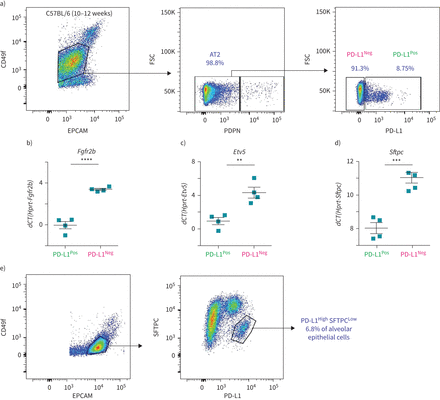
为了解决PD-L1是否可以用于分离Tom的等效物低和汤姆高在不需要谱系追踪方法的情况下,对分离的C57BL/6肺进行基于流式细胞仪的分析。PD-L1抗体最初通过免疫荧光染色证实其在肺泡巨噬细胞中的表达图6 e)和流式细胞术(补充图S6c).AT2细胞的选择基于EPCAM的门控Pos, CD49f中间(标记肺泡上皮细胞),PDPN负的人群(排除AT1细胞),其中分析PD-L1阳性和阴性细胞的百分比(图7).平均8.99±0.51% (n=4)的AT2细胞为PD-L1PosPD-L1为90.23±0.58% (n=4)负的(图7).这一比例与大多数(80%)谱系追踪AT2细胞由Tom组成的发现是一致的高(PD-L1负的)细胞(图1 c).筛选PD-L1的qPCR分析Pos和PD-L1负的AT2细胞提示较高水平的Fgfr2b,Etv5而且Sftpc在PD-L1负的比PD-L1Pos细胞(图7 b- d)。这一结果也与PD-L1一致负的对应Tom的细胞高而PD-L1的表达谱高这些细胞就相当于汤姆低.最后,流式细胞术分析肺泡上皮细胞(EPCAMPos, CD49f国际米兰)经SFTPC和PD-L1染色后,发现一个AT2细胞亚群(6.8%)显示低水平的SFTPC和高水平的PD-L1 (图7 e).这SFTPC低PD-L1高群集可能包含汤姆低细胞。
AT2 PD-L1的鉴定Pos野生型小鼠肺部的细胞。a)具有代表性的野生型小鼠肺流式细胞仪分析显示EPCAM的门控策略PosCD49f国际米兰其次是AT2细胞的阴性选择,排除AT1 PDPNPos细胞。第三个图是基于PD-L1标记对AT2细胞进行的具有代表性的流式细胞术分析。b-d)基于荧光激活细胞分选(FACS)分选的PD-L1的定量PCR分析Pos和PD-L1负的表达的细胞Fgfr2b(b),Etv5(c)和Sftpc(d) (n = 4)。数据以均数±表示扫描电镜.* *: p < 0.01;* * *: p < 0.001;* * * *: p < 0.0001。e) SFTPC与PD-L1共染的代表性流式细胞仪分析。FSC:前向散射;dCT:增量周期阈值。
通过qPCR分析验证分离的AT2 PD-L1的潜在污染Pos和AT2 PD-L1负的细胞。我们的结果证实,这两个亚群没有受到内皮细胞、造血细胞、巨噬细胞和成纤维细胞的污染(补充图S6).此外,将这些细胞与常驻SCA1共培养Pos肺泡间充质细胞实验显示只有AT2 PD-L1负的细胞(相当于汤姆高细胞)显示自我更新能力(补充图S7).最后,AT2 PD-L1的数量也较高PosPNX中的细胞与虚假的(补充图S8).总之,我们的数据表明AT2 PD-L1Pos和AT2 PD-L1负的细胞的功能相当于汤姆低和汤姆高,分别。
的识别PD-L1Pos人类AT2 scRNA-seq数据集中的细胞
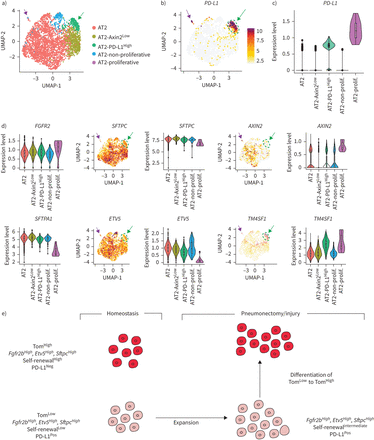
scRNA-seq结果来自最近一项报告人类肺细胞全球分析的研究[17]被用来进一步研究PD-L1Pos人类AT2池中的细胞。使用统一流形近似和投影(UMAP)图进行生物信息学分析,以改善最初的AT2细胞池聚类。我们的结果允许最初的由3198个细胞组成的AT2簇被分离成五个亚簇(图8).分析PD-L1表达区分两个阳性簇,命名为AT2PD-L1高和at2增殖,显示高水平PD-L1(图8 b、绿色箭头和淡紫色箭头)。注意at2增殖簇表达较高MIK67而且PCNA(补充图S9).然而,由于at2增殖簇只包含三个细胞,它与我们的Tom相关低在小鼠中鉴定的种群尚不清楚。另一个子集群(AT2PD-L1高)包含186个细胞(占初始AT2池的5.82%)。基因表达分析用小提琴图表示(图8 b- d)。与AT2子集群(红色标记)相比,PD-L1AT2表达PD-L1高(绿色标示)的含量明显增加(图8 b).此外,FGFR2b表情没有改变SFTPC只是略有下降。然而,表达较低AXIN2,SFTPA1而且ETV5观察到(图8 d).因此很可能AT2PD-L1高子集群相当于人类的AT2汤姆低我们在老鼠身上发现的。有趣的是,与AT2亚簇相比,AT2增殖亚簇也显示出较低水平的ETV5,SFTPC而且SFTPA1而是更高层次的AXIN2.基因在AT2中富集PD-L1高也分析了(补充图S10).跨膜4L6家族成员1 (TM4SF1),编码膜蛋白的基因在AT2中高度富集PD-L1高细胞(图8 d).有趣的是,该标记以前被用于分离AEP细胞,该细胞被认为在人肺中表达高水平的AXIN2 [9].很明显,这个标记在AT2中也有表达AXIN2低PD-L1高人类细胞(在汤姆身上也是如此低与汤姆高在小鼠中,数据未显示),说明需要更多的工作来表征人类和相应的小鼠祖细胞,并识别更多的标记。最后,我们使用IPF细胞图谱的在线资源为AT2的存在添加了进一步的证据PD-L1Pos人类肺中的细胞(数据未显示)。CD274Pos(PD-L1Pos)细胞在所有四个分析的人类数据集(Banovitch/Kropski, Kaminski/Rosas, Lafyatis和Misharin)中都被观察到。的表达水平ETV5,FGFR2而且SFTPC在at₂PD-L1Pos这些数据集中的细胞符合它们的静态(低表达水平)或激活(高表达水平)(数据未显示)。
PD-L1的鉴定Pos人类AT2单细胞rna测序(scRNA-seq)数据集中的细胞。a)初始AT2细胞簇的UMAP图显示存在5个不同的AT2子簇。b) UMAP和c)小提琴图显示PD-L1在AT2-中富集PD-L1高子集。d) UMAP和小提琴图显示AT2-PD-L1高子集群显示低水平的ETV5,SFTPC而且AXIN2高水平的TM4SF1。绿色箭头表示AT2PD-L1高淡紫色箭头表示at2增殖。e) tdTomato模型低(汤姆低)和tdTomato高(汤姆高)细胞内稳态和肺切除术/损伤后。汤姆低细胞在成人肺内稳态期间是静止的,但在损伤后被激活。它们获得增殖能力并分化成成熟的AT2细胞。
讨论
我们已经确定了一个AT2祖细胞亚群,它与已经确定的成熟AT2祖细胞亚群不同。汤姆低与AT2 AXIN2不同,AT2 AXIN2是稳定状态下的静止和未成熟细胞Pos细胞,表达低水平的AT2分化标记。此外,汤姆低细胞表达显著降低Axin2比汤姆高细胞内稳态,和Axin2汤姆的表情低与假手术相比,PNX后细胞没有变化(补充图S11a, b).Zacharias等.[9]的研究表明,AEPs比成熟的AT2s表达更高水平的肺和管发育相关基因。然而,根据我们的基因阵列数据,这些基因在Tom中表达水平较低低与汤姆相比高单元格(数据未显示)。这表明AEP细胞是Tom的一部分高人口。新确认的汤姆低细胞也不同于整合素α6β4群体,因为这些细胞是阴性的Sftpc因此,SftpcCreERT2驱动系无法追踪此种群[7,26].最后,汤姆低由于几个原因,大多数人不含有支气管肺泡干细胞(BASCs)。首先,大部分的汤姆低细胞位于呼吸道上皮,不显示高水平的Scgb1a1(数据未显示)。其次,scRNA-seq数据表明,与AT2细胞相比,BASCs表达相似水平Sftpc而且Fgfr2[13],表明BASCs可能包含在Tom中高人口。有趣的是,损伤时BASCs的谱系追踪表明,这些细胞并不是进行气道损伤后新形成的支气管气道细胞或肺泡损伤后AT2/AT1细胞的唯一贡献者,这表明其他驻体干细胞如AT2 Tom低或者AT2可以帮助修复过程。此外,PD-L1在Tom体内高表达低.PD-L1表达在腺癌中也增加,并似乎与肿瘤增殖和侵袭性升高有关[14,16,25,27,28].需要进一步的研究来阐明PD-L1在Tom中的功能低细胞及其与免疫系统的潜在相互作用以及它们对癌症的贡献。在未来,基于的表达式设计双沿袭跟踪策略将是非常重要的Sftpc而且Pd-l1给汤姆贴标签低细胞特别。
最近发表的一项scRNA-seq数据集检测了成年小鼠在博莱霉素损伤后不同时间点的肺细胞状态[29].对这些scRNA-seq结果的数据挖掘表明AT2 .Pd-l1Pos在对照(生理盐水)和实验(博莱霉素)条件下都无法检测到细胞。由于实验的设计是为了捕获肺中的所有细胞,相应的上皮部分显然是动力不足的,因为没有足够的AT2细胞亚群可用于可靠的分析。这种AT2检测的缺失Pd-l1Pos细胞也可能是由于scRNA-seq手术前肺部酶消化相关的创伤,我们对Tom的观察也支持这一点低与汤姆细胞相比,它们的存活率要低得多高单元格(数据未显示)。博莱霉素治疗小鼠的初步实验(n=2只小鼠)与盐渍处理(n=3只小鼠)野生型小鼠显示AT2 PD-L1显著增加Pos与AT2 PD-L1相比负的细胞(21.2%与8.1%;数据未显示)。因此,我们得出结论,AT2 PD-L1Pos(汤姆低)细胞似乎对至少三种类型的损伤(PNX,博莱霉素和PCLS)有反应。
在本研究中,我们试图回答的一个重要问题与Tom所扮演的潜在角色有关低作为成熟AT2细胞的祖细胞。支持这样一个角色的理由如下:1)汤姆低细胞代表一段时间内稳定的种群(补充图S4);2) PCLS模型中番茄标记细胞的凋亡和增殖分析(图5)表明汤姆高细胞大量死亡,而汤姆低细胞在增殖;3)汤姆增加了低(PD-L1Pos)在PNX的上下文中与虚假的(图4而且补充图S8),汤姆的数目并没有明显的变化高细胞;4)汤姆低未损伤肺的细胞表明这些细胞不能自我更新和分化(图3),我们的初步数据(未显示)表明Tom低细胞SftpcCreERT2 / +; Fgfr2b液氧/液氧番茄;液氧/液氧肺泡形成明显增加,说明汤姆低细胞获得自我更新和分化能力。
总之,我们发现了一种新的静止和未成熟的AT2祖细胞群,其基因表达谱与成熟的AT2细胞不同,后者在PNX后增殖,并富集Pd-l1表达。在人类的肺中也发现了类似的人群。这些细胞在稳态和修复/再生条件下的进一步特征将允许识别这些细胞中激活的信号通路,最终目标是增强损伤后的修复。
补充材料
补充材料
请注意:补充材料不是编辑部编辑的,上传时是作者提供的。
补充方法和表格erj - 04168 - 2020。补充
补充图S1。汤姆体内没有污染低和汤姆高亚种。a)他莫西芬治疗的时间表SftpcCreERT2 / +;tdTomato液氧/液氧老鼠。EPCAM的代表性流式细胞术分析Pos和CD3Pos、CD45Pos种群选择和Tom的进一步门控负的汤姆低和汤姆高细胞。b)基于facs分类CD31的qPCR分析Pos、CD45Pos汤姆,负的汤姆,低,汤姆高细胞的表达Pecam1,Ptprc,Adgre1而且Vim.dCT:增量周期阈值。数据以均数±标准差表示。*: p < 0.05;* *: p < 0.01;* * *: p < 0.001。erj - 04168 - 2020。Figure_S1
补充图S2。的验证SftpcCreERT2 / +;tdTomato液氧/液氧老鼠。a)饼图表示tdTomato的百分比Pos上皮细胞(96.6%)、间充质细胞(0.8%)和CD31细胞的百分比(20.5%)PosCD45Pos标记细胞(2.6%)。b) tdTomato的代表性SFTPC免疫荧光染色及定量PosSFTPCPos总tdTomatoPos以及tdTomato的量化PosSFTPCPos总SFTPCPos(n = 4)。数据以均数±标准差表示。c) EPCAM的代表性流式细胞术分析PosEPCAM和tdTomato在单个FACS图中显示。erj - 04168 - 2020。Figure_S2
补充图S3。AT2细胞在有无他莫昔芬治疗时的标记。a)他莫西芬治疗时间表。一组SftpcCreERT2 / +;tdTomato液氧/液氧在饮用水中加入他莫西芬治疗小鼠7天,另一组水中不加入他莫西芬。b)具有代表性的流式细胞术单细胞选择分析及EPCAM进一步分析Pos两组的人口。c) Tom的代表性流式细胞术分析低(4.5%)和汤姆高(6.9%)。饼状图显示了汤姆的百分比低(39.2%)和汤姆高占tdTomato阳性细胞总数的60.8%。d) Tom的代表性流式细胞术分析低(10.3%)和Tom高(44.1%)。饼状图显示了汤姆的百分比低(18.9%)和Tom高占tdTomato阳性细胞总数的81.1%。erj - 04168 - 2020。Figure_S3
补充图S4。汤姆低和汤姆高AT2亚群在6个月和9个月大的小鼠。他莫昔芬治疗时间表SftpcCreERT2 / +;tdTomato液氧/液氧小鼠和肺收获。流式细胞术分析EPCAMPos细胞。量化汤姆的百分位数低和汤姆高(超过总EPCAMPos细胞)在6个月和9个月大的小鼠。erj - 04168 - 2020。Figure_S4
补充图S5。汤姆可达区基因集富集高与汤姆低.a) Tom在ATAC-seq实验中获得的峰分析高和汤姆低细胞使用Kobas的Reactome数据库。将重叠基因体或靠近基因转录起始位点的峰标注到相应的基因上。所有标注的峰被分解成在汤姆身上显示更多开放染色质的基因列表高和汤姆低在统一峰区使用DESeq2。多重试验的Benjamini-Hochberg校正(FDR)调整观察显著性。生成的列表被用作输入,供Kobas在不同的数据库中搜索丰富的术语。根据显著性(FDR <0.2)选择前10个术语。结果表明,汤姆体内免疫系统一词高度富集低细胞,表明汤姆的染色质低细胞在与免疫系统相关的基因位点(基因体或启动子)中更容易接近。更高的可及性与更高的转录活性相关。括号中的数字显示已识别的基因数量/数据库中某个术语的基因总数。DEG:差异表达基因。括号之间:术语中发现的基因/总基因。b)使用Tom进行基因阵列后的差异表达基因热图高和汤姆低分离的细胞SftpcCreERT2 / +;tdTomato液氧/液氧肺处于稳态。erj - 04168 - 2020。Figure_S5
补充图S6。PD-L1中无污染Posat₂细胞。a) CD31的代表性流式细胞术分析PosCD45Pos(内皮细胞和造血细胞)和EPCAM负的CD31负的CD45负的(间充质)种群以及EPCAM的进一步门控Pos用PDPN分离AT2细胞。PD-L1抗体染色阴性,选择PD-L1Pos细胞。PD-L1的分离Pos和PD-L1负的从AT2细胞中取出。b)基于facs分类的间充质细胞的qPCR分析,CD31PosCD45Pos细胞,PD-L1Pos和PD-L1负的AT2细胞的表达Pecam1,Ptprc,Adgre1而且Vim.数据以均数±标准差表示。dCT:增量循环阈值(Ct)。*: p < 0.05;* *: p < 0.01;***: p <0.001。c) EPCAM的代表性流式细胞术分析负的进一步选择CD31PosCD45Pos人群的选择。进一步的流式细胞术分析显示CD31 .PosCD45Pos群体中含有PD-L1Pos细胞。PD-L1抗体染色阴性对照。erj - 04168 - 2020。Figure_S6
补充图S7。PD-L1的菌落形成能力Pos和PD-L1负的at₂细胞。a) AT2 PD-L1对肺泡球进行代表性Lysotracker免疫荧光染色Pos和AT2 PD-L1负的细胞培养14天后(比例尺:100 μm)。b) PD-L1菌落形成效率(CFE)的量化Pos和PD-L1负的培养细胞(n=3)。数据以均数±标准差表示。*: p < 0.05;* *: p < 0.01;***: p <0.001。erj - 04168 - 2020。Figure_S7
补充图S8。PD-L1百分比升高Pos肺切除术后的AT2细胞。a)假手术或PNX术后肺收获时间线。具有代表性的野生型小鼠肺流式细胞仪分析显示EPCAM的门控策略Pos其次是AT2细胞的阴性选择,排除AT1 PDPNPos细胞。b)基于PD-L1标记和PD-L1抗体染色阴性对照的AT2细胞代表性流式细胞术分析。c) PD-L1的定量PosSham组和PNX组AT2细胞百分比比较(n=4)。数据以均数±标准差表示。*: p < 0.05;* *: p < 0.01;***: p <0.001。erj - 04168 - 2020。Figure_S8
补充图S9。at2增殖亚簇的ScRNA-seq分析。a)初始AT2细胞簇的UMAP图显示存在5个不同的AT2子簇。b) UMAP图表示显示PCNA而且MKI67在at2增殖亚簇中富集。c)对应的小提琴情节表现。erj - 04168 - 2020。Figure_S9
补充图S10。不同AT2亚簇之间基因表达差异的热图表示(使用LFC)。a)成人肺中AT2细胞scRNA-seq分析的热图。b)注意AT2 PD-L1的富集高与免疫系统有关的基因(Cxcl1, cxcl2, cxcl3, icam1, zc3h12a, irf1, cxcl8, xbp1)以及先前被描述为由AEP细胞表达的基因(TM4SF1)。erj - 04168 - 2020。Figure_S10
补充图S11。Axin2Tom基因表达分析低与汤姆高在稳态和汤姆体内低在PNX和Sham。a)基于facs分类的Tom qPCR分析低和汤姆高细胞的表达Axin2在成年老鼠的肺里。b)基于facs分类的Tom qPCR分析低细胞的表达Axin2术后第7天假肺和PNX肺。数据以均数±标准差表示。*: p < 0.05;* *: p < 0.01;***: p <0.001。erj - 04168 - 2020。Figure_S11
可共享的PDF
确认
我们感谢Stefan Guenther(马克斯普朗克心肺研究所生物信息学和深度测序平台)在ATAC-seq数据分析方面的帮助。我们也感谢Kerstin Goth对小鼠的饲养和基因分型。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
利益冲突:N. Ahmadvand没有什么可透露的。
利益冲突:科斯拉维没有什么可披露的。
利益冲突:A. Lingampally没有什么可透露的。
利益冲突:R. Wasnick没有什么可透露的。
利益冲突:I. Vasquez-Armendariz没有什么可透露的。
利益冲突:G.卡拉罗没有什么可透露的。
利益冲突:海纳先生没有什么可透露的。
利益冲突:S. Rivetti没有什么可透露的。
利益冲突:吕毅没有什么可透露的。
利益冲突:j·威廉没什么可透露的。
利益冲突:A.甘瑟没有什么可透露的。
利益冲突:s·赫罗尔德没什么可透露的。
利益冲突:D. Al Alam没有什么可透露的。
利益冲突:陈冠希没有什么可透露的。
利益冲突:P. Minoo没有什么可透露的。
利益冲突:js。张没有什么可透露的。
利益冲突:贝鲁西没有什么可透露的。
支持声明:S. Bellusci得到了德国肺科研究中心(DFG) (BE4443/1-1, BE4443/4-1, BE4443/6-1, KFO309 P7和sfb1213项目A02和A04)和德国肺科中心(DZL)的资助。P. Minoo和S. Bellusci感谢国家心肺血液研究所(NHLBI) (HL143059)的支持。D. Al Alam感谢NHLBI的支持(R01HL141856)。j s。他是由温州医科大学和国家自然科学基金(81472601)共同资助的。S. Herold得到了UKGM (FOKOOPV)、DZL和吉森大学医院的支持,并得到了DFG (KFO309 P2/8;Sfb1021 c05, SFB tr84 b9)。本文的资助信息已存入交叉参考基金注册.
- 收到了2020年5月22日。
- 接受2021年3月26日。
- 版权所有©作者2021。
本版本根据知识共享署名非商业许可4.0的条款发布。为商业复制权利和权限联系权限在}{ersnet.org