摘要
背景罕见呼吸道疾病的治疗方法的发展受到阻碍,因为缺乏能够对受感染患者的完全分化呼吸道上皮进行中-高通量筛查的系统。对于原发性纤毛运动障碍(PCD)来说,这是一个特别的问题,PCD是一种罕见的遗传性疾病,由基因突变引起,对纤毛运动产生不利影响,从而影响粘液纤毛运输。从鼻刷活检中进行基底上皮细胞的原代细胞培养,然后在气液界面(ALI)处进行纤毛分化,已被证明是PCD诊断的有用工具,但该技术的更广泛应用,包括临床前PCD研究,受到从此类活检中可以扩增的基底细胞数量有限的限制。
方法我们描述了一种免疫荧光筛查方法,通过广泛扩增PCD患者的基底细胞,并将这些细胞在小型96孔跨孔ALI培养中定向分化为纤毛上皮。作为原理证明,我们对一名患有罕见而严重的PCD(运动纤毛生成减少)的患者进行了个性化调查,在这种情况下,PCD是由基因中的纯合子无义突变引起的MCIDAS基因。
结果对96孔转孔格式ALI培养中睫状体超微结构、搏动模式和搏动频率的初步分析表明,在这些培养中可以保留一系列不同的PCD缺陷。我们的主要证明研究中的筛选系统允许单独或与无意义介导的衰变抑制剂联合评估诱导翻译读通的药物。我们观察到患者鼻部上皮细胞恢复了基底体的形成,但没有发现纤毛的产生体外。
结论我们的研究为气道上皮的高通量分析提供了一个平台,适用于一系列环境,并为无义突变引起的PCD的药物评估和开发提供了新的途径。
摘要
原发性睫状体运动障碍患者鼻上皮细胞的原代细胞培养(包括分化为多纤毛细胞)使小型气液界面培养中的免疫荧光筛查成为可能https://bit.ly/3rjoxBF
简介
原发性纤毛运动障碍(PCD)是一种罕见的常染色体隐性遗传疾病,是由运动纤毛的结构和功能异常引起的。该病的特点是反复呼吸道感染和早发性支气管扩张、慢性鼻症状和鼻窦炎,许多患者因胶耳而出现严重的听力障碍。从遗传学上讲,PCD是一种异质性疾病,超过40种不同基因的变异占PCD患者的70% [1- - - - - -3.].虽然这些突变引起的特定超微结构缺陷各不相同,但它们通常发生在编码参与轴突结构、调节复合物、纤毛组装或纤毛运输的蛋白质的基因中[4].纤毛功能异常取决于潜在缺陷,可能导致静态纤毛、搏动幅度显著降低的纤毛、旋转纤毛或多动纤毛。
由于疾病的多样性,没有单一的PCD诊断测试:临床病史,遗传分析,低鼻一氧化氮水平,在高速视频分析的鼻刷活检中通过光学显微镜直接观察纤毛上皮细胞,以及通过电子显微镜分析纤毛精细结构,通常结合使用,以达到PCD诊断[5].在专门的中心,细胞培养用于提高诊断,因为继发于感染和炎症的睫状体运动障碍会使解释困难。当活检样本不含纤毛细胞时,检查培养细胞也可减少重新活检的要求[6],细胞培养在描述非典型PCD表型时是有利的,如内动力蛋白臂缺陷,纤毛定向障碍或多运动纤毛减少的产生。
PCD患者基因型和表型的多样性表明它是个性化医疗方法的沃土。然而,从PCD患者的刷活检中获得的鼻上皮细胞培养价值有限,因为基底细胞在培养开始后很快就会衰老。由于在鼻腔或下气道活检过程中获得的细胞很少,迄今为止的大多数研究直接在气液界面(ALI)培养中(其中细胞在转井中培养,并将其基本暴露在空气中)或经过最小传代后种子细胞[7].上皮细胞培养技术的改进导致了允许广泛扩张气道的方法[8]和鼻的[9]健康供体和遗传性疾病(如囊性纤维化)患者的上皮细胞[10- - - - - -12].在PCD中,先前的研究RSPH1-突变PCD患者表明患者的表型在分化后得到了概括在体外[13].在这里,我们证明了在含有Y-27632 (rho相关蛋白激酶(ROCK)抑制剂)的培养基中共培养的PCD患者的3T3-J2成纤维细胞喂养细胞的各种致病突变的基底细胞的广泛扩增,以及ALI培养中患者纤毛表型的维持。我们还将PCD患者和健康志愿者的ALI培养缩小到96孔的格式,这比传统的ALI培养可以进行更高的通量筛选。大约四分之一的PCD患者携带无义突变,将一个过早终止密码子(PTC)引入到mRNA中,导致蛋白质缺失或产生不活跃的、截断的形式[14].PTC-“读通”可以绕过PTC,导致功能蛋白的部分或全部表达[15].已经描述了几种通读剂,包括抗生素庆大霉素和正在开发的治疗杜氏肌营养不良症的药物阿塔卢伦[16]也在囊性纤维化中进行了试验[17].在HEK293FT细胞中克隆到荧光素酶报告结构的PCD ptc的分析表明,氨基糖苷读通剂可以抑制ptc的一个子集[18].
专注于我们的一个特征良好的患者,由多纤毛分化和DNA合成相关细胞周期基因突变引起的多运动纤毛(RGMC)纤毛病的生成减少(MCIDAS) (c.441C >;p.Cys147 *) (19],我们使用免疫荧光筛选方法评估了在小型化ALI培养中多个基底体的形成,在多纤毛发生过程中组织微管的结构。尽管在该疾病患者的鼻刷中观察到孤立的基底体,但由于ALI培养中缺乏该蛋白,多个基底体的形成受到损害[19,20.].读通剂和无意义介导衰变(NMD)抑制剂的组合能够恢复患者上皮细胞中基底体的形成,但不能恢复纤毛的形成。
材料与方法
受试者和遗传分析
根据欧洲呼吸学会诊断指南[188bet官网地址5].用于基因筛查的样本经伦敦布卢姆茨伯里研究伦理委员会(08/H0713/82)的伦理批准收集。在参加研究之前,所有参与者或其监护人都获得了知情的书面同意。如前所述进行基因筛选[21]或使用有针对性的下一代测序面板方法[22].
鼻刷活检中上皮细胞的分离
人鼻上皮细胞培养来源于经知情同意的鼻刷活检。通过国家研究伦理委员会(REC文献14/NW/0128)和伦敦大学学院研究伦理(文献4735/001)获得伦理批准。活组织检查在由medium 199 (Life Technologies)添加100 U·mL的运输介质中的冰块上进行−1青霉素100µg·mL−1链霉素(Gibco), 25µg·mL−1两性霉素B (Gibco)和20.5µg·mL−1脱氧胆酸钠。将细胞直接镀入T25烧瓶,置于支气管上皮生长介质(“P0”;BEGM, Lonza),第一次传代前培养7-10天。第一次传代后,细胞在BEGM中扩增或与3T3-J2成纤维细胞共培养,如下所述。
供料细胞培养
3T3-J2小鼠胚胎成纤维细胞在添加100 U·mL的DMEM (Gibco)中培养−1青霉素100µg·mL−1链霉素(Gibco)和8%牛血清(Gibco)成纤维细胞在37°C和5% CO中培养2中号每周换三次。为了产生饲养层,用4µg·mL处理细胞,使细胞有丝分裂失活−1丝裂霉素C (Sigma)在培养基中培养2-3小时。灭活的成纤维细胞被胰蛋白酶化,并以20 000细胞·厘米的密度被镀−2在成纤维细胞生长介质中,让其粘附一夜。
人鼻上皮细胞3T3-J2共培养
与3T3-J2成纤维细胞共培养,如前所述[23].上皮细胞培养液由DMEM (Gibco)、F12 (Gibco)与1X盘尼西林/链霉素(Gibco)、5%胎牛血清(Gibco)按3:1比例添加5 μM Y-27632 (Cambridge Bioscience), 25 ng·mL组成−1氢化可的松(Sigma), 0.125 ng·mL−1EGF (Sino Biological), 5 μg·mL−1胰岛素(Sigma), 0.1 nM霍乱毒素(Sigma), 250 ng·mL−1两性霉素B (Fisher Scientific)和10 μg·mL−1庆大霉素(Gibco)。从培养基中去除链霉素和庆大霉素进行RGMC细胞培养。上皮细胞在37°C和5% CO下培养2每周更换三次培养基。群体倍增(PD)计算为PD=3.32×(log(收获细胞数/播种细胞数))。冷冻保存使用Profreeze冷冻介质(Lonza),按照制造商的说明进行,并使用上述定义的上皮细胞培养基稀释原液。
ALI培养中的分化
在汇合处,利用差速胰蛋白酶化将基底细胞与喂食细胞分离[8],在0.05%胰蛋白酶/EDTA的短暂初始孵育下,足以去除成纤维细胞,但上皮细胞仍然粘附。清洗后,第二次较长时间的孵育有效地去除上皮细胞。将基底细胞接种在i型胶原蛋白涂层的半透膜支架上(Transwell-Col, 0.4µm孔径;康宁)在含有5 μ M Y-27632的BEGM中浸泡培养。对于12井转井,请访问1×106每膜接种于250µL培养基中。微型ALI培养在96个transwell板中进行(Corning;1 μ M孔隙,聚酯膜)其中0.2×106每膜接种75µL培养基。汇合时,只从基底外侧用ALI培养基喂养细胞。ALI培养基由50% BEGM和50%高葡萄糖最低必需培养基(DMEM, Gibco)组成,其中含有100 nM额外的维甲酸(Sigma Aldrich)。对于96个跨孔ALI培养,BEGM被Promocell的气道上皮细胞生长培养基取代。每周交换三次培养基,每周用支气管上皮基础培养基(BEBM)或Promocell基础培养基温和洗涤一次,去除根尖表面产生的粘液。每个实验的基底细胞传代数表示在补充表S1.
免疫荧光
培养的基底细胞在8孔载玻片中播种,或在4%多聚甲醛室温孵育30min后直接固定在跨孔膜上。细胞保存在4°C在PBS中,直到染色。用阻滞缓冲液(含0.01% Triton X-100的PBS中含3% BSA)在室温下阻断并渗透细胞1小时,然后在4℃下用一抗(含1% BSA的PBS中)染色过夜。一抗为抗c - nap1 (Sigma;1:50)用于基底体染色,抗-β-微管蛋白(Abcam;1:100)和anti-MUC5AC (Invitrogen;1:10 0)。细胞在PBS中洗涤三次5分钟,二抗(在1% BSA PBS中;分子探针;AlexaFluor染料)在室温下应用2小时。成像前,在室温下应用Hoechst 33258染色液(Sigma)作为核反染色20分钟。
基于免疫荧光的小型ALI培养物筛选
从筛选试验中检查的患者中分离细胞,并在上述3T3+Y细胞培养条件下进行扩增。庆大霉素(50、100 μg·mL)−1)和阿塔卢伦(5、10 μg·mL)−1)单独或与氨lexanox联合使用(1.5µg·mL−1)和escin(5.6和11.3µg·mL−1)从分化开始就应用于ALI培养的基底外侧(即。空气升)。每次给培养物喂食时刷新药物。在ali后第12天固定细胞进行免疫荧光,以评估基底体形成。从筛选中选择的药物和药物/组合也应用于12孔跨孔ALI培养,7天后收集细胞进行Western blot和定量PCR (qPCR)分析。
为了评估基底体形成,使用自动共聚焦显微镜在96孔转井中直接对细胞成像(Opera Phenix高含量筛选系统,PerkinElmer, ×5 objective)。为了进行高倍成像,将细胞安装在80%甘油,3%正丙基没食子酸酯(PBS)安装介质中,并使用倒置蔡司LSM 710共聚焦显微镜获得图像。使用自定义ImageJ宏对基体进行分析;分析方法总结在补充图S1这个宏可以从以下链接免费获得:https://github.com/DaleMoulding/Fiji-Macros/blob/master/DanielaSpotClustersv9.ijm。
经上皮电阻
使用EVOM2电阻计和Endohm腔(世界精密仪器公司)测量经上皮电阻(TEER)值,并使用与培养插入物尺寸相适应的杯型(24孔转孔培养杯为6mm, 12孔转孔培养杯为12mm)。将transwell放入培养杯中,在TEER读数稳定后(通常为5-10秒)进行读数。培养物完全分化后,从三个独立的转井中读取读数,即。在ALI培养至少5周后,获得每个培养的平均TEER值(每个供体9-12个读数)。
睫状体搏动频率和搏动模式
对于纤毛分析,纤毛上皮从transwell插入物上用刮刀轻轻刮除。细胞用运输介质洗涤(如上所述),并通过温和的移液分离。对细胞悬液进行分离,对未固定的细胞进行睫状体搏动频率和搏动模式分析,对固定在戊二醛中的细胞进行透射电镜(TEM)分析。
使用数码高速摄像机(Motion Pro 4x;IDT)在500帧·秒的速率下−1使用×100目标[24].每个供体获取10个视频,每个视频包含大约7-10个纤毛细胞,通过计算对清晰可见的纤毛尖进行5次完整扫描所需的帧数来确定单个纤毛细胞的纤毛搏动频率。这被转换为睫状拍频率,其中睫状拍频率=500/(5拍的帧数)×5。计算运动障碍纤毛细胞相对于运动纤毛细胞总数的百分比[25].为了分析96孔跨孔ALI培养中分化细胞的睫状体活性,使用倒置显微镜系统(尼康Ti-U)以×20为目标观察鼻上皮细胞。记录每个供体至少20个自上而下的视频,并使用ImageJ插件CiliaFA分析睫状体搏动频率[26].
qPCR
qPCR时,收集培养的上皮细胞,在TRIzol中提取mRNA,并在−80°C保存。如上所述,对含有3T3-J2成纤维细胞的培养物进行胰蛋白酶化以去除喂养细胞。在冰上解冻后,使用Direct-zol RNA分离试剂盒(Zymo Research)分离总RNA。使用Nanodrop One系统评估RNA数量,使用qScript cDNA SuperMix (Quantabio)进行反转录。以下Taqman预先设计的库存探针,以及2X PCR Master Mix(应用生物科学),用于qPCR反应:KRT5(Hs00361185_m1),KRT14(Hs00265033_m1),KRT8(Hs01595539_g1),TP63(Hs00978339_m1),NGFR(Hs00609977_m1),ITGA6(Hs01041011_m1),MUC5AC(Hs01365616_m1),MUC5B(Hs00861595_m1),FOXJ1(Hs00230964_m1)和B2M(Hs00187842_m1)。qPCR在标准条件下使用Eppendorf Real-Time PCR仪进行。相对RNA定量基于ΔCT计算,所有样本都与管家基因β2微球蛋白进行比较。为MCIDAS检测、引物(补充表S2)和Power SYBR™Green PCR Master Mix(赛默飞世尔科学公司)在标准条件下使用,相对RNA定量归一化到管家基因GAPDH.
免疫印迹
用刮刀从转井中收集细胞,然后制成颗粒,用PBS洗涤两次。核蛋白部分用NE-PER核和细胞质提取试剂(赛默飞世尔科学公司)提取,浓度用Pierce BCA检测试剂盒(赛默飞世尔科学公司)测定。核提取物通过SDS-PAGE分离,转移到PVDF膜上(在100 V下1小时)。膜在5% (w/v)牛奶中被PBST (3.2 mM Na2HPO4, 0.5 mM KH2阿宝4, 1.3 mM KCl, 135 mM NaCl, 0.05%吐温20,pH 7.4)在室温下孵育1小时,然后在4℃下与一抗(抗multicilin, Atlas抗体,1:500;anti-HDAC1, NovusBio, 1:500)。然后膜在PBST中洗涤三次,并与辣根过氧化物酶偶联抗兔抗体孵育(细胞信号技术;1:3000) 1小时。印迹用PBST清洗三次,并根据制造商的协议使用ECL系统(Bio-Rad)进行显像。
TEM
上皮细胞从转井中刮取到Medium 199中,固定于4%戊二醛的Sorensen磷酸缓冲液(pH 7.4)中。然后将细胞重新悬浮在Sorensen缓冲液中,并在4°C下存储,直到如前所述进一步加工成树脂[25].将超薄切片(70 nm)切割并收集在铜网格上,用1%的醋酸铀酰染色,用雷诺磷酸铅反染色,并用透射电镜检查[27].
统计数据
使用GraphPad Prism进行统计分析,并使用图例中所示的统计检验。
结果
PCD患者基底上皮细胞的细胞培养扩增
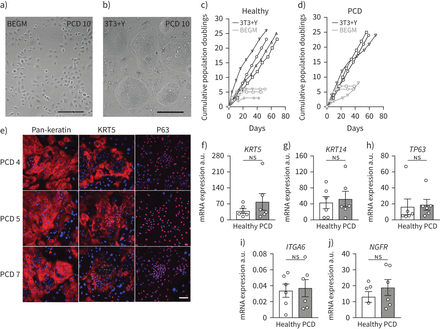
从12例有一系列遗传缺陷的PCD患者、1例RGMC纤毛病患者和11例无已知纤毛缺陷的健康供体中培养刷子活检来源的鼻上皮细胞(表1).在BEGM隔离后[28,29],在两种BEGM (图1一个),并在ROCK抑制剂的存在下与3T3-J2小鼠胚胎成纤维细胞喂养细胞共培养(Y-27632;3 t3 + Y) (图1 b).在BEGM中,两种健康(图1 c)和PCD培养(图1 d).相比之下,与之前的观察一致[9], 3T3+Y的扩张迅速,并持续至少8次(图1 c, d).来自健康和PCD供体的3T3+Y培养物在形态上无法区分,正如预期的那样,PCD培养物表达了基底细胞相关蛋白角蛋白5和P63 (图1 e).进一步,比较基底细胞相关mrna的丰度KRT5(图1 f),KRT14(图1 g),P63(图1 h),ITGA6(图1我),NGFR(图1 j)证实对照组和PCD培养物中的细胞均为基底上皮细胞。
原发性睫状体运动障碍(PCD)患者鼻上皮基底细胞的扩增。a, b)亮场显微镜显示鼻腔上皮细胞(PCD 10)在支气管上皮生长培养基(BEGM)传代1 (a)和传代2 (b) 3T3+Y培养中的代表性样本。比例尺:100 μm。c) BEGM和3T3+Y中四种健康供体鼻上皮细胞培养的累积群体翻倍。d) BEGM和3T3+Y中三个PCD患者鼻上皮细胞的累积群体加倍。e) 3个PCD患者3T3+Y培养物中泛角蛋白、角蛋白5 (KRT5)和P63表达(红色)的免疫荧光图像的代表性例子。核反染DAPI示(蓝色)。比例尺:100µm。f-j)定量PCR分析比较KRT5(f),KRT14(g),TP63(h),整合素α6 (ITGA6) (i)及神经生长因子受体(NGFR) (j)健康人与PCD供体基底细胞培养在3T3+Y中的差异。p值采用双尾配对t检验,显著性设为p<0.05。A.u:任意单位;ns:不重要的。
共培养PCD基底细胞形成黏液纤毛上皮
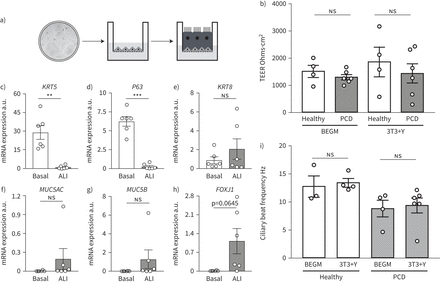
在建立了广泛扩增和冷冻保存PCD供体鼻上皮细胞的方法后,我们优化了在ALI中分化细胞的方法(图2一个).这种方法使我们能够评估他们的纤毛表型[8,19,28,30.].与健康对照组相比,3T3+Y培养的PCD细胞形成了融合的ALI培养。健康和pcd衍生的ALI培养物的屏障功能也相似,一旦培养物完全分化,通过TEER测量进行评估(图2 b).ALI培养5周后,基底细胞相关基因表达KRT5(图2 c),P63(图2 d)显著减少,分化相关基因的表达有增加的趋势KRT8(图2 e),MUC5AC(图2 f),MUC5B(图2 g),FOXJ1(一种在纤毛细胞谱系中表达的转录因子;图2 h),与预期的基底细胞培养向含纤毛细胞和粘液分泌细胞的成熟上皮细胞分化一致。
原代纤毛运动障碍(PCD)上皮细胞的纤毛发生在体外.a)气液界面(ALI)培养示意图,将基底细胞培养至融合,去除顶端培养基以刺激纤毛发生。二维培养中的图像取自图1 b.b)培养28天后,4名健康和6名PCD供体在支气管上皮生长培养基(BEGM)或3T3+Y中扩增的ALI基底细胞的上皮电阻(TEER)值。每个点代表每个人从四口井连续三次读数的平均值。p值采用双因素方差分析,采用Holm-Sidak检验进行多重比较,p<0.05为有统计学意义。c-h)定量PCR分析比较角蛋白5 (KRT5) (c),P63(d),KRT8(e),MUC5AC(f),MUC5B(g)和FOXJ1(h)培养28-30天后,3T3+Y基底细胞培养与供体匹配的分化ALI培养之间的差异。p值采用双尾配对t检验,p<0.05为差异有统计学意义。i)在BEGM或3T3+Y中扩增的3至6名健康和PCD供体的ALI培养中,对ALI培养28-35天的基底细胞进行睫状体搏动频率分析。我们在分析中排除了静态表型的PCD患者。p值采用双因素方差分析,采用Holm-Sidak检验进行多重比较,p<0.05为有统计学意义。ns:不重要的。* *: p < 0.01;* * *: p < 0.001。
PCD表型在ALI培养中被保留
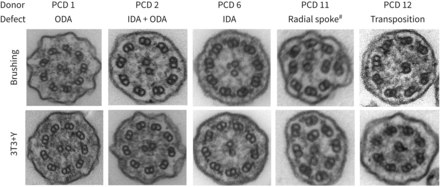
将培养的原代上皮细胞用于诊断和基础研究目的的先决条件是ALI培养中产生的纤毛细胞保持其PCD表型。在所有培养物中,使用高速视频显微镜都能轻易检测到纤毛,但RGMC1除外,在RGMC1中纤毛是不存在的(根据患者的表型,这是预期的)。我们发现ALI培养中来自健康对照组和PCD患者的睫状体搏动频率在基底细胞扩张条件下是一致的(图2我).健康供体鼻上皮细胞产生的纤毛在ALI培养中保持正常的纤毛搏动模式(表1),与先前对支气管上皮细胞的实验结果相符[8].重要的是,在BEGM或3T3+Y条件下进行基底细胞培养并随后分化后,PCD患者ALI培养维持了原始鼻刷中存在的睫状搏动缺陷。PCD患者细胞显示完全静止、僵硬或运动障碍的纤毛,与原始的鼻刷一致,反映了各自潜在遗传缺陷预期的纤毛搏动模式。关于测量节拍频率(图2我)和搏动模式,在直接患者活检和培养细胞之间观察到非常相似的结果(表1).在细胞培养中也重现了预期的超微结构缺陷(图3).在这些实验中,3T3+Y培养使我们能够分析一名健康供体和三名PCD供体的睫状肌搏动频率和模式,对于这些供体,如果使用传统BEGM培养,培养失败将无法进行分析(图2我,表1).
原发性睫状体运动障碍(PCD)细胞培养中持续的超微结构缺陷。具有代表性的睫状体横截面的电子显微图,说明了在最初的患者刷毛(上面板)和源于3T3+Y PCD原代上皮细胞培养的气液界面(ALI)培养中观察到的缺陷的例子。对每位患者进行3T3+ y衍生ALI培养,评估如下:PCD 1(219个纤毛;97.7% IDA, 2.3%无DA), PCD 2(305纤毛;100% DA), PCD 6(231纤毛;97.4% ODA, 2.6%无DA), PCD 11(269纤毛;98.1% ODA, 1.9%无DA;13.6%微管缺陷)和PCD 12(265纤毛;98.1%正常,ODA 0.4%, 1.5%无DA;9.3%的转置)。 ODA: outer dynein arm; IDA: inner dynein arm; DA: dynein arm.#放射状辐条是指轴突组织紊乱,IDAs缺失。
PCD ALI培养的微型化
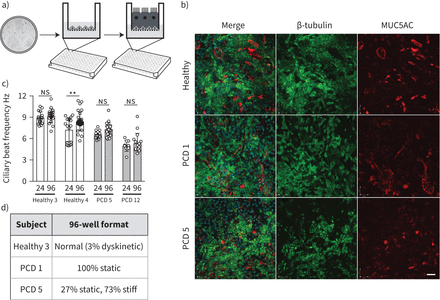
能够以高成功率扩增患者特异性原代PCD上皮细胞,并在培养中评估其睫状体功能,这代表了对人鼻上皮细胞的传统培养方法的进步。在了解到我们可以提供大量的基底细胞作为个体患者的输入后,我们接下来寻求将PCD ALI培养体小型化到96-transwell格式,这将与使用显微镜的复合筛查兼容(图4一).我们评估了五名捐赠者的培养能力,其中包括两名健康捐赠者(健康3号和4号;表1), 2例PCD患者有圆形搏动模式(PCD 5和12;表1)和1例静态纤毛PCD患者(PCD 1;表1).所有供体培养形成了含有两种MUC5AC的合流上皮+粘膜分泌细胞和β微管蛋白+纤毛细胞(图4 b),可透过高速视像显微镜(辅助视像)轻易观察。目视检查培养的纤毛,24孔和96孔格式的表面纤毛比例一致。睫状搏动频率分析(图4 c)和模式(图4 d)的结果表明,上述96口井和24口井格式的结果一致。虽然在96孔格式的一个健康供体中发现了一个小的、统计上显著的心跳频率增加(图4 c),这在生物学上不太可能有显著意义,因为所有数据点都在预期的正常范围内。
将气液界面(ALI)培养缩小到96孔格式,以生成原发性睫状体运动障碍(PCD)患者模型。a) 96孔跨孔ALI系统免疫荧光筛选实验装置示意图。二维培养中的图像取自图1 b.b)免疫荧光图像显示96孔格式ALI培养中存在表达β小管蛋白的纤毛(绿色)和表达muc5ac的粘液分泌细胞(红色)。两个PCD供体,一个有静态纤毛(PCD 1),一个有环状纤毛(PCD 5)缺陷,与健康供体对照进行比较。图像代表了两名健康捐赠者和四名PCD捐赠者的测试。比例尺:50µm。c)睫状肌搏动频率分析,比较来自两名健康供体(健康3和4)和两名PCD患者(PCD 5和12)的24孔和96孔格式的多个记录。数据点是4 ~ 5口井的单个记录,每口井记录5个视频。p值采用双因素方差分析,采用Holm-Sidak检验进行多重比较,p<0.05为有统计学意义。ns:不重要的。* *: p < 0.01。d) 96孔格式睫状搏动图分析。24井的等值值为表1.
通读剂与NMD抑制剂联合使用可增加基底体形成
因为庆大霉素在血清浓度范围内对人是有毒的,在细胞培养中可读透[31]和长期使用雾化庆大霉素可能会增加全身毒性,我们评估了通读药物(庆大霉素和阿塔鲁仁)与NMD抑制剂(氨列克诺、埃霉素)联合使用,试图提高我们发现的治疗相关性。在96孔格式中,我们处理了来自RGMC纤毛病患者的鼻上皮细胞,该患者由纯合子无义突变(c.441C> a;p.Cys147*)MCIDAS基因,庆大霉素剂量范围为50 ~ 100 μg·mL−1)和阿塔卢伦(2.5 ~ 10 μg·mL)−1)与NMD抑制剂(图5一个).从ALI产生开始,药物就被包括在内,因为多林素的表达先于纤毛发生(补充图S2) [19].12天后,我们评估了C-Nap1的表达,这是一种与β-微管蛋白共同定位的中心粒蛋白+培养鼻上皮细胞中的纤毛[32,33],使用Opera Phenix高含量筛选共聚焦显微镜系统。在ali后第12天,健康对照细胞中C-Nap1表达与β-微管蛋白共定位(补充图S3).在未处理的对照条件下,上皮细胞含有少量C-Nap1+基体(图5 bc补充数字S1和S4).然而,在各种药物治疗组合中,基底体形成增加(图5 c,补充图S1).这在高分辨率共聚焦显微镜下更加明显,因为单个C-Nap1+细胞可见(图5 b).ALI培养10天后未检测到MCIDAS蛋白(补充图S5),MCIDAS在ALI后第7天未处理的培养物中,qPCR检测不到mRNA,但在独立的12孔格式ALI培养物中重复药物处理后,mRNA在不同程度上恢复(图5 d).尽管如此,在使用最有希望的药物组合的长期实验中,培养28天后,我们无法通过视频显微镜或免疫荧光染色观察到纤毛的形成(数据未显示)。
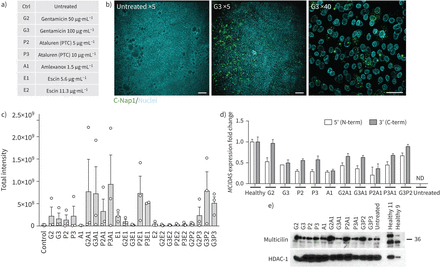
免疫荧光筛查评估通读性治疗的患者MCIDAS -突变的多运动纤毛(RGMC)纤毛病。a)用于RGMC 1患者免疫荧光筛查的药物名称和剂量关键字。b)存在100µg·mL的基体形成示例−1庆大霉素(G3)通读药物治疗显示基于C-Nap1(一种基础体相关蛋白;绿色,异硫氰酸荧光素)和Hoechst 33258反染剂(青色,4 ',6-二氨基-2-苯基吲哚)。比例尺:200 μm (×5图片)和34 μm (×40图片)。每个条件的示例显示在补充图S3.c)根据c - nap1染色的总强度,使用定制的ImageJ宏量化(如(a)所示),通过读透药物和无意义介导的衰变抑制剂联合治疗后基底体形成的定量。未治疗患者对照与治疗患者样本进行比较。与多重比较的Holm-Sidak检验相比,在单向方差分析中未发现显著差异。d)定量PCR分析比较MCIDAS患者细胞在药物处理条件下的mRNA丰度与一名健康对照供体,在7天的气液界面(ALI)培养后,使用传统的12孔transwell支架进行独立培养。未处理的培养中未检测到mRNA的表达。e) ali后第7天,在独立培养中使用传统的12孔transwell支撑,Western blot分析药物处理条件下的多林素表达。MCIDAS:多纤毛虫分化和DNA合成相关细胞周期;ND:未检测到;HDAC-1:组蛋白脱乙酰酶1。
Western blot检测这些培养物中全长多林蛋白的恢复情况;在多种药物治疗条件下,与对照组未治疗的患者细胞培养物和健康对照培养物相比,检测到预期38 kDa大小的条带表达增加(图5 e).透射电镜显示形成了不同成熟度的基底(图6,补充图S6).基底体的生物发生由不同的机制驱动,其中典型的机制涉及先前存在的中心粒的复制。然而,在多缘细胞中,多个基底体的形成也可以遵循一种非典型的途径,这种途径是由称为氘体的结构的形成所介导的[34].就在氘小体形成之前,观察到富集在微管中的电子致密“纤维颗粒物质”[34].我们在经读通剂处理的RGMC细胞中检测到这种类型的微管团聚(图6).这些电子密集的颗粒然后冷凝形成空心的球形结构,称为后体,它也是高电子密集的[34].未成熟中心粒由子中心粒通过氘小体的形成而扩增[35,36].我们在处理过的RGMC细胞中观察到一些我们认为可能是氘体的物质(图6,补充图S6).尽管氘体明显存在,但我们没有观察到源自它们的原心粒,尽管在类似氘体的结构附近可以发现一些结构化的中心粒。这些中心粒具有未成熟中心粒特有的“cartwheel”结构,直径约为0.2 μm (图6),如先前报道[37].
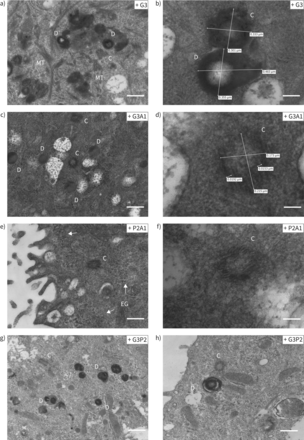
在药物处理的多运动纤毛(RGMC)细胞中发现的结构的高倍放大图像。不同的面板显示了a, b) G3处理后在RGMC细胞中观察到的基底体“前体”积累的代表性高倍放大图像(标尺:a为400 nm, b为100 nm);c, d) G3A1(比例尺:c为400 nm, d为50 nm);e, f) P2A1(比例尺:e 400 nm, f 100 nm);和g, h) G3P2(比例尺:g为800 nm, h为400 nm)。观察到大量电子致密的氘小体,我们观察到几个中心粒呈“cartwheel”结构。中心粒直径~ 0.2 μm (c-f [50])。在未处理的对照组中没有观察到这些结构。(e)中,箭头表示电子致密颗粒。D: deuterosomes;C:中心粒;MT:微管团聚;EG:电子密集颗粒。
讨论
本研究表明,在允许上皮细胞强壮扩张的条件下,PCD鼻上皮细胞表达基底细胞特有的蛋白质,在ALI培养中形成分化的粘液纤毛上皮,并保留先前在BEGM低传代培养中描述的患者特异性纤毛运动障碍表型[28,29].培养起始一致,广泛培养后分化能力强,无病毒永生[38]和可靠的低温保存[39为PCD研究提供了一个主要的好处。这与原代气道上皮细胞培养的其他进展一起[40- - - - - -42],将鼓励开发已知基因型的表型良好的患者特异性PCD上皮细胞的大型生物库,并将允许在相同的遗传背景下重复实验。
目前PCD的治疗途径主要集中在早期诊断和临床治疗,以防止肺功能下降。然而,目前还没有恢复睫状体功能的治疗方法。在未来,扩大大量人类上皮细胞的能力也可能为PCD中的基因编辑、mRNA、寡核苷酸和细胞治疗方法打开大门。值得注意的是,使用在3T3-J2喂养层上扩增的上皮细胞的细胞疗法已被批准用于严重烧伤和角膜缘干细胞缺乏的临床应用[43- - - - - -45]并且可以从单细胞来源的克隆进行扩增[46].然而,由于遗传性肺病的细胞治疗仍是一个遥远的前景[47],因此非常需要能够测试基因疗法或小分子方法的模型系统。为此,从个体供体中生产许多细胞使我们能够将ALI培养缩小到96孔格式。这反过来允许在RGMC病例的背景下使用更高通量的基于免疫荧光的化合物筛查进行个性化调查。在一个患有MCIDAS通过对基底蛋白C-Nap1的免疫荧光筛查,我们能够证明,结合读通和NMD抑制增强了基底形成,尽管培养物没有产生活动纤毛。这可能是由于我们在分化培养中可以测试的浓度范围有限:在较高剂量下,庆大霉素、氨lexanox和escin等化合物是有毒的。另一种可能性是,读通转录本产生了一种错误折叠的蛋白质,无法产生蛋白质-蛋白质相互作用和生成功能性纤毛所需的复杂三维结构。我们进一步证明了使用高速视频显微镜筛选96孔格式培养的可行性,这意味着这种方法也可以用于筛选纠正其他PCD表型中睫状体搏动模式缺陷的药物。
仅含有基底上皮细胞的培养物由于缺乏屏障功能,缺乏分化的细胞类型,对呼吸道疾病建模具有局限性[48]以及某些病毒在特定上皮细胞类型中的优先复制(如。多纤毛细胞中的呼吸道合胞病毒[49])。ALI培养通常是低通量的,因此不太适合用于筛选应用。虽然药物是在细胞培养基中基底外侧应用的,但有可能开发出一种将雾化药物应用于培养的系统。因此,这里描述的方法可能广泛适用于基础肺生物学、吸入毒理学[50]以及其他涉及上皮细胞的呼吸道疾病的研究,如慢性阻塞性肺病、哮喘和肺纤维化。类器官培养已被开发为囊性纤维化背景下可扩展的原代细胞培养模型[51],其中类器官肿胀可作为离子通道功能的代理[52,53].然而,这种方法,即使随着气道类器官的发展[54,55],对睫状体疾病的治疗效果较差,因为睫状体运动在类器官结构中比ALI培养中更难观察,而且治疗性化合物在根尖表面的应用也提出了技术挑战。
我们的方法能够产生和长期维持分化能力的原代上皮细胞培养从PCD患者不同的致病突变。因此,它与PCD的诊断和基础PCD研究相关,据我们所知,这是使用分化的人类呼吸道上皮细胞在罕见呼吸道疾病中进行个性化筛查的第一个例子。培养方法和检测方法的小型化表明,在无义突变的PCD患者亚群中,读通药物和NMD抑制剂可作为进一步临床前探索的靶点。
补充材料
可共享的PDF
确认
我们感谢参与这项研究的家庭,并感谢英国PCD家庭支持小组和成本行动BEAT-PCD (BM1407)的支持。我们感谢Simon Broad和Fiona Watt(伦敦国王学院,英国)提供了我们研究中使用的3T3-J2成纤维细胞。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
利益冲突:D.D.H. Lee没什么可透露的。
利益冲突:d·卡迪纳尔没什么可透露的。
利益冲突:e·尼格罗没有什么可透露的。
利益冲突:C.R.巴特勒没有什么可透露的。
利益冲突:A.拉特曼没有什么可透露的。
利益冲突:法阿萨德先生没有什么可透露的。
利益冲突:R.A.赫斯特没有什么可透露的。
利益冲突:D. Moulding没有什么可透露的。
利益冲突:A.阿格蒂斯没有什么可披露的。
利益冲突:E.福赛斯没有什么可透露的。
利益冲突:d·佩卡姆没有什么可透露的。
利益冲突:E.罗布森没有什么可透露的。
利益冲突:C.M.史密斯没有什么可透露的。
利益冲突:S. Somavarapu没有什么可透露的。
利益冲突:P.L.比尔斯没有什么可透露的。
利益冲突:S.L.哈特没有什么可透露的。
利益冲突:S.M.简斯没什么可透露的。
利益冲突:h。m。米契森没什么可透露的。
利益冲突:R. Ketteler没有什么可透露的。
利益冲突:R.E.海因兹没有什么可透露的。
利益冲突:c·奥卡拉汉没有什么可透露的。
支持声明:这项工作得到了行动医学研究(2336:“恢复原发性纤毛运动障碍儿童的纤毛功能-克服遗传障碍”)、大奥蒙德街医院慈善机构和2017/2018年斯巴克斯国家资助呼吁(V4818 -恢复原发性纤毛运动障碍儿童的纤毛功能)和NIHR大奥蒙德街医院生物医学研究中心的支持。这项工作也得到了医学研究委员会对MRC LMCB (MC_U12266B)和英国痴呆症平台(MR/ m02492 /1)的核心资助。在NIHR GOSH BRC奖17DD08的支持下,在UCL GOS儿童健康研究所的光学显微镜核心设施进行了显微镜检查。本文仅代表作者个人观点,并不代表NHS、NIHR或卫生部的观点。mr . Fassad是由英国文化协会Newton-Mosharafa基金和埃及高等教育部资助的。R.E. Hynds是威康基金会亨利·威康爵士研究员(WT209199/Z/17/Z), S.M. Janes是威康基金会临床科学高级研究员(WT107963AIA)。R.E. Hynds和S.M. Janes作为英国再生医学平台(UKRMP2)工程细胞环境中心(MRC;MR/R015635/1)和Longfonds BREATH肺再生联盟。S.M. Janes得到了Rosetrees信托基金、Roy Castle肺癌基金会和UCLH慈善基金会的进一步支持。本文的资助信息已存入交叉参考基金注册.
- 收到了2020年2月27日。
- 接受2021年3月1日。
- 版权所有©作者2021。
本版本根据创作共用授权协议4.0发布。