摘要
2019年12月,严重急性呼吸综合征2型冠状病毒(SARS-CoV-2)出现,导致2019冠状病毒病(COVID-19)大流行。SARS- cov是导致2003年SARS爆发的病原体,它利用血管紧张素转换酶2 (ACE2)和跨膜丝氨酸蛋白酶2 (TMPRSS2)宿主分子进入病毒。ACE2和TMPRSS2最近与SARS-CoV-2病毒感染有关。其他宿主分子包括ADAM17、组织蛋白酶L、CD147和GRP78也可能作为SARS-CoV-2的受体。
来确定表达式和原位为了定位呼吸道黏膜中的候选SARS-CoV-2受体,我们分析了515名健康受试者气道上皮细胞的基因表达数据集,使用包含120种不同样本类型的FANTOM5数据集进行基因启动子活性分析,10名健康受试者的单细胞RNA测序(scRNAseq),蛋白质组学数据集,多种气道上皮细胞类型的免疫印迹,以及98例人类肺部样本的免疫组织化学。
我们证明缺席到低ACE2启动子活性在多种肺上皮细胞样本中均较低ACE2基因表达在微阵列和scRNAseq数据集的上皮细胞群体。与基因表达一致,在人肺气道上皮和肺泡中观察到罕见的ACE2蛋白表达,并经蛋白质组学证实。我们证实了TMPRSS2、CD147和GRP78蛋白的存在在体外在气道上皮细胞和证实广泛原位CD147和GRP78蛋白在呼吸黏膜中的表达。
总的来说,我们的数据表明,可能在SARS-CoV-2感染期间,存在一种动态调节人类肺部ACE2表达的机制,并且还表明存在SARS-CoV-2的替代受体,以促进初始宿主细胞感染。
摘要
ACE2基因和蛋白在人肺的气道和肺泡上皮细胞中表达低到不表达。本研究表明,ACE2在人肺或其他SARS-CoV-2受体中的表达存在动态调节机制。https://bit.ly/3f85R1I
简介
2003年,由SARS冠状病毒(SARS- cov)引起的严重急性呼吸系统综合症(SARS)爆发,导致8096例疑似病例,774例确诊死亡[1,2].在SARS患者中,死亡归因于与弥漫性双侧肺炎和肺泡损伤相关的急性呼吸窘迫[3.].2019年12月,SARS-CoV-2出现,引发COVID-19大流行。SARS-CoV-2的传播速度比SARS-CoV快得多[4- - - - - -6].类似的弥漫性双侧肺炎和肺泡损伤的临床报道也有报道[7- - - - - -9].SARS-CoV-2重症病例与下呼吸道感染有关,在整个组织和上呼吸道都能检测到病毒[7- - - - - -9].可能导致SARS和COVID-19病例数量差异的生物学机制仍不明确。SARS-CoV-2可能具有独特的分子机制,通过病毒蛋白影响毒性、宿主细胞对感染的更大易感性、宿主细胞对病毒复制的允许性,或这些因素和其他潜在未知因素的某种组合[10- - - - - -13].在分子水平上了解SARS-CoV和SARS-CoV-2病毒在宿主体内的异同,可以为了解传播、发病机制和干预措施提供参考。
鉴定SARS-CoV受体的开创性报告使用HEK293细胞过表达系统,通过与SARS-CoV spike结构域1共免疫沉淀,鉴定血管紧张素转换酶2 (ACE2)为受体[14].随后,SARS-CoV的刺突蛋白被确定为ACE2的病毒相互作用伙伴。跨膜丝氨酸蛋白酶2 (TMPRSS2)的宿主蛋白酶活性促进ACE2外膜裂解和SARS-CoV膜与宿主细胞膜的融合[15- - - - - -17].ADAM17 (ADAM金属肽酶结构域17,ADAM(一种分解素和金属蛋白酶结构域)家族的成员)也被证明能切割ACE2外膜结构域,但这对SARS-CoV感染不是必需的[18- - - - - -20.].也报道了SARS-CoV进入不同于ACE2的机制,包括由内体组织蛋白酶L激活和CD147(也称为basigin (BSG))或GRP78 (78-kDa葡萄糖调节蛋白;亦称热休克蛋白家族A (Hsp70)成员5 (HSPA5)) [21- - - - - -23].对这些受体进行了机械地询问,结果表明SARS-CoV可以通过多种机制启动宿主细胞进入和感染。最近在体外有报道表明,类似的宿主蛋白参与了促进SARS-CoV-2进入细胞的过程,如ACE2和TMPRSS2 [5,24].生物物理和结构证据强烈支持ACE2与SARS-CoV-2刺突蛋白相互作用,类似于SARS-CoV刺突蛋白[12,13].分子对接研究也表明SARS-CoV-2刺突蛋白可与细胞表面GRP78相互作用[25].CD147在SARS-CoV-2结合中发挥作用的间接证据已经得到证实在体外通过使用抗cd147干预来阻止病毒复制[26].此外,一项抗cd147干预的临床研究减少了COVID-19患者的症状和住院时间[27].总之,尽管有证据表明SARS-CoV-2和SARS-CoV都利用ACE2作为受体促进病毒进入,但宿主进入机制的差异可能在两种病毒之间的巨大流行病学差异中发挥了作用,这可能包括其他未知受体。
通过机制研究,ACE2和TMPRSS2被确定为SARS-CoV的细胞进入决定因素。的原始报告原位肺泡和气道上皮细胞免疫组化染色显示ACE2阳性,A549型肺泡上皮细胞免疫组化染色显示ACE2阳性[28].ACE2蛋白在人肺腺癌细胞Calu-3中也有表达[29].与ACE2类似,TMPRSS2在人呼吸道黏膜中的表达的原始报道也描述了TMPRSS2在气道上皮和II型肺泡上皮细胞中的表达[30.].ACE2和TMPRSS2抗体用于人类肺组织表达模式分析的特异性仍有待解决。
为了解决人类肺部SARS-CoV-2受体的不确定性,我们进行了基因表达和检测原位人气道上皮细胞和肺组织中候选受体的蛋白谱分析。我们的计算分析使用了来自515名独特受试者的气道上皮细胞的公开可用的微阵列基因表达数据集,来自10名受试者的单细胞测序数据,以及74种肺相关细胞和组织类型的启动子活性的FANTOM5数据集。我们的蛋白质组分析使用了来自人类蛋白质组图的数据[31]和在气液界面培养条件下生长的原代人气道上皮细胞数据集[32].为我们的原位蛋白质分析,我们对98个人类肺组织样本进行了免疫组化分析。为了确定抗体特异性,我们对Calu-3细胞、原代人气道上皮细胞、原代II型肺泡上皮细胞、人支气管上皮细胞(HBEC)-6KT细胞系、A549 II型肺泡上皮细胞系和HEK细胞分离的蛋白进行免疫印迹。总的来说,我们的数据与之前的报道形成对比,表明在人类肺的气道上皮和肺泡中存在罕见的ACE2蛋白表达。我们的蛋白表达数据与low一致ACE2启动子活性在多种肺上皮细胞样本中均较低ACE2基因表达在微阵列和单细胞RNA测序(scRNAseq)数据集。我们证实了TMPRSS2、CD147和GRP78蛋白的存在在体外在气道上皮细胞和证实广泛原位CD147和GRP78蛋白在呼吸黏膜中的表达。我们的数据表明,可能在SARS-CoV-2感染期间,存在一种动态调节人类肺部ACE2表达的机制,并且/或存在SARS-CoV-2的替代受体,以促进肺组织中的初始宿主细胞感染。
方法
人类的道德
Hamilton (ON, Canada)综合研究伦理委员会(HiREB 5099T, 5305T, 11-3559和13-523-C)批准了用于免疫印迹和肺组织免疫组化的原代人气道上皮细胞的采购。英属哥伦比亚大学(Vancouver, BC, Canada)研究伦理办公室批准心脏组织档案和原代人气道上皮细胞收集。
上、下气道基因表达分析
公共微阵列实验使用Affymetrix芯片(HuGene-1.0-st-v1和HG-U133 Plus 2)对健康非吸烟者鼻腔(GSE19190)或支气管(GSE11906)刷取的气道上皮细胞样本进行,这些样本来自NCBI基因表达综合(GEO)数据库[33,34].这导致来自两个不同实验的总共80个个体样本,其中包括11个上呼吸道样本(鼻腔n=11)和69个下呼吸道样本(气管n=17,大气道n=17,小气道n=35)。对于所有数据集样本,使用GEOquery R包(版本2.52.0)下载原始强度值和注释数据[35]来自Bioconductor项目[36].探针定义文件从Bioconductor下载,探针使用Bioconductor的“注解”包进行注解。所有基因表达数据被统一到一个数据集中,然后通过稳健多阵列平均(RMA)归一化,只有在两个Affymetrix平台上都存在的基因(n=16 013)被保留用于后续分析。使用ComBat方法对实验特定批次效应进行修正[37]使用sva R包(3.32.1版本)实现[38].常规的rma归一化表达水平(ACE2,TMPRSS2,ADAM17而且CTSL(组织蛋白酶L1))和非传统(CD147而且GRP78)在四个确定的气道水平上对SARS-CoV-2受体基因进行了比较背景(E-cadherin)的表达水平作为阳性对照,在肺组织中已知表达。检测基因表达水平是否存在显著差异通过使用stats R包(3.6.1版)进行成对Wilcoxon秩和检验和Benjamini-Hochberg多重检验校正。使用ggplot2 R包(3.2.1版本)生成基因表达框图。
支气管上皮细胞涂刷数据集分析
从NCBI GEO数据库中选取了1859个使用Affymetrix芯片(HG-U133 Plus 2和HuGene-1.0-st-v1)的气道上皮细胞样本公共微阵列实验。这些样本通过去除哮喘或COPD患者进一步过滤,得到总共504个健康个体样本(GSE4302, 28个样本;GSE67472, 43个样品;GSE37147, 159个样品;GSE108134, 274个样品)。在该数据集中,包括310个样本的性别和/或年龄信息;其中,有86名女性和106名男性的性别数据可用。研究人员还提供了451个样本的吸烟状况信息,其中包括260名当前吸烟者、82名前吸烟者和109名从不吸烟者。
对于所有数据集样本,原始强度值和注释数据按照描述下载。探测定义文件按照描述检索。所有基因表达数据被统一到一个单独的数据集中,然后进行rma标准化,只有在两个Affymetrix平台(n=16 105)中都存在的基因被保留以供后续分析。如所述,对实验特定批效应进行校正。
FANTOM5数据集启动子活性分析
FANTOM5启动子组数据集[39]用于hg38组件[40]用于检测sars - cov -2相关人类基因的启动子活性,即ACE2,TMPRSS2,ADAM17,CTSL,CD147而且GRP78.使用ZENBU基因组浏览器[41],在上游和与上述每个基因位于同一链上的最近的基因表达帽分析(CAGE)峰被提取并分析。该数据集包括1866个人类原代细胞、细胞系和组织的CAGE启动子活性数据,并被量化为每百万归一化转录本(TPM)。本文介绍了FANTOM5 CAGE数据的一个子集(120个样本),仅考虑与肺、肠道、心脏和前列腺组织相关的样本(分别由74、19、15和12个样本组成)。记录每个CAGE峰值的归一化TPM值,即启动子活性的近近值10根据组织和细胞类型进行转换和分离,每个点的半径与这些转换后的归一化TPM值成正比。
从蛋白质组学数据集中分析蛋白质丰度
公开的人类蛋白质组学数据来自K即时通讯et al。[31]和F奥斯特et al。[32],评估不同人体组织和实验条件下SARS-CoV-2受体相关蛋白的表达情况。从K的数据集中提取表达式值即时通讯et al。[31以CDH1为气道细胞对照,对ACE2、TMPRSS2、ADAM17、CTSL、CD147和GRP78进行检测。数据是使用R(版本1.0.12)中的pheatmap包创建的,并表示为log10-转换以方便可视化。蛋白质组学数据来自F奥斯特et al。[32]由取自健康非吸烟者的支气管上皮细胞组成(n=4;雄性),并暴露于PBS对照组。提取ACE2、TMPRSS2、ADAM17、CD147和GRP78的强度值,CDH1作为阳性对照。强度值由原研究作者确定通过所有检测到的与给定亲本蛋白相关的肽强度的正常化[32].使用ggplot2 R包(版本3.2.1)生成强度值log的箱形图10-转换为可视化的目的。
单细胞RNA测序数据分析
使用Cell Ranger管道(10x Genomics)预处理的数据来自GSE135893。10例对照组和12例特发性肺纤维化患者的样本下载并使用R中的Seurat包进行后处理[42].使用源论文中提供的标记定义细胞群[43].10个对照组的细胞被用于进一步分析。小提琴情节的可视化是用修拉创作的。
原代人气道上皮细胞
人肺腺癌细胞系Calu-3在供应商(ATCC HTB-55)定义的培养条件下生长。原代人气道上皮细胞分离通过来自同意的健康个体的支气管刷在PneumaCult ExPlus (Stemcell Technologies, Vancouver, BC, Canada)的水下单层培养条件下生长,并在第1代和第4代之间使用。人支气管上皮细胞系HBEC-6KT在添加表皮生长因子(0.4 ng·mL)的无角化细胞血清培养基中,在单层培养条件下培养−1)和牛垂体提取物(50 μg·mL−1) [44- - - - - -47].
免疫印迹
细胞蛋白用RIPA裂解缓冲液(VWR, Mississauga, ON,加拿大)分离,辅以蛋白酶抑制剂鸡尾酒(Sigma, Oakville, ON,加拿大),定量使用Bradford测定试剂(Bio-Rad, Mississauga, ON,加拿大)。使用无染色的4-20%预浇筑梯度凝胶进行免疫印迹,并在ChemiDoc XRS+成像系统(Bio-Rad)上成像。每个免疫印迹每巷添加20 μg蛋白。ACE2 (MAB933,单克隆,克隆号171606,2 μg·mL−1(研发系统)),TMPRSS2 (HPA035787,多克隆,0.4 μg·mL−1(Atlas抗体))、CD147 (ab666,单克隆,克隆mem - m6 / 1,1 μg·mL−1(Abcam))和GRP78(610979,单克隆,克隆40/BiP, 0.25 μg·mL−1(BD生物科学公司)和HPA038845,兔多克隆(阿特拉斯抗体))一抗稀释在5%脱脂牛奶/TBS和0.1% ten -20中,在4°C的rocker上孵育过夜,第二天使用抗小鼠(ACE2, CD147和GRP78 (BD生物科学公司))或抗兔(TMPRSS2和GRP78(阿特拉斯抗体公司)辣根过氧化物酶(HRP)偶联二抗在1:3000室温下检测2小时(Cell Signaling, Danvers, MA, USA)。TMPRSS2、CD147和GRP78的显像使用Clarity Western enhanced chemiluminescence (ECL) Substrate,而ACE2的显像使用Clarity Max ECL Substrate (Bio-Rad)。收集总蛋白质负荷图像,作为样品类型之间蛋白质负荷的定性可视化[48].ACE2一抗的免疫原是小鼠骨髓瘤细胞系ns0来源的重组人ACE2 Gln18-Ser740(预测)。TMPRSS2一抗的免疫原是重组蛋白表位标记标记抗原序列,GSPPAIGPYYENHGYQPENPYPAQPTVVPTVYEVHPAQYYPSPVPQYAPRVLTQASNPVVCTQPKSPSGTVCTSKT。CD147一抗的免疫原是与人CD147相对应的重组全长蛋白。GRP78 BD生物科学一抗的免疫原是人BiP/GRP78氨基酸525-628。GRP78 Atlas Antibodies一抗的免疫原是重组蛋白表位标记标记抗原序列EKFAEEDKKLKERIDTRNELESYAYSLKNQIGDKEKLGGKLSSEDKETMEKAVEEKIEWLESHQDADIEDFKAKKKELEEIVQPIISKL。
对A549、HEK和永生化人支气管上皮细胞进行独立免疫印迹分析(L. Organ, C. Joseph, A. John和G. Jenkins)。等量的蛋白质(20µg)加载到4-12%,Bis-Tris梯度凝胶(NP0326BOX;ThermoFisher)抗ace2 (ab108252,兔单克隆,克隆EPR4435(2), 1/500稀释备用抗体;Abcam)。用GAPDH负载对照来演示蛋白负载(ab181603,兔单克隆,EPR16884, 1/10 000稀释的储备抗体;Abcam)。在Licor C-DiGit上使用ECL Clarity (Bio-Rad)进行可视化。
免疫组织化学
福尔马林固定石蜡包埋的人肺组织来自于非病变区域,来自于接受肺切除术的患者的存档组织块,用于临床护理。人类心脏组织来自英属哥伦比亚大学心血管组织登记处。切取4 μm厚的切片,对15 μg·mL的ACE2进行染色−1)、TMPRSS2 (10 μg·mL−1), CD147 (5 μg·mL−1)和GRP78 (HPA038845, 1/200稀释)使用与免疫印迹分析相同的抗体。所有染色均在Leica Bond RX系统上进行,使用Leica Bond试剂,在pH值6(20分钟)下进行热诱导抗原提取,一抗培养20分钟。数字玻片扫描使用Olympus VS120-L100虚拟玻片系统,放大40倍,使用VS-ASW-L100 V2.9软件和VC50彩色相机,然后使用HALO图像分析软件进行图像可视化。
结果
在人呼吸道上皮细胞和肺组织中检测到在SARS-CoV-2感染中重要的候选基因
我们进行了针对性的分析ACE2,TMPRSS2,ADAM17,CTSL,CD147而且GRP78在人呼吸道上皮细胞中作为SARS-CoV-2感染的重要候选基因的表达。在这里和整个基因表达分析中,背景(E-cadherin)作为肺上皮细胞表型的对照。我们首先在从鼻窦到肺中第12代气道的上下气道上皮细胞基因表达的策展数据集中检测了这些基因(图1)。
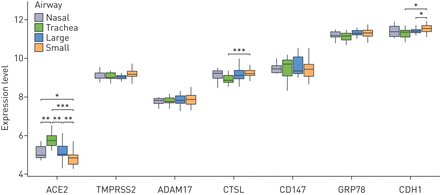
SARS-CoV-2候选受体基因在上呼吸道和下呼吸道的表达谱正常的日志2表达水平ACE2(血管紧张素转换酶2),TMPRSS2,ADAM17,CTSL(组织蛋白酶L1),CD147而且GRP78比较了上气道(鼻腔)和下气道(气管,大气道和小气道)的基因。背景(E-cadherin)基因表达水平作为阳性对照。计算每个气道世代每个基因的比较统计值;未显示的无显著性。*: p < 0.05;* *: p < 0.01;* * *: p < 0.001。
在上呼吸道,所有候选表达,最高水平观察到GRP78以及观察到的最低水平ACE2.对多代下气道(气管,大气道(第4 - 6代)和小气道(第10 - 12代)的分析显示相同的相对表达模式,与ACE2成为最少被表达的人GRP78最高的:最高表达的ACE2基因表达沿上、下气道变化最大,在气管样本中表达量最大,在小气道中表达量最低(图1)。
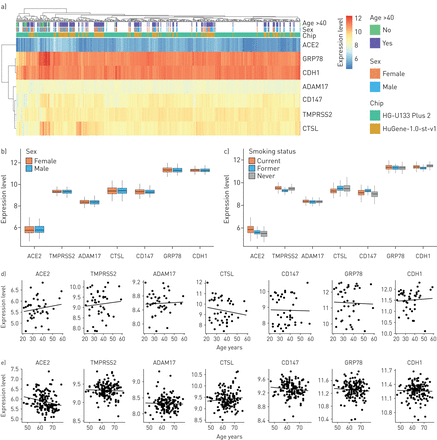
在我们观察到在SARS-CoV-2感染中重要的候选基因沿上呼吸道和下呼吸道的一致表达后,我们使用来自504名健康受试者的支气管刷诊数据集(补充表S1)。候选基因在健康受试者中的表达水平与在上呼吸道、气管、大气道和小气道的小规模调查中观察到的模式相似(图2)。中位数ACE2基因表达最低,而GRP78基因表达最高(图2一个)。没有候选基因在表达水平上表现出性别依赖(图2 b)。ACE2,TMPRSS2,CD147而且GRP78在当前吸烟者中相对于从不吸烟者中升高(图2 c而且补充表S2)。CTSL相对于从不吸烟的人来说,正在吸烟的人减少了。在性别或吸烟状况与基因表达之间的关系中,没有观察到微阵列芯片依赖的影响。对于年龄和基因表达相关的定量分析,由于年龄分布的差异,我们的数据库被分为使用HG-U133 Plus 2或HuGene-1.0-st-v1微阵列的数据集。在HuGene-1.0-st-v1数据集中(n=181),其中包括较大比例的老年人(>50岁),我们观察到减少ACE2随年龄变化的基因表达(图2 e;p < 0.05)。
候选SARS-CoV-2受体基因在气道下上皮细胞中的基因芯片表达谱,按年龄和性别分析.a)日志的聚类热图2NCBI基因表达综合(GEO)样本(n=504)的表达水平,按年龄、性别和微阵列芯片平台标注。表达值反映信号强度,表示检测到的最低表达ACE2(血管紧张素转换酶2)和最高表达GRP78而且背景(钙)。b和c)按b)性别(n=194)和c)吸烟状况(n=451)分隔的表达水平的箱形图。d和e)基因表达水平图与d) HG-U133 Plus 2微阵列(n=43)或e) HuGene-1.0-st-v1微阵列(n=181)的数据集。由于年龄分布的差异,各平台之间的相关性是单独进行的。e)为弱负相关(r=−0.20,p=0.015)ACE2在使用HuGene-1.0-st-v1微阵列的数据集中。
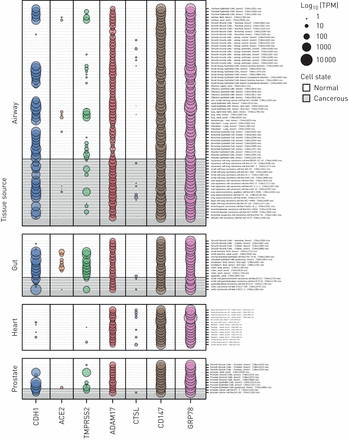
从FANTOM5数据集中提取并分析了在SARS-CoV-2结合和感染中重要的每个候选基因的启动子活性数据,其中包括1866个原代细胞、细胞系和组织样本类型(图3)。我们选择了包括“肺”、“鼻腔”、“气道”或“嗅觉”的所有样本格式,以确定肺部特定的样本类型。肠道、心脏和前列腺组织样本作为对照进行分析。与我们沿上气道和下气道观察到的基因表达分析一致,每个CAGE峰值的归一化TPM值表明CD147启动子活性相对于ACE2启动子活性横跨气道上皮细胞和肺组织样本。CTSL启动子活性是所有候选基因中最低的,这与在基因水平上观察到的适度表达形成对比(图2一个)。微阵列基因表达分析和启动子活性均与10名健康受试者的scRNAseq数据集的候选基因表达结果一致(补充图S1)。
来自基因表达(CAGE)数据集FANTOM5帽分析的sars - cov -2相关基因启动子活性。FANTOM5 CAGE数据包括来自原代细胞、细胞系和组织样本的1866个人类基因组的定量启动子表达水平。几个sars - cov -2相关基因的FANTOM5 CAGE启动子活性数据显示了与肺、肠道、心脏和前列腺组织相关的样本(n=120)。网点大小与启动子活性成正比,用log表示10-每百万转换规范化转录本(TPM)。值得注意的是,血管紧张素转换酶2 (ACE2)在气道中要么不表达,要么低水平表达(除一个样本外,所有样本均< 1tpm),包括对健康细胞和癌细胞的测量。
总的来说,我们对不同年龄的健康男性和女性的上气道和下气道的基因表达分析表明ACE2在人气道上皮细胞中,基因表达相对于所有其他候选SARS-CoV-2受体基因较低。此外,我们在基因水平上没有观察到任何候选基因的性别依赖或年龄依赖的表达模式,尽管吸烟状态确实对基因表达水平有影响。
在体外而且原位蛋白质分析揭示了在SARS-CoV-2感染中重要的候选基因的不同表达模式
转录数据的分析可能不能说明原位蛋白质表达水平[49].为了扩展我们的基因表达观察,我们从全肺和原代人气道上皮细胞培养中挖掘了公开可用的蛋白质组学数据,并进行了实验在体外人气道上皮细胞裂解物和免疫印迹原位蛋白质免疫组化在人肺组织上使用相同的抗体每种方法。
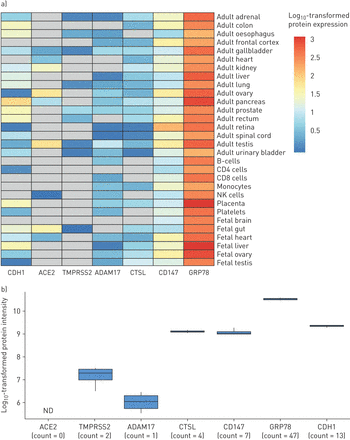
人类蛋白质组图谱是一种公开资源,其中包括精选的成人和胎儿组织以及循环免疫细胞群[31].利用这一资源,我们检测了ACE2、TMPRSS2、ADAM17、CTSL、CD147和GRP78的蛋白表达。在人类肺组织匀浆中未检测到ACE2,而在心脏、肠道和睾丸等已知阳性对照组织中检测到ACE2 (图4一)。人肺组织匀浆中剩余分子的排列顺序为:GRP78>CD147>CTSL>ADAM17>TMPRSS2。人类肺组织匀浆是一种异质的细胞群,排除了将蛋白质表达与特定细胞类型相关联的能力。因此,我们询问了一个公开的蛋白质组学数据集,这些数据来自于在气液界面培养条件下生长的原代人类气道上皮细胞[32),审查同样的候选人。同样,ACE2蛋白表达未检测到(图4 b)。CD147、GRP78和CTSL在多肽计数中表达,TMPRSS2和ADAM17在低肽计数中仅少量表达。总的来说,来自不同肺样本格式的两个蛋白质组学数据集提供了在SARS-CoV-2感染中重要的候选分子的互补和一致的表达谱。
人体组织和气道上皮细胞SARS-CoV-2候选受体基因的蛋白质组学分析a) K的蛋白表达强度值即时通讯et al。[31血管紧张素转换酶2、TMPRSS2、ADAM17、组织蛋白酶L1、CD147和GRP78基因。CDH1 (E-cadherin)强度被包括为气道细胞表达的阳性对照。强度值已被记录10-转化,以方便在不同组织类型中具有不同基础表达水平的候选之间进行比较。热图中的灰色细胞对应于未转换的强度为0,代表不可检测的信号。b)强度值log10-转化用于健康非吸烟者气道上皮细胞ACE2、TMPRSS2、ADAM17、CTSL、CD147和GRP78蛋白的可视化(n=4;雄)在气液界面培养条件下生长[32].CDH1强度作为阳性对照。提供了指示与每个亲本蛋白相关的检测到的肽的数量的计数。ND:在这项研究中没有检测到这种蛋白质。
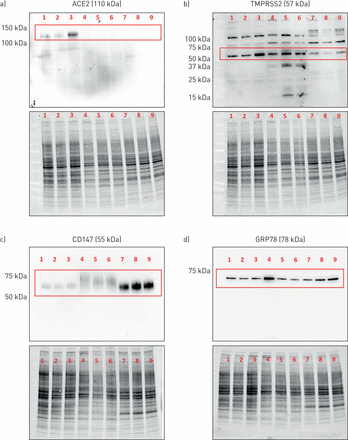
本地化原位在蛋白水平表达感兴趣的候选分子时,我们采用免疫组化分析和免疫印迹验证所选抗体的特异性,以识别预测分子量的蛋白质。抗ACE2抗体在Calu-3细胞中仅检测到ACE2蛋白预测分子量(约110 kDa)的单个条带(图5一个, 1-3车道)。抗ace2抗体需要使用超灵敏的ECL溶液。在原代气道上皮细胞或HBEC-6KT细胞系中未检测到ACE2蛋白,尽管确认了蛋白负载(图5一个,通道4-9,蛋白质含量显示在主印迹下方)。使用独特的抗ace2一抗进行独立免疫印迹,在HEK细胞中观察到单一条带,但在永生化人支气管上皮细胞或A549细胞中没有观察到(补充图S2)。
血管紧张素转换酶2 (ACE2)、TMPRSS2、CD147和GRP78蛋白在人气道上皮细胞蛋白裂解物中的表达。a) ACE2单条带预测分子量为110 kDa(红框)。b) TMPRSS2具有多条条带,其中预测分子量为57 kDa的优势条带(红框)。c) CD147,预测分子量为55 kDa(红框)。d)预测分子量为78 kDa的单条带GRP78(红框)。通道1-3:Calu-3细胞。通道4-6:原代人气道上皮细胞。Lanes 7-9:人支气管上皮细胞(HBEC)-6KT细胞系。所有细胞在水下单分子膜条件下生长,n=3个独立传代(Calu-3或HBEC-6KT)或供体样本(原代人气道上皮细胞;不吸烟、健康的受试者)。 For each independent blot of each protein, all of the same samples were run. A total protein loading control is provided to demonstrate protein loaded for each sample.
一种抗tmprss2抗体在所有气道上皮细胞样本中检测到多个条带,其中一个优势条带的预测分子量约为57 kDa (图5 b)。这些模式在所有被分析的细胞类型中都是保守的。
抗cd147抗体在所有气道上皮细胞样本中检测到一个单一的条带,其主导条带的预测分子量为~ 55 kDa (图5 c)。免疫印迹条带与CD147的重度糖基化一致[50].
一种抗grp78抗体(BD Biosciences 610979)在所有气道上皮细胞样本中检测到一条单一的条带,其主导条带的预测分子量为~ 78 kDa (图5 d)。
使用抗ace2、抗cd147和抗grp78的免疫印迹显示了单一的预测分子量条带,这表明观察到的免疫组织化学染色应该是基于目标表位的特异性蛋白,因为这两种方法都检测变性蛋白[51].同样的抗ace2和抗cd147抗体在免疫组化中得到验证。抗tmprss2用于免疫组化,尽管免疫印迹观察到的多个条带提醒了任何观察到的特异性原位染色。优化抗grp78抗体应用于免疫组织化学的尝试是不成功的,需要用HPA038845 (Atlas抗体)进行额外的抗体询问,这适用于免疫印迹和免疫组织化学(补充图S3)。
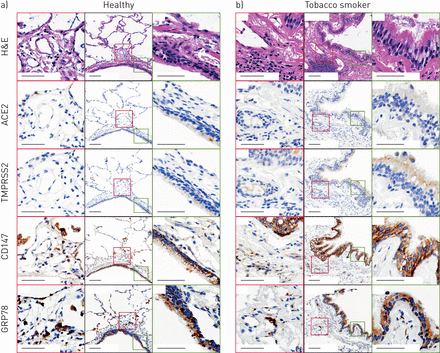
ACE2免疫组化结果显示,98例人类肺样本(包括健康受试者和慢性肺部疾病患者)的气道和肺泡中,只有少数细胞有选择性染色(图6)。一个健康的人样本含有一个阳性的气道上皮细胞,在肺外周的II型肺泡上皮细胞形态的细胞中有另外的阳性染色(图6)。患有慢性阻塞性肺病的吸烟者样本的代表性图像(图6 b)在气道上皮细胞中未见ACE2蛋白染色,在基底下膜组织中见罕见的阳性细胞。ACE2染色的阳性像素计数归一化到总组织像素计数的定量显示,健康的非吸烟者和吸烟者之间没有差异(补充图S4)。肺微血管及人心脏组织染色呈阳性(补充图S5和S6),与先前报道的ACE2蛋白染色模式一致[52,53].
血管紧张素转换酶2 (ACE2)、TMPRSS2、CD147和GRP78蛋白在人肺组织中的免疫组化定位代表性样本来自a)没有潜在慢性气道疾病的健康非吸烟者和b)患有慢性阻塞性肺病的吸烟者。黑色轮廓:低倍率(12倍)导气管与气道上皮;比例尺为100 μm。绿色轮廓:低倍率图像中绿色方块所界定的气道传导上皮高倍区域(60倍);比例尺为50 μm。红色轮廓:低倍率图像中红色方框所界定的肺组织远离气管腔的高倍区域(50倍);比例尺为50 μm。H&E:苏木精和伊红。免疫组化阳性为锈褐色。 Total number of independent samples analysed was 49–98.
TMPRSS2免疫组化显示气道上皮细胞和肺周围免疫细胞弥漫性染色,COPD吸烟者染色更明显(图6)。这些观察结果在被检查的98个人类样本中的大多数是一致的。
CD147免疫组化显示气道上皮细胞呈膜限制性染色,肺周围免疫细胞呈弥漫性染色(图6)。CD147在COPD吸烟者中显示出更大的染色。这些观察结果在被检查的98个人类样本中的大多数是一致的。
GRP78免疫组化显示气道、肺泡上皮及肺周围免疫细胞弥漫性染色(图6;49个样本)。GRP78染色在健康受试者和COPD吸烟者之间无定性差异。
总的来说,我们的在体外而且原位蛋白分析与我们的基因表达分析一致,CD147和GRP78蛋白的表达优势于TMPRSS2和ACE2。中提供了肺组织染色的其他例子补充图S7.ACE2蛋白表达在人类肺组织中很少见,在健康个体和慢性肺部疾病患者的特定细胞中都有发现。TMPRSS2和CD147蛋白表达在有吸烟史和COPD诊断的个体中增强。
讨论
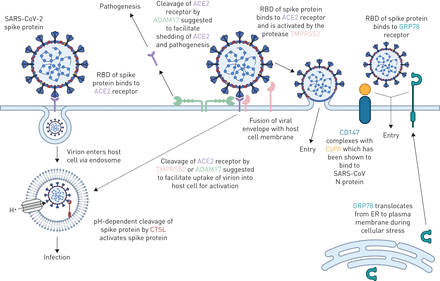
2019年底出现的全球COVID-19大流行是由SARS-CoV-2引起的。在人类肺组织中,尚未在基因和蛋白质水平上对SARS-CoV-2可能的宿主受体进行全面研究。了解宿主肺组织中候选SARS-CoV-2受体的表达水平和定位可能为减少疾病传播、病毒复制或疾病病理的治疗干预提供见解。为了解决这一知识鸿沟,我们在组织和细胞水平上进行了基因表达、蛋白质组学分析原位人气道上皮细胞和肺组织中候选受体的蛋白谱分析(综述于图7)。总的来说,我们的数据证明了罕见的ACE2蛋白在人气道上皮细胞中的表达在体外而且原位.我们的蛋白表达数据与low一致ACE2启动子活性在一组肺上皮细胞样本中较低ACE2基因在支气管上皮细胞(微阵列)和肺细胞(scRNAseq)中的表达。我们证实了TMPRSS2、CD147和GRP78蛋白的存在在体外在气道上皮细胞和证实广泛原位CD147和GRP78蛋白在呼吸黏膜中的表达。我们的数据表明,ACE2是SARS-CoV-2的一个完整受体,可能存在动态调节人类肺部表达的机制,可能是在SARS-CoV-2感染期间[54].SARS-CoV-2的替代受体也可能在初始宿主细胞感染中起重要作用。
提出了宿主气道上皮细胞分子与SARS-CoV-2相互作用的功能。显示了与SARS-CoV-2进入宿主细胞和SARS-CoV-2刺突蛋白(SARS-S)激活相关(或可能相关)的蛋白质。血管紧张素转换酶2 (ACE2)被认为是病毒进入SARS-S的主要受体(ACE2与SARS-S受体结合结构域(RBD)相互作用导致内体病毒摄取),随后是SARS-S的激活通过组织蛋白酶L1 (CTSL)介导的ph依赖性卵裂。病毒进入和SARS-S激活的次要方法可能涉及蛋白酶(如。TMPRSS2和ADAM17)和/或次级受体(CD147和GRP78)。虚线表示尚未完全验证的机制。CyPA:亲环素A;N蛋白:核衣壳蛋白;ER:内质网。改编自[20.]以更新候选宿主分子的信息。用BioRender.com创建的图。
考虑到合并来自不同来源的多个数据集的局限性,我们使用由504名健康受试者的支气管刷刷生成的策划微阵列基因表达数据集,观察到性别与任何涉及SARS-CoV-2感染的候选宿主分子的基因表达无关ACE2而且TMPRSS2对最低表达的基因进行了检测。在一个数据集中,ACE2基因表达随着年龄的增长而适度下降,尽管蛋白质水平无法确认。低水平的ACE2而且TMPRSS2大量支气管上皮细胞基因表达样本表明在肺组织中表达这两种基因的细胞水平较低。我们证实吸烟与血压升高有关ACE2支气管上皮细胞样本的基因表达水平[55],尽管我们无法通过免疫组织化学分析人类肺样本上的蛋白质来证实这一点。
转录组学的进步使scRNAseq能够识别出人类肺部中独特和罕见的细胞类型,这些细胞类型可能对健康和疾病具有重要意义[56,57].scRNAseq提供了一个机会来观察细胞群亚群中的转录谱,这可能会从大量样本中分离出细胞信号。因此,我们利用来自健康人类肺部样本的scRNAseq数据作为并行方法。scRNAseq对上皮细胞亚群的分辨率显示低表达或不表达ACE2基因在所有人群中被检测,然而CD147而且GRP78存在于所有人群中。我们的结果与目前公开的有关罕见ACE2/ tmprss2阳性细胞存在的数据一致[54].使用来自8个个体的肺样本(4个HIV和活动性结核病双阳性,2个HIV阳性和结核病阴性,2个双阴性对照),Ziegler等.[54在人类中,只有0.8%的II型肺泡上皮细胞同时表达ACE2而且TMPRSS2基因。对纤毛细胞的进一步分析发现,5.3%的纤毛细胞同时表达这两种基因ACE2而且TMPRSS2基因。在体外带有SARS-CoV的模型与这一发现一致,因为这种冠状病毒优先针对纤毛细胞[58].最有趣的是ACE2而且TMPRSS2基因表达细胞只在HIV和结核病双阳性样本中被发现。这些观察结果在上呼吸道中得到重复,只有极少数的分泌上皮细胞(占该细胞群的0.3%)共表达ACE2而且TMPRSS2.报告的scRNAseq结果与仅关注的集中分析一致ACE2多种肺细胞类型的基因表达[59].重要的是,这些出色的转录组分析证实了我们在大量组织微阵列数据集中的观察结果。
基于联盟的公开可用数据集代表了另一种并行方法来确认我们的数据。我们使用了FANTOM5数据集,其中包含1866个人类原代细胞、细胞系和组织样本的CAGE启动子激活数据[39]以检测每个候选SARS-CoV-2受体基因的启动子活性水平。FANTOM5 CAGE数据提供了一种额外和补充的方法来量化基因表达,因为给定基因的共享启动子可以产生不同表达水平的多个转录本,并且部分独立于任何给定转录本在细胞中的半衰期。一般来说,启动子的活性ACE2在呼吸道相关组织中低或无;只有来自成人肺的单个样本产生了正常的CAGE启动子表达水平>1 TPM,而在肠道细胞中观察到表达,与已知的ACE2表达模式一致[60].与微阵列数据一致CD147启动子活性相对于ACE2横跨呼吸道相关细胞和组织,虽然相对较低CTSL启动子活性与适度水平的基因表达不一致。
基因的表达并不总是与蛋白质的表达相关[49].考虑到这一点,我们进行了结合蛋白质组学分析和免疫印迹分析。对于我们的免疫印迹,我们使用了人类Calu-3腺癌细胞系,因为该细胞系对SARS-CoV-2感染敏感且允许,并表达ACE2,我们证实了这一观察结果[24,29].我们还使用了原代人气道上皮细胞和支气管上皮细胞系(hbec6kt)。我们对ACE2和TMPRSS2进行了免疫印迹检测,因为这些已被强调为与SARS-CoV-2相互作用,而我们对CD147进行了检测,因为最近的临床前和临床研究已经为CD147作为候选SARS-CoV-2受体提供了概念证明[26,27].最后,GRP78在整个转录组研究中主要表达,并被选为阳性对照,因为之前已在人类气道上皮细胞中证实表达[61].由于组织蛋白酶L的启动子活性较低(图3),而ADAM17被排除在外,因为在冠状病毒感染中被提议的功能是通过ACE2 [5,24],纳入分析。所有抗体的免疫印迹分析显示了预测分子量的主要条带,抗tmprss2多克隆抗体在所有检测的细胞样本中显示了额外的小条带。这些其他条带的身份尚不清楚,提示下游免疫组化分析可能被该抗体的特异性所混淆。而ACE2、CD147和GRP78抗体具有特异性,可用于免疫组化而不考虑特异性。有趣的是,ACE2蛋白只能在超敏感的ECL溶液中检测到,并且只能在Calu-3细胞中检测到,这表明原代人气道上皮细胞和HBEC-6KT细胞系中缺乏该蛋白。我们的数据与之前使用相同一抗在单分子膜浸泡条件下培养的人气道原代上皮细胞的免疫印迹结果一致,其中ACE2蛋白不存在,仅在气液界面培养条件下表达[62].CD147和GRP78也在Calu-3细胞中表达的观察鼓励了对这些宿主蛋白的进一步研究,因为它们可能有助于ACE2和TMPRSS2在该细胞类型中SARS-CoV-2结合和融合中的功能。总的来说,通过气道上皮细胞的免疫印迹对抗体进行分析,揭示了不同的条带模式,表明对ACE2、CD147和GRP78的抗体特异性,对TMPRSS2的特异性较低。
免疫组织化学分析已在人肺中定位ACE2和TMPRSS2 [28,30.].这些蛋白在人肺组织中的阳性染色观察没有伴随免疫印迹或补充方法来确定所使用抗体的特异性[51].在未确定抗体特异性的情况下,应谨慎解释所提供的历史数据。为了解决免疫组化染色的抗体特异性问题,我们使用了通过免疫印迹验证的相同抗体,并使用蛋白质组学作为一种正交的、抗体独立的方法来确认结果。我们再次关注ACE2和TMPRSS2,因为它们是对SARS-CoV-2感染宿主细胞很重要的候选蛋白。我们的ACE2免疫组化染色模式与转录谱和免疫印迹一致,98个人类样本中只有一个在气道和肺泡上皮中显示罕见的染色。心脏组织和肺微血管区ACE2染色阳性表明我们的染色方案是成功的。这些结果与使用缺乏特异性验证的抗体报道的结果形成了直接对比[28,30.].TMPRSS2在所有检查样本中表达频率更高,气道上皮的变化与吸烟史和/或COPD状态相关。与此相反,CD147在所有样本的气道上皮中均有表达。与TMPRSS2相似,CD147表达升高与吸烟史和/或COPD状态相关,与先前的报道一致[50].我们最初选择用于免疫印迹的GRP78抗体未进行免疫组化验证。因此,我们使用额外的抗体(HPA038845)进行了验证性GRP78免疫印迹和免疫组化,并提供了在人气道上皮细胞中的表达在体外而且原位.重要的是,GRP78在正常生理条件下存在于内质网(ER)中,作为ER的分子伴侣,促进正确的蛋白质折叠。然而,在内质网应激条件下,包括病毒感染,一部分居住在内质网的GRP78重新定位到细胞表面,在那里它可能作为病毒共受体[63,64].据报道,在动脉粥样硬化斑块中存在细胞表面GRP78 [65]、前列腺癌[66]和肾[67].然而,目前还没有商业上可用的抗GRP78抗体特异性结合到细胞表面GRP78,双免疫荧光用于显示细胞表面GRP78与已建立的表面受体的共定位[65].这一缺陷使我们无法对肺组织进行精确的细胞表面GRP78免疫组化,从而在SARS-CoV-2受体的背景下进一步研究这一概念。利用前列腺癌患者来源的GRP78自身抗体,特异性的细胞表面GRP78 [65]可能适用于肺组织,通过GRP78评估细胞对SARS-CoV-2感染的易感性。
我们的研究有几个局限性还没有解决。我们观察到的上气道和下气道之间以及沿气道树的基因表达差异在蛋白质水平上没有得到证实。上呼吸道中仍有可能存在完全不同的候选分子蛋白表达谱,这为SARS-CoV-2与呼吸道粘膜相互作用提供了不同的环境。鼻咽拭子可检测SARS-CoV-2病毒[68]而这个解剖区域可能对随后的下呼吸道感染很重要[8,69].与这种潜在的暂时性影响相关,SARS-CoV-2可能在感染后诱导宿主细胞上受体的表达[54].我们的研究也受到了在基础条件下检查SARS-CoV-2感染中重要的候选分子的限制,在没有可能调节基因转录和蛋白质翻译的病毒或环境刺激的情况下。
SARS-CoV-2感染和传播已导致全球COVID-19大流行。需要了解SARS-CoV-2用于宿主细胞感染的受体及其在人类样本中的平行特征,以便为制定旨在减轻COVID-19的干预策略提供信息。我们的数据显示了罕见的ACE2蛋白在人气道上皮细胞中的表达在体外而且原位,与低一致ACE2启动子活性ACE2支气管上皮细胞的基因表达。我们证实了TMPRSS2、CD147和GRP78蛋白的存在在体外在气道上皮细胞和证实广泛原位CD147和GRP78蛋白在呼吸黏膜中的表达。由于大量证据表明,SARS病毒与ACE2相互作用,在SARS- cov -2感染的背景下,呼吸黏膜中可能存在调节ACE2的替代机制,和/或其他共受体,而不是在蛋白质水平的基础条件下表达。
补充材料
补充材料
请注意:补充材料不是编辑部编辑的,上传时是作者提供的。
补充表S1。原代人气道上皮细胞的GEO沉积数据集的元数据和参考文献。erj - 01123 - 2020。Table_S1
补充表S2。吸烟状态相对于从不吸烟对候选SARS-CoV-2受体基因表达影响的统计。erj - 01123 - 2020。Table_S2
补充图S1。非纤维化个体周围肺组织的scRNAseq。A表达水平的小提琴图:ACE2B:TMPRSS2C:ADAM17D:CTSL(组织蛋白酶L), E:CD147, F:GRP78健康受试者的肺上皮细胞群(参见细胞群标记物的数据集参考方法)。erj - 01123 - 2020。Figure_S1
补充图S2。ACE2免疫印迹分析的独立证实。第1道=梯子。Lane 2 = A549细胞系。Lane 3 - HEK293细胞。巷4 -永生化的人支气管上皮细胞。以GAPDH作为负载对照,ACE2的预测分子量为110 kDa。抗人ACE2抗体不同于免疫印迹图4。erj - 01123 - 2020。Figure_S2
补充图S3。使用Atlas抗体HPA038845进行GRP78的独立免疫印迹分析。通道1至3:Calu-3细胞。通道4至6:原代人气道上皮细胞。所有细胞在水下单分子膜条件下生长,n=3个独立传代(Calu-3)或供体样本(原代人类气道上皮细胞:非吸烟者,健康受试者)。较大的频带可能代表GRP94,其中包含与GRP78共同的KDEL域[69]。图5所示为该免疫印迹所运行的相同样本。总蛋白加载控制(底部图像)提供演示蛋白质加载为每个样品。erj - 01123 - 2020。Figure_S3
补充图S4。健康受试者与吸烟受试者的ACE2免疫组化染色定量免疫组化染色阳性像素表示为每个样本总组织像素数的百分比。N = 49。健康受试者与吸烟受试者的样本间无统计学差异。erj - 01123 - 2020。Figure_S4
补充图S5。ACE2在人肺组织微血管系统中的免疫组化定位。人类肺组织ACE2蛋白染色阳性(锈色/棕色)的代表性例子(n=3个供体),其区域与含有传导气道的视野不同。取自图5中相同幻灯片的图像(相同的染色程序和图像采集条件)。红色和绿色框为整个组织核心样品3倍放大60倍放大。erj - 01123 - 2020。Figure_S5
补充图S6。我mmunohistochemical localisation of ACE2 in human heart tissue. Representative examples (n=4 donors) of positive ACE2 protein staining (rust/brown) in human heart tissue. Staining protocol identical to Figure 5 and Supplementary Figure S3. Heart tissues stained on same staining run on Leica Bond Rx autostainer as for lung tissue in Figure 5. Red and green boxes are 60× zoom of 3× magnification of entire tissue core sample.erj - 01123 - 2020。Figure_S6
补充图S7。ACE2, TMPRSS2, CD147和GRP78蛋白在人肺组织中的免疫组织化学定位的另一个例子。黑色方框代表低倍率(12倍)的有气道上皮的导气管。绿色方块对应低倍率图像中定义的导气管上皮的高倍区域(50倍)。红色方块对应低倍率图像中定义的肺组织远离气道腔的高倍区域(50×)。第一排:苏木精、伊红;第二行:ACE2;第三行:TMPRSS2;第四行:CD147;第5行:GRP78/HSPA5。 Positive immunohistochemical staining is rust/brown.erj - 01123 - 2020。Figure_S7
可共享的PDF
确认
我们要感谢麦克马斯特免疫研究中心核心组织学设施(麦克马斯特大学,汉密尔顿,ON,加拿大)的Mary Jo Smith,她在免疫组织化学抗体染色方面的及时和专业的知识。我们要感谢Sam Wadsworth (Aspect Biosystems, Vancouver, BC, Canada)和John McDonough (Yale University, New Haven, CT, USA)关于CD147和气道上皮细胞生物学的学术讨论。我们要感谢Charles Plessy (Okinawa Institute of Science and Technology, Onna, Japan)提出分析FANTOM5数据的建议。我们要感谢三位作者各自的家人(Candace Lee Bastedo、Julianne Meiko Hirota和Hana Lee Hirota)和研究机构的所有个人和专业支持,最重要的是,感谢COVID-19大流行期间一线医护人员的支持。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
利益冲突:j·a·阿吉亚尔没什么可透露的。
利益冲突:bj - m。特伦布莱没有什么可透露的。
利益冲突:m。j。曼斯菲尔德没什么可透露的。
利益冲突:伍迪没什么可透露的。
利益冲突:B. Lobb没有什么可透露的。
利益冲突:A.班纳吉没有什么可透露的。
利益冲突:A.钱迪拉莫汉没有什么可透露的。
利益冲突:N. Tiessen没有什么可透露的。
利益冲突:问:曹没有什么可透露的。
利益冲突:A. Dvorkin-Gheva没有什么可透露的。
利益冲突:瑞维尔没有什么可透露的。
利益冲突:米勒女士没什么可透露的。
利益冲突:c·卡尔斯滕没有什么可透露的。
利益冲突:L. Organ没有什么可透露的。
利益冲突:C.约瑟夫没有什么可透露的。
利益冲突:约翰没有什么可透露的。
利益冲突:P. Hanson没有什么可透露的。
利益冲突:R. Austin拥有专利US7524826B2,已授予麦克马斯特大学和麦克马斯特大学汉密尔顿健康科学公司。
利益冲突:B.M.麦克马纳斯没有什么可透露的。
利益冲突:G. Jenkins报告了阿斯利康、Biogen、Galecto和葛兰素史克的资助;勃林格殷格翰(Boehringer Ingelheim)、大雄(Daewoong)、加拉帕戈斯(Galapagos)、Heptares、Promedior和Roche的个人费用;Pliant提供的赠款和个人费用;Redx和NuMedii的非财政支持;并且是肺纤维化行动的受托人,在提交的工作之外。
利益冲突:莫斯曼没有什么可透露的。
利益冲突:K. Ask没有什么可透露的。
利益冲突:ac·多克西没什么可透露的。
利益冲突:j·a·广田没有什么可透露的。
支持声明:这项工作得到了J.A. Hirota的启动资金和K. Mossman的CIHR资助。J.A. Hirota受到加拿大研究主席计划和安大略省早期研究员奖的支持。A.C. Doxey得到了NSERC和安大略省早期研究员奖的支持。本文的资助信息已存入交叉参考基金注册.
- 收到了2020年4月10日。
- 接受2020年7月1日。
- 版权所有©ERS 2020
本版本根据知识共享署名非商业许可4.0的条款发布。