文摘
上皮细胞对儿童过敏性呼吸道疾病的自然历史的贡献仍然知之甚少。我们的目标是识别上皮通路中特异表达的不同表型的呼吸道过敏。
我们建立的基因表达特征从尘埃mite-allergic鼻炎患儿鼻刷牙,相关或不相关或不受控制的哮喘控制。监督学习和无监督聚类是用来预测不同子组的病人和定义改变信号通路。这些概要文件与主文化的人类鼻腔上皮细胞的刺激与白介素(IL) 4, IL-13,干扰素(干扰素)-αIFN-βIFN-γ或期间在体外分化。
监督方法歧视儿童过敏性鼻炎与健康对照组(预测精度91%),根据61年的成绩单,包括21个辅助细胞(Th)类型2-responsive基因。这种方法被应用于预测控制或不受控制的哮喘患儿(75%)预测精度,基于41成绩单:9,抑制在控制哮喘,直接与干扰素。这组还包括GSDML,这是基因与哮喘有关。
我们的数据显示Th2-driven上皮表型共同向所有儿童尘螨过敏性鼻炎。它突出的影响上皮表达分子的控制哮喘,在协会与特异反应性和病毒反应受损。
哮喘是一种异构的和复杂的疾病,常伴有过敏性鼻炎。古典致病模型描述哮喘和过敏性鼻炎炎症增加辅助细胞(Th) 2型反应。尽管慢性炎症过程,几个额外的气道上皮的固有缺陷可能导致发病。在哮喘气道重构可以出现几年前任何明确的临床诊断,甚至影响学前儿童哮喘(1]。哮喘患者更容易出现呼吸道病毒感染的(2]。上皮细胞来源于哮喘病人表现出纤连蛋白分泌能力降低,在受损的气道上皮修复的一个重要因素,与有缺陷的抗氧化途径和紧密连接(3- - - - - -5]。一些研究试图把特定的基因表达谱与哮喘或过敏性鼻炎,主要在成人(3,6- - - - - -10]。收集的信息也被全基因组关联研究。单核苷酸多态性(snp)GSDML轨迹(靠近ORMDL3),一种蛋白质中发现上皮组织,同儿童疾病[紧密相关11]。基于这些发现,我们的理由是,气道上皮的缺陷可能对应于主要缺陷或早期次要的事件,这可能有利于慢性炎症,导致哮喘或过敏性鼻炎。因此,我们决定鼻刷牙的转录特征收集从儿科患者不同的临床表型尘螨呼吸道过敏。数据分析显示的几个信号通路改变行为的进一步分析在体外人类鼻腔上皮细胞分化模型(HNECs)。
材料和方法
主题和样品
患者年龄在6 - 17日年(n = 45)。33被进行了灰尘mite-allergic鼻炎。14也有哮喘,哮喘控制(集团“一个”;n = 7)或不受控制的哮喘(集团“一个”;n = 7)。19有鼻炎没有哮喘(R组)。对照组(C组)由12个健康的孩子。临床诊断和哮喘控制分期与过敏性鼻炎及其对哮喘的影响和美国国家儿科哮喘教育和预防计划专家报告3标准(有关详细信息,请参阅在线补充文件1)。项目收到了不错的大学医院伦理委员会的批准(不错,法国)和所有的志愿者的父母给书面知情同意。
抽样是由鼻呼吸道上皮细胞刷下鼻甲。
病毒性呼吸道感染的检测实时定量PCR (qPCR)都使用了RealAccurate™呼吸设备根据制造商的指示(PathoFinder马斯特里赫特,荷兰)。七个孩子(一个哮喘,五rhinitics没有哮喘和一个控制)呼吸道病毒阳性并不包括在进一步分析。总结了病人和样本的特点表1E1和在线补充表。
隔离和初级HNECs文化
HNECs派生的主要文化下鼻甲鼻粘膜的进行如前所述[12]。每个实验都使用三种不同的捐赠者。细胞因子治疗之前,HNECs在气液界面培养4周获得分化良好型的上皮细胞(12]。测试代理(白介素(IL) 4(美国圣地亚哥BD Pharmingen CA)和IL-13(美国新泽西PeproTech,落基山),10 ng·毫升−124小时;干扰素(IFN) -αA / D和IFN-β1a (Sigma-Aldrich, Saint-Quentin Fallavier,法国),1000 IU·毫升−16小时;和IFN-γ(BD Pharmigen), 100 ng·毫升−16 h)被添加在基底外侧。
基因表达分析
微阵列分析进行GeneChip人类基因第1.0位数组(美国Affymetrix,圣克拉拉,CA)根据制造商的指示。微阵列基因表达综合数据存档(www.ncbi.nlm.nih.gov地理)引用GSE19190 GSE22147, MEDIANTE数据库发展在我们的实验室13,14]。qPCR过程详细的在线补充文件1中,引物和探针在线补充表中列出E2。
生物统计学
大多数统计计算和预测分析使用limma和随机森林,R统计环境的两个包(15]。我们使用的功能注释集群报告可用数据库的注释,可视化和综合发现(大卫)[16]。层次聚类与MultiExperiment执行查看器程序,4.3版(美国TM4,波士顿,MA),使用一个曼哈顿距离度量和平均链接(17]。生物网络建成使用创造力通路分析™软件(智慧系统公司红木市,CA,美国)。基因集富集分析(GSEA)被用来确定是否定义的一组基因先天的可以描述两个生理状态之间的差异18,19]。编码(百科全书的DNA元素)功能基因组学数据被用来确定潜在的结合位点干扰素监管因素。
免疫组织化学
免疫组织化学方法在线补充文件1所示。
ELISA试验
HNECs MUC5AC发布水平IL-13刺激用ELISA测定根据制造商的指示(EIAab USCNLIFE;武汉,武汉EIAab科学有限公司,中国)。
结果
鼻上皮细胞的基因差异表达儿童尘螨过敏
转录签名的尘埃mite-allergic鼻炎(n = 27)与儿童的健康儿童(n = 11)。我们确定了169个差异表达成绩单(p < 0.05)(数据请求)。其中,24调制的绝对值的日志记录2(比率)> 1 (表2)。功能注释提供了由大卫E3在线补充表。变异的基因(CST1,POSTN,nt,CD44,内脏大神经和ALOX15)证实了qPCR(在线补充图E1)。
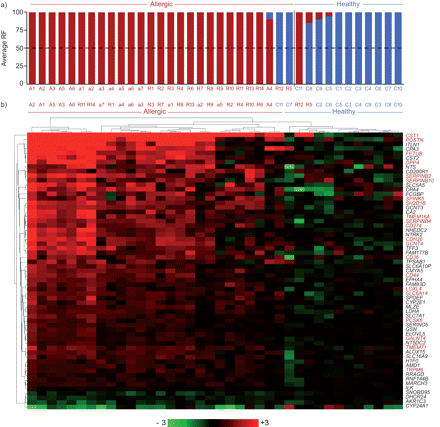
监督聚类是用来预测状态的每个38例(过敏或健康)。35的38例正确预测(预测精度为91%)(图1一个)。特异性和敏感性概括在一个接受者操作特征(ROC)曲线在图ea2在线补充,显示的ROC曲线下面积0.88。允许使用的随机森林方法识别最有影响力的基因的预测,导致的一组61年成绩单是常见的20个独立的交叉验证。大多数基因上调了过敏的条件(图1 b)。16他们先前与哮喘或过敏性鼻炎的基因表达分析(在线补充表E4) (3,6- - - - - -10]。签名与哮喘的过敏状态但独立地位。事实上,监督聚类是无法区分13 14名过敏性鼻炎患者的哮喘病人没有哮喘。这两组之间没有发现微分表达式的病人(数据未显示)。
歧视,随机森林(RF)尘螨过敏性鼻炎患儿的健康儿童和61个最判别的热图表示基因。直方图显示,对于每一个病人,分类的百分比作为灰尘mite-allergic鼻炎(红色)和健康(蓝色)的孩子。b) Nonsupervised,层次聚类相同的病人使用的61个基因共同随机森林分类器(见细节在材料和方法部分)。每个方块都代表一个给定的基因的表达水平在一个给定的样本相对于平均表达水平控制。红绿色色标表示基因表达水平高于(红色)或低于(绿色)的平均水平在健康受试者表达相同的记录。聚类进行了使用平均连接方法,使用一个曼哈顿距离。红色的基因名称(右)表明基因诱导在体外白介素(IL) 4和IL-13。
上皮Th2签名是过敏的儿童健康对照组的歧视
我们观察到一些记录对尘螨过敏患者特异表达也与文献中il - 4或IL-13 [20.]。我们模仿这种情况在体外通过刺激主要HNECs il - 4或IL-13。这个模型中,我们证实IL-13刺激增加了表达式(在线补充图E3A)和MUC5AC的分泌,杯状细胞标记(在线补充图E3B)。我们也观察到,同时,FoxJ1的表达减少,纤毛细胞标记(在线补充图E3A)。46气道上皮记录被选中时,基于他们的高响应Th2细胞因子和检测在高度分化的气道上皮细胞(在线补充表E5)。21日记录的“Th2签名”的61记录预测过敏或健康儿童(图1)。Th2监管的重要性被正常化浓缩评估分数> 1(1.61,名义假定值和错误发现率< 0.001),由GSEA的核反应能量(18,19]。有趣的是,我们注意到,与Th2签名相关的成绩单显示更大的日志2(比率)控制(A组)比在控制(A组)哮喘(图1)。这使我们探讨一个特定的表达谱的存在与不受控制的哮喘相关。
控制哮喘影响鼻上皮细胞基因表达的特征
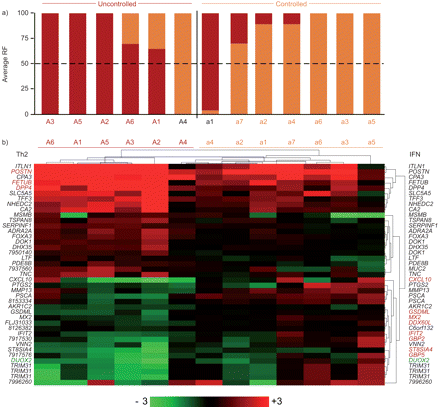
接下来的分析比较了两组受试者不受控制或控制哮喘。表1描述了这些病人的特点。160个基因的表达两组差别显著(在线补充表E6)。功能注释是发表在在线E7补充表。随机森林方法正确预测类12的14个样本,预测精度(75.4%图2一个)。归纳了特异性和敏感性ROC曲线在图E2B在线补充,显示的ROC曲线下面积0.833。它还发现了一组最小的41个最有影响力的基因预测(图2 b)。上调的POSTN,FETUB或DPP4(也属于Th2签名)(在线补充表E5)的控制与大集团是连贯的日志2(比率)观察Th2反应记录图1和2。我们也注意到的几个IFN-stimulated下调基因(isg)等CXCL10,(,IFIT2,DUOX2,2英镑和5英镑,在一个更大的集群的抑制基因(图2)。这是说明了创新路径分析(在线补充图E4)。我们的下调基因还包括集群GSDML17号染色体的基因位于区域温度系数,而最近有关青少年哮喘在几个全基因组关联研究(11]。的微分表达式CXCL10,(,IFIT2,DUOX2和GSDML证实了qPCR(在线补充图E1)。GSDML和DUOX2蛋白质被组织化学immunodetected鼻和支气管气道上皮细胞(图3)。
歧视,随机森林(RF)的儿童不受控制与控制哮喘和41岁的热图表示大多数判别基因。直方图显示,对于每一个病人,分类的百分比是不受控制的哮喘(红色)和控制哮喘(橙色)。b) Nonsupervised,层次聚类相同的病人使用41探测器共同随机森林分类器(有关详细信息,请参阅材料和方法部分)。每个方块都代表一个给定的基因的表达水平在一个给定的样本。红绿色色标表示基因表达水平高于(红色)或低于(绿色)的平均水平的健康对照组相同的记录。聚类进行了使用平均连接方法,使用一个曼哈顿距离。红色基因名称显示记录由白介素(IL) 4和IL-13(左)或干扰素(ifn)(右)(对应于一个日志2人类鼻腔上皮细胞(比率)> 1 (HNECs))。基因名字的绿色显示转录抑制il - 4和IL-13(左)(日志2在HNECs(比率)> 1)。
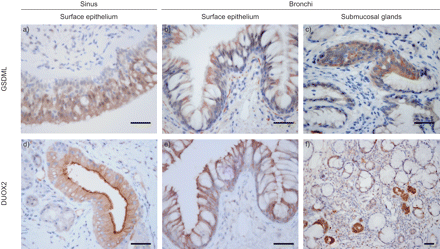
免疫组织化学染色的窦和支气管活检。代表a - c)组织化学染色GSDML和d-f) DUOX2表面上皮和粘膜下腺体是获得健康的成年人。积极观察疣状窦和支气管两种蛋白质的部分。强信号也被发现在黏膜下腺体不同的标记。酒吧= 100μm规模。
干扰素在病人和培养HNECs响应分析
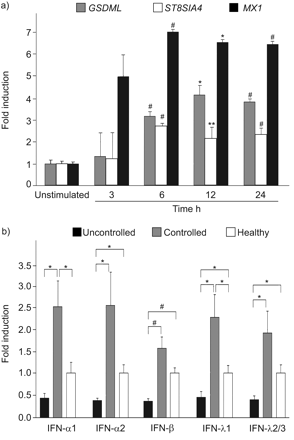
干扰素监管研究在体外通过刺激主要与IFN-αHNECs IFN-β或IFN-γ。我们选择IFN-responsive成绩单(在线补充表E8)。GSEA方法揭示了重要的正常化浓缩分数为所有亚型的干扰素控制/控制哮喘比较(IFN-βIFN-α1.7,1.64和1.56 IFN-γ)。干扰素诱导的表达的能力mx₁,ST8SIA4和GSDML证实了qPCR HNECs主要文化。的峰值GSDML观察诱导12 h IFN-α刺激后,而感应的高峰mx₁和ST8SIA4了6 h (图4)。的基因组上下文的调查(,IFIT2,CXCL10,GSDML,ST8SIA4和DUOX2透露一些共识的存在绑定序列干扰素监管因素(完整的数据请求)(在线补充图E5)。总之,这些观察结果表明干扰素的这些不同基因的直接监管。IFN-λ1,重要的是,转录水平的IFN-βIFN-λ2/3 IFN-α1和IFN-α2降低相比,不受控制的哮喘患者控制哮喘患者或健康受试者(图4 b)。内源性上皮干扰素的生产,而不是有缺陷的干扰素信号通路,因此可能参与这些过程。
描述的干扰素(IFN)的反应。)测量实时定量PCR (qPCR)的感应GSDML,ST8SIA4和mx₁人类鼻腔上皮细胞由IFN-α(HNECs)。水平的GSDML,ST8SIA4和mx₁评估在分化HNECs 3、6、12和24小时后与IFN-α刺激。测量使用SYBR执行绿色。结果表示为叠化相对于如果HNECs。b)测量qPCR干扰素的病人。水平的IFN-α1,IFN-α2、IFN-βIFN-λ1 IFN-λ2/3成绩单不受控制的哮喘患者,控制哮喘患者和健康对照组。数据是表示相对于平均11健康对照组。使用Taqman探测器进行测量。结果表示为叠化相对于健康对照组。数据意味着±扫描电镜。#由未配对t检验,p < 0.005;*:p < 0.05未配对t检验;* *:未配对t检验p < 0.01。
气道上皮再生和变应性疾病的严重性
气道上皮的修复能力受损是过敏性气道疾病的标志(5]。我们最近建立了基因表达在签名在体外HNEC再生和分化12]。“终端分化”签名是用来丰富注释来源于Th2细胞因子和干扰素的表达谱获得的实验。正如所料,病人是主要的分类与Th2细胞因子的影响和干扰素。然而,一些与疾病相关的成绩单也与终端分化签名(在线补充表E9)。第一组的基因,包括PLK4,CDC20B,GSDML和CYFIP2期间,显然是诱导分化,抑制在不受控制的哮喘患者。这让分组重要multiciliogenesis标记(PLK4和CDC20B)[12)和分子与哮喘相关的全基因组分析(GSDML和CYFIP2)。第二组,包括POSTN,SPINK5,CD44,TFF3,ITLN1,FOXA3和SPDEF,显然是与基底或粘液细胞(21]。他们中的大多数都在下降在体外分化而不受控制的哮喘患者都上调。
讨论
气道上皮细胞是一个复杂的物理屏障,发挥内在的天然免疫与适应性免疫的作用,通过大量的细胞因子和趋化因子的生产。我们的工作强调了干扰素的重要性,Th2-driven上皮反应过敏性呼吸道疾病的发病机理。我们的研究结果是基于biostatistical方法,如随机森林、独创性和GSEA,它不仅考虑到病人的数量,而且基因簇的大小可以由这些细胞因子。重要的是,这些方法提高我们的观察的统计意义。
选择执行我们的调查上,而不是低,气道上皮是出于它的非侵入式取样,很容易适用于儿童。它允许真正控制免除肺病的招聘,情况显然是不可能的在研究使用支气管镜的抽样[1]。它还允许调查严重或不受控制的哮喘患者表型没有停止他们的长期吸入激素治疗哮喘、鼻沉积可以被认为是微不足道的与本研究中使用的设备(22]。有趣的是,我们观察到一个好的重叠的“鼻上皮”基因列表和几个在支气管上皮细胞基因表达谱,尽管鼻和支气管上皮细胞之间的差异(23,24),如在鼻腔上皮缺乏改造附近(25]。在这种情况下,使用替代技术收获低气道细胞在全身麻醉可以值得研究[26]。我们无法确定特别的生物标志物识别哮喘和鼻炎患者可能是由于抽样的选择材料。如果这是真的,一个全面的比较支气管和鼻腔上皮细胞从同一病人将有助于探索这个问题。这是不幸的是没有计划在目前的研究。研究规模相对较小的样本(45)也可以限制。第三个解释可能是,歧视从过敏性鼻炎哮喘的主要差异,而是依赖于其他细胞类型(树突或间充质细胞,等。)。从这个角度来看,发展从过敏性鼻炎哮喘无法检测到的上皮细胞本身。
我们的研究建立了上皮由Th2细胞因子激活的核心特质气道过敏性呼吸道疾病。这是符合IL-13最能概括的观察哮喘的特征在一些疾病的实验模型(27]。我们的临床和在体外结果清楚地演示Th2细胞因子的重大影响过敏主题,反映出特异反应性状态的力量。几个Th2-induced基因,如POSTN,ITLN1,ALOX15,CD44和SERPINB4,曾与哮喘。其他人可以代表其他相关的生物标记物,由于其大过敏组和一致的变化。例如,CST1编码一种半胱氨酸蛋白酶抑制剂,已经与肺纤维化相关系统性硬化患者(28]。另一个例子是nt,与伤口愈合在慢性结肠炎29日]。
一个增强的老年病Th2-responsive基因(以更大的日志2(比)值)在控制哮喘。事实上,儿童哮喘严重程度已经与特异反应性在流行病学研究30.]。这种联系似乎专门针对儿童哮喘,因为据报道在成人(成反比关系31日]。有趣的是,IL-13已被证明导致profibrotic支气管表型通过连续分泌的改变增长factor-β2 [32]。引人注目的是,第一个基因本体的主题比较不受控制和控制哮喘对应于“结构的细胞外基质成分”这个词,表达增强POSTN,过渡委员会,FBN2,FBLN2,在你和COL4A6。人们很容易推测,这种失调可以直接相关的结构修饰和改造上皮特别观察严重哮喘(33]。与此同时,POSTN据报道诱导分化造成的哺乳动物心肌细胞进入细胞周期,与组织修复(34]。粘液分泌过多,杯状细胞化生是哮喘的重要特征,也与IL-13失调。我们也注意到,TFF3,这是粘液细胞和表达能促进人类气道纤毛上皮细胞的分化21),是上调过敏的病人。这说明机制的复杂性导致异常的维修和改造。
Th2细胞因子可能掩盖弱的重大影响,内在上皮功能。我们相信这是一个混杂因素在分析上皮易感性与微阵列技术。为了抑制Th2反应的影响,我们有子组的患者相比,不受控制或控制哮喘。
我们研究的另一个观察是一个的存在改变了干扰素反应不受控制的哮喘病人的鼻腔上皮;这种性格可能更直接关系到一个内在上皮易感性。干扰素反应是减少不受控制的哮喘组相对于控制哮喘和健康组。我们排除了这些效应是由病毒感染引起的可能性:1)病毒PCR鉴定,能够检测呼吸道病毒感染的90%,排除病毒感染病例;和2)仔细评估CXCL10转录水平“感染”确定额外的感染患者样本。
isg在控制哮喘患者减少代表四分之一的第二个监督发现的基因分析。出乎意料,我们确定了GSDML在这个集群。我们的研究报告几个额外的观测表明直接关联这个基因的异常影响儿科哮喘上皮:首先,几个响应元素IFN监管因素的存在在其启动子区域;其次,其转录诱导上皮HNECs干扰素;第三,它在气道上皮细胞蛋白表达。这是符合这一事实的单核苷酸多态性(rs7216389)与哮喘的早期发病,严重急性发作(80%的病毒诱导的儿童)和哮喘严重程度(11,35,36]。米offatt等。(37]最初注意到儿童哮喘风险的协会与修改后的表达ORDML3位于附近的GSDML。变异的识别在接头地点GSDML在强大的连锁不平衡ORMDL3最近建议GSDML将致病基因与哮喘相关(38]。
IFN-α水平下降,IFN-β,IFN-λ1 IFN-λ2/3平行IFN-stimulated下调的基因控制的哮喘患者中观察到。这证实了和扩展研究德B地方政府投资公司et al。(39]显示相关性哮喘症状和干扰素反应在一群28儿童难治性哮喘。在他们的研究中,低水平的IFN-γ与持久性相关症状(39]。上皮细胞不足IFN-βIFN-λ生产期间rhinovirus-induced哮喘发作与病毒载量增加,有缺陷的细胞凋亡和细胞死亡的偏见2]。流行病学研究哮喘的发病与IFN-γ生产减少了外周血单核细胞在9个月的年龄,而IFN-γ正常化生产观察显示分辨率的儿童哮喘症状(40,41]。
不管具体的分子机制导致受损干扰素生产,从我们的研究结果,可以预测一些好处之一在不受控制的哮喘患者,干扰素治疗是最近提出的在体外实验IFN-β[42]。有缺陷的上皮细胞干扰素通路之间的关系和哮喘控制的缺乏的病人可能是特定于儿科哮喘,仔细评估治疗的选择基于先天免疫的发展需要组织临床试验解决这个特定问题在儿科人口。最后,我们的工作展示了一些特异性的严重儿科哮喘,这不仅源于T-cell-mediated偏见的适应性反应的发展,但也从一个低效率的上皮先天免疫。
确认
我们承认好sophia antipolis功能基因组学平台的技术专长(法国)。作者还要感谢,优秀的技术援助,美国Farion (d 'Anatomopathologie楚不错,服务,医院l 'Archet 2, Nice)细胞学分析,n . Treillet和诉Foussard (CHU不错,服务d 'Explorations Fonctionnelles Pediatriques, Hopitaux Pediatriques de CHU-LENVAL不错,Nice)对肺量测定法测量,和f·阿古里亚·(Sophia Antipolis不错,科学研究所及大学研究所de Pharmacologie Moleculaire Cellulaire, 6097年UMR Sophia Antipolis,法国),协助数据的准备。
脚注
可以从本文的补充材料www.www.qdcxjkg.com
支持声明
CNRS提供的研究支持,楚de不错,协会Vaincre la Mucoviscidose ADPHUN, anr - 09 -基因族群- 039、农场和SP2A拨款(阿斯特拉捷利康SP2A)。
临床试验
这项研究被注册为www.clinicaltrials.gov标识号NCT00569361。
感兴趣的语句
一份声明中对研究本身可以发现www.www.qdcxjkg.com/site/misc/statements.xhtml
- 收到了2011年4月26日。
- 接受2011年9月15日。
- ©2012人队