摘要
VEGFR2在血管稳态稳定中起着关键和特殊的作用,VEGFR2突变为扰乱血管系统直接参与多种肺部疾病提供了坚实的临床证据http://bit.ly/383ixTb
越来越多的认识到血管介入肺部疾病超出了经典的肺血管医学的范围。例如,有报道描述了COPD的血管表型,或提出了肺气肿消失的肺毛细血管综合征[1,2]。虽然支持肺部疾病血管假说的临床和流行病学研究数量在稳步增长,但临床研究的生物学基础仍有待提供。
在这个问题上欧洲呼吸杂志Eyry等。(3.在建立血管稳定性和肺部疾病之间的联系方面迈出了前所未有的一步。分析血管内皮生长因子受体2 (VEGFR2 / KDR基因肺动脉高血压患者(PAH),他们两个指数报告病例来自两个不同的家庭,和证明的杂合突变VEGFR2 / KDR基因cosegregate肺气肿的临床特征和较低的扩散能力的肺一氧化碳(DLCO)在几乎所有的携带者中,而在一些患者中观察到间质性疾病和严重的肺动脉高压。由于在这些家族中观察到的突变被预测对VEGFR2的蛋白功能有害,本研究提供了血管稳定性和人类多种肺部疾病之间的因果关系。
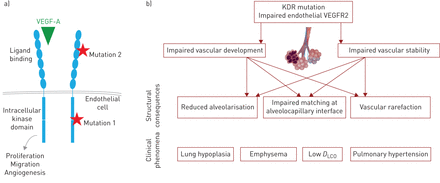
VEGFR2是一种跨膜受体,可将细胞外信号转化为细胞行为的改变(图1一个)。其在血管中的主要配体是血管内皮生长因子- a (VEGF-A),而淋巴细胞的VEGFR2也可能结合VEGF-C,一种淋巴特异性生长因子[4,5]。小鼠模型中VEGFR2 (KDR)的基因敲除在第8-9天会由于血管生成和血管生成受损而导致胚胎死亡[6,7,表明VEGFR2在血管发育中至关重要。在肺中,VEGFR2是粗壮的,几乎只在血管内皮中表达,这两种情况都发生在发育过程中[8]和成人的肺[4]。由于在胚胎发育早期具有致命性,目前尚不清楚VEGFR2基因敲除如何影响肺发育。然而,一般认为VEGFR2对肺的发育,特别是肺泡-毛细血管界面的发育是至关重要的。出芽肺泡分泌的VEGF-A与血管生成内皮细胞的VEGFR2结合,使出芽血管跟随肺泡芽,在发育中的肺中实现灌注与通气匹配[9,10]。此阶段药物抑制血管生成(VEGFR2抑制剂)可减少肺泡形成[11]。虽然有证据表明,VEGFR2在肺的非内皮细胞中低表达,如II型肺泡上皮细胞和造血祖细胞[4,8,12,由于缺乏条件敲除研究,目前尚不清楚VEGFR2在这些细胞类型中的功能。
a)配体血管内皮生长因子(VEGF)-A与内皮细胞上的VEGF受体2 (VEGFR2)结合,导致受体同源二聚和激活。这导致了细胞内增殖、迁移和血管生成的信号。Eyry等。(3.]位于家族1的胞内酪氨酸激酶结构域,以及家族2的胞外配体结合位点。预计这两种突变都会严重损害受体的功能。b) VEGFR2功能和信号传导对血管的发育和维持至关重要。当VEGFR2表达在肺血管内皮减少,肺泡化减少,肺泡乳头界面受损和血管损失发生。这导致了许多临床表型,包括肺气肿、一氧化碳肺弥散能力低(DLCO)和肺动脉高压。
采用条件基因敲除或慢性药物抑制对成人肺进行的动物研究表明,血管VEGFR2对于肺的维持和修复是必需的。与体质敲除相比,成年时条件敲除内皮细胞VEGFR2不是致命的,除非受到挑战,否则不会携带表型[13,14]。然而,这些小鼠在全肺切除术后再生肺泡形成严重受损[13,提示内皮细胞VEGFR2协调肺组织再生。慢性给药VEGFR2抑制剂SU5416可导致大鼠肺泡间隔细胞凋亡、肺泡增生减少、气道增大和肺气肿[12]。重要的是,在这个大鼠模型中,肺气肿是通过修剪肺血管树来平行的,将肺气肿与血管不稳定联系起来[12]。这些动物数据表明,内皮细胞VEGFR2在肺实质的发育、维持和恢复中发挥了关键作用,尽管其临床意义仍有待确定。
在VEGFR2生物学的这一背景下,Eyry等。(3.形成了将两个指数家族中VEGFR2表达自然发生的变异与临床肺部现象联系起来的最后一块拼图。鉴于肺血管的维持和稳定严重依赖VEGFR2,本研究提供了破坏血管稳定性的临床证据本身(VEGFR2单倍不足)可导致多种肺部疾病,包括肺动脉高压、肺气肿和间质性疾病(图1 b)。除此之外,E的研究yry等。(3.在几个层面上对呼吸研究具有重要意义。首先,它为正在进行的关于VEGF/VEGFR信号在肺动脉高压中的作用的争论提供了有力的证据,这一争论围绕着一个自相矛盾的发现而发展,即VEGF- a和VEGF受体据报道在一侧肺动脉高压丛状病变中上调[15,16,阻断VEGF-A [17]或VEGFR2 [18,19结果产生多环芳烃。Eyry等。(3.为后者提供了证据,表明VEGFR2单倍体不足参与了PAH,表明VEGF-A和受体的上调是继发性事件,或者是通过负反馈,或者是通过局部受体重排。其次,这些观察结果加强了使用Sugen/hypoxia大鼠模型作为肺动脉高压动物模型的理论基础。本研究除了总结了毛细管前PAH的重要形态学特征,包括丛状病变,还表明Sugen/hypoxia模型概括了毛细管前PAH的病理生理机制,即。减少VEGFR2表达式。第三,本研究为COPD/肺气肿的血管假说提供了机制支持[20.]。虽然观察性研究报道COPD/肺气肿早期发生肺血管重构[1,潜在的机制仍未完全被了解。基础研究表明,吸烟会降低内皮细胞VEGFR2表达[21, VEGFR2突变的强共分离与低DLCO观察到Eyry等。(3.七家运营商中有六家患有a型肝炎DLCO<65%)关闭循环,认为血管完整性的丧失是COPD/肺气肿的重要原因。
话虽如此,仍有太多的不确定性,不能称之为结束的篇章。在未来的研究中,有许多未回答的问题需要澄清。第一个问题是,这两个家族中描述的突变是如何影响VEGFR2功能的。描述的突变包括截断外显子的突变24,影响细胞内激酶结构域(家庭1),和一个突变在内含子的剪接供体7中,导致跳过外显子7和蛋白质截断(家庭2)。两种突变预计将严重影响翻译的功能产品,通过配体结合受损或废除了细胞内信号(图1一个)。然而,由于VEGFR2经历了同型二聚[4,仍有待确定截断的产物是否会影响二聚作用,从而产生除单倍体不足外的有害影响。其次,考虑到这些突变的遗传性质以及VEGFR2在胚胎发育和成人肺血管维持中的关键作用,观察到的现象是否源于产前和产后发育受损是一个有趣的问题与体内平衡受损和修复(脆弱性)。虽然这个问题适用于所有描述的现象,但它可能对肺动脉高压特别有兴趣,在7个突变携带者中只有3个被观察到。这种相对较低的外显率可能意味着需要第二次命中,因此指向增加的脆弱性,而不是发展问题。最后,鉴于在指数患者中观察到广泛的临床现象(肺动脉高压,低DLCO目前尚不清楚这种类型的肺动脉高压应被分为I组还是III组肺动脉高压。特别的是,由于cos隔离的KDR突变与低DLCO(七分之六)似乎比肺动脉高压(七分之三)更完整。间质性疾病的进一步特征,如。通过组织学检查,可在此提供答案。
总的来说,E的工作yry等。(3.证实VEGFR2/KDR是与遗传性肺动脉高压相关的新基因。更重要的是,鉴于VEGFR2在血管稳态稳定中的关键和特殊作用,它提供了强有力的临床证据,表明紊乱的血管系统直接参与了多种肺部疾病。
可共享的PDF
脚注
利益冲突:L. Botros没有什么可透露的。
利益冲突:A. Vonk Noordegraaf没有什么可透露的。
利益冲突:J. Aman没有什么可透露的。
- 收到了2020年2月14日。
- 接受2020年2月15日。
- 版权©2020人队