摘要
体重和脂肪分布可能与慢性阻塞性肺病风险有关。有限的前瞻性证据表明慢性阻塞性肺病与腹部肥胖有关。在一项前瞻性队列研究中,我们调查了体重指数(BMI)和腹部肥胖与COPD风险的关系。
中国Kadoorie Biobank招募了来自中国10个地区的30-79岁的参与者。在2004 - 2008年期间在基线调查中客观地测量了人体测量指数。排除普遍存在的COPD和主要慢性病的参与者后,包括452个259名参与者并随访,直到2016年底。我们使用COX模型来估计与COPD住院或死亡风险有肥胖的调整后危险比。
在平均10.1年的随访中,报告了10739例COPD住院事件和死亡。受试者相比,与正常体重指数(18.5 < 24.0公斤·m−2)、体重过轻(BMI <18.5 kg·m−2)个人的风险增加了COPD,调整后危险比1.78(95%CI 1.66-1.89)。超重(BMI 24.0- <28.0 kg·m−2)肥胖(BMI≥28.0kg·m−2)与腰围调整后的风险增加无关。调整BMI后,较高的腰围(男性≥85 cm,女性≥80 cm)与COPD风险呈正相关。此外,腰臀比和腰高比与COPD风险呈正相关。
腹部肥胖和体重过轻是中国成人慢性阻塞性肺病的危险因素。COPD的预防应同时考虑BMI和腹部肥胖的测量。
摘要
腹部肥胖和体重过轻是中国成人慢性阻塞性肺病的危险因素。COPD的预防应同时考虑BMI和腹部肥胖的测量。http://bit.ly/36To4fk
介绍
慢性阻塞性肺病是全球性的健康问题,每年造成约300万人死亡[1].在中国,COPD的普遍率估计成年人为20年的成年人8.6%,相当于9990万普遍案例[2].如此沉重的疾病负担是一个很好的关注。识别和修改风险因素对于控制COPD的流行病至关重要。
肥胖是一系列慢性疾病的既定风险因素。保持适当的体重一直被认为是健康生活方式的重要组成部分[3.,但肥胖与慢性阻塞性肺病风险之间的关系尚不完全清楚。横断面研究的证据表明,体重指数(BMI)与COPD患病率呈负相关[2,4].然而,观察到的关系可能不是因果关系,因为慢性阻塞性肺病患者经常经历体重减轻,往往比健康人更瘦[5].前瞻性队列研究可以解决反向因果关系,但现有的前瞻性证据并不充分。除了使用BMI测量的一般肥胖,脂肪分布可能是COPD发展的一个重要因素。腹部脂肪组织参与了全身性炎症,与COPD的发病机制有关。美国的一项大型队列研究发现,肥胖,特别是以腰围衡量的腹部肥胖与慢性阻塞性肺病风险增加有关[6].不同种族的人在体型和组成上存在差异。一般来说,中国人的身体质量指数(BMI)比白种人低,体脂比例高[7].肥胖与慢性阻塞性肺病在中国人群中是否存在关联尚不清楚。
本研究的目的是在中国嘉多利生物银行(CKB)的一项基于人群的前瞻性队列研究中,研究普通肥胖和腹部肥胖与慢性阻塞性肺病住院或死亡风险的相关性。
方法
研究人群
CKB研究的详情已于先前述及[8,9].年龄在30-79岁的成年人来自中国10个地区,包括5个城市和5个农村地区(补充图S1).CKB的研究不是旨在代表中国人口,队列不是随机样本。然而,该研究选择了10个地理位置各种各样的地区,以代表中国疾病模式,生活方式和经济水平的主要区域差异。在每个行政单位中,确定并没有重大残疾的所有雄性和女性都被确定并邀请参加。参与率为30%。共有512个715名参与者完成了基线调查。确定0.5百万的样本量,确定可接受的统计能量,以检测常见慢性疾病的环境和遗传因素之间的复杂相互作用。CKB研究经受中国疾病控制和预防中心(北京,中国)和牛津大学牛津大学(英国牛津)的牛津热带研究伦理委员会批准。从所有参与者获得签署的知情同意书。
暴露和协变量的评估
经训练的人员按标准程序收集人体测量数据[10.]在2004年6月至2008年7月的基线调查中。在不穿鞋的情况下,用测距仪测量站立高度,最接近0.1厘米。使用tpf - 300gs身体成分分析仪(Tanita Inc.,东京,日本)测量不穿鞋但穿着轻便衣服的体重,最接近0.1公斤。衣服的重量是根据季节估计的,然后减去。用软带测量腰围和臀围至最接近0.1 cm。2008年,在一项重新调查中,对随机抽取的5%的参与者进行了人体测量的可靠性评估。身高(0.99)、体重(0.96)、腰围(0.84)和臀围(0.82)的相关系数较高。BMI的计算方法为体重(kg)除以身高(m)的平方2).腰部到臀部比和腰围高比分别作为臀周圆周和高度分别计算为腰围。
在基线调查中,通过访谈者发放的问卷收集了协变量信息,包括社会人口学因素(年龄、性别、婚姻状况、最高教育程度)、生活方式(吸烟、被动吸烟、饮酒、体育活动、饮食、家庭空气污染)和病史(呼吸道症状、哮喘,肺结核)。被动吸烟的评估方法是询问参与者是否与吸烟者住在同一屋檐下以及接触时间长短。通过室内做饭和取暖使用固体燃料来评估家庭空气污染。一份由12种主要食物组成的食物频率问卷被用来评估饮食。通过计算代谢当量任务小时(MET-h)来评估日常体育活动水平。支气管扩张器前1秒用力呼气量(FEV)1)和强迫肺活量(FVC)由训练有素的技术人员按照建议的程序进行测量[11].
评估结果
随访至COPD(国际疾病分类-10 J41-J44)发病、死亡、随访失败日期或2016年12月31日(以先到者为准)。生死状况和死亡原因是通过官方的居住记录和死亡证明获得的。此外,还通过与国家健康保险系统的电子链接收集了关于COPD发病率的信息,该系统最近在所有研究区域建立,包含了详细的住院信息。来自健康保险数据库的事件病例是住院事件,不包括在门诊环境中作出的诊断。参与者可能因COPD加重、严重呼吸道症状或合并症而住院并接受COPD诊断。98%的队列参与者与健康保险数据库建立了联系。每年对未能与当地健康保险数据库建立联系的参与者进行积极的跟踪。在积极随访中,采访者询问参与者在过去一年中是否接受过医生的COPD诊断。小于1%(4875)的参与者在随访中丢失。为了评估CKB研究中COPD诊断的有效性,我们随机选取1069例患者进行评估。 A diagnosis of COPD was confirmed in 85% of reported cases [12].
统计分析
我们排除了被医生诊断为慢性支气管炎或肺气肿的参与者(n=13 288),或被定义为FEV的气流阻塞的参与者1/FVC比率<0.7 (n=27 483)。此外,我们排除了流行癌症(n=2578)、冠心病(n=15 472)、哮喘(n=2806)或结核病(n=7659)的参与者,因为这些疾病可能导致显著的体重变化。另外两名参与者因为缺少BMI而被排除在外。最后,452 259名参与者被纳入本研究。
根据《中国成年人超重和肥胖防治指南》,以BMI为基础,采用分界点定义一般肥胖[13,14].参与者被分为四组:体重过轻(<18.5 kg·m)−2),正常(18.5 - <24.0 kg·m−2)、超重(24.0 - <28.0 kg·m−2)和肥胖(≥28.0 kg·m−2).腹部肥胖是通过腰围、腰臀比和腰高比来评估的,根据之前推荐的分界点[13,15].此外,我们在肥胖测量分布的第5、35、65和95个百分位上使用四节限制性三次样条来检验非线性关系。
以年龄为时间尺度,采用Cox回归模型计算肥胖指标与COPD住院或死亡风险之间的危险比(HRs)和95%置信区间,并按地区和5岁出生队列联合分层。在多变量Cox模型中对潜在混杂因素进行了调整:性别、教育、婚姻状况、吸烟状况、被动吸烟、烹饪和取暖燃料类型、饮酒、身体活动(MET-h·day)−1)、红肉、新鲜水果和蔬菜的摄入频率,以及呼吸道症状。这些协变量是基于先验知识选择的,包括社会人口学变量、COPD已确定的危险因素和可能影响体重的健康相关生活方式。我们使用Schoenfeld残差来检查所有模型的比例危害假设,并没有发现违反。
我们检查了由基线特征定义的不同亚组之间的关联:性别(男、女)、地区(城市、农村)、年龄(<50岁、50 - 59岁、≥60岁)、教育程度(小学及以下、初中/高中、大学及以上)、吸烟状况(非吸烟者、目前吸烟者)、更年期(否、是)和体育活动(按性别划分的三组)。关节分析的一般和腹部肥胖措施进行。我们进行了以下敏感性分析以检验我们的结果的稳健性:排除了随访前3年患COPD的参与者;把分析限制在不吸烟者身上;使用正常下限(LLN)定义排除基线时气流阻塞的参与者;并排除基线糖尿病患者。所有分析均使用Stata(版本14.0;StataCorp, College Station, TX, USA)。显著性水平设为0.05。
结果
452 259人中,男性182 209人(40.3%),农村255 031人(56.4%)。均值±sd基线年龄为51.1±10.4岁。总体均值±sdBMI为23.7±3.3 kg·m−2,3.9%不体重,超重33.5%和10.5%肥胖。总体均值±sd腰围80.3±9.6 cm,腹部肥胖者41.9%(男性腰围≥85 cm;女性≥80厘米)。BMI较高的参与者更有可能是城市居民,每天食用新鲜水果、蔬菜和红肉,目前吸烟的可能性较小(p<0.001)。与BMI正常的参与者相比,BMI较低或较高的参与者更有可能是年龄较大、女性、缺乏运动和基线时有呼吸道症状(p<0.001)。由腰围、腰臀比和腰高比(表1和补充表S1).
一般肥胖和慢性阻塞性肺病
在中位随访10.1年(四分位范围2.2-11.1年)中,我们记录了10739例COPD住院事件和死亡。COPD住院或死亡的总发病率为2.40 / 1000人年。体重指数<18.5 kg·m的个体−2有较高的发病率(7.08 / 1000人年)。校正主要协变量后,与BMI正常的参与者相比,体重不足和肥胖参与者的HRs (95% CI)分别为1.75(1.64-1.86)和1.10(1.02-1.19)。在进一步调整腰围后,肥胖与COPD之间的相关性消失,而体重过轻仍是一个具有统计学意义的危险因素,HR (95% CI)为1.78(1.66-1.89)。
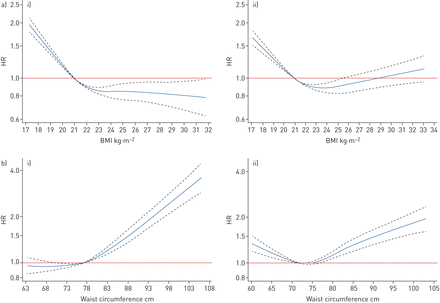
我们观察到BMI和COPD之间的相关性在性别上有所不同(交互作用的p值<0.001),分层结果显示在表2.BMI与男性COPD风险呈负相关。超重和肥胖似乎是保护因素,调整HRs (95% CI)分别为0.84(0.77-0.90)和0.76(0.65-0.90)。女性的负相关弱于男性,女性肥胖与COPD之间没有统计学意义的关联。此外,我们使用限制性三次样条来研究BMI和COPD之间的非线性关系。在男性中,慢性阻塞性肺病风险随BMI升高而降低,当BMI为23 kg·m时趋于平稳−2.女性患COPD的风险在BMI ~ 23-24 kg·m时最低−2, BMI >24 kg·m−2似乎与慢性阻塞性肺病风险增加相关(图1).BMI与COPD风险之间的关联被基线年龄、面积、吸烟状况和体力活动水平(补充表S2).
a)体重指数(BMI)和b)腰围与i)男性和ii)女性COPD风险的关系。在Cox模型中,BMI或腰围被作为限制三次样条项纳入,在第5、35、65和95个百分位上使用4个节。协变量调整基于模型3。参考BMI为21 kg·m−2.男性参考腰围为77厘米,女性为72厘米。非线性的p值均<0.0001。
腹部肥胖和慢性阻塞性肺病
总体而言,最低腰围组的参与者因慢性阻塞性肺病住院或死亡的粗发病率最高(4.78 / 1000人年)。校正协变量和BMI后,腹部肥胖与慢性阻塞性肺病相关,且风险随腰围增大而增加。最高腰围组的调整HR (95% CI)(男性≥95 cm;正常组(男性腰围70 ~ <85 cm)为1.57 (1.43 ~ 1.73);女性身高65 - 80厘米)(表3).男性和女性腹部肥胖与慢性阻塞性肺病呈正相关趋势相似,而低腰围与慢性阻塞性肺病的关联仅限于女性。基于样条项模型,男性腰围与COPD呈正相关,腰围<75 cm者风险最低。在女性中,腰围与慢性阻塞性肺病呈u型关系,腰围~ 72 ~ 75厘米的发病率最低。图1).腰围与慢性阻塞性肺病风险之间的关系被基线年龄、面积和体力活动水平(补充表S3).当使用腰臀比和腰高比作为腹部肥胖的测量值时,观察到一致的结果(补充表S4).
全身和腹部肥胖的关节分析
腰围和BMI类别在COPD风险方面没有显著的交互作用(交互作用的p值为0.703)。在每个BMI类别中,COPD的风险随腰围增加而增加。超重的低腰围参与者(男性小于85厘米;<80 cm的女性患COPD的风险最低(HR 0.87, 95% CI 0.80-0.95) (表4).腰高比也与COPD呈正相关,BMI分类间无显著异质性(交互作用p值0.462)。腰臀比与COPD的关系在BMI分类中并不一致(交互作用的p值为0.017),在体重过轻组中观察到负趋势。
敏感性分析
在敏感性分析中,主要结果基本保持不变,排除了随访前3年患COPD的参与者(n=1849),排除了基线时患糖尿病的参与者(n=28 214),或使用LLN定义的气流阻塞。在从不吸烟者中(n=284 259),体重过轻组的HR (95% CI)降低到1.64(1.48-1.81)。当仅限于从不吸烟的人进行分析时,腹部肥胖测量的风险估计并没有显著改变(补充表S5).
讨论
在这项随访10年的以人群为基础的队列研究中,腰围定义的腹部肥胖与中国成年人COPD住院或死亡的高风险相关。这种关联与BMI定义的一般肥胖无关。此外,腰臀比和腰高比与COPD风险呈正相关。体重指数低(<18.5 kg·m)−2超重(BMI 24.0 ~ <28.0 kg·m)是COPD的显著危险因素−2)肥胖(BMI≥28.0kg·m−2)在腰围调整后,似乎没有增加COPD风险。在男性中,超重或肥胖与较低的慢性阻塞性肺病风险相关。
与一般肥胖相比,腹部肥胖(反映脂肪分布)可能与慢性阻塞性肺病风险更相关。腰围是流行病学研究中广泛使用的腹部肥胖测量方法。许多研究发现,高腰围与肺功能下降有关[16- - - - - -19].在国立卫生 - 美国退休人员(NIH-AARP)饮食和健康研究中,腰围显示出与BMI调整后COPD风险的正相关[6].在我国人群中也观察到类似的结果。此外,我们评估了BMI和腰围对慢性阻塞性肺病住院或死亡风险的联合影响,没有发现有统计学意义的相互作用。在BMI分类中,高腰围始终与更高的风险相关。腰围较低的超重人群患慢性阻塞性肺病的风险最低,因为他们有较高的肌肉质量和较低的腹部脂肪质量。此外,本研究发现腹部肥胖的其他指标,包括腰臀比和腰高比与COPD呈正相关。腹部肥胖与慢性阻塞性肺病的关系可能与炎症有关。众所周知,炎症在慢性阻塞性肺病中起着至关重要的作用。脂肪组织是一种活跃的内分泌器官,是促炎介质的来源。炎症介质的增加可能吸引炎症细胞并放大炎症过程,导致小气道的结构改变[20.].在我们的研究中,在不吸烟者中,慢性阻塞性肺病的风险随着腰围的增大而增加,这表明腹部肥胖可能是不吸烟者的一个重要风险因素。无论是否吸烟,都应建议减少腹部肥胖以预防慢性阻塞性肺病。
既往文献一致表明BMI较低的参与者肺功能较低,患慢性阻塞性肺病的风险较高[21- - - - - -23].与之前的数据一致,我们的前瞻性研究发现,体重过轻的人患慢性阻塞性肺病的风险增加。在敏感性分析中,我们排除了前3年随访中的事件病例,以解决反向因果关系。我们还限制了对从不吸烟者的分析,因为吸烟可能是较低的BMI和较高的COPD风险之间的混淆因素[24].可能的解释包括营养不良、对呼吸道感染抵抗力差和体重过轻者肌肉无力[25- - - - - -27].体重过轻者患慢性阻塞性肺病的风险增加可能与肌少症有关,肌少症在慢性阻塞性肺病患者中经常出现[28].
现有的研究结果一般肥胖与慢性阻塞性肺病之间的关系有些不一致。一项荟萃分析发现,肥胖成年人的肺功能指标下降[29].然而,高BMI似乎没有增加COPD风险[4,21].最近在中国进行的一项大型横断面研究[2],与健康体重(BMI 18.5 ~ 24.9 kg·m)相比−2)、超重和肥胖(BMI≥25 kg·m−2)与COPD患病率降低25%相关(OR 0.75, 95% CI 0.62-0.92)。在我们的分析中,超重(BMI 24.0 - <28.0)或肥胖(BMI≥28.0 kg·m−2)在调节腰围后,还显示出在雄性后的保护因素。要正确地解释这一结果,了解我们统计模型的含义非常重要。当保持腹部肥胖常数时,BMI主要反映瘦体重而不是脂肪[30.].骨骼肌,瘦身组织的主要部分,与肺功能呈正相关[27].因此,超重组的风险较低可能是由于肌肉发达的保护作用。类似地,先前的研究表明,超重和肥胖的慢性阻塞性肺病患者的死亡率较低,称为“肥胖悖论”[31].在进一步阐明其作用机制时,可考虑肌质量因素。我们还观察到,只有在体力活动水平较高的人群中,超重与COPD风险显著降低相关,这表明这种保护作用可能与体力活动有关。锻炼和增加肌肉量可能有助于预防慢性阻塞性肺病。
据我们所知,这是中国首个调查全身性肥胖和腹部肥胖与COPD住院或死亡风险关系的大型队列研究。在基线研究中客观测量了各种人体测量指标,使我们能够评估全身性肥胖和腹部肥胖对COPD的独立影响。我们的主要优势包括前瞻性的设计,大样本量和严格的质量控制过程。在数据分析中,我们努力减少反向因果关系和吸烟混淆的偏倚。敏感性分析结果表明我们的主要发现是可靠的。
本研究有局限性。第一个是结果错误分类。在随访期间的所有参与者上没有进行肺活量测定,通过健康保险数据库和死亡证书确定COPD病例。COPD经常在中国下降[32],而在肥胖人群中诊断不足可能更为严重[33].这种错误的分类会导致低估肥胖个体的相对风险。另一个令人担忧的问题是肺活量测定在慢性阻塞性肺病患者中的应用较低(13.9%)[12].同样,在最近一项具有全国代表性的调查中,只有12.0%的COPD患者报告此前进行过肺功能检测[2].然而,在我们的研究中,大多数COPD诊断(85%)得到了不同来源的证据支持,包括呼吸道症状、危险因素和放射检查[12].其次,尽管排除了有特定既往疾病或随访前3年发展为COPD的参与者,但由于亚临床条件,反向因果关系仍不能完全消除。第三,许多协变量是自我报告的,可能存在测量误差。然而,重要混杂因素的测量,如吸烟显示良好的重现性。
总之,腹部肥胖是独立于一般肥胖的COPD风险预测因子。对于任何BMI水平的人来说,如果这种关联被证实是因果关系,保持推荐腰围将有助于预防慢性阻塞性肺病。体重指数低(<18.5 kg·m)−2)也是慢性阻塞性肺病的一个重要危险因素。因此,保持健康的BMI (18.5-24 kg·m)−2)和避免腹部肥胖都应考虑到体重管理,以降低未来COPD的风险。我们的数据为确定中国人的最佳BMI和腰围分界点提供了有用的信息。
补充材料
可共享的PDF
确认
最重要的是要感谢研究的参与者和10个区域中心调查小组的成员,以及位于北京、牛津和10个区域中心的项目开发和管理团队。
脚注
本文有一篇社论评论:https://doi.org/13993003.00107-2020
本文提供了补充材料www.qdcxjkg.com
利益冲突:J. Li没有什么可披露的。
利益冲突:L. Zhu没有什么可披露的。
利益冲突:魏玉玲没有什么可透露的。
利益冲突:吕杰没有什么可披露的。
利益冲突:郭敬明没有什么可披露的。
利益冲突:Z. Bian没有什么可披露的。
利益冲突:H. DU没有什么可披露的。
利益冲突:杨立没有什么可透露的。
利益冲突:陈宇没有什么可透露的。
利益冲突:周永明没有什么可披露的。
利益冲突:R. Gao没有什么可披露的。
利益冲突:J. Chen没有什么可透露的。
利益冲突:陈Z.没有什么可透露的。
利益冲突:曹文轩没有什么可披露的。
利益冲突:C. Yu没有什么可披露的。
利益冲突:李没有什么可透露的。
基金资助:国家重点研发计划项目(no . 2016YFC1303904, no . 2016YFC0900500, no . 2016YFC0900501, no . 2016YFC0900504)资助长白基线调查及第一次重新调查均获嘉道理慈善基金资助。英国威康信托基金资助项目(212946/Z/18/Z, 202922/Z/16/Z, 104085/Z/14/Z, 088158/Z/09/Z),国家自然科学基金资助项目(91846303,91843302,81390540,81390541,81390544),科技部资助项目(2011BAI09B01)。资助方在研究设计、数据收集、数据分析和解释、报告的撰写或提交文章发表的决定中没有作用。本文的资金信息已存入Crossref资助者注册表.
- 已收到2019年9月25日。
- 接受2019年12月20日。
- 版权©2020人队
这个版本是在知识共享署名非商业许可4.0的条款下发布的。