抽象
在囊性纤维化和血管内皮生长因子,可能会出现支气管周的血管生成(VEGF)-A调节血管生成中的气道。
使用免疫细胞化学和形态测定分析中在10名囊性纤维化患者在移植获得肺切片支气管周围血管和VEGF-A的表达进行了检查与对照组为不吸烟者,两种cftr缺陷小鼠与野生型小鼠交配。采用囊性纤维化跨膜传导调节剂(CFTR)抑制剂(CFTR-inh)治疗人气道上皮NCI-H292细胞和原代培养的非囊性纤维化细胞172或用CFTR小干扰(si)RNA转染,无论是否有选择性的表皮生长因子受体酪氨酸激酶抑制剂。ELISA检测VEGF-A和磷酸化的表皮生长因子受体的浓度。
支气管周围血管在囊性纤维化患者有所增加,但不Cftr公司有缺陷的老鼠。VEGF-A免疫染色定位于气道上皮,囊性纤维化患者和in患者的VEGF-A免疫染色增加Cftr公司有缺陷的老鼠。在培养的气道上皮细胞中,使用CFTR抑制剂或使用CFTR siRNA转染可使VEGF-A产量增加两倍。CFTR抑制剂触发表皮生长因子受体磷酸化,这是合成VEGF-A所必需的。
囊性纤维化在移植气道显示增加支气管周围血管和上皮VEGF-A表达。CFTR功能障碍引发VEGF-A的合成的上皮,这可能有助于血管重塑。
抽象
CFTR功能障碍可触发上皮合成VEGF-A,这可能有助于血管重构http://ow.ly/p7ebY
介绍
囊性纤维化(CF)是一种遗传性疾病,是由囊性纤维化跨膜电导调节因子(CFTR)基因1]。CFTR蛋白功能异常导致异常离子转运跨越气道上皮细胞[2],逐渐导致慢性肺病[1,3.]。CF肺疾病的特征在于气道结构异常,其包括具有粘液堵塞,皮下纤维化支气管扩张,重塑的气道上皮细胞和粘膜下腺,以及气道平滑肌的增生[4- - - - - -6]。
支气管循环具有增殖日益被认为是慢性气道疾病[一个重要组成部分的能力和支气管周围的血管生成(新血管从现有血管的增殖)7,8]。在支气管周围血管异常可能导致免疫反应通过微血管渗漏和炎性细胞的募集[9,10]。增加支气管周围血管据报道,哮喘和慢性阻塞性肺疾病[7,8]。然而,据我们所知,支气管周围血管尚未在CF病理研究审查。
血管内皮生长因子(VEGF)-A是一个关键的血管生成在呼吸道介体[8]。Baluket al。(11]已经表明,在小鼠气道上皮VEGF-A的选择性表达触发气管血管生成。在CF患者以前的研究报告中增加血清VEGF-A浓度[12- - - - - -14],但知之甚少在CF气道VEGF-A表达。Krennet al。(15在肺移植患者肺匀浆中发现VEGF-A mRNA和蛋白水平升高。相比之下,米注视者et al。(13]研究发现在成年CF患者的支气管肺泡灌洗液VEGF-A的水平没有增加。因此,表达模式和VEGF-A的在气道CF细胞定位有待确定。
在本研究中,我们检测了来自CF受试者肺组织切片的支气管周围血管分布和VEGF-A免疫染色与控制非吸烟者和两种不同菌株的肺部Cftr公司缺陷小鼠与野生型的同胞。因为在CF和in中,气道上皮是VEGF-A表达的主要部位Cftr公司-缺陷小鼠,我们研究了CFTR功能障碍对培养的气道上皮细胞中VEGF-A合成的影响。
方法
人和小鼠组织
外围人肺组织(含有noncartilaginous气道)在移植10周不吸烟的成人的CF和10个经历肺切除术对周围型肺癌不吸烟的对照获得。在网上补充表S1提供了这些患者的临床特点。肺组织样品固定在由充气浸10%中性缓冲的福尔马林中并包埋在石蜡中。减少与CF患者形态异常的不规则分布的潜在的采样偏压,从两个到四个块(取决于组织的可用性),其位置随机选择获得的组织。在对照组中,只有一个块是可供研究。
Cftr公司m1UNC(Cftr公司- / -)小鼠,通过基因打靶建立[16)和它们的野生同窝(Cftr公司+ / +)是从分布中心、分类动物和档案动物(法国奥尔良)获得的。Cftr公司tm1Eur(F508▽/▽)的老鼠17]和它们的野生型同窝出生仔畜(F508重量/重量)老鼠是B.scholet(荷兰鹿特丹伊拉斯谟大学)的一种礼物。断奶后,所有小鼠在饮用水中都被提供商业渗透性泻药(Movicol;Norgine,Harefield,UK),以防止肠阻塞。处死8~10周龄小鼠,用4%福尔马林固定肺,石蜡包埋。每组对5至7只动物进行研究。这项研究符合赫尔辛基宣言和地方人类和动物研究委员会的所有规则。所有患者均获得知情同意。
免疫组化染色和定量形态分析
物对5-微米石蜡包埋的切片进行免疫组织化学染色,如先前描述的18]。以下主要抗体:多克隆抗体对VEGF-A(A 20,1:200; Santa Cruz Biotechnology公司公司,Santa Cruz公司,CA,USA);多克隆抗体的内皮细胞标记物血管性血友病因子(vWF,1:50; DakoCytomation公司,Carpinteria的,CA,USA)来识别血管。抗原揭露孵育用蛋白酶从链霉菌属将(0.01%; Sigma-Aldrich公司有限公司,吉林汉姆,UK)中的溶液需要20分钟以提高染色的vWF的质量。生物素化的抗 - 兔抗体(1:200; Vector Laboratories公司,Burlingame的,CA,USA)被用于次级抗体,和结合的抗体,根据标准方法用于抗生物素蛋白 - 生物素 - 过氧化物酶复合物方法(精英ABC试剂盒可视化; Vector Laboratories公司,彼得伯勒,英国)。组织切片用苏木精复染。初级抗体和具有免疫球蛋白无关孵育省略用作阴性对照。
VEGF-A上皮免疫染色的支气管周围血管的和定量通过点计数进行的,如先前所描述[4,18,19]。VEGF-A阳性染色细胞在上皮细胞中所占体积按上皮细胞体积表达。支气管周血管量定义为vwf阳性血管在支气管周空间(上皮基底膜与肺泡附着物基底之间的空间)每体积支气管周空间所占的体积。所有分析都是在至少20个随机选择的高倍镜(400×)显微照片上进行的,这些照片是在每个病人或每只小鼠的2至4个远端切片上获得的。
人呼吸道上皮细胞的培养
表达功能性CFTR的NCI-H292人气道上皮细胞[20],并产生VEGF-A [18],10岁时被镀5细胞·毫升−1在24孔板(BD猎鹰;BD生物科学,美国加州圣何塞),并在含有10%胎牛血清(FCS)、青霉素(100 U·mL)的RPMI 1640培养基中生长−1),链霉素(100μg·mL−1)和HEPES(25毫摩尔)在37℃下在潮湿的5%二氧化碳的水套培养箱。
HAECs原代培养来自5例接受鼻息肉手术的非cf患者,如前所述[21]。将细胞以10镀6细胞·好−1在插入物(12 mm;Transwell,Costar,Cambridge,MA,USA)中,使用直径为12 mm的IV型胶原涂层(Sigma-Aldrich)聚碳酸酯微孔膜,并与含有2%Ultroser G(Gibco BRL,Life Technologies,Gaithersberg,MD,USA)的1 mL DMEM/F12/抗生素孵育。细胞在气液界面培养3周,此时细胞与纤毛细胞和粘液细胞完全分化[22]。以前的研究已经表明,这些细胞:1)产生VEGF-A蛋白与在培养的第一周生产的峰,和此后产量下降,直到培养21天[21]。和2)具有在培养的第一周没有CFTR表达和功能,但培养2周[后表达功能性CFTR23]。因此,使用CFTR抑制剂(见下文)的研究在培养第21天进行。
CFTR抑制HAECs
用选择性CFTR抑制剂(CFTR-inh)处理气道上皮细胞,可抑制CFTR介导的离子转运172或PPQ-102;Calbiochem公司,英国诺丁汉)24,25),据报可使通道稳定在封闭状态。总之,NCI-H292细胞在60-80%融合后,分别用CFTR-inh处理172(10−5M)或PPQ-102(10−5M)用二甲基亚砜(DMSO)稀释,或单独用DMSO (Sigma)稀释72小时。抑制剂的暴露时间和浓度是根据以前的文献选择的[24- - - - - -26]。在初步实验中,我们发现,CFTR抑制剂诱导的VEGF-A合成时,细胞血清饥饿(无FCS)培养的最后48小时期间,并且当细胞FCS(数据未示出)的存在下进行培养;所有后续实验在含FCS的培养基中进行。因为HAECs通过滴加培养基的150微升在空气 - 液体界面培养,因为CFTR是在上皮细胞的顶侧表示,治疗物在基底外侧级别应用两者(在培养基中),并在顶电平在细胞表面上[26]。文化传媒日新月异。使用CFTR抑制剂或DMSO孵育72小时后,收集细胞培养基并在-80℃保存。采用ELISA法测定24小时内VEGF-A产生的相应浓度(见下文)。
CFTR敲低表达的是通过转染NCI-H292细胞与特定CFTR小干扰(si)的RNA(Sigma)中获得的,并且非靶向siRNA用作阴性对照[27]。Transfections使用TransIT-siQUEST1进行,根据制造商的说明(Mirus, Madison, WI, USA) [27]。正如我们报道组在以前的手稿[27]中,CFTR的siRNA导致CFTR表达60-70%击倒,通过Western印迹检查作为(数据未显示)。转染后24小时,将细胞用新鲜培养基冲洗三次,并温育收获培养基之前另外24小时其储存在-80℃。
在所选实验,上皮细胞温育24小时与选择性表皮生长因子受体(EGFR)抑制剂(AG1478,10−5M;Calbiochem公司)或它的无效类似物(AG9,10−5M;Calbiochem) [28]。为了评估CFTR抑制对EGFR活化的影响,NCI-H292细胞用CFTR-inh处理172或单独15分钟,1个小时,3小时,6小时,8小时和24小时的DMSO。在每个时间点,将细胞在10由增溶的细胞获得的无菌磷酸盐缓冲盐水和细胞裂解物洗涤两次7细胞·毫升−1在裂解缓冲液(1%NP-40的替代(Santa Cruz Biotechnology公司,海德堡,德国),20毫摩尔Tris,在pH 8.0,137mM的氯化钠,10%甘油,2mM EDTA的,1mM的活化的原钒酸钠,10微克·毫升−1抑肽酶和10μg·mL−1亮肽素)。样品在-80℃下坐在冰上保存前15分钟。
VEGF-A的测量值和磷酸化EGFR蛋白质浓度
细胞培养上清液中的VEGF-A和细胞裂解液中磷酸化的EGFR (EGFR- p)按照制造商的说明用夹心ELISA试剂盒进行测定(DuoSet IC;研发系统,明尼阿波利斯,明尼苏达州,美国)。EGFR-P结果表示为pg的EGFR-Pμg总蛋白质。细胞裂解液中的蛋白浓度使用基于双肌球蛋白酸的蛋白检测试剂盒(Pierce, Rockford, IL, USA)测定。每个样品都是一式两份测量的。
定量PCR检测VEGF mRNA
总RNA使用RNeasy微型试剂盒(Qiagen,德国希尔登)NCI-H292细胞中提取。用于以下VEGF-A的定量PCR(qPCR)扩增,并使用7900HT快速实时PCR系统(应用生物系统;生命技术有限公司,佩斯利,UK)β肌动蛋白表达逆转录1μg的总RNA。qPCR的引物作为VEGF-A:5'-AGGGCAGAATCATCACGAAGT-3'(正向),5'-AGGGTCTCGATTGGATGGCA-3'(反向),和作为β肌动蛋白:5'-GCAAACGTGCGTGACAT-3'(正向),5'-TCGCGACAGGTCTTTGC-3'(反向)。基因表达的相对定量使用ΔΔCT方法计算和结果表示为倍数增加与在每个时间点相应的对照相比。
统计分析
从形态学分析获得的数据表示为%,并使用非参数Mann-Whitney U-检验和斯皮尔曼等级相关进行分析。进行形态测量变化的观察者间系数分别为<15%。从细胞培养物实验中获得的数据被表示为平均值±扫描电镜至少有三个独立的实验进行了重复和分析使用单因素方差分析的重复测量,其次是事后学生 - 纽曼-Keuls检验进行多重比较。使用Prism 5软件(GraphPad软件公司,圣地亚哥,CA,USA)进行所有的分析。p值≤0.05被认为具有统计学意义。
结果
支气管周围血管和VEGF-A在人类和小鼠呼吸道免疫
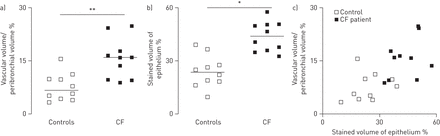
对照组不吸烟者支气管周围间隙较薄,免疫组化vWF检测可见稀疏的支气管周围血管。在CF受试者中,支气管周围空间明显增厚,并含有大量血管。形态计量学分析显示,CF气道支气管周围血管增加2倍(p<0.01)(图。1A)。所有对照组和CF组的肺切片VEGF-A免疫染色均为阳性。VEGF-A的染色主要局限于气道上皮,在纤毛细胞中可见,而在杯状细胞中不可见。在CF气道中,巨噬细胞中也有VEGF-A染色,但中性粒细胞中没有(未显示)。形态学分析显示,CF组气道上皮VEGF-A染色明显增加(p<0.05) (图。1B)。当分组对照和CF个体,上皮VEGF-A-染色体积密度和支气管周围血管容积密度之间的强相关性被发现(R = 0.65; P <0.05)(图。1C). 然而,当将分析局限于CF受试者时,这种相关性并不显著(r=0.45;p=0.19)。
对照组(n=10)和囊性纤维化(n=10)受试者气道中的支气管周围血管和血管内皮生长因子(VEGF)免疫染色的形态计量学分析。对气道切片进行血管内皮标志物血管性血友病因子(von Willebrand factor,以识别血管)或血管内皮生长因子A(VEGF-A)的免疫染色。采用点计数法进行形态计量分析(见方法部分)。a) 显示支气管周围血管,定义为支气管周围空间中血管所占的体积(血管体积)/支气管周围空间的体积(百分比)。b) 显示VEGF-A阳性的上皮体积百分比。c) 显示血管体积/支气管周围体积(以百分比表示),VEGF-a阳性的上皮体积(以百分比表示)。用非参数Spearman秩相关分析上皮VEGF-A与支气管周围血管的相关性。在同时考虑对照组和CF组时,这种相关性非常显著(r=0.65;p<0.05),但仅考虑CF组时不显著(r=0.45;p=0.19)。横条表示中间带。*:p<0.05;**:p<0.01。
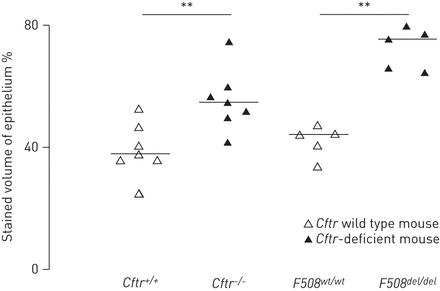
在Cftr公司- / -和F508▽/▽小鼠和野生型小鼠,免疫染色VEGF-A也被定位于气道上皮细胞。形态分析显示增加VEGF-A-染色的上皮Cftr公司- / -和F508▽/▽与各自的野生型幼鼠比较(图2). 比较时,支气管周围的血管没有发现差异Cftr公司缺陷型和野生型小鼠(数据未显示)。
在气道上皮细胞的血管内皮生长因子(VEGF)-A免疫染色的形态测定分析囊性纤维化跨膜电导调节器(Cftr公司)缺陷和野生型小鼠。在获得了气道段Cftr公司m1UNC(Cftr公司- / -)小鼠和野生型(Cftr公司+ / +)同窝小鼠(左),和在Cftr公司tm1Eur(F508▽/▽)和他们的野生型(F508重量/重量)同窝(右)。切片进行免疫染色VEGF-A和如在方法部分中的描述进行形态测定分析。单杠代表中位数。** P <0.01。
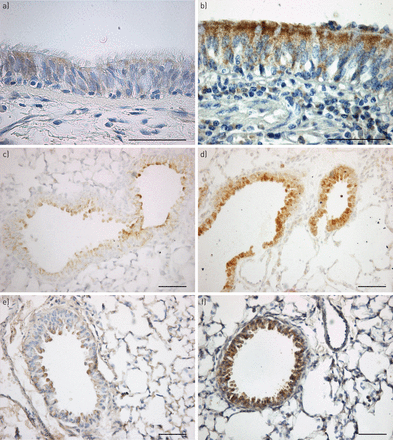
在人类和小鼠的免疫染色VEGF-A的代表性显微照片显示在图3。在人类受试者的vWF免疫染色的代表性显微照片在网上补充图S1呈现。
的血管内皮生长因子(VEGF)-A的免疫染色在人类和小鼠中气道代表性显微照片。在a)中的人类对照患者获得的气道部与B)囊性纤维化(CF)的患者,在c)中囊性纤维化跨膜电导调节器(Cftr公司)+ / +与d)Cftr公司- / -老鼠和在e)F508重量/重量与f)F508▽/▽老鼠。切片用VEGF-A抗体(棕色)染色,苏木素染色。对照组和对照组Cftr公司+ / +和F508重量/重量在小鼠中,只有稀疏染色的VEGF-A在上皮细胞中存在。在CF患者和两者中Cftr公司- / -和F508▽/▽小鼠中,对于VEGF-A广泛染色存在于上皮。显微照片是在代表10和控制,并在10名CF患者获得的结果的,在七个Cftr公司+ / +和Cftr公司- / -老鼠,五只F508重量/重量和F508▽/▽老鼠。比例尺=50μm以下。
在培养的人气道上皮NCI-H292细胞上的VEGF-A的合成CFTR抑制的效果
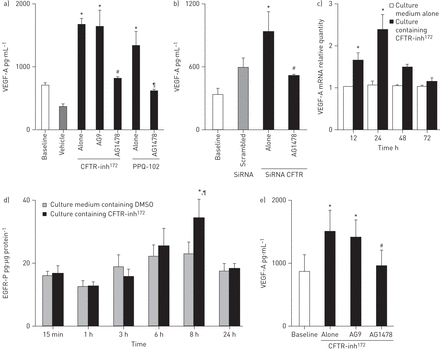
短路电流的测量证实,NCI-H292细胞具有将其通过选择性CFTR抑制剂所抑制的氯离子转运,CFTR-INH172或PPQ-102(见在线补充)图2)。NCI-H292细胞的治疗CFTR-INH172(10−5M)或PPQ-102(10−5M)诱导VEGF-A合成增加2倍(p<0.05)与基线)(图。4A)。类似地,NCI-H292细胞与特定的CFTR的siRNA转染增加VEGF-A合成(P <0.05与基线)(图。4B]),而具有非定标siRNA转染无影响。
囊性纤维化跨膜传导调节因子(CFTR)抑制气道上皮细胞血管新生生长因子(VEGF)-A合成及表皮生长因子受体(EGFR)活化的作用。a)选择性CFTR抑制剂对NCI-H292细胞中VEGF-A合成的影响:细胞单独在培养基(基线)、含有二甲基亚砜的培养基(vehicle)或含有选择性CFTR抑制剂的培养基(CFTR-inh)中培养172或PPQ-102;10−5M). ELISA法测定VEGF-A浓度(见方法部分)。在一些实验中,细胞用选择性EGFR酪氨酸激酶抑制剂AG1478 (10−5M)或具有其无效类似物AG9(10−5M)。结果以均数±表示扫描电镜以双份N≥3独立的实验。*:P <0.05与基线;#:P <0.05与CFTR-inh172单独;¶:P <0.05与ppq - 102。b) CFTR小干扰RNA (si)转染对NCI-H292细胞VEGF-A合成的影响。细胞单独在细胞培养液中培养(基线),培养基中转染非靶向(搅乱)siRNA或培养基中转染特定的CFTR siRNA(见方法部分)。结果以均数±表示扫描电镜一式两份N≥3独立的实验。*:P <0.05与基线;#:P <0.05与CFTR的siRNA孤单。c)中CFTR-INH的效果172NCI-H292细胞中VEGF-A mRNA的表达。细胞单独在培养基(基线)或含CFTR-inh的培养基中培养172(10−5M)。VEGF表达是使用定量PCR量化和报告的相对量。中n = 3个重复独立实验。*:P <0.05,与在每个时间点基线进行比较。d)CFTR-INH的效果172NCI-H292细胞EGFR磷酸化的研究。NCI-H292细胞在含有二甲基亚砜(DMSO)的培养基或含CFTR-inh的培养基中培养172(10−5M).收集不同时间点的细胞裂解液,采用ELISA法测定磷酸化EGFR (EGFR- p)浓度(见方法部分)。结果以均数±表示扫描电镜从一式两份N≥3独立的实验。*:P <0.05与8小时DMSO;¶:P <0.01与CFTR-inh172e) CFTR-inh的作用172人气道上皮细胞(HAECs)气液界面原代培养中VEGF-A的合成。培养第21天,HAECs单独在培养基(基线)或含CFTR-inh的培养基中培养172(10−5M) 72小时内,结果以平均值±扫描电镜表示,来自5个重复的独立实验。*:p<0.05与基线;#:P <0.05与CFTR-inh172单独。
为了检查CFTR抑制对VEGF-A的合成的效果是否与转录作用,我们使用qPCR检测VEGF-A mRNA表达。NCI-H292细胞的治疗CFTR-INH172(10−5M)诱导的增加的VEGF-A的mRNA在12小时,在24小时达到峰值,然后下降(见图。4C)。
CFTR抑制NCI-H292细胞中EGFR磷酸化在VEGF-A合成中的作用
因为EGFR磷酸化是VEGF-A合成所必需的,而VEGF-A的合成是由气道上皮细胞的各种刺激所诱导的[18,29],我们研究了其在VEGF-A的合成由CFTR抑制诱导作用。NCI-H292细胞的治疗CFTR-INH172在8小时诱导的EGFR磷酸化一个显著增加(p <0.05与车辆,p < 0.05与CFTR-inh172在15分钟时)(图。4D)。NCI-H292细胞用AG1478的预处理(10−5男,防止VEGF-A的合成由CFTR化学抑制剂或通过CFTR的siRNA诱导的(对的EGFR酪氨酸激酶)的选择性抑制剂<0.05与基线)(图。图4a和b)。NCI-H292细胞与AG9的预处理(10−5男,AG1478的无活性类似物)则没有任何效果。
讨论
我们发现,气道上皮细胞中VEGF-A的在移植获得的CF患者的肺的免疫染色的主要部位,并在该CF VEGF-A的表达增加,与对照受试者相比。免疫染色VEGF-A也被用在气道上皮细胞中与CFTR功能障碍两种不同小鼠品系增加。在培养的气道上皮细胞中,CFTR的抑制(使用化学抑制剂或siRNA)导致增加的VEGF-A的合成,其需要EGFR活化。这些数据表明,在CF患者的气道上皮细胞是CFTR功能障碍有助于VEGF-A上调。他们出现在CF气道的支气管周围血管重构进一步表明上皮VEGF-A的作用。
我们首次报道了VEGF-A在CF气道上皮细胞中的表达增加。米cCOLLEYet al。(12报道稳定的CF患者血清VEGF-A水平升高与与非CF肺部疾病的受试者,但VEGF-A水平气道隔室没有测定。米注视者et al。(13]测定VEGF-A的相似浓度在9 CF和16年龄匹配的健康志愿者的支气管肺泡灌洗液。由于VEGF-A被降解在体外由CF支气管肺泡灌洗液,其中含有高弹性蛋白酶的活性,这些作者未能获得在CF患者肺生产VEGF-A的[一个明确的结论13]。Krennet al。(15与不吸烟者获得的肺相比]发现增加VEGF mRNA和蛋白质在CF患者在移植肺匀浆。我们的数据证实了这些后者的调查结果和通过显示气道上皮细胞是VEGF-A表达的CF肺部的主要部位扩大这些数据。
我们的结论是,CFTR功能障碍触发VEGF-A合成是基于培养的气道上皮细胞的数据。此前,V二黑河et al。(三十]报道与控制人类胎儿细胞系相比,携带纯合突变F508del人胎细胞系增加VEGF-A的合成。后面的这些数据提供了用于在VEGF-A的生产CFTR功能障碍的作用的间接证据;然而,这两种细胞系之间的差异可能是无关的CFTR功能障碍[31]。在本研究中,使用CFTR通道功能的抑制的化学抑制剂,或使用CFTR的siRNA在非CF细胞系和非CF HAECs提供了直接的证据表明,CFTR功能障碍引发VEGF-A的合成的CFTR拦截。在气道上皮细胞增加免疫染色VEGF-ACftr公司缺陷小鼠这一发现提供了进一步的证据。
该增加的VEGF-A表达的发现是不与增加的支气管周围血管相关联的Cftr公司缺陷小鼠有点令人吃惊。因为VEGF-A刺激的内皮细胞增殖和血管生成通过其对血管内皮生长因子受体2的效果(VEGFR2)32],我们研究了VEGFR2的小鼠肺中的表达。在野生型和Cftr公司缺陷型(包括Cftr公司- / -和F508▽/▽)小鼠,VEGFR2的免疫染色定位于气道上皮,但在支气管周围血管的内皮中缺失(见网上补充图S4)。相比之下,Baluket al。(11]发现VEGF-A过表达在气道上皮细胞,这导致采用气管的血管生成,与气管血管内皮VEGFR2的表达相关联。我们认为,缺乏内皮VEGFR2表达的可能占在没有增加血管的Cftr公司有缺陷的老鼠。
我们的研究力量依赖于使用互补的模型和信息来源,包括人类CF组织、小鼠模型和培养的HAECs。我们也认识到我们的方法的局限性。只有在分组对照和CF受试者时,上皮细胞中VEGF-A与支气管周围血管分布的相关性才显著。在CF患者中,支气管周围血管和上皮VEGF-A之间缺乏相关性,这可能与可获得的CF组织相对较少有关,也与移植时招募的这些患者的同质性有关。另外,上皮VEGF-A可能与CF患者的支气管周围血管生成无关,并可能发挥不同的作用(如。上皮增生(33])。接受移植的CF组比对照组更年轻。因为之前有一项关于肺功能正常的年轻成人中VEGF-A免疫染色的研究报道,在气道上皮中没有免疫染色[34],这种差异不会影响到我们的研究结果。的CFTR功能障碍的小鼠模型不再现典型的人类CF肺部疾病的结构异常[35]。因此,由于没有增加支气管周围血管Cftr公司缺陷小鼠应谨慎解释。然而,人们可能推测,除了CFTR功能障碍,其他因素诱导VEGF-A的表达,如细菌感染[18],可能是促进支气管周围血管生成所必需的。最后,CFTR抑制诱导VEGF-A mRNA和蛋白合成增加,提示有转录作用。然而,还需要进一步的研究来确定这种效应是否与mRNA合成或mRNA稳定有关。
我们的发现表明,CFTR功能障碍在气道上皮细胞中触发VEGF-A合成,与感染和炎症无关。然而,移植时CF气道上皮中VEGF-A表达的增加可能与多种因素有关:促炎性细胞因子(如。肿瘤坏死factor-αinterleukin-1β),从革兰氏阴性和革兰氏阳性细菌(微生物产品18,29]和病毒[29,以及缺氧[36也有报道称它能增加气道上皮细胞中VEGF-A的合成。
VEGF-A定位于纤毛细胞,可能是由于在纤毛细胞或纤毛细胞前体(如。基底细胞)。气道上皮EGFR活化的其他主要产物(如。粘蛋白和白细胞介素8)已经被定位于分泌细胞[4]。EGFR在气道上皮细胞亚群中的定位在文献中存在争议:Tynet al。(37报道EGFR在纤毛细胞中的选择性表达体内在培养的上皮细胞中,提示纤毛细胞转分化为粘蛋白产生细胞。另一些人发现EGFR在基底细胞和无规则分泌细胞中表达,但在纤毛细胞中没有表达[4,38]。有人建议,EGFR本地化是一个动态过程,可以在各种病理生理条件下变化。
CFTR-inh对CFTR功能的抑制作用172CFTR抑制后EGFR磷酸化,VEGF合成增加,需要气道上皮细胞EGFR活化。NCI-H292细胞的治疗CFTR-INH172导致分钟内的氯离子转运的抑制,证实用P以前的研究结果埃雷斯et al。(26],但EGFR磷酸化物在8小时增加。因为EGFR的活化通过它的配体(如。表皮生长因子(EGF)或转化生长因子α(transforming growth factor-α)通常在几秒钟内出现,这一数据表明CFTR-inh172不是EGFR配体,并建议在这些情况下EGFR的活化发生通过上皮细胞内的级联反应。导致EGFR活化的确切分子机制仍有待建立。
气道上皮细胞VEGF-A合成增加可促进血管生成[11,三十],增加血管通透性,促进炎性细胞的募集(如。以及呼吸道中的蛋白质。此外,支气管周围血管生成可能导致大量咯血的发生,这是CF患者的一种潜在的危及生命的并发症[39]。CF患者大量咯血通常通过支气管动脉栓塞治疗。在这些患者栓塞后观察到高复发率,可能与正在进行的支气管周围血管生成和炎症有关。反复栓塞不能控制的复发性咯血是CF患者肺移植的公认标准。我们认为直接针对血管生成的治疗可能对复发性咯血的CF患者有用,但在考虑将这种治疗用于人类之前还需要进一步的研究。
综上所述,移植时CF气道上皮中VEGF-A表达明显增加,提示其在CF患者支气管周围血管生成中发挥作用[11]。CFTR功能障碍直接导致气道上皮VEGF-A上调通过EGFR激活。疗法直接靶向CFTR功能障碍[40,41]可导致支气管周围和血管分布减少显著VEGF-A的合成。此外,生长因子(如。EGF和/或VEGF)受体拮抗剂可以代表用于降低气道CF血管重塑一个有前途的方式。
致谢
作者感谢苏菲丹尼尔 - 博凯尔(科钦医院,巴黎,法国),与免疫组化染色和克莱尔丹尼尔(比沙医院,巴黎,法国)提供人类组织CF帮助。
脚注
对于编辑评论见1438页。
这篇文章有提供补充材料www.www.qdcxjkg.com
支持声明:这项工作是由赠款资助的巴黎大学总理府(Legs Poix),协会Vaincre拉Mucoviscidose和协会CARDIF。
利益冲突:披露能够随本文的在线版本中找到www.www.qdcxjkg.com
- 收到2012年10月14日。
- 接受2013年3月5日。
- ©ERS 2013