摘要
严重儿童哮喘的病因尚不清楚。我们的目标是定义在患有严重的抗治疗和控制哮喘的儿童中的基因表达的全球模式。
白血细胞的分离和使用Affymetrix人类基因ST 1.0芯片重症,治疗抗性哮喘(N = 17),哮喘控制(N = 19)的儿童和健康对照全局转录分布进行了表征(N = 18)。在哮喘的成年人(N = 12)分离白细胞组分受体的表达进行了研究。
总的来说,1378个基因在患有严重/受控哮喘的儿童和对照组之间有差异表达。三个显著丰富的基因和基因组京都百科全书的途径:自然杀伤细胞介导的细胞毒性(上调控制哮喘);n -糖的生物合成(严重哮喘时降低);和苦味转导受体(TAS2R(在严重哮喘时上调)。定量PCR实验证实TAS2R■在严重的哮喘。TAS2R表达在成人哮喘患者的白细胞中被复制TAS2R激动剂还抑制LPS诱导的细胞因子释放。的表达之间的相关性显著TAS2R在成人和儿童中均发现了哮喘严重程度的s和临床标记物。
综上所述,在患有严重的难治性哮喘的儿童中观察到特异的基因表达模式。支气管扩张剂表达增加TAS2Rs提出了治疗哮喘的新目标。
介绍
哮喘是一种异质性疾病,影响到全球数百万的成年人和儿童。儿童哮喘的5%左右的慢性症状和/或严重恶化,尽管遭受了多种药物治疗,包括高剂量的吸入糖皮质激素[1]。“有问题的严重哮喘”一词已被提出用来对这些儿童进行分类,其中一个亚群患有严重的、难以治疗的哮喘,这可能需要新的治疗方法[2]。难治性儿童应与其他形式的“有问题的哮喘”儿童区分开来,这些“有问题的哮喘”由于不明的恶化因素、社会问题或依从性差而难以治疗。严重的治疗性儿童哮喘的原因仍然知之甚少。
哮喘是众所周知的在家庭中运行,研究还表明,有病情严重程度相当的遗传成分[3.]。到目前为止,有对儿童性治疗哮喘几个基因研究,很少有研究探讨了这一特征表型基因表达谱4]。重度哮喘,慢性炎症和呼吸道的随后的结构变化,肺功能和合并症[恶化的临床特征5- - - - - -7,表明参与这些过程的基因可能会引起特别的兴趣。利用基于基因组学的方法,包括在急性哮喘加重期和恢复期从儿童收集的血细胞中进行微阵列分析,基因表达模式已被确定,并突出了与前列腺素代谢和先天免疫等相关的通路[8]。
我们的主要目的是对广泛特征化的儿童白细胞进行全基因组表达阵列分析,这些儿童参与了一项全国性的问题性严重哮喘研究[5]。我们评估了17名对治疗有抵抗性的哮喘儿童、19名有控制的持续性哮喘患者和18名健康对照者的新鲜白细胞,我们的数据清楚地表明,在严重的、治疗有抵抗性的哮喘和有控制的持续性哮喘之间存在不同的基因表达模式。
发现了一种特殊的新途径来表征严重的抗治疗哮喘表型,即苦味受体信号。这一发现有点出乎意料,因为直到最近,人们还认为苦味受体(TAS2Rs)只存在于舌头上,它们被特定的配体激活,使我们能够感知苦味。然而,维eshpandeet al。(9表明这些受体存在于人的肺中,而且它们的刺激会导致支气管扩张。因此,当前研究的次要目的是对TAS2R在分离的血液白细胞中的表达和功能。为此,我们从另外12名哮喘患者身上采集了血液,我们的发现尤其丰富TAS2R表达于淋巴细胞上,并有抑制作用TAS2R促炎性介质释放的激动剂。我们也发现了它们之间的相关性TAS2R表达和临床特征,这表明该途径可能是严重哮喘一个重要的内源性保护机制。
方法
研究设计
本研究采用了两组不同的患者。全基因组表达阵列分析来自参与全国性疑难重症哮喘研究的儿童混合血液白细胞。5]。随后,上分离血液中的白细胞从附加12成人哮喘患者进行苦味受体的表达和功能的更详细的检查。
研究对象:儿童
瑞典全国性的问题性严重哮喘研究是一项多中心的观察性调查,将患有问题性严重哮喘的学龄儿童与患有受控的持续性哮喘的同龄儿童进行比较。所有患者在检查前的两周内均要求无呼吸道感染或哮喘加重。纳入准则载于表E1,而有关的详情则载于其他地方[5]。在符合问诊性严重哮喘定义的儿童中,我们根据详细的临床特征确定了对治疗有严重抗拒的儿童(称为严重哮喘)(根据全球哮喘倡议(GINA),尽管进行了4级治疗,但哮喘控制不足)[10]。本研究使用的样本集包括20名患有严重哮喘的儿童(ACT评分≤19分),20名患有受控哮喘的儿童(选自受控的持续性哮喘组,ACT评分20 - 24分)和19名来自瑞典斯德哥尔摩阿斯特丽德·林德格伦儿童医院的健康对照组。对照组接受选择性手术,如阴囊疝,并在计划手术前采集血样。所有参与研究的儿童和他们的父母均知情同意,该研究也得到了当地伦理委员会的批准。
一氧化氮,肺功能和支气管高反应性的评估
使用NIOX™分析仪器(Aerocrine AB, Solna,瑞典),呼出的一氧化氮的比例(FeNO的)在肺量测定前已按照国际准则进行了测定[13]。治疗短期和/或长效β2-激动剂和/或白三烯拮抗剂分别停用8、24和72小时,然后测量基线肺功能和用甲基胆碱激发。根据已发表的建议,使用Vitalograph®2120 (Vitalograph, Ennis, Ireland)进行肺量测定[14],并使用P报告的参考值olgar和W英格(15]。使用Spira星状喷雾器(Spira Respiratory Care Centre, Hameenlinna, Finland)评估了支气管对甲氧胆碱挑战的高反应性[16,结果以剂量-响应曲线的斜率(DRS .)表示乙酰甲胆碱)[17]。
血液分析
局部麻醉(EMLA乳膏;收集静脉血标本,阿斯利康,索德塔列耶,瑞典)。检测白细胞和IgE。特异反应被定义为特异性IgE >0.35kU·L−1吸入过敏原(Phadiatop®(Phadia AB,乌普萨拉,瑞典),混合猫,狗,马,桦木,提摩太,艾草,屋尘螨和枝孢过敏原)。然而,在健康对照组中并没有检测到特异反应,因为有特异反应病史是该组的排除标准。新鲜的白细胞从血液中分离出来,立即放入RNA中晚些时候®(Applied Biosystems/Ambion, Austin, TX, USA),并储存在-20°和-80°C,直到RNA提取。
RNA提取
根据制造商的说明,使用RiboPure™-Blood extraction kit (Applied Biosystems/Ambion)从白细胞(buffy coat)中提取总RNA。使用NanoDrop 8000 (Thermo Scientific, Wilmington, DE, USA)和Agilent 2100生物分析仪(Agilent, Santa Clara, CA, USA)对RNA的质量和数量进行了评估。
微阵列分析
使用Affymetrix人类基因ST 1.0芯片进行转录组分析(Affymetrix, Santa Clara, CA, USA)。该基因ST 1.0芯片包含28 875个基因/转录集,每个转录集的分辨率为26个(中位)探针。根据制造商的建议,进行了cDNA合成和杂交。使用标准Affymetrix基因表达方案(www.affymetrix.com)。实验数据使用统计软件R (www.R-project.org)及Bioconductor (www.bioconductor.org),然后从.cel文件中提取表达式值,并使用稳健的多阵列平均值(justRMA)进行归一化。至于数据正常化后的质素评估,则采用arrayQualityMetrics软件[18]。检测到的离群除去并将数据集再次标准化。进一步分析之前,滤除标准化控制基因。进行实施LIMMA包和hugene10sttranscriptcluster库数据分析和注释。
为了验证微阵列分析的结果,进行附加的定量(Q)PCR实验,以检查所有的表达TAS2R作者发现在学科组之间的差异表达。cDNA合成和qPCR为11市售的人TAS2Rs完全按照“针对苦味受体的qPCR”部分的描述进行。这些实验是在一组儿童中进行的:健康对照组(n=18)和患有严重治疗性哮喘的儿童(n=19),他们有足够的RNA。正态分布的数据用非配对t检验和偏态数据用Mann-Whitney u检验进行比较。
儿童临床特征的统计和芯片数据
双尾t检验或ANOVA被用于测试在重度哮喘,哮喘控制组和对照组,以及用于与偏态分布变量Wilcoxon秩和检验之间临床变量的差异(重度哮喘与控制哮喘)。分类变量(性别)的差异采用卡方检验。p值≤0.05为显著。我们将f -统计数据应用于微阵列数据,作为一项全球测试,以生成在三种对比中任何一种差异表达的基因列表:受控哮喘与健康对照组(哮喘控制组),严重哮喘与控制哮喘(重度哮喘哮喘控制)和重度哮喘与健康对照组(严重哮喘对照组)。使用默认的Benjamini-Hochberg方法纠正了多次检测,所有调整后的p值≤0.05的基因都被认为是显著的,产生了一个顶部表,表中有1378个基因在任何对比中有显著差异表达。慢化t统计揭示了每个对比对差异表达的整体检验的贡献。
聚类和功能富集分析
产生无监督层次聚类和热图执行使用由F-统计牵连所有1378个显著基因gplots包。功能注释和富集分析进行,以确定更多的基因比偶然预期是否从给定的生物学途径或过程。生物过程(BP_FAT)和途径(京都基因百科全书和基因组)使用DAVID 6.7(评估http://david.abcc.ncifcrf.gov)[19,20.]。benjamin - hochberg校正p值相对于Affymetrix人类基因ST 1.0背景值≤0.05时,富集被认为是显著的。基因表达资料库(www.ncbi.nlm.nih.gov项目/地理/)(登录号GSE27011)。
研究对象:成人
为了研究苦味感受器在分离的血液白细胞组分上的表达和功能,我们收集了另外12例成人间歇性过敏性哮喘患者的血液,他们的气道对甲氧胆碱的高反应性和对花粉或动物皮屑的皮肤针刺试验呈阳性。受试者特征如表E2所示。这些受试者是从瑞典斯德哥尔摩卡罗林斯卡大学医院呼吸内科和过敏科的门诊招募的,所有受试者都提供了参与研究的书面同意,并得到了当地伦理委员会的批准。
血液白细胞分离
将外周血静脉血收集到含肝素的吸尘器®管中(Beckton Dickinson, Franklin Lakes, Franklin Lakes, USA)。红细胞经右旋糖酐沉降后,淋巴球®(英国邓迪,Axis-Shield)密度梯度分离,分离出富含粒细胞的颗粒和外周血单核、富核的间期。中性粒细胞和单核细胞分别用CD16和CD14 MACS®microbeads (Miltenyi Biotech, BergischGladbach,德国)进行阳性选择,淋巴细胞按照制造商说明去除单核细胞后进行阴性选择。这些制剂的纯度为>的95%。
苦味受体的定量PCR检测
RNA的提取使用RNeasy®Mini kit (Qiagen, Hilden, Germany),根据制造商的说明,使用柱上脱氧核糖核酸酶消化。简而言之,新鲜细胞在供应的RLT裂解缓冲液中均质,并在-80℃保存,然后进行RNA提取协议。使用NanoDrop 8000评估RNA浓度和质量。cDNA合成使用定量逆转录试剂盒(Qiagen, Hamburg, Germany)根据制造商说明进行。qPCR使用ABI PRISM 7500序列检测系统(Applied Biosystems, Foster City, CA, USA)和TaqMan®试剂(Life Technologies/Invitrogen, Carlsbad, CA, USA)进行。11个商用TaqMan®引物TAS2RS(hTAS2R4,5,10,13,14,19,20,31,45,46和50)和管家基因甘油醛-3-磷酸脱氢酶(GAPDH)使用。作为阴性对照,PCR反应是在没有逆转录酶的情况下使用水或cDNA反应产物进行的。基因表达相对于GAPDH根据2计算−ΔCT公式。
TAS2R的影响激动剂对白细胞功能
为了检验的效果TAS2R激活对白细胞功能的影响TAS2R激动剂氯喹和地那铵用于一种标准化的试验,已知可增加血液白细胞释放促炎介质。简单地说,全血与100μg·毫升孵化−1脂多糖(LPS) 24 h,有或没有10,100年或1000年μM苦味受体激动剂或相关的车辆控制。在测量促炎细胞因子和前列腺素(PG)E之前,血浆被取出并储存在-80°C2。17种细胞因子的面板(白介素(IL)-1β,IL-2,IL-4,IL-5,IL-6,IL-7,IL-8,IL-10,IL-12,IL-13,IL-17A,粒细胞集落刺激因子(G-CSF),粒细胞/巨噬细胞集落刺激因子(GM-CSF),干扰素(IFN)-γ,单核细胞趋化蛋白(MCP)-1,巨噬细胞炎性蛋白1β和肿瘤坏死因子(TNF)-α)在血清中测定(稀释1:4),使用Bio-Plex的Pro™的17-plex的试剂盒用Luminex®分析仪(Bio-Rad实验室,赫拉克勒斯,CA,USA)。PGE2用酶免疫分析法(美国密歇根州安娜堡市开曼化学公司)测定其含量。
统计数据
显示的大部分数据集TAS2R根据Kolmogorov-Smirnov试验,分离的血液白细胞的表达呈正态分布,因此采用配对t检验进行比较。受体表达与临床特征的相关性采用Pearson检验。p值<0.05为差异有统计学意义。
结果
基因细分严重哮喘,哮喘控制和控制的识别
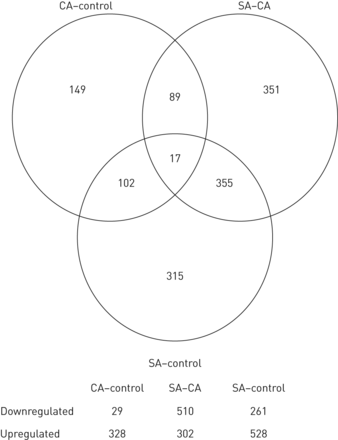
的59名受试者转录进行测定上的Affymetrix人类基因ST 1.0表达阵列。预处理和后杂交阵列的质量控制后,五个样品被视为离群值和除去。剩余的样本集17重度哮喘,19控制哮喘和18个健康对照的被用于下游分析。和F检验的线性建模方法中的应用统计鉴定的1378个转录簇/基因被显著差异在一个表达,或几个,受控哮喘控制的,重度哮喘哮喘控制或重度哮喘控制对比度的顶表(见表E3)。T-测试统计被应用到识别的反差造成了整体意义,图1说明了这种分布。从这1378个基因中,似乎有大量的基因可以将严重哮喘组与控制哮喘组(n=351个基因)和控制哮喘组(n=315个基因)区分开来,而将控制哮喘组与控制哮喘组(n=149个基因)区分开来的基因较少。在严重哮喘控制组和严重哮喘控制组之间也共享355个基因,这支持了一种观点,即与其他两组相比,严重哮喘的特征是一组独特的基因。
维恩图表示的差异表达的基因之间的儿童严重哮喘(SA)的分布,控制的哮喘(CA)和控制。在圆圈中的数字示出了唯一的基因差异表达或对比度之间共享的数目:CA与健康对照组(CA-control), SA与CA (SA - CA)和SA与健康对照组(SA-control)。每个对比中下调或上调基因的数量如下图所示。
三组的临床数据(重度哮喘,哮喘控制和控制)中呈现表1。在支气管高反应性方面,重症哮喘患者明显高于对照哮喘患者(DRS乙酰甲胆碱对照组年龄略小于重度哮喘组和控制型哮喘组。然而,用力呼气量在1 s (FEV)组中没有显著差异1)、白细胞总数、嗜酸性粒细胞、中性粒细胞、FeNO的、特异反应性或总IgE。ACT和吸入糖皮质激素均未进行统计学分析,其表达分析的纳入标准分别为分数或剂量的来源。
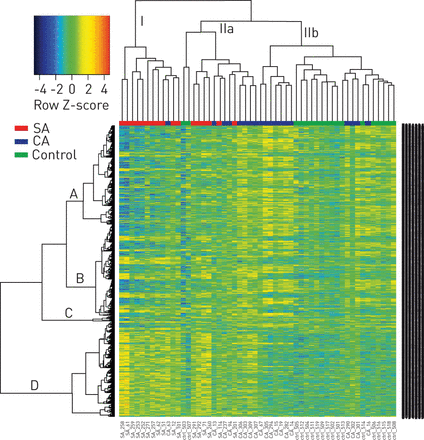
对1378个差异表达基因的标准化原始强度的无监督分级聚类和热图显示了对预先定义的严重哮喘、受控哮喘和对照组(图。2)。柱状树状图将大多数严重哮喘患者与控制的哮喘患者和控制的哮喘患者分开(分别为第一组和第二组),也将大多数控制的哮喘患者与严重哮喘患者和控制的哮喘患者分开(IIb中发现的两组对照组除外)。控制性哮喘患者在IIa和IIb中均有发现。
严重哮喘(SA)、控制哮喘(CA)和健康对照组儿童的全球基因表达模式。无监督层次聚类和heatmap分析了1378个差异表达基因中每个个体的表达模式(p≤0.05)。柱状树状图将受试者分为三个主要的簇(I、IIa和IIb)。行树图表示基因簇大致分为A、B、C、d四组。行z分数表示基因表达正常,其中黄红代表上调基因,蓝色代表下调基因。
哮喘的新途径和过程
利用DAVID数据库进行的途径富集分析使用了两种不同的方法。首先,使用顶部表中所有1378个差异表达基因,发现三个显著丰富的基因和基因组京都百科全书途径:味觉传导(主要在严重哮喘时上调);自然杀伤(NK)细胞介导的细胞毒性(哮喘控制组上调);和n -糖生物合成(在严重哮喘中下调)(表2)。其次,我们利用了由热图(图。2)。我们粗略地从行树图(A、B、C和D in)中分割出四个块图2),并对这些集群(表2)。Cluster A包含NK细胞介导的细胞毒性通路,但也揭示了两个额外的通路:t细胞受体信号通路和柠檬酸循环;所有这些在控制哮喘中都被上调。Cluster D包含苦味受体通路,在所有重症哮喘患者和部分对照哮喘患者中均上调,p值显著提高(从表1基因的0.03提高到4.2×10)-10)。
为了寻找其他功能丰富的分组,我们进行了基因本体富集分析。严重的哮喘与健康对照,味觉感官知觉是显著丰富。与代谢过程和免疫过程的其他显著生物过程进行了鉴定。有关完整列表,请参阅表E3。出的1378点差异表达的基因的总列表,转录物簇的15%被注释为已知的,或者在大多数情况下,新的非编码RNA(ncRNA的),主要是通过小核RNA,小核仁RNA,核糖体RNA,杂表示RNA和微小RNA(见表E4)。大多数非编码RNA的发现在重度哮喘中被上调相比哮喘控制或控制。
确认TAS2RqPCR在儿童中的表达
11种不同基因的mRNA表达TAS2R(4、5、10、13、14、19、20、31、45、46和50)通过qPCR在健康儿童和严重难治性哮喘儿童的混合血液白细胞样本中得到确认(图E1)。一般情况下,重症哮喘患儿的苦味受体表达水平高于健康对照组,差异有统计学意义TAS2R13(p = 0.028),TAS2R14(p = 0.009)TAS2R19(p = 0.037)。
哮喘相关基因的共表达
对我们的1378个差异表达基因列表我们比较的97个原确认的哮喘候选基因名单,通过精心复制的相关研究,或通过全基因组关联分析确定任[21]。在这两个列表中都有12个基因(表3)。大多数基因在单独控制哮喘时上调,但有三个例外:RORA基因,在严重哮喘和控制哮喘中均有上调PEX19和MYB,这在严重的哮喘患者显著下调孤单。功能注解揭示了没有共享的途径,但一些基因(RORA基因,TBX21,ADRB2,IL2RB,PDE4D,MYB和PAFAH2)参与了相同的生物学过程,如各种代谢过程的正向调节、细胞死亡的调节和白细胞活化。
相关的表达TAS2Rs在分离的血液白细胞中
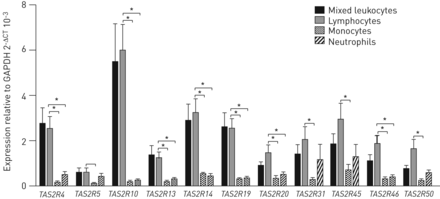
与GAPDH相关的11个商用人类苦味受体的mRNA在混合白细胞、淋巴细胞、中性粒细胞和单核细胞中的表达如表所示图3。所有的苦味觉受体的表达是显著最大的淋巴细胞群相比单核细胞。的表达TAS2R淋巴细胞也比中性粒细胞多,但是TAS2R50,TAS2R45,TAS2R31和TAS2R5这些差异没有达到统计学意义。在淋巴细胞中,的相对表达TAS2R10比另一个高吗TAS2R检查。的表达TAS2R5对混合血液中的白细胞显示出在这些受试者肺功能显著逆相关,二者FEV1%预测(p=0.011, Pearson相关系数= -0.83)和强迫肺活量% pred (p=0.029)。有趣的是,在哮喘患儿中,TAS2R5混合血白细胞mRNA表达(log)2TAS2R5Affymetrix人类基因ST 1.0芯片的表达也与支气管对乙酰胆碱的高反应性有统计学意义上的相关性,用剂量-反应曲线的斜率来测量(p=0.008, Pearson相关系数=0.47)。
人类苦味受体的表达(TAS2R)从成人哮喘患者中分离的白细胞中。的相对表达式TAS2R(4、5、10、13、14、19、20、31、45、46和50)与甘油醛3-磷酸酶脱氢酶(GAPDH)进行比较,采用定量PCR方法检测混合白细胞和分离淋巴细胞、单核细胞和中性粒细胞(n=12)。结果以均数±表示扫描电镜与表达水平不同TAS2R在不同的细胞群体小号采用t检验进行比较。CT:循环阈值。*:P <0.05。
TAS2R激动剂对LPS诱导的炎症介质的释放效应
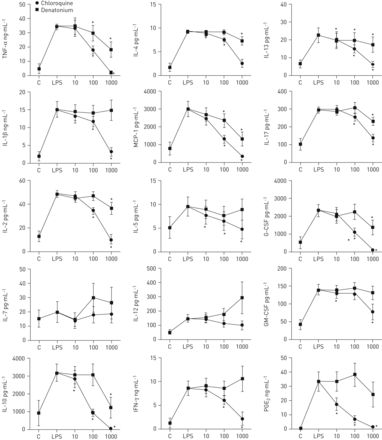
以考察其可能的作用TAS2R活化对血液白细胞功能、原型的影响TAS2R对LPS诱导的炎性介质释放激动剂氯喹和地那铵(10-1000μM)进行了研究。结果表明,氯喹和地那铵显著抑制TNF-α的释放,IL-13和MCP-1。氯喹也抑制IL-1β的释放,IL-2,IL-4,IL-5,IL-10,IL-17,G-CSF,GM-CSF,IFN-γ和PGE2以剂量依赖的方式(图。4)。
苦味受体(的影响TAS2R)对脂多糖(LPS)诱导的激动剂促炎症细胞因子和前列腺素(PG)电子2发布。从12名成人哮喘血液样品孵育24小时,未刺激(C)或用LPS(100微克刺激·毫升−1),在没有(LPS)或存在氯喹或denatoniumμM (10 - 1000)。17血清细胞因子(白介素(IL) 1β- 2、IL - 4, IL-5, IL - 6, IL-7,引发,IL - 10、IL - 12, IL-13, IL-17,肿瘤坏死因子(TNF) -α,粒细胞集落刺激因子(g - csf)、粒细胞/巨噬细胞集落刺激因子(gm - csf)、干扰素(IFN) -γ,单核细胞趋化蛋白1 (MCP)和巨噬细胞炎性蛋白(MIP) 1α)分析了luminex和铂族元素2通过酶免疫测定法。结果IL-6,IL-8和MIP-1α中没有示出,因为这些出席上面使用的测定法的检测极限水平。*:P <0.05,与单独的LPS。
讨论
利用全基因组表达序列分析了54例哮喘患者和健康对照者的转录组,我们发现在严重的难治性哮喘和控制良好的持续性哮喘之间存在基因表达的分离。传统的免疫相关功能,如t细胞受体信号和NK细胞介导的细胞毒性,在控制型哮喘患者中被发现上调,而在重症哮喘患者中却没有观察到这种模式。相反,我们看到了一个深刻的丰富和提高TAS2Rs,这强调了途径先前没有与严重治疗抗性哮喘相关。这些发现被我们的qPCR分析进一步加强,也呈现出上升TAS2R在这些主题中的表达。
在这项研究中,我们观察了整个白细胞的全基因组表达模式,目的是寻找独特的表达谱,从而将预定的患者群体分离开来。通过使用一种全局方法来识别在任何对比中差异表达的基因,我们能够识别出1378个显著(p≤0.05)改变的基因。所有样本中基因表达的无监督层次聚类和热图(图。2)分离了大部分的严重哮喘患者的(簇I)从控制哮喘患者和健康对照组(簇II)。虽然表达模式可以在患者组进行分类相当好,显而易见的是,其它生物和生理参数也促成了这些复杂的哮喘表型。
因此,我们观察到一个深刻的丰富和上调TAS2R这一途径在重症哮喘患者的白细胞中起重要作用,在heatmap树木图的聚类分析中变得更加重要。直到最近,TAS2Rs在哮喘中没有任何作用。然而,TAS2R目前已有四项独立研究将s与呼吸系统联系起来。年代嘿et al。(22)表明,TAS2R表达在人气道上皮细胞的活动纤毛上,苦味化合物增加细胞内钙离子的含量2 +浓度和刺激纤毛搏动频率。运动细胞负责将粘液和有害物质排出肺外,研究表明,病毒感染和吸烟会导致这些纤毛的损失,并可能破坏防御机制[23]。最近的数据表明,一个特定的TAS2R(38)涉及上呼吸道的固有免疫防御和变异在该基因有助于容易感染呼吸系统疾病的个体差异[24]。Deshpandeet al。(9]发现TAS2Rs在人气道平滑肌(ASM)中表达,苦味剂可引起离体ASM松弛和气道扩张。吸入苦味剂也能减少哮喘小鼠模型的气道阻塞。我们最近和扩展这些观察记录证实,苦味受体受体激动剂也诱发豚鼠气管的放松,他们也可能最大限度放松支气管收缩反应迟钝的β-agonists [25]。此外,我们目前发现的抑制作用有两种TAS2R白细胞功能激动剂提示苦味受体的激活可能也具有抗炎作用。综上所述,这些研究提示了一种保护作用TAS2R■在哮喘。我们的研究是首次报道的上调TAS2R在患有严重的难治性哮喘患者的白细胞中发现s。
为了更详细地检测哪些白细胞表达苦味受体,我们对11个白细胞进行了qPCRTAS2R在分离的淋巴细胞、单核细胞和中性粒细胞中,来自12个特征明确的成人哮喘患者。结果表明,所有苦味受体在淋巴细胞中的表达均以淋巴细胞部分的表达为主hTAS2R10似乎是表达得最丰富的。虽然hTAS2R10在不同的儿童组之间没有差异表达吗TAS2R10被认为是最有能力表达苦味受体之一在由d研究气道平滑肌eshpande等(9]。尽管这些研究结果涉及到不同的组的患者中,在特定的差异TAS2R对淋巴细胞表达可依据受控和严重哮喘患者之间观察到的差异,如TAS2R淋巴细胞的表达常与混合白细胞样本相似。在有控制和严重哮喘的儿童中观察到相似的白细胞计数(表1),观察到的TAS2R上调不太可能是由于白细胞数量的差异。到底是哪淋巴细胞亚群,与生物相关TAS2R在这些细胞上的表达,应该是未来研究的重点。我们最初的实验表明TAS2R激动剂氯喹和地那铵能够抑制几种促炎细胞因子的释放和血白细胞的二十烷样释放(图。4),表明这些药物可能具有抗炎和支气管扩张的特性;然而,还需要更详细的功能研究。然而,氯喹与地那溴铵的更广泛的活性谱证实了最近在气道平滑肌中的发现[25]。
途径分析还表明,T细胞相关的途径,如NK T细胞介导的细胞毒性,在控制哮喘被上调,而N-聚糖生物合成的重度哮喘组中下调。NK细胞在哮喘中的作用已经被讨论和研究都显示NK T细胞的哮喘患者[支气管肺泡灌洗液广阔上调26],以及没有增加在所有[27]。小鼠模型显示,缺乏NK t细胞的小鼠不会发展或出现由过敏原引起的气道高反应性受损,从而支持了NK t细胞在哮喘中的作用[28,29]。我们的研究结果指向NK t细胞在哮喘中的作用。n -聚糖生物合成途径负责生成与细胞膜上的蛋白质和脂质结合的聚糖。糖蛋白在细胞表面分布的改变被认为是导致许多慢性人类疾病的原因,包括自身免疫性[30.]。
识别,主要在重度哮喘的基因的大量,注释为ncRNA或新颖的ncRNA。最近的全基因组表达的研究表明,人类基因组中产生的这些法规,非蛋白编码RNA的成千上万,他们在几乎所有的发育过程中发挥作用,但主要是在转录和转录后调控[31]。随后,ncRNAs被发现与多种人类疾病有关,如癌症、中枢神经系统疾病和心血管疾病[31]。然而,ncRNA在哮喘,特别是难治性哮喘中的作用尚不清楚,仍是进一步研究的目标。
12出来的97公复制哮喘基因1378组差异表达的基因中,发现(表3)。因此,这些基因在DNA和RNA水平上与哮喘相关,这支持了它们在疾病发病机制中的作用。大多数基因仅在控制哮喘患者中上调(PEX19,RORA基因和MYB是例外)。这可能是由于大多数的关联研究,以及全基因组关联研究,都是在主要由轻度/中度哮喘患者组成的合并患者材料上进行的。
我们的研究有局限性。首先,我们测量了外周血细胞(主要是白细胞)的基因表达模式,这些细胞只是控制/严重哮喘的几个可能的靶细胞之一。然而,免疫系统是哮喘病因学的重要组成部分。其他一些研究测量了支气管肺泡灌洗或支气管活检获得的细胞的基因表达水平[32- - - - - -34]。这些研究的直接比较,因此很难作出;然而,结合数据在各种相关组织进行可能帮助我们绘画哮喘的更完整的画面。我们的途径分析是严格的,只知道探索的途径,这始终是一个限制因素。的差异表达的基因(P≤0.05,无论倍数变化的)一个自由夹杂物与所述功能注释的更严格的方法补偿。这是在试图提高功率,但减少误报完成。较大的研究规模会被优选的,但几乎60研究受试者是仍然用于全基因组表达分析一个相当大的数字。虽然遗传性过敏症的历史是为健康对照组的排除标准,我们不能完全排除一些控制孩子们的特异性IgE> 0.35 KU·L−1(因为这是未经测量的)。
综上所述,本研究为了解儿童重症难治性哮喘的特点提供了新的视角。值得注意的是,这种足够强大的全基因组转录组分析之所以成为可能,是因为它可以用于一组表型异常良好的哮喘患者。我们在哮喘对照研究中的数据支持已知通路的差异表达,如t细胞相关网络。然而,新的发现是,该研究揭示了以前在严重哮喘组中与哮喘无关的通路的特异性上调,例如n -糖的生物合成,尤其是苦味转导。支气管扩张型苦味受体表达的增加和这些受体介导的抗炎反应的初步迹象,肯定值得进一步探索其作为哮喘治疗新靶点的潜力。最后,使用氯喹治疗哮喘的有益治疗效果已被报道,这可能不仅仅是巧合[35]。
致谢
我们要感谢瑞典国家研究所有参与儿童重症哮喘和他们的父母,所有成年哮喘患者在临床哮喘和过敏研究实验室(卡罗林斯卡大学医院胡丁厄,瑞典斯德哥尔摩),生物信息学和表达分析Affymetrix公司的核心在NOVUM,斯德哥尔摩卡罗林斯卡研究所,和Ingegerd弗兰森(斯德哥尔摩卡罗林斯卡研究所,瑞典)的技术援助,以及工作人员在临床哮喘和过敏研究实验室和全球过敏和哮喘欧洲网络(GA设施2LEN)。
脚注
这篇文章有补充资料www.www.qdcxjkg.com
支持声明:这项工作得到了德国科隆医学院过敏研究中心的支持。c·马瑞医生的基础,共济会儿童基金会在斯德哥尔摩,瑞典哮喘和过敏协会研究基金会,儿科研究基金会的儿童医院,阿斯特德。林格伦的瑞典心肺基础,诺和诺德基金会,瑞典战略研究基金会,斯德哥尔摩郡议会研究基金(ALF) Vinnova (CIDaT) KI-AZ-TSC-JRP项目,赫尔辛基大学和瑞典医学研究委员会(VR-M)的研究基金。E. Melen是由Riksbankens Jubileumsfond资助的,这是Erik Ronnberg为研究儿童早期疾病而设立的奖学金。A. James和M. Kupczyk是卡洛林斯卡研究所伯纳德·奥舍尔严重哮喘研究项目的博士后研究员。
利益冲突:未申报。
- 收到2012年5月15日。
- 接受2012年11月13日。
- ©2013人队