摘要
背景自2015年以来,欧洲肺动脉高压指南建议大多数肺动脉高压(PAH)患者使用联合治疗。然而,目前尚不清楚这种治疗策略在临床实践中被采用的程度,以及它是否与提高长期生存有关。
方法我们分析了欧洲大型肺动脉高压注册中心COMPERA的数据,以评估2010年至2019年期间新诊断的PAH患者使用联合治疗和生存的时间趋势。对于生存分析,我们查看了2010-2014年和2015-2019年期间的年度数据和累积数据。
结果共纳入2531例患者。早期联合治疗(诊断后3个月内)的使用在2010年诊断为PAH的患者中从10.0%增加到2019年诊断为PAH的患者中的25.0%。确诊后1年接受联合治疗的患者比例由27.7%增加到46.3%。在比较2010-2014年和2015-2019年期间,1年生存估计相似(分别为89.0% (95% CI 87.2-90.9%)和90.8% (95% CI 89.3-92.4%)),而3年生存估计略有但不显著改善(分别为67.8% (95% CI 65.0-70.8%)和70.5% (95% CI 67.8-73.4%))。
结论2010年至2019年,联合治疗的使用有所增加,但大多数患者仍接受单一治疗。诊断后1年的生存率没有随时间变化。未来的研究需要确定所观察到的3年生存率提高的趋势是否可以得到证实。
摘要
在对2010-2019年多环芳烃治疗模式和生存期的时间趋势进行分析时,本研究发现,靶向联合治疗的使用有所增加,但诊断后3年的生存期只有轻微的、不显著的改善趋势https://bit.ly/3FExlK5
简介
术语肺动脉高压(PAH)描述了一种潜在致命的肺血管病变,其特征是肺血管阻力(PVR)进行性增加,可能导致右侧心衰。多环芳烃最常见的形式是特发性(IPAH),但也有遗传性(HPAH)和药物相关性(DPAH)形式,以及与各种疾病相关的疾病表现,如结缔组织病(CTD)、艾滋病毒感染、门脉(门肺)高血压和先天性心脏病(CHD) [1].
在靶向治疗可用之前,多环芳烃患者的前景是严峻的。1991年发表的一项美国登记研究发现,IPAH患者(当时称为原发性肺动脉高压)在诊断后的中位生存期为2.8年[2].在随后的30年里,人们开发了各种治疗方法,改善血流动力学、运动耐受性和无恶化生存[3.].PAH患者的预期寿命也有所增加,诊断后的中位生存期现已超过5年[4- - - - - -6].然而,对于目前批准的大多数疗法,在随机临床试验中没有证明对死亡率有影响(除了注射。在一项随机、开放标签研究中,在没有其他治疗方法可用的情况下,环氧前列醇可提高生存率)[7- - - - - -11].
多年来,随着越来越多的多环芳烃药物的出现,治疗策略也在不断发展。在2004年的欧洲肺动脉高压指南中,几乎所有患者和所有疾病阶段都推荐单药治疗,“可能会考虑”联合治疗作为最后的手段[12].在2009年欧洲肺动脉高压指南中,初始单药治疗仍然是大多数患者的推荐策略,对于世界卫生组织功能等级IV的患者,考虑初始联合治疗,如果单药治疗反应不足,则考虑顺序联合治疗[13].2015年,发表的AMBITION(氨布里森坦和他达拉非治疗肺动脉高血压患者)研究结果显示,与这些化合物的单一治疗相比,氨布里森坦(一种内皮素受体拮抗剂(ERA))和他达拉非(一种磷酸二酯酶-5抑制剂(PDE5i))的初始联合治疗在运动耐受性和疾病进展方面的治疗效果明显更好[8].与该领域的其他研究一样,AMBITION的设计不是为了检测,在研究结束时也没有显示出生存益处[8,11].尽管如此,2015年发布的修订后的欧洲肺动脉高压指南首次建议对大多数新诊断的PAH患者使用初始联合治疗[14,15].
在多环芳烃疗法发展的同时,患者表型也发生了变化,特别是在人口老龄化的国家。虽然这种疾病最初主要见于年轻、健康的女性,但如今多环芳烃的诊断主要见于年龄较大的男性和女性患者。在最近的几项登记中,PAH诊断的中位年龄为> - 60岁,许多老年患者伴有多种心肺合并症[6,16- - - - - -19].这些患者在临床试验中没有得到很好的代表,从而导致了多环芳烃药物的批准。上述AMBITION研究选取了一小部分(n=105)患有多种合并症的老年患者(平均年龄62岁),对这些患者进行了单独分析,并不能证明联合治疗对他们有明显的益处[20.].根据登记数据,与年轻患者相比,老年患者往往接受较少的积极治疗,对多环芳烃药物的反应较差,有更高的可能性停止他们的多环芳烃药物,并有更高的死亡风险[5,6,17,21].
目前尚不清楚多环芳烃的新治疗方法和新治疗策略的引入,以及在该患者群体中观察到的人口统计学变化,如何随着时间的推移影响治疗模式和生存率。在这里,我们提出来自COMPERA(肺动脉高压新启动治疗的比较、前瞻性注册)的数据。本分析的目的是描述2010年至2019年诊断为PAH患者的治疗模式和生存期的时间趋势,即。超过10年。
方法
数据库
COMPERA的详情(www.COMPERA.org;ClinicalTrials.gov:NCT01347216)已在以前报导过[6,22].简而言之,COMPERA是一个基于网络的肺动脉高压登记系统,于2007年启动,前瞻性地收集接受肺动脉高压靶向治疗的患者的基线、随访和结局数据。最初,COMPERA是作为接受ERA治疗的PAH患者的登记,但在2009年6月,COMPERA演变为一个全面的肺动脉高压登记,登记了接受任何批准用于PAH的药物治疗的所有形式的肺动脉高压患者。中心必须在肺动脉高压诊断后6个月内接收患者,以确保纳入新诊断的患者。来自欧洲各国的肺动脉高压中心参与(奥地利、比利时、德国、希腊、匈牙利、意大利、拉脱维亚、立陶宛、荷兰、斯洛伐克、瑞士和英国),其中80%的入选患者来自德国肺动脉高压中心。
COMPERA已获得所有参与中心伦理委员会的批准,所有患者在纳入前均提供书面知情同意。
病人
对于目前的分析,患者根据以下标准从COMPERA数据库中选择:1)treatment-naïve 2010年1月1日至2019年12月31日期间新诊断为任何形式PAH的年龄≥18岁的患者,2)至少有一次随访,3)静息平均肺动脉压≥25 mmHg,平均肺动脉楔压≤15 mmHg基线。怀疑或确诊肺静脉闭塞性疾病或肺毛细血管瘤病的患者被排除,其他形式的肺动脉高压患者也被排除。
统计分析
这是一个事后前瞻性收集变量的分析。连续数据以带标准差的平均值或中位数(四分位范围)表示。分类数据以数字(百分比)表示。分析了截至2021年9月1日的数据集。在诊断后3个月内使用单一疗法和联合疗法的年化数据,在本文中也称为早期联合疗法,以及在1年后(±6个月)根据诊断年份显示。通过现场访问或打电话给患者或其护理人员来确定生命状况。接受肺移植的患者和失去随访的患者在最后一次联系之日被审查。生存率采用Kaplan-Meier分析和log-rank检验进行评估。1年和3年的估计生存概率显示,每年诊断的置信区间为95%。所有的趋势都是在没有正式的统计测试的情况下用数字可视化的。 The 1-year survival analyses were performed for all patients diagnosed between 2010 and 2019, while the 3-year survival analysis was done only for patients diagnosed between 2010 and 2018. All analyses were done for the entire cohort, for subgroups of patients divided by age (<65与≥65岁),对于I/H/D-PAH和CTD-PAH患者的亚组,以及对于I/H/D-PAH患者的亚组,他们没有合并症和肺对一氧化碳的扩散能力(DLCO) >45%预测[23,24].此外,我们比较了2010年至2014年诊断的患者的累积生存率与2015年至2019年诊断的患者的累积生存率。
所有统计分析均采用R 3.5.2版本(www.r-project.org).
结果
患者特征,治疗和整个队列的生存
本分析共纳入2531例患者(图1).患者的基线特征,包括I/H/D-PAH和CTD-PAH患者亚组的基线特征显示在表1.<65岁(n=1031(40.7%)),≥65岁(n=1500(59.3%))患者的基线特征,以及无合并症的I/H/D-PAH和DLCO>45%预测(n=128(5.1%))显示在补充表S1a-c.年化基线特征并未显示患者人口统计学或疾病严重程度随时间的时间趋势(补充表S2而且补充图S1).
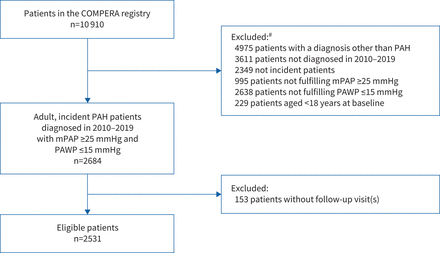
STROBE(加强流行病学中观察性研究的报告)图表显示分析的资格。PAH:肺动脉高压;mPAP:平均肺动脉压;肺动脉楔形压。#:可适用多于一个排除理由。
多环芳烃药物的使用,在整个登记期间的累积,显示在表2对整个小组来说补充表S3a-e对于子组。总体而言,19.6%的患者在诊断后3个月内接受联合治疗,42.9%的患者在1年后接受联合治疗,49.8%的患者在3年后接受联合治疗。在接受联合治疗的患者中,大约三分之二的病例使用了ERA和PDE5i。其他联合疗法使用频率较低,三联疗法包括注射。或南卡罗来纳州。入组时0.9%的患者使用前列腺环素类似物(pca),随访时3.5%的患者使用。多环芳烃药物在3个月和1年的中位剂量显示在补充表S4.
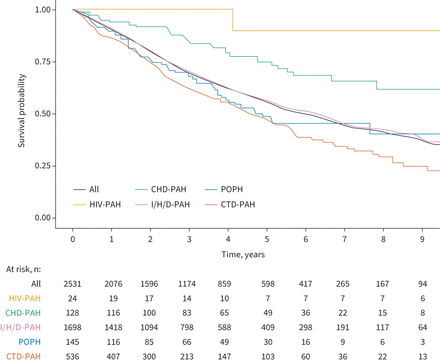
整个队列的中位随访时间为2.8年,<65岁和≥65岁患者亚组的中位随访时间分别为3.3年和2.5年。观察期内共有978例(38.6%)患者死亡,29例(1.1%)患者行肺移植,160例(6.3%)患者失访。Kaplan-Meier估计生存曲线见图2.整个队列的估计生存率为1年后的90.0%,3年后的69.2%和5年后的55.3%。与其他形式的PAH相比,HIV-PAH和冠心病-PAH患者的生存期更好,而CTD-PAH患者的预后最差。亚组中患者队列的生存估计见补充图S2a-c.
Kaplan-Meier生存率总体估计和肺动脉高压(PAH)亚型。CHD:先天性心脏病;POPH:端口-肺动脉高压;I / H / D:特发性/遗传/药物相关;CTD:结缔组织疾病。
多环芳烃治疗的时间趋势
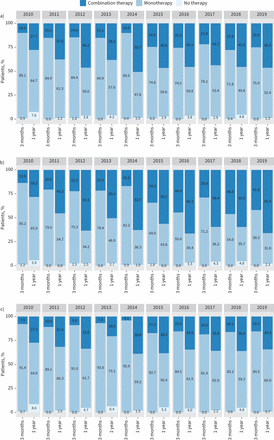
在诊断后3个月内和1年后使用联合治疗的年化趋势显示在图3.在整个队列中,早期联合治疗的使用在2010年诊断为PAH的患者中从10.0%增加到2019年诊断为PAH的患者中的25.0%。早期联合治疗的使用在2014年至2015年期间增长最快。诊断后1年接受联合治疗的患者比例由27.7%增加到46.3% (图3一).
在a)整个队列和b) <65岁和c)≥65岁患者亚组中,肺动脉高压诊断后1年使用初始联合治疗和联合治疗的时间趋势。
在诊断时年龄<65岁的PAH患者亚组中,早期联合治疗的使用从13.6%增加到41.8%,在观察期间,诊断后1年联合治疗的使用从28.2%增加到65.9% (图3 b).
在诊断时年龄≥65岁的PAH患者亚组中,联合治疗的频率低于年轻队列。联合治疗的使用率在3个月后由7.9%上升至15.5%,在1年后由27.3%上升至34.3% (图3 c).
I/H/D-PAH、CTD-PAH和无合并症的I/H/D-PAH患者亚组使用联合治疗的时间趋势DLCO>45%预测与全组变化一致(补充图S3a-c).
随着时间的推移生存
1年和3年生存率的时间趋势显示在图4.在整个队列中,1年生存率在82.3% (95% CI 77.4-87.5%)和93.3% (95% CI 90.3-96.4%)之间变化,随着时间的推移没有明显改善(图4一).整个队列的年化3年生存率在65.0% (95% CI 58.8-71.8%)和75.3% (95% CI 69.9-81.2%)之间;在这方面,不排除有轻微改善的趋势(图4一).
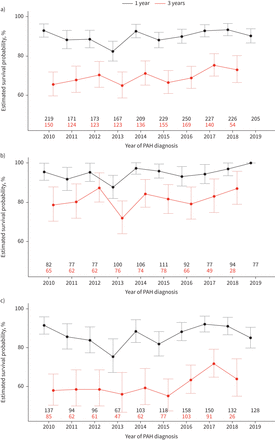
肺动脉高压(PAH)诊断后1年和3年的年化生存率(95% CI)在a)整个队列中,在b) <65岁和c)≥65岁的患者亚组中。黑色和红色数字分别表示可用于1年和3年生存率的患者数量。
在诊断时年龄<65岁的患者中,年化1年生存率估计在87.7% (95% CI 82.1-93.8%)和100.0% (95% CI 100.0-100.0%)之间变化,3年生存率估计在72.0% (95% CI 64.2-80.8%)和87.3% (95% CI 80.3-95.0%)之间变化(图4 b),也表明随着时间的推移可能会有所改善。
在诊断时年龄≥65岁的患者中,年化1年生存率估计在75.3% (95% CI 67.3-84.5%)和92.1% (95% CI 88.1-96.1%)之间变化,3年生存率估计在55.1% (95% CI 47.6-63.9%)和71.7% (95% CI 64.9-79.3%)之间变化(图4 c).在两个队列中,1年生存期估计值随着时间的推移有波动,没有明显的趋势,而3年生存期估计值有可能增加。在I/H/D-PAH和CTD-PAH患者亚组中观察到类似的趋势(补充图S4a和b).
2010年至2014年和2015年至2019年诊断为PAH患者的累积1年和3年生存率显示在表3.在这项分析中,整个队列的1年生存率在两个时间段之间没有差异,而3年生存率略有改善(尽管95%置信区间重叠)。在所有亚组中都出现了类似的模式。
讨论
在本研究中,我们评估了COMPERA数据库,以描述2010年至2019年间新诊断为PAH患者的治疗策略和生存的时间趋势,即。超过10年。在此期间,我们观察到口服联合疗法的使用有所增加,尤其是在年轻患者中。虽然诊断后1年的生存率没有随着时间的推移而改善,但3年生存率可能会略有改善,但尚未得到证实。
尽管联合治疗的使用随着时间的推移而增加,但它仍然出乎意料地低。早期联合治疗的使用在2014年至2015年期间出现了最急剧的增长,这可能是由于AMBITION研究的发表,该研究表明,与最初接受单一治疗的患者相比,接受ERA和PDE5i联合治疗的PAH患者具有更明显的临床改善和更少的临床恶化事件[8].尽管如此,即使在观察期结束时,整个队列中只有25%的患者使用早期联合治疗,在诊断时年龄<65岁的患者中使用早期联合治疗的比例<50%。在诊断时年龄≥65岁的患者亚组中,无论是在诊断初期还是在诊断后1年,联合治疗的使用频率都比年轻患者低得多。
联合疗法使用相对较少的原因尚不清楚。安全问题可能会起到一定作用。然而,在AMBITION研究中,初始联合治疗的耐受性良好,与单药治疗相比,初始联合治疗的过早停用研究药物的情况并不多[8].此外,其他几项大规模研究也证明了各种序贯联合疗法的安全性和有效性[9,10].然而,这些研究和荟萃分析均未显示联合治疗优于单一治疗的生存优势[8- - - - - -11,25,这可能会阻止医生更广泛地使用联合疗法。
在本系列研究中,与年轻患者相比,老年PAH患者有更多的合并症,接受联合治疗的可能性更低,死亡风险更高,这与其他PAH登记中观察到的情况相似[16- - - - - -18].由于老年患者的死亡风险较高,人们可能会认为联合疗法会比年轻患者更频繁地使用,然而观察到的情况恰恰相反。我们以前曾报道,老年患者较少使用联合疗法不仅是因为较低的起始率,而且还因为药物停药的可能性较高[6,21].对于高龄多环芳烃和多种合并症患者使用联合治疗,医生似乎不太有信心。这可能与这类患者在该领域的关键试验中代表性不足有关,至少在一定程度上是这样。临床惯性,即。认识到问题,但未能采取行动,这是其他疾病领域众所周知的现象[26],也可能发挥作用。前瞻性研究正在进行中,以进一步探索多环芳烃患者拒绝联合治疗的原因。
虽然我们不能排除随着时间的推移,3年生存率略有增加,但我们惊讶地发现没有更清晰的信号,甚至在年轻患者中也没有,这是我们预期的,随着联合疗法的使用越来越多。有几个原因可能适用。首先,尽管联合治疗的使用随着时间的推移而增加,但大多数患者接受单一治疗,因此联合治疗对生存的任何影响都可能被稀释。其次,本系列中主要用于治疗多环芳烃的药物在2010年就已经上市了,即。当分析开始的时候。在观察期间,欧洲唯一新引进的药物是马西坦,一种ERA [9],前列环素受体激动剂selexipag [10],以及可溶性鸟苷酸环化酶刺激剂riociguat [27].对于所有这三种化合物,已证明可改善无事件生存期,但不能改善总生存期[9,10,27].以目标为导向的联合治疗概念已于2005年提出[28]并可能在2010年被许多肺动脉高压中心采用,即。本研究观察期的开始。这一点以及临床研究观察到,使用联合疗法的临床研究一直表明,无事件生存期有所改善,但总生存期没有改善[8- - - - - -10],可能表明在临床恶化事件发生时加强治疗可能会延迟一些患者的进一步临床恶化和死亡。如果是这样的话,早期联合治疗对总生存期的影响将小于临床恶化的时间。
我们的发现证实了Boucly等.[5],他们最近分析了法国肺动脉高压登记处的初始治疗策略和长期结果,发现接受初始单药治疗或初始口服联合治疗的患者的生存期没有差异(除了中等风险患者的生存期存在微小但具有统计学意义的差异)。值得注意的是,在法国系列中,唯一与长期生存获益相关的治疗策略是初始三联治疗,包括ERA, PDE5i和注射。或南卡罗来纳州。PCAs [5].在法国系列中,这种治疗策略用于~ 5%的患者,而在我们的本系列中,这种治疗策略用于<1%的患者,这表明最初的三联治疗包括注射。或南卡罗来纳州。前列环素还不能被认为是治疗标准。然而,两项基于1611名患者的大型注册研究[5和2531例患者(我们的研究)现在独立表明,初始或早期口服联合治疗可能与口服单药治疗的长期生存获益不一定相关,进一步探索初始三联治疗的效果变得越来越重要,包括注射。或南卡罗来纳州。评估长期结果。此外,未来探索PAH治疗策略的研究应设计为显示潜在的生存差异。
值得注意的是,我们的观察结果不应阻止医生对PAH患者使用初始或早期口服联合治疗。基于前瞻性随机对照试验的当前指南推荐了这种治疗策略,这些试验在几个临床重要终点上显示出有意义的改善[3.,8,15].考虑到事后我们的研究的性质以及Boucly等.[5],我们的发现应该被认为是产生假设的,我们需要前瞻性研究来比较各种初始治疗策略对长期生存的影响。基于注册的实用试验已成功应用于其他疾病领域[29可以被认为是解决这个根本重要问题的方法。
我们的研究有优势也有局限。优点包括大样本量和在整个研究期间相对稳定的新入组患者数量。主要的限制是注册中心固有的限制,包括事后分析和丢失或错误输入数据的可能性。为了将此类风险降至最低,COMPERA采用了几种预防策略,包括自动合理性检查、定期查询不可信条目以及独立的现场监测与源数据验证。此外,将年龄分组划分为65岁进行亚组分析是武断的,尽管这个阈值经常被用来定义老年。在多环芳烃的情况下,这一阈值的价值可能有限,因为先前的研究表明,18-45岁的多环芳烃患者与46-64岁的患者在治疗模式、治疗反应和生存期方面存在差异[16].
总之,目前对comera数据库的分析显示,在2010年至2019年的10年期间,口服联合治疗的使用有所增加,但约一半的患者在诊断1年后仍接受单药治疗。虽然1年生存率没有随时间变化,但3年生存率有轻微改善,但不具有统计学意义。这将是一个重要的未来任务,以找出是否更积极地使用联合治疗,包括注射。或南卡罗来纳州。pca可以改善PAH患者的长期生存。
补充材料
可共享的PDF
确认
作者非常感谢COMPERA调查人员和他们的同事。
脚注
利益冲突:M.M. Hoeper接受Acceleron, Actelion, Bayer, GlaxoSmithKline, Janssen, MSD和Pfizer的讲座和/或咨询费用。
利益冲突:C. Pausch没有披露。
利益冲突:E. Grünig接受了Actelion、拜耳、葛兰素史克、杨森、MSD、辉瑞和联合治疗公司的讲座和/或咨询费用。
利益冲突:G. Staehler曾为Actelion、拜耳、葛兰素史克、诺华和辉瑞公司提供讲座和/或咨询服务。
利益冲突:D. Huscher从Actelion收取了咨询费。
利益冲突:D. Pittrow收取了来自Actelion、Amgen、Aspen、Bayer、Biogen、Boehringer Ingelheim、Daiichi Sankyo、Sanofi、Takeda和Viatris的咨询费。
利益冲突:K.M. Olsson曾收取Acceleron、Actelion、拜耳、葛兰素史克、杨森、默沙东、辉瑞和联合治疗公司的讲座和/或咨询费。
利益冲突:C.D. Vizza接受Acceleron、Actelion、拜耳、葛兰素史克、杨森、MSD、辉瑞和联合治疗公司的讲座和/或咨询费用。
利益冲突:H. Gall报告了来自Actelion、阿斯利康、拜耳、BMS、葛兰素史克、杨森-西莱格、礼来、MSD、诺华、OMT、辉瑞和联合治疗公司的个人费用。
利益冲突:在硬皮病及其并发症(包括多环芳脂)的潜在治疗领域,O. Distler与4D Science、Actelion、Active Biotec、Bayer、Biogen Idec、Boehringer Ingelheim Pharma、BMS、ChemoAb、EpiPharm、Ergonex、EspeRare基金会、葛兰素史克、Genentech/Roche、Inventiva、Janssen、礼来、medac、MedImmune、Mitsubishi Tanabe、Pharmacyclics、辉瑞、赛诺菲、Serodapharm和Sinoxa有咨询关系和/或获得研究资金;此外,作者拥有“mir-29用于治疗系统性硬化症”专利授权。
利益冲突:C. Opitz获得了Actelion、拜耳、葛兰素史克、礼来、诺华和辉瑞的演讲费和咨询酬金。
利益冲突:J.S.R. Gibbs接受Acceleron、Actelion、Aerovate、Bayer、Complexia、Janssen、MSD、Pfizer和United Therapeutics的讲座和/或咨询费用。
利益冲突:M. Delcroix报告来自Actelion/J&J的研究经费,来自拜耳、MSD、Acceleron、AOP和Daiichi Sankyo的演讲者和咨询费,在提交的工作之外;鲁汶大学肺动脉高压Janssen教授。
利益冲突:H.A. Ghofrani曾获得拜耳医疗保健公司、Actelion、Encysive、辉瑞、Ergonex、礼来和诺华公司的咨询和/或会议演讲酬金;是Acceleron、Bayer HealthCare AG、Pfizer、GlaxoSmithKline、Actelion、Lilly、Merck、Encysive和Ergonex的顾问委员会成员;还获得了德国研究基金会(DFG)、卓越集群心肺研究(ECCPS)、黑森州政府(LOEWE)和德国教育与研究部(BMBF)的政府资助。
利益冲突:S. Rosenkranz接受了雅培、Acceleron、Actelion、拜耳、BMS、吉利德、葛兰素史克、杨森、默沙东、诺华、辉瑞、联合治疗和Vifor的讲座和/或咨询费用;阿斯利康(AstraZeneca)、Actelion、拜耳杨森(Bayer Janssen)和诺华(Novartis)向机构提供研究资助。
利益冲突:D-H。朴槿惠没有什么可透露的。
利益冲突:R. Ewert曾获得Actelion、拜耳、葛兰素史克、杨森、礼来、MSD、诺华、辉瑞和联合治疗公司的演讲费和咨询酬金。
利益冲突:H. Kaemmerer曾获得Actelion, BMS和Janssen的讲座和/或咨询的酬金。
利益冲突:T.J. Lange已获得Acceleron、Actelion、拜耳、葛兰素史克、Janssen-Cilag、MSD、辉瑞和联合治疗公司的演讲费和咨询酬金。
利益冲突:H-J。Kabitz已收到Löwenstein Medical、Weinmann、Philips呼吸onics、ResMed、Vivisol、Sapio Life和赛诺菲-健zyme的费用。
利益冲突:D. Skowasch接受Actelion、拜耳、葛兰素史克、杨森、默沙东和辉瑞等机构的讲座和/或咨询和/或研究支持费用。
利益冲突:A. Skride报告没有利益冲突。
利益冲突:M. Claussen在勃林格殷格翰制药有限公司和罗氏制药的讲座中获得荣誉,并在勃林格殷格翰咨询委员会任职。
利益冲突:J. Behr获得了Actelion、拜耳、Biogen、勃林格殷格翰、加拉帕戈斯、诺华、罗氏和赛诺菲/健酶的资助。
利益冲突:K. Milger接受了Actelion、阿斯利康、葛兰素史克、杨森、MSD、诺华和赛诺菲-安万特的费用。
利益冲突:M. Halank曾获得Acceleron、Actelion、阿斯利康、拜耳、柏林化学、葛兰素史克、杨森和诺华的演讲费和咨询酬金。
利益冲突:H. Wilkens从Actelion, Bayer, Biotest, Boehringer, GlaxoSmithKline, Janssen, Pfizer和Roche收取个人费用。
利益冲突:H-J。赛法尔斯获得了Actelion、拜耳、葛兰素史克、杨森和默沙东的演讲费和咨询酬金。
利益冲突:M. Held曾获得Actelion、拜耳、勃林格殷格翰制药、葛兰素史克、杨森、MSD、诺华、辉瑞、奈科明、罗氏和施维耶的演讲费和咨询酬金。
利益冲突:D. Dumitrescu宣布为Actelion、阿斯利康、拜耳、葛兰素史克、杨森、MSD、诺华、辉瑞和施维耶的讲座和/或咨询提供酬金。
利益冲突:I. Tsangaris接受了Actelion、拜耳、ELPEN、葛兰素史克、杨森、MSD、辉瑞和联合治疗公司的费用。
利益冲突:A. Vonk-Noordegraaf报告从Actelion、拜耳、葛兰素史克、杨森、默沙东和辉瑞收取讲座和/或咨询费用。
利益冲突:S. Ulrich在提交的工作之外报告Actelion、Janssen和MSD的个人费用。
利益冲突:H. Klose曾获得Actelion、拜耳、葛兰素史克、杨森、MSD、诺华、辉瑞和联合治疗公司的演讲费和咨询酬金。
支持声明:这项工作得到了德国肺研究中心(DZL)的支持。COMPERA由Acceleron、拜耳、葛兰素史克、杨森和OMT提供无限制资助。这些公司没有参与数据分析或手稿的撰写。
- 收到了2021年7月21日。
- 接受2021年10月5日。
- 版权所有©作者2022。
本版本根据知识共享署名非商业许可4.0的条款发布。为商业复制权利和权限联系权限在}{ersnet.org