摘要
简介较高的类黄酮摄入量与肺功能参数有益相关;然而,它们与慢性阻塞性肺病(COPD)的关系尚不清楚。这项研究旨在研究丹麦饮食、癌症和健康研究参与者摄入1)总黄酮、2)类黄酮亚类和3)主要类黄酮化合物与COPD发病之间的关系。
方法该前瞻性队列包括55413名无COPD的男性和女性,招募时年龄为50-65岁。基线时的习惯类黄酮摄入量由使用苯酚探索者的食物频率问卷估计。丹麦全国登记册用于确定慢性阻塞性肺病事件病例。在Cox比例风险模型中使用限制性三次样条来建立关联模型。
结果在23年的随访中,5557名参与者被诊断患有COPD。其中,4013人现在吸烟,1062人以前吸烟,482人从不吸烟。在多变量调整后,总黄酮摄入量最高的参与者比总黄酮摄入量最低的参与者患COPD的风险低20%(五分位数5与五分位数1:HR 0.80, 95% CI 0.74-0.87);每个类黄酮子类的风险降低了6-22%。总黄酮摄入量与COPD之间的负相关在男性和女性中都存在,但仅在当前吸烟者(HR 0.77, 95% CI 0.70-0.84)和前吸烟者(HR 0.82, 95% CI 0.69-0.97)中存在,不存在从不吸烟者。此外,较高的类黄酮摄入量似乎降低了与吸烟强度相关的COPD高风险,但并不能消除这种风险。
结论饮食中的黄酮类化合物可能对部分减轻吸烟相关的COPD风险很重要。然而,戒烟仍应是最高优先事项。
摘要
虽然戒烟仍然是预防COPD的首要任务,但这项研究的结果表明,饮食中的类黄酮在部分减轻吸烟或曾经吸烟的人患COPD的风险方面很重要https://bit.ly/3r6wWt8
简介
慢性阻塞性肺病(COPD)是一种常见的肺部疾病,其特征是肺部炎症反应异常导致持续的呼吸道症状和不可逆的气流限制,通常是由于大量接触有毒气体或颗粒引起的[1,2].虽然吸烟是慢性阻塞性肺病最常见的原因,但其他可改变的危险因素包括空气污染;职业性接触灰尘、蒸汽和烟雾;以及早期的呼吸道感染[3.].不可改变的危险因素包括年龄和遗传易感性[4].鉴于COPD在全球范围内的高患病率和高负担,且目前尚无治愈方法[5],应优先考虑预防策略。
越来越多的证据表明,饮食对肺功能有影响,并可能对COPD发挥保护作用[6- - - - - -8],可能是通过调节炎症和氧化应激途径,这些途径与这种慢性疾病的发展有关[9].在一项针对瑞典男性的前瞻性队列研究中,在目前和曾经吸烟的人群中观察到水果和蔬菜总摄入量与COPD之间存在很强的负相关,但在从不吸烟的人群中则没有[10].水果和蔬菜,以及茶、可可和其他植物性食品和饮料,都是类黄酮的膳食来源,类黄酮是一种生物活性化合物,可以减少氧化应激和系统性炎症[11].类黄酮是一种多酚类物质,可以根据其化学结构进一步分为亚类。虽然缺乏专门调查类黄酮摄入量与COPD之间关系的流行病学研究,但有一些证据表明类黄酮摄入量与肺功能参数有良好的相关性[12,13]和较少的与年龄相关的肺功能衰退[14].
这项研究的主要目的是调查丹麦饮食、癌症和健康队列中1)总黄酮、2)类黄酮亚类和3)各自亚类中的关键类黄酮化合物摄入量与COPD发病之间的关系。在我们之前的工作中,一个一致的发现是类黄酮摄入量与一系列慢性疾病(包括心血管疾病、痴呆症和糖尿病)之间的联系[15,16)在目前和曾经吸烟的人身上更强烈。鉴于吸烟作为COPD风险因素的重要性,黄酮类化合物的抗氧化和抗炎特性,以及有证据表明COPD风险和结果的性别差异[17],次要目的是探索类黄酮摄入量与COPD危险因素(即性和吸烟)之间的相互作用。
方法
研究人群
本研究使用的数据来自丹麦饮食、癌症和健康研究的参与者。最初研究的详细描述已在以前发表过[18].简而言之,在1993年至1997年间,从丹麦的哥本哈根和奥胡斯招募了57053名参与者。在参与研究时,其中56468名参与者完成了一份食物频率问卷(FFQ),并且没有被诊断出患有癌症。收集的数据使用分配给所有丹麦居民的唯一和永久民事登记号码与以下全国登记册交叉链接:民事登记系统、劳动力市场研究综合数据库和丹麦全国病人登记册。后者登记册[19]保存了自1978年以来丹麦所有医院入院和门诊和急诊中心就诊的信息。它包括《国际疾病分类》(ICD)(1993年之前的第8版(ICD-8)和1994年至今的第10版(ICD-10)定义的一种主要诊断和一种或多种次要诊断。在本研究中,如果参与者在参加丹麦饮食、癌症和健康研究之前被诊断患有COPD、未指明的慢性支气管炎或肺气肿,则被排除在外(n=479;ICD-8: 491.00-492.09, ICD-10: J42-J44),如果他们报告了不可能的能量摄入(n=202;<2092 kJ /天(<500 kcal /天)和>20 920 kJ /天(>5000 kcal /天))或协变量缺失或极端值(n=374;补充图E1).
这项研究得到了丹麦数据保护机构的批准。2012-58-0004 I-Suite nr: 6357, VD-2018-117)。
曝光
本研究的主要研究对象是总类黄酮摄入量(通过219种类黄酮化合物的摄入量之和计算)、类黄酮亚类和单个类黄酮化合物的摄入量,基线时的平均摄入量为>5 mg /天。详细描述了如何使用苯酚资源管理器数据库从FFQ中估计类黄酮摄入量[20.]已于以前出版[15].简而言之,FFQ (n=174)中每种食品和饮料的类黄酮估计值(每100克新鲜食品重量毫克)来自苯酚探索者数据库,考虑到使用保留因子进行食品加工。然后再乘以相应食物和饮料的摄入量(每天g)。在一个事后调查分析,吸烟包年(一生平均吸烟数乘以吸烟年数除以20)被建模为兴趣暴露。
研究结果
主要终点为首次住院或门诊就诊,主要或次要诊断为COPD (ICD-10: J44)、未指明的慢性支气管炎(ICD-10: J42)或肺气肿(ICD-10: J43)。ICD-10代码J44此前已在丹麦国家患者登记册中得到验证,其阳性预测值为92% (95% CI 91-93%) [21].由于COPD患者可能被编码为患有未指明的慢性支气管炎(ICD-10: J42)或肺气肿(ICD-10: J43),这些也被包括在内。在丹麦登记中,首次诊断COPD是唯一有效的识别COPD的方法;以下简称为偶发COPD。大多数病例由ICD-10编码DJ449(~ 69%)、DJ441(~ 12%)和DJ429(~ 8%)识别。
统计分析
多变量Cox比例风险模型用于调查自我报告的类黄酮摄入量与COPD发病之间的关系。每位参与者的事件发生时间从参加丹麦饮食、癌症和健康研究之日起计算,直到首次诊断为COPD、死亡、从丹麦移民或随访结束之日(2017年8月),以先到者为准。通过绘制Schoenfeld残差检验Cox比例风险假设,未发现违规。为了允许所有连续协变量(包括感兴趣的曝光)与结果之间的关联是非线性的,这些变量使用限制性三次样条建模,使用“rms”R包和rcs()函数[22R (www.r-project.org)。生成每个类黄酮暴露变量的五分位数(Q1-5),并计算每个五分位数的中位数。从上述Cox比例风险模型中得出的风险比,是相对于Q1中位类黄酮摄入量的(参考值);这些数据根据暴露变量绘制,并提供95%置信区间。此外,根据拟合模型计算风险比和95%置信区间,将每个五分位数的中位数与Q1中位数的参考值进行比较,并制成表格。为了更简单的可视化,数字只包括摄入量≤3的个体sd高于平均值。采用三种调整模型:1)最低限度调整:年龄(岁)和性别;1b)多变量调整:年龄、性别、身体质量指数(BMI)、吸烟状况(现在/以前/从未)、吸烟包年、体育活动(总每日代谢当量)、纯酒精摄入量(每天g)、教育程度(≤7年/ 8-10年/≥11年)和社会经济状况(收入);2)多变量调整,包括潜在的饮食混杂因素:模型1b中的所有变量加上鱼、红肉、加工肉、全谷物、精制谷物、多不饱和脂肪酸、单不饱和脂肪酸和饱和脂肪酸的能量摄入量(千焦/天)和摄入量(克/天)。混杂因素的选择基于先天的知识(23- - - - - -25].
第二个目的是研究与既定COPD危险因素的相互作用[3.],并在基线时收集数据(特别是吸烟状况和性别)。首先,分析按性别和吸烟状况进行分层,以检验相关性的一致性。由于吸烟强度存在残留混杂的可能性,在按吸烟状况分层时,将吸烟包年作为协变量纳入模型。通过Cox比例风险模型的似然比检验,评估了有和没有相互作用项的乘数尺度上的相互作用。其次,使用标准的逻辑回归模型来获得20年的COPD医疗访问的绝对风险估计。这些分析使用了一个二元结果,即在随访的前20年里COPD医疗就诊的发生情况。除非有相关的分层变量表明,这些估计值是针对“平均”吸烟队列参与者的,即。吸烟者,56岁,BMI为25.5 kg·m−2平均家庭年收入为394 701-570 930丹麦克朗,每天酒精摄入量为13克。在一个事后在调查分析中,我们探讨了类黄酮摄入量是否改变了吸烟强度(以包年表示)与COPD之间的关系,方法是分别在类黄酮摄入量最高和最低五分位数的男性和女性中绘制20年随访后COPD的预测风险。在上述分析中,吸烟包年作为限制性三次样条输入模型。最后,为了避免临床前COPD导致反向因果关系的可能性,作为敏感性分析,我们省略了随访前5年内发生的所有病例。所有分析均使用STATA/IC 14.2 (StataCorp LLC)和R统计数据(www.r-project.org)进行。
结果
在55 413名丹麦居民中,中位年龄为56岁,在长达23年的随访中发现了5557例COPD事件(中位(IQR)随访:21年(19-22岁))。此外,11 195名参与者在没有住院诊断COPD的情况下死亡,276名(约0.5%)失去随访。
基线特征
总的来说,队列报告的每日中位数(IQR)习惯性类黄酮摄入量为496毫克(287-805毫克)。总黄酮摄入量较高的参与者多为女性,且更有可能不吸烟、BMI较低、运动较多、教育程度和收入较高。平均而言,那些摄入更多类黄酮的人也会吃更多的鱼、全谷物、水果和蔬菜,而较少的红肉和加工肉类(表1).
总类黄酮和类黄酮摄入量与COPD发病的关系
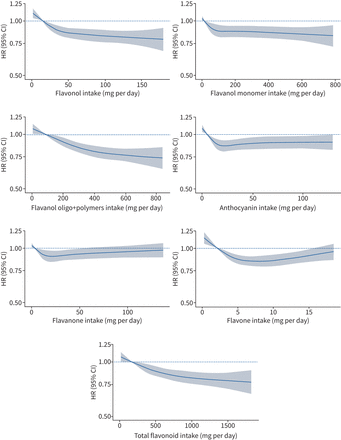
总黄酮摄入量与COPD发病呈非线性负相关(p非−线性< 0.001);随着类黄酮摄入量的增加,坡度降低(图1).与Q1的参与者相比,Q5的参与者在多变量调整后COPD风险降低了20% (HR 0.80, 95% CI 0.74-0.87)(模型1b,表2).非线性关联也观察到所有类黄酮子类(p非线性全部<0.001,图1).与高(Q4或Q5)摄入量与低(Q1)摄入量相比,经多变量调整后,黄烷醇组COPD风险降低18%,黄烷醇单体组降低14%,黄烷醇低聚物+聚合物组降低22%,花青素组降低12%,黄烷酮组降低9%,黄酮组降低15%(模型1b),表2).总黄酮摄入量显著相关(Q5与Q1: HR 0.85, 95% CI 0.78-0.92)和所有类黄酮子类的摄入量,当潜在的饮食混杂因素包括在模型中作为预测因素时(模型2,表2).
三次样条曲线描述了丹麦饮食、癌症和健康队列参与者总黄酮和类黄酮亚类摄入量与慢性阻塞性肺疾病(COPD)相关医疗就诊之间的关系(n= 55413)。危害比和95%置信区间基于Cox比例危害模型,该模型经年龄、性别、体重指数、吸烟状况、吸烟包年、体育活动、教育程度、社会经济地位(收入)和酒精摄入量(模型1b)调整,并将最低摄入量五分位数参与者的黄酮类化合物摄入量的具体水平(横轴)与中位数摄入量进行比较。
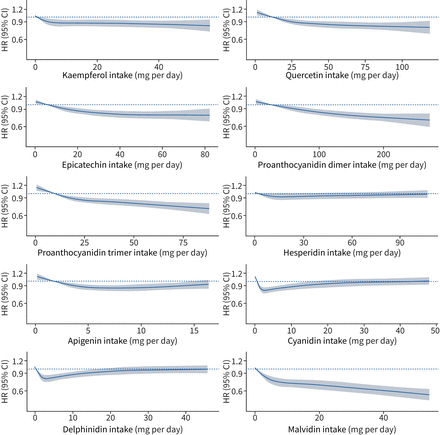
三次样条曲线描述了丹麦饮食、癌症和健康队列参与者中主要类黄酮化合物摄入量与慢性阻塞性肺疾病(COPD)相关医疗就诊之间的关系(n= 55413)。危害比和95%置信区间基于经年龄、性别、体重指数、吸烟状况、吸烟包年、体育活动、社会经济地位(收入)和酒精摄入量(模型1b)调整后的Cox比例危害模型,并将最低摄入量五分位数参与者的黄酮摄入量(横轴)的具体水平与中位数摄入量进行比较。
主要类黄酮化合物摄入量与COPD发病之间的关系
观察到所有主要类黄酮化合物的摄入量与COPD发病的非线性关联(p非线性全部<0.001,图2).山奈酚、槲皮素、表儿茶素、橙皮苷和芹菜素的摄入量存在明显的相关性高原。对malvidin和原花青素二聚体和三聚体的摄入,相关性似乎是线性的,而对cyanidin和delphinidin的摄入,相关性似乎是“u型”的。观察到的最低的危险比是最高摄入量的受试者(Q5与Q1: hr 0.63, 95% ci 0.57-0.70;模型1 b;补充表E2).
总黄酮摄入量与COPD发病之间的关系按性别和吸烟分层
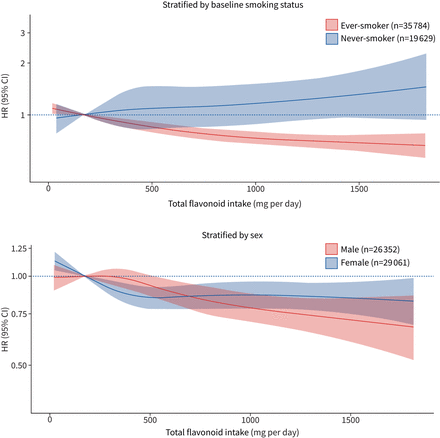
在随访期间诊断为COPD的5557名参与者中,2605人为男性,2952人为女性。总黄酮摄入量与COPD发病之间的关联在男性和女性中都存在,尽管关联的形状不同;女性的相关性最初更明显,在每天摄入总类黄酮约500毫克时趋于稳定(p非线性=0.013),而男性的相关性则更为线性(p非线性= 0.506, p交互< 0.001,图3).在绝对尺度上,女性患COPD的风险高于男性,与吸烟状况或类黄酮摄入量无关(表3).
总黄酮摄入量与慢性阻塞性肺疾病(COPD)相关医疗就诊之间的多变量调整相关性(按基线吸烟状况和性别分层)风险比和95%置信区间基于Cox比例风险模型,并比较了最低摄入量五分位数(174毫克/天)参与者的类黄酮摄入量的具体水平(横轴)和中位数摄入量。所有分析均按年龄、性别、体重指数、吸烟状况、吸烟包年限、体育活动、社会经济状况(收入)、教育程度和酒精摄入量进行了标准化(模型1b)。
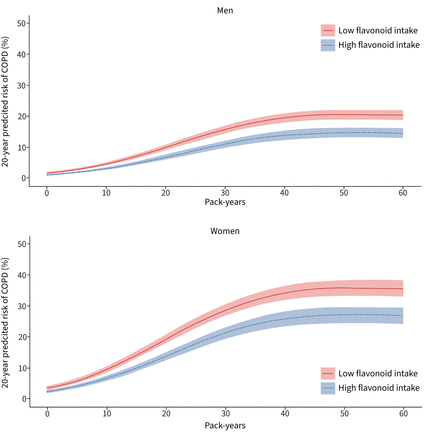
在5557例COPD事件中,4013例发生在当前吸烟者中,1062例发生在前吸烟者中,482例发生在从不吸烟者中。虽然总黄酮摄入量与COPD发病之间的明显负相关存在于当前/以前的吸烟者(称为永远吸烟者)中,但在从未吸烟的人中没有负相关(p交互= 0.017,图3).总黄酮摄入量最高的当前吸烟者和前吸烟者COPD风险分别降低23%和18%(当前吸烟者Q5与Q1: hr 0.77, 95% ci 0.70-0.84;前吸烟者Q5与Q1:多变量调整后的HR 0.82, 95% CI 0.69-0.97)(模型1b,补充表E3和E4).其他类黄酮子类和化合物在当前和曾经吸烟者之间的危害比显示在补充表E3-E6.在绝对规模上,无论类黄酮摄入量如何,目前和曾经吸烟的人患COPD的风险比不吸烟的人高得多,尽管类黄酮摄入量低的当前吸烟者的风险最高(表3).对于基线时仍在吸烟的参与者,20年预测COPD风险的差异在吸烟人数最高的参与者之间与类黄酮摄入量最低的五分位数男性为5.21%,女性为6.20% (表3).此外,对于男性和女性,类黄酮摄入量似乎改变了吸烟强度(包年)与20年COPD预测风险之间的关系,类黄酮摄入量最高的参与者(Q5)比类黄酮摄入量低的参与者(Q1)的COPD预测风险更低(图4).
高吸烟包年慢性阻塞性肺疾病(COPD)的20年预测风险(%)和95%置信区间(五分位数5)与低(五分位数1)总黄酮摄入量,分别为男性和女性。预测风险由逻辑回归模型计算,适用于56岁的参与者,体重指数为25.5 kg·m−2平均家庭年收入为394 701-570 930丹麦克朗,每天酒精摄入量为13克。
敏感性分析
排除随访前5年内的事件并没有显著改变所观察到的相关性(补充表E7).
讨论
在这项为期23年的55 413名丹麦居民的前瞻性队列研究中,我们观察到每个类黄酮亚类以及所有主要类黄酮化合物的基线摄入量与COPD发病呈非线性负相关。总黄酮摄入量与COPD事件之间的关联仅存在于当前和以前的吸烟者中,他们占观察到的COPD事件的91%。在本研究中,“平均”队列参与者既吸烟又在基线时低类黄酮摄入量,其COPD风险比高类黄酮摄入量的参与者高~ 6%(女性)至~ 5%(男性)。此外,高类黄酮摄入量似乎降低了,但不能消除与高吸烟强度相关的COPD风险。
2001年,第一项检验膳食类黄酮摄入量与肺功能之间关系的研究报告称,儿茶素、黄酮醇和黄酮(当时唯一可获得食物含量数据的类黄酮子类)的摄入量与1秒内的用力呼气量(FEV)之间存在有益的负相关1) [26].尽管有这些发现,但此后的研究却很少。退伍军人事务规范老龄化研究参与者的纵向分析[14]表明花青素摄入量与年龄相关的肺功能下降呈负相关,这是COPD的危险因素[27,包括现在吸烟、曾经吸烟和从不吸烟。最近,两项横断面研究报告了不同类黄酮亚类与肺功能参数之间的保护性关联[12,13].据我们所知,目前的研究是第一个调查饮食类黄酮摄入量与COPD发病之间关系的研究。我们发现,在对人口统计学、生活方式和饮食混杂因素进行多变量调整后,所有类黄酮子类都存在明显的负相关,这突出了在这一重要但研究很少的领域进行进一步研究的必要性。此外,我们看到有证据表明,即使在高危人群中,黄酮类化合物的最佳摄入量也可以通过饮食来实现。
在本研究中,类黄酮摄入量与COPD之间的关联仅存在于当前和以前的吸烟者中,对于类黄酮摄入量最高的人,当前和以前的吸烟者患COPD的绝对风险较低;这与黄酮类化合物可能在一定程度上抵消吸烟引起的全身炎症和氧化应激增加的假设一致[28]导致慢性阻塞性肺病[29].我们的研究结果支持了这一假设事后探索性分析表明,在摄入更多富含类黄酮食物的参与者中,与较高吸烟包年相关的COPD风险较低。吸烟引起的炎症和氧化应激的途径有很大的重叠[29,30.]和被确定为由类黄酮调节的[31].黄酮类化合物可通过这些信号通路抑制氧化应激和炎症来预防COPD,这已在香烟烟雾诱导的COPD小鼠模型中得到证实,该模型补充了枇杷叶中提取的黄酮类化合物[32]和香烟烟雾诱导的COPD大鼠模型,在该模型中动物补充了类黄酮非瑟酮[33].虽然缺乏人体干预研究,但在对健康吸烟者进行的随机对照试验中,补充富含黄酮类化合物的葡萄汁2周可减少吸烟引起的炎症[34].在本研究中,在相对尺度上,总黄酮摄入量与COPD之间的关联在男性和女性中都很明显,尽管关联的形状似乎有所不同。由于相互作用的生理、行为和/或遗传因素的复杂性,其背后的原因难以确定,目前尚不完全清楚为什么女性患COPD的风险高于男性[35].
目前吸烟者和低类黄酮摄入量的“平均”队列参与者的20年COPD绝对风险比高类黄酮摄入量的参与者高~6%(女性)或~5%(男性)。前吸烟者的风险差异较小(男性和女性各约2%),尽管他们患COPD的风险约为当前吸烟者的三分之一。将前吸烟者的COPD病例减少~ 2%,将当前吸烟者的COPD病例减少~ 5-6%,将对公共卫生产生巨大影响,这就引出了一个问题,即饮食调整是否应该在当前和以前的吸烟者中更优先考虑。然而,无论黄酮摄入量如何,目前和以前的吸烟者患COPD的风险都比不吸烟者高得多(分别高出~ 8倍和~ 3倍),这提醒我们,以戒烟为目标是,而且必须继续是降低COPD风险的首要任务。
目前的研究有许多优势,包括对大量成年人群进行了23年的随访,其中有相对较多的事件,使我们能够检查亚人群中的相关性,并且随访损失可以忽略不计,从而可以估计绝对风险。虽然我们的假设和随后的发现得到了机械证据的支持,但本研究本质上是观察性的,因此我们不能确认因果关系。我们也承认,在这个队列中,类黄酮摄入量较高的人往往有更健康的饮食和生活方式,我们不能排除残留或未测量混杂的可能性。此外,由于饮食是使用FFQ自我报告的,并且可能随着时间的推移而改变,因此暴露中可能存在错误分类。同样,吸烟状况和强度仅在基线时被捕获,因此随访期间的变化不能被解释。在丹麦国家患者登记册中,COPD诊断漏报,仅在初级保健中的诊断不会被捕获,这可能导致随访期间对COPD事件的估计较低[21].然而,这些暴露和结果错误分类可能会使所检查的关联偏向零。此外,关于COPD严重程度的临床数据,如肺功能测定数据和COPD症状严重程度,目前尚不清楚。
我们发现,目前和以前的吸烟者食用富含类黄酮的饮食比低类黄酮摄入量的人患COPD的风险更低。虽然这项研究的结果表明,饮食中的黄酮类化合物在一定程度上降低了吸烟者患COPD的风险,但目前和曾经吸烟的人患COPD的风险仍然比不吸烟的人高得多,这表明饮食调整应该是戒烟之后的次要因素。
补充材料
可共享的PDF
脚注
如果作者被确定为国际癌症研究机构/世界卫生组织的工作人员,作者仅对本文中表达的观点负责,他们不一定代表国际癌症研究机构/世界卫生组织的决定、政策或观点。
利益冲突:作者声明没有利益冲突。
支持声明:丹麦饮食、癌症和健康研究由丹麦丹麦癌症协会资助。N.P. Bondonno由澳大利亚国家卫生和医学研究委员会早期职业奖学金(资助号APP1159914)资助。刘易斯的薪水由澳大利亚国家心脏基金会未来领袖奖学金(ID 102817)支持。霍奇森博士的薪水由澳大利亚国家卫生和医学研究委员会高级研究奖学金(资助号APP1116937)支持。本文的资助信息已存入交叉参考基金注册.
- 收到了2021年9月30日。
- 接受2021年12月18日。
- 版权所有©作者2022。
本版本根据知识共享署名非商业许可4.0的条款发布。为商业复制权利和权限联系权限在}{ersnet.org