摘要
背景我们的目的是确定抗白细胞介素(IL)-6受体是否能改善2019冠状病毒病(COVID-19)肺炎危重患者的预后。我们报告了两个队列嵌入、研究者发起、多中心、开放标签的贝叶斯随机对照临床试验。
方法患者被随机分配接受常规治疗(UC)或UC+托珠单抗(TCZ) 8 mg·kg−1(TOCI-2试验)或UC或UC+sarilumab (SARI) 200 mg (SARI-2试验),均在第1天静脉注射,如果有临床症状,则在第3天静脉注射。
结果在2020年3月31日至4月20日期间,TOCI-2试验随机分配了97例患者,分别接受UC (n=46)或UC+TCZ (n=51)。第14天,不需要无创通气(NIV)或机械通气(MV)且存活的TCZ或UC患者数量相似(47%)与42%;中位后验风险比(HR) 1.19, 90%可信区间(CrI) 0.71-2.04), HR >1的后验概率为71.4%。2020年3月27日至4月4日期间,91例患者在SARI-2试验中被随机分组,分别接受UC (n=41)或UC+SARI (n=50)。第14天,不需要NIV或MV且存活SARI或UC的患者数量相似(38%)与33%;中位后验HR 1.05, 90% CrI 0.55-2.07), HR >1的后验概率为54.9%。总的来说,到第90天的死亡风险为:UC+TCZ 24%与UC 30% (HR 0.67, 95% CI 0.30-1.49), UC+SARI 29%与Uc 39% (hr 0.74, 95% ci 0.35-1.58)。TCZ和SARI均增加严重感染事件。
结论在COVID-19危重患者中,到第14天,抗il -6受体并没有显著增加无NIV或MV存活的患者数量。
摘要
在两项前瞻性随机研究中,在ICU的COVID-19患者中,抗il -6受体并没有显著提高无机械通气的早期生存率。然而,由于患者数量较少,无法得出明确的结论。https://bit.ly/3GoFAJV
简介
2019冠状病毒病(COVID-19)是一种由一种新型冠状病毒(严重急性呼吸综合征冠状病毒2型(SARS-CoV-2))诱导的呼吸道疾病,截至2021年2月已在全球造成250多万人死亡[1- - - - - -4].大多数COVID-19患者只有轻微或不复杂的症状。尽管如此,约10-15%的患者患有中度或重度疾病,需要住院和氧气支持,3-5%的患者需要入住重症监护病房(ICU),主要是为了辅助通气[4,5].
COVID-19肺炎患者出现非特异性炎症反应,包括肺部水肿和炎症细胞浸润。除了SARS-CoV-2的特异性致病作用外,宿主免疫反应除了在控制病毒复制方面的作用外,还可能导致高炎症,导致肺功能恶化。它至少在一定程度上与几种促炎细胞因子和趋化因子的产生有关,包括白介素(IL)-6。康复合作小组证明,地塞米松(DXM) 6 mg·天−1接受氧气治疗(包括机械通气(MV)、高流量氧气(HFO)和无创通气(NIV)的患者28天死亡率下降[6].因此,糖皮质激素对中、重度和危重症患者的益处表明,过度的宿主炎症反应是导致COVID-19严重疾病和死亡的主要原因。
在法国疫情初期,当时还没有确定护理标准,包括使用糖皮质激素和抗凝血,我们决定建立公共支持的corimuni -19平台,致力于在两组定义明确的患者中进行队列、开放标签、随机的免疫调节药物临床试验:中-重度COVID-19肺炎住院患者和重症监护室(icu)住院且采用无创通气或有创通气的患者(世界卫生组织临床进展量表(WHO-CPS)评分<5分且至少3 L·min)−1O2或者>5)。
鉴于IL-6在COVID-19高炎症反应中的潜在有害作用[7- - - - - -11,我们评估了tocilizumab (TCZ)和sarilumab (SARI)这两种抑制IL-6信号的抗人IL-6受体(IL-6R)单克隆抗体的受益-风险效应。在非icu患者中,我们发现TCZ [12,13但不是莎丽[14],但对第28天的存活没有影响,对第90天的存活率有更好的趋势。然而,这些研究并不是为了评估总体生存率。在这两项研究中,我们考察了TCZ和SARI的有效性与常规护理(UC)对新冠肺炎危重患者无通气生存率的影响。
方法
试验设计和研究监督
在SARS-CoV-2大流行之初,我们建立了一个COVID-19中、重度或危重性肺炎患者队列(CORIMUNO-19队列;ClinicalTrials.gov:NCT04324047).该队列用于对COVID-19患者的不同治疗方案进行一系列随机对照试验。招募了两个独立的人群:中、重度肺炎患者和危重患者。2020年4月6日,由机构审查委员会批准的议定书修正案对这两个人群的定义进行了如下明确(见补充材料1) WHO-CPS评分为10分5的中、重度肺炎患者至少接受3 L·min的治疗−1O2但没有HFO(通过使用高流量设备(Optiflow;Fisher & Paykel,奥克兰,新西兰)>15 L·min−1O22) WHO-CPS评分≥6分的危重肺炎(即。HFO, NIV或MV)。本文报道了两项针对COVID-19危重患者的多中心、开放标签、随机对照临床试验:ClinicalTrials.gov:NCT04331808,这是在中度或重度肺炎患者中进行的cor免疫no - toci -1试验的常见标识符,此前已有报道[12])和CORIMUNO-SARI-2 (SARI治疗)(ClinicalTrials.gov:NCT04324073,这是在中度或重度肺炎患者中进行的CORIMUNO-SARI-1试验的常见标识符,最近也有报道[14])。在12所(TOCI-2)和8所(SARI-2)不同的法国大学医院进行了研究。每个中心只能接受一种治疗方案的患者。由于试验的紧急性质和可行性问题,没有制备TCZ和SARI的安慰剂。
CORIMUNO-19队列和所有嵌入试验(即。使用在CORIMUNO-19队列中收集的数据的试验)得到了伦理委员会(CPP Île-de-France VI)和相关当局的批准。在SAP中对法律问题和审判程序进行了详细的阐述补充材料.所有患者或患者的法定代表人在进入CORIMUNO-19队列时都获得书面知情同意,并记录纵向数据(包括临床状态、生物学数据和结果),作为他们参与队列的一部分。在这份同意书中,患者和/或他们的家属被告知可能会进行一些试验通过他们可能会被邀请参加其中的一些活动。实际上,由于后勤方面的原因,每个地点在同一时间内只进行一次审判。随机选择合格的患者或其家属接受TCZ或SARI治疗,并获得额外的书面同意。随机分配TCZ/SARI但拒绝治疗或无法治疗的患者在随机分组(TCZ/SARI)的意向治疗基础上进行分析。被分配接受UC治疗的合格患者没有被告知该试验,但他们的CORIMUNO-19队列数据可用于分析。这是队列嵌套多随机对照试验的经典过程[15].所有纳入的患者都在ICU,因此有些患者无法给出同意。在这种情况下,根据法国法律,急诊同意书须经家属同意后由医生签署。当病人康复后,必须签署一份追踪同意书。如果患者拒绝签署,就会被认为是同意退出,患者的数据就不能被分析。根据CONSORT指南报告试验。
病人
如果患者确诊为SARS-CoV-2感染(逆转录pcr阳性和/或典型胸部计算机断层扫描阳性),并伴有中度、重度或危重肺炎(O2> 3 L·分钟−1, WHO-CPS评分≥5分;看到SAP在补充材料[16])。
如果来自corimno -19队列的患者WHO-CPS评分为>5,包括NIV或MV患者,那么他们有资格参加TOCI-2或SARI-2试验。排除标准在SAP中有详细说明补充材料.
随机化和治疗
参与者按1:1的比例被随机分配到TOCI-2协议的UC+TCZ或UC,或sar -2协议的UC+SARI或UC通过基于网络的安全集中系统。一名独立的统计学家提供了一份计算机生成的分配随机列表,按中心分层,并以调查人员未知的不同块大小进行阻塞。中心有资格参加TOCI-2或SARI-2试验,但不能同时参加。两项试验均在同一时期进行。
TCZ静脉滴注8 mg·kg−1第1天,给予SARI注射。第一天服用固定剂量400mg。给药额外的固定剂量tcz400 mg注射。或SARI 400毫克注射。第3天建议,并留给治疗医师。UC(抗生素、抗病毒药物、糖皮质激素、血管加压剂支持和抗凝剂)的提供由临床医生自行决定,因为当时没有确定护理标准,包括糖皮质激素的使用。
结果测量
早期共同主要结局是第4天WHO-CPS评分至少下降1分的患者比例。结果以改善患者的比例表示,因此有效的治疗将与比例的增加相关联。较长期的共同主要转归是第14天成功气管拔管(定义为拔管时间>48小时)的累积发生率,如果患者在第14天前插管,或如果患者通过NIV或HFO吸入氧气(评分6)且仍未插管,则取出NIV或HFO(>48小时)的累计发生率。死亡或新的不复苏命令(如果在纳入患者后应用)被视为竞争事件。这两项结果都符合世卫组织提出的核心成果集(见《世界卫生组织报告》)补充材料) [16].次要结局包括第4、7和14天用WHO-CPS评估的临床状态、第90天的总生存期、出院时间、独立供氧时间以及c反应蛋白(CRP)水平、淋巴细胞和中性粒细胞计数等生物学因素的变化。
数据质量监控
数据质量监测包括远程数据监测和独立于现场调查人员的专职人员进行的现场监测,对每个地点招募的所有患者的所有关键数据点进行100%的源数据验证。
统计分析
为了从产生的有限数据中最大化信息,同时允许快速决策,我们使用了基于共同主要结果的贝叶斯监测和分析试验。样本量定为120人,每周向数据和安全监测委员会提交中期分析报告,并规定在取得有希望但不确定的结果时增加样本量。我们计算得出,该试验检测主要转归率从0.50增加到0.80的频率率为97.2%,检测事件率从0.50减少到0.70的频率率为73.9%。对于第4天的结果,我们使用β先验分布,参数为1和1的比例在每个臂。对于第14天的结果,我们使用均值为0、方差为10的高斯先验分布6为日志风险比(HR)。然后使用一系列的先验分布进行敏感性分析(见补充材料).治疗效果以第4天结果的绝对风险差(ARD)和第14天结果的子分布HR表示。采用马尔可夫链蒙特卡罗马尔可夫方法,计算了ARD <0和HR >1的后验概率。根据该方案,中期分析的后验概率>0.99或最终分析的>0.95表示有效。我们还计算了ARD < - 5.5%和HR >1.18 (即。1/0.85),均表示中等或较大的影响。由于决策规则是片面的,一致可信区间(CrIs)将是片面的95% CrIs。然而,我们选择报告双侧90% CrIs,其下界与单侧95% CrIs相同。根据抗病毒药物在基线时的使用情况进行亚组分析是在方案中预先规定的。根据糖皮质激素或DXM和CRP的使用情况进行分析事后根据最近的出版物[11].除WHO-CPS得分作为序变量分析外,次要结果采用频率分析框架进行分析。SAP和统计分析的全部细节在补充材料.在缺乏统计学异质性证据的情况下,联合IL-6抑制剂效应与一阶段方法一起使用(见文献中的SAP)补充材料).这些分析是在频率论框架下进行的。
在意向治疗基础上进行分析,没有对次要结果的多重性进行校正。因此,次要结果应被视为探索性的,并以点估计和95%置信区间(ci)的形式报告。使用SAS 9.4 (SAS Institute, Cary, NC, USA)和R 3.6.1 (www.r-project.org).
结果
病人
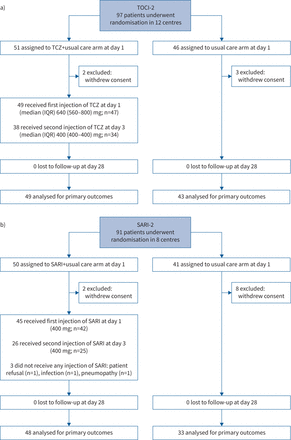
从2020年3月31日至4月18日和2020年3月27日至4月4日,97名患者和91名患者分别随机参加TOCI-2试验(51名患者参加UC+TCZ, 46名患者单独参加UC)和SARI-2试验(50名患者参加UC+SARI, 41名患者单独参加UC)。数据和安全监测委员会没有建议进一步增加样本量,因为4月中旬(法国第一波疫情结束)后,新冠肺炎病例数量急剧下降,因此停止了试验。在被分配接受TCZ或SARI的51名和50名患者中,两种方案中都有两名患者撤回了同意,没有进行分析。在分配接受UC治疗的46和41名患者中,TOCI-2方案的3名患者和SARI-2方案的8名患者撤回了同意,没有进行分析。在49名或45名接受TCZ或SARI治疗的患者中,38名(47%)和26名(58%)分别在第3天接受了第二次注射(图1).患者的人口学和基线临床和生物学特征描述在表1.中位(四分位范围(IQR))年龄分别为64.6(58.7-70.6)和61.2(53.9-66.9)岁,在TOCI-2和SARI-2协议中,分别为72%和77%为男性。在TOCI-2和SARI-2协议的注册方面,组间无主要差异。
流程图。a) TOCI-2方案(tocilizumab (TCZ)治疗+常规护理与常规治疗)。b) SARI-2方案(SARI治疗+常规护理与常规治疗)。IQR:四分位范围。
在随机分组中,很少有患者接受抗病毒治疗或糖皮质激素,值得注意的是,没有患者接受DXM (补充表S1).
主要的结果
第4天,随机接受TCZ和SARI治疗的49名患者中有35名(71%)和48名患者中有34名(71%)的情况没有改善,因为他们的WHO-CPS评分至少降低了1分与UC组43例中有30例(70%),33例中有26例(79%)(中位后路ARD +1.7% (90% CrI−13.6至+17.1)或- 7.3% (90% CrI−22.5至+8.7)(补充图S1而且补充表S2).ARD <0 (TCZ或SARI优于UC)的后验概率分别为42.9%和77.7%,ARD <−5.5%的后验概率分别为22%和57.5%。
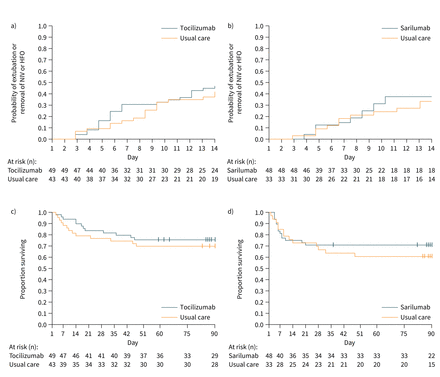
在第14天,累积成功的气管拔管的发生率或删除和合高频振荡器(持续时间> 48 h)发生在23个(16插管和七和合/高频振荡器)或18(11插管和七和合/高频振荡器)患者TCZ或纱丽,分别(事件的累积发生率为47% (95% CI 32 - 60%)或38% (95% CI 24 - 51%)和18个(12插管和六个和合/高频振荡器)和11(6插管和五个和合/高频振荡器)在UC患者TOCI-2或SARI-2协议,分别是(表2).TCZ或SARI任何疗效的后验概率(HR >1)分别为71.4%和54.9%,中等或较高疗效(HR >1.18)分别为51.9%和38.9%(后验校正HR中位数1.19 (90% CrI 0.71-2.04)和1.05 (90% CrI 0.55-2.07)) (补充表S3).在没有调整年龄和中心的情况下观察到类似的结果(补充表S4而且补充图S2).发生主要事件(拔管或取出NIV或HFO >48小时无死亡)的患者比例显示在图2.
随访期间发生的事件。Kaplan-Meier累积估计主要结局(撤除设备(机械通气、高流量氧气(HFO)或无创通气(NIV)支持))和14天内死亡的概率:a) TOCI-2(使用托珠单抗治疗)和b) SARI-2(使用萨莱单抗治疗);c) TOCI-2(托珠单抗组与常规护理组比较)和d) SARI-2(萨罗单抗组与常规护理组比较)的总生存率。
预先指定(抗病毒药物)或事后没有进行亚组分析(皮质类固醇,包括DXM),因为两种方案中使用抗病毒药物或皮质类固醇的患者比例太低(<5%)(补充表S5(TOCI-2)和补充表S6(SARI-2))。此外,我们执行了附加操作事后亚组分析根据WHO-CPS评分和从ICU住院到随机化的时间(≤1与>1天)和CRP水平(<150或>150 mg·mL−1) (补充表S5和S6).
二次结果
给出了14天随访期间WHO-CPS评分的变化补充图S3而且补充表S7.虽然观察到了一些趋势,但在无呼吸机的第28天,TOCI-2和SARI-2方案均未观察到显著差异(补充表S8)、供氧独立性(59%)与49%和44%与36%) (补充表S9)累积出院发生率(59%与49%和44%与36%) (补充表S10)或ICU出院时间(72%与60%或60%与71%) (补充表S11).
总的来说,中位随访(范围)为95(59-217)天和91(36-210)天,第90天,TCZ和SARI组中有12(24%)和14(29%)例患者死亡与13人(30%)和13人(39%)在各自的UC对照组(调整HR 0.67 (95% CI 0.30-1.49)和0.74 (95% CI 0.35-1.58)) (图2 c和d,和补充表S12).所有组的死亡原因相似,主要是由于急性呼吸窘迫综合征,并总结在表3.
生物反应
TCZ组和SARI组的平均CRP水平迅速下降,淋巴细胞计数增加(补充图S4)主要是在TCZ臂,而不是在SARI臂。
讨论
在纳入corimno -19队列的这两项试验中,我们没有发现TCZ和SARI对需要HFO、NIV或MV的危重COVID-19肺炎患者在第14天去除插管、NIV或HFO(>48小时)后存活的患者比例有任何疗效。然而,两种抗il - 6r抗体在90天前的存活率有轻微的增加(但在统计学上不显著)(76%和71%)与UC患者分别为70%和61%;HR分别为0.67 (95% CI 0.30-1.49)和0.74 (95% CI 0.35-1.58)(合并分析HR 0.71, 95% CI 0.61-1.23)。TCZ和SARI没有引起任何严重不良事件的显著增加,但严重感染的数量增加。
在ICU需要HFO、NIV或MV (WHO-CPS评分≥6)的患者中,唯一的护理标准为DXM [6在RECOVERY试验中,它已被证明可以提高第28天的总生存率,特别是对入院后不久就接受治疗的患者。IL-6R拮抗剂引入的时间似乎很重要,一项涉及433名患者的大型模拟多中心试验也表明,该试验发现,尽管继发感染的风险增加,但与未早期使用TCZ治疗的患者相比,在ICU住院的前2天接受TCZ治疗的患者住院死亡的风险较低[17].TCZ和SARI是两种注册用于治疗类风湿性关节炎和细胞因子释放综合征的抗il - 6rs(仅TCZ),也已在治疗COVID-19患者中进行了广泛试验,其效果仍有待讨论。在需要吸氧的非危重症患者(WHO-CPS评分5)中,多项研究表明TCZ降低了第28天的死亡率,与严重不良事件(特别是感染)的减少相关[18].对于严重急性呼吸道感染,检验其效果的研究较少,其疗效甚至不确定[19].
我们的结果与近期REMAP-CAP报告的结果形成对比,在较低程度上,与同一组危重患者的康复研究结果形成对比[20.,21].在REMAP-CAP研究中,对于分配到TCZ(中位数OR 1.64, 95% CI 1.25-2.14)或SARI(中位数OR 1.76, 95% CI 1.17-2.91)组的患者,无器官支持天数的中位数优于前者,这与更好的总生存率相关。在所有二次分析中,包括在第14天和出院时WHO-CPS的改善[20.].在RECOVERY试验中,TCZ提高了需要氧支持的患者的总生存率。然而,尽管在MV患者中观察到有利于TCZ的趋势,但没有达到显著性(HR 0.93, 95% CI 0.74-1.18) [21].有趣的是,在这两项研究中,大多数患者接受了皮质类固醇,特别是DXM(>80%),而TCZ和SARI的效果似乎为DXM提供了额外的好处。此外,在REMAP-CAP研究中观察到的较高效果可能是由于患者在开始MV后24小时内入组并接受治疗。最近,在世界卫生组织的前瞻性meta分析(包括REMAP-CAP和RECOVERY)中,对27个试验中随机抽取的10 390名肺炎住院患者进行了前瞻性meta分析,证实了REMAP-CAP和RECOVERY研究的结果,IL-6拮抗剂治疗在第28天降低了死亡率(OR 0.86, 95% CI 0.79-0.95;p=0.003),这些结果在接受皮质类固醇的患者组甚至更好(或0.77 (95% CI 0.68-0.87) TCZ和0.92 (95% CI 0.61-1.38) SARI) [18].此外,在亚组分析中,在随机接受MV的1171名患者(9个试验招募)中,在MV持续时间内,IL-6拮抗剂与UC或安慰剂的加权平均差异为−0.84 (95% CI−1.82 - 0.13),有利于IL-6拮抗剂(本分析中95%接受TCZ的患者)。综上所述,DXM和可能的抗il - 6r抑制剂的益处可能在某些时间点对某些人群有益,且不会过早抑制有益的免疫反应,可能依赖于抑制高炎症反应或平衡损伤修复,或两者兼有。
在TOCI-2和SARI-2方案中,DXM的使用非常少,大多数患者(146例中84例(56%))在ICU住院第1天后被纳入并治疗,这可能太晚了,因为肺部病变已经确定。
即使没有达到主要终点,观察到抗il - 6r两种抗体在第90天总体生存期改善的非显著趋势是有趣的和有些令人惊讶的。这可能是由于在第28天使用TCZ和SARI之前,无呼吸机的天数略有减少与UC(平均差值分别为−2.5 (95% CI−6.9-1.7)和−1.5 (95% CI−6.1-3.9)天)。有趣的是,在我们的两个试验中,UC和UC+抗il - 6r抗体在90天内的总生存期的差异与REMAP-CAP研究中观察到的差异并不大。事实上,在REMAP-CAP中,TCZ到第90天的存活hr为0.63 (95% CrI 0.49-0.81), SARI为0.55 (95% CrI 0.30-0.82),与我们研究中到第90天的死亡hr相差不远:TCZ为0.67 (95% CI 0.30-1.49), SARI为0.74 (95% CI 0.35-1.58)。
在安全性方面,这两项在ICU患者中的试验与之前在医疗病房吸氧患者中的抗il - 6r抗体试验之间的主要区别是SARI和TCZ组中严重感染的数量增加(n=46)。与加州大学(n = 17)。抗il - 6r抗体严重感染的风险增加(仅在TCZ中有统计学意义),很容易解释这些患者在ICU中比在医疗病房中的患者更脆弱。然而,在我们的研究中,细菌性败血症很少是两组患者死亡的原因,因此在危重患者中抗il - 6r抗体的总体好处[18]可能是在减少有害的肺高炎症和不增加太多细菌和真菌并发症风险之间的一种妥协。
限制
在第一波COVID-19大流行浪潮开始时,CORIMUNO-19队列的设计目的是快速进行几项探索性临床试验,并快速提供潜在感兴趣的候选药物的信息。该试验不是盲法试验,因为在大流行时期,从逻辑上讲不可能足够快地建立一个双盲研究。然而,在这组危重患者中,开盲不太可能导致测量偏差,因为拔管的决定是基于与动脉氧张力/吸气氧分数(PaO2/FIO2)的比例。另一个限制是UC在不同的中心和时间会有所不同。然而,短期的累积和随机化的分层可能限制了这种缺乏标准化的影响。由于CORIMUNO-19平台的设计,由于第一波流行波的结束,无法增加样本量,样本量较小,没有设计出生存率差异,可信区间较宽,治疗效果可能被低估[22].我们的研究也不是为了比较TCZ和SARI各自的效果,但在这里有类似的效果。
结论
综上所述,本研究并没有提供证据证明TCZ或SARI可有效缩短COVID-19危重患者组的通气支持时间。然而,世卫组织最近的元分析结果[18的结果与我们在第90天的死亡率结果一致,这表明抗il - 6r抗体加DXM可能是COVID-19危重患者的一种选择。
补充材料
补充材料
请注意:补充材料不由编辑部编辑,上传时由作者提供。
补充材料:数字和表格erj - 02523 - 2021。补充
附录1:投稿者名单erj - 02523 - 2021。附录
统计分析方案erj - 02523 - 2021。SAP
可共享的PDF
确认
一个指导委员会负责试验的设计、实施和报告,一个独立的数据和安全监测委员会监督所有CORIMUNO-19试验(补充附录)。作者保证了数据和分析的准确性和完整性,以及试验对协议的保真性。我们感谢所有参与CORIMUNO-19研究的患者和他们的家人。作者还感谢负责后勤工作的Maxime Dougados (Université de Paris, Paris, France),以及参与本研究的调查人员(补充附录),以及巴黎大学、巴黎-萨克雷大学、巴黎-索邦大学、巴黎-北索邦大学、巴黎- est大学Créteil、凡尔赛-圣昆汀大学、斯特拉斯堡大学和里尔大学(医学院学生支持)、INSERM和反应学院。
脚注
撰写委员会:Olivier Hermine, Université de Paris, AP-HP, Hôpital Necker, INSERM, Imagine Institute,巴黎,法国;泽维尔·马里耶特,Université巴黎-萨克莱,AP-HP, Hôpital Bicêtre, INSERM, Le Kremlin-Bicêtre,法国;Pierre-Louis Tharaux,巴黎心血管中心(PARCC), Université de Paris, INSERM,巴黎,法国;Matthieu Resche-Rigon流行病学和统计研究中心(CRESS), Université de Paris, INSERM, Hôpital Saint Louis,法国巴黎;Raphael Porcher,流行病学和统计研究中心(CRESS), Université de Paris, INSERM, INRAE, AP-HP, Hôpital Hôtel-Dieu,法国巴黎;Philippe Ravaud,流行病学和统计研究中心(CRESS), Université de Paris, INSERM, INRAE, AP-HP, Hôpital Hôtel-Dieu,法国巴黎。
这项研究注册在ClinicalTrials.gov带有标识符编号NCT04331808而且NCT04324073.作者将在获得CORIMUNO-19平台指导委员会批准后分享数据。经批准后,将为任何目的共享个人去识别的参与者数据、研究方案和统计分析计划(SAP)。数据公布后将提供15年。
作者贡献:所有作者都对数据的概念和设计或获取、分析或解释,以及手稿的起草或关键修订做出了实质性贡献。所有作者都可以访问数据,并为工作的完整性负责。所有作者都批准了投稿出版。
利益冲突:P-L。Tharaux曾因参与Travere therapeutics的顾问委员会而获得酬金。所有其他作者均未披露与本工作相关的潜在利益冲突。
支持声明:该试验由卫生部、研究诊所项目(PHRC COVID-19-20-0143, PHRC COVID-19-20-0029)、医学研究基金会(FRM)、AP-HP基金会和反应方案)提供公共资金。资助者无法获得试验数据,也不能参与试验的设计、实施或报告。罗氏和赛诺菲分别以无限制赠款的形式捐赠了TCZ和SARI,并没有参与试验的设计或实施;数据的收集、管理、分析或解释;或在准备、审稿或审稿时。本文的资助信息已存入Crossref基金管理人登记处.
- 收到了2021年6月25日。
- 接受2021年12月23日。
- 版权所有©作者2022。
本版本按照创作共用署名非商业性许可4.0的条款发布。商业复制权利及许可请联系权限在}{ersnet.org